ICP-MS碰撞反应池检测食品中10种元素
文 / 张 建,田志强,卢垣宇,孙宗奇,周筑萍,朱丽波,李丽,邵飞龙
(1.国家酒类及饮料质量监督检验中心,贵州 贵阳 550004;2.贵州省产品质量监督检验院,贵州 贵阳 550004)
ICP-MS碰撞反应池检测食品中10种元素
文 / 张 建1,2,田志强1,2,卢垣宇1,2,孙宗奇1,2,周筑萍1,2,朱丽波1,2,李丽1,2,邵飞龙1,2
(1.国家酒类及饮料质量监督检验中心,贵州 贵阳 550004;2.贵州省产品质量监督检验院,贵州 贵阳 550004)
建立了电感耦合等离子体质谱法(ICP-MS)测定食品中Pb、As、Hg、Cd、Ba、Cr、Se、Ni 、Mg、、Al10种元素的方法。样品经微波消解后,直接用ICP-MS 同时测定上述10种元素,结果10种元素的检出限分别在5~200 ng/L之间;线性良好,线性相关系数均为r≥0.9993;精密度RSD<4.3%;回收率在91.44%-100.20%之间;对不同食品类型的标准物质GBW 10052(GSW-30)、GBW 10015、GBW 10018进行测定,结果令人满意。方法操作简便、分析速度快、灵敏度高,各项分析性能指标均达到要求,适用于食品中元素的测定。
微波消解、ICP-MS、食品、铅、砷、汞、镉、钡、铬、硒、镍、镁、铝
食品安全问题一直是人类关注的焦点。随着工农业生产的迅速发展,食品污染问题越来越严重,其中重金属是最主要的污染物之一。重金属可积累在土壤中和在作物内残留,通过食物链进入人体内蓄积,构成对人体的潜在危害,人体内重金属含量过量时,会导致各种疾病甚至死亡。食品重金属污染问题已引起全世界的高度重视和深入研究,对不同种类食品和水体中的重金属污染进行监测和分析研究,对于评价食品质量、保护人类健康和维持社会经济可持续发展具有重要的现实意义。我国对食品中重金属有严格的限量标准。但是,目前对各元素的测定,往往采用单一元素测定法,手续繁琐,分析时间长。微波消解-电感耦合等离子体质谱(ICP-MS)法同时测定食品中的Pb、As、Hg、Cd、Ba、Cr、Se、Ni、Mg、Al,操作简单、快速、基体干扰少,准确度、灵敏度高,结果可靠,已成为近年来元素分析的重要手段。
1、试验部分
1.1 试剂和材料
硝酸、高氯酸、30%过氧化氢(均为优级纯);超纯水(电阻率18.2MΩ·cm)。多元素标准溶液、质谱最佳化调谐液(美国PerkinElmer公司)。
多元素标准溶液(100mg/L,CAS号为[7697-37-2]),汞元素溶液标准物质(1000μg/ mL,GBW08617) ,以5%硝酸为介质,临用时逐级稀释;质谱最佳化调谐液(10mg/L),仪器普通灵敏度条件优化需用质量浓度为10μg/L的调谐液(1%硝酸为介质)[1]。
注:除非另有说明,本方法所用试剂均为优级纯,水为GB/T6682规定的一级水。
注:汞标准稳定剂亦可采用0.2%半胱氨酸溶液配制成相应溶液。
1.2 仪器与设备
DRC-e ICP-MS System电感耦合等离子体质谱仪(美国PerkinElmer公司)[2-3];Milli-Q Gradient纯水处理系统(French Millipore);MARS微波消解仪(美国CEM公司);HotPlate(EH45APlus)微控数显电热板(LabTech有限公司)。
1.3 方法
1.3.1 样品处理
1.3.1.1 干样:取可食部分,必要时经高速粉碎机粉碎,混匀,备用。
1.3.1.2 湿样:取可食部分,必要时水洗干净,晾干或纱布揩干,经匀浆器匀浆,备用。
1.3.2 试样预消解
1.3.2.1 酒类试样取样后需在电热板上于100℃左右挥去醇类物质,然后加入硝酸进行消解。
1.3.2.2 高脂肪、高蛋白、高淀粉、高纤维等难消解试样,取样加硝酸后,需进行冷消化(放置至少1h,最好过夜)。
1.3.3 试样消解
1.3.3.1 微波消解:称取固体干样0.2g~0.5g、湿样0.2g~0.8g(精确到0.001g)或移取液体试样1mL~3mL于微波消解罐中,加入5mL~8mL硝酸,加盖放置1h,旋紧罐盖,按照微波消解仪的标准操作步骤进行消解(消解参考条件见表1)。冷却后取出,缓慢打开罐盖排气,用少量水冲洗内盖,将消解罐放在控温电热板上或超声水浴箱中,于100℃加热或超声脱气2 min~5min,赶去棕色气体,取出消解内罐,将消化液转移至25mL或50mL容量瓶中,并定容至刻度,混匀备用;同时做试剂空白试验[4]。
1.3.3.2 压力罐消解:称取固体干样0.2g~1.0g、湿样0.5g~2.0g(精确到0.001g)或移取液体试样1mL~5 mL于消解内罐中,加入5 mL 硝酸,盖好内盖,放置1 h,旋紧不锈钢外套,放入恒温干燥箱消解(消解参考条件参见表1),在箱内自然冷却至室温,然后缓慢旋松不锈钢外套,将消解内罐取出,用少量水冲洗内盖,放在控温电热板上或超声水浴箱中,于100 ℃或超声脱气2 min ~ 5 min赶去棕色气体。将消化液转移至25 mL或50 mL容量瓶中,并定容至刻度,混匀备用;同时做试剂空白试验。

表1 消解参考条件Table 1 Digestion conditions
1.3.4 仪器优化
优化仪器操作条件,使灵敏度、氧化物和双电荷化合物达到测定要求。
1.3.5 内标的选择
内标使用液:取适量单元素贮备液(1000 mg/L)混合,用硝酸溶液(5+95)配制合适浓度的内标使用液。内标使用液浓度见表2,推荐选择的内标元素见表3。
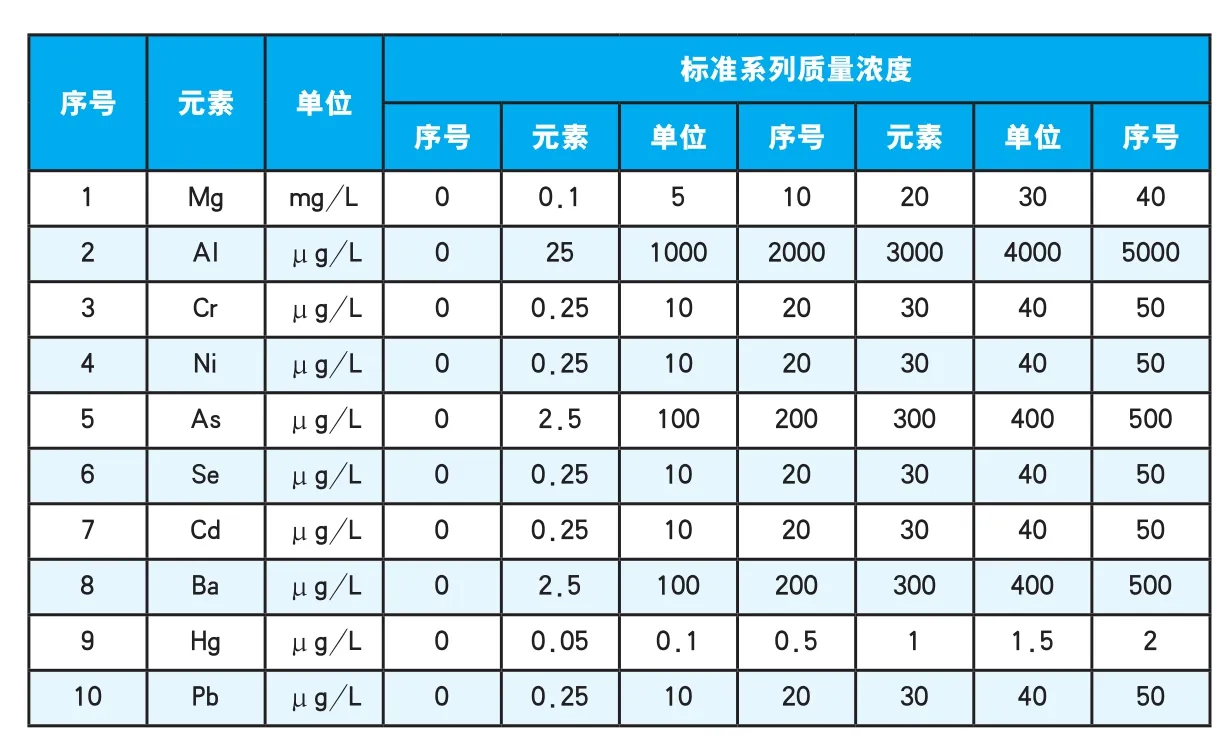
表2 10种元素的标准系列溶液质量浓度Table 2 A series of standard solution concentration of 10 elements
内标使用液浓度:内标既可在配制标准系列工作溶液和样品溶液时手动加入,亦可由仪器在线加入。由于不同仪器采用不同内径蠕动泵管在线加入内标,致使内标进入样品中的浓度不同,故配制内标使用液浓度时应考虑使内标元素在样液中的浓度约为0.025 mg/L ~ 0.05 mg/L[5-7]。

表3 待测元素推荐选择内标元素Table 3 The measured elements recommended selection of internal standard elements
1.3.6 仪器条件
样品测定按表4的仪器工作条件,将标准系列、试剂空白、样品溶液分别导入ICP-MS进行测定[6-7],由工作站软件分析数据,绘制标准曲线,计算样品含量[8-10]。
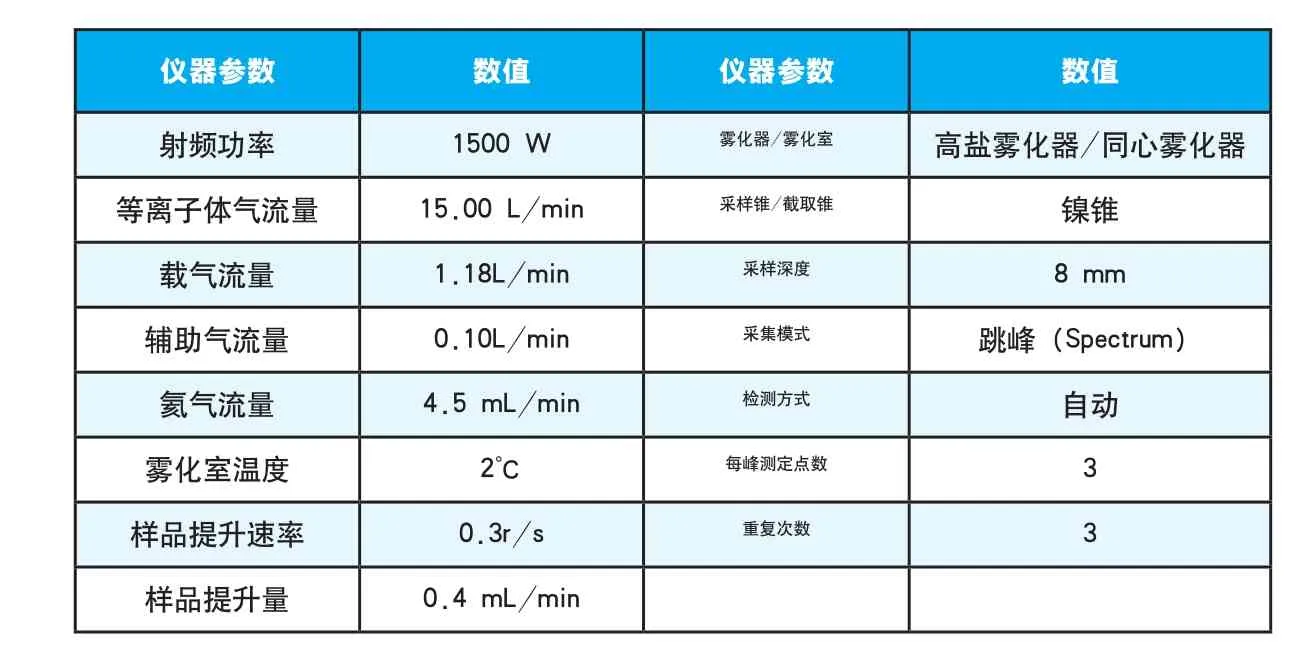
表4 电感耦合等离子体质谱仪操作参考条件Table 4 Inductively coupled plasma mass spectrometer operating reference conditions
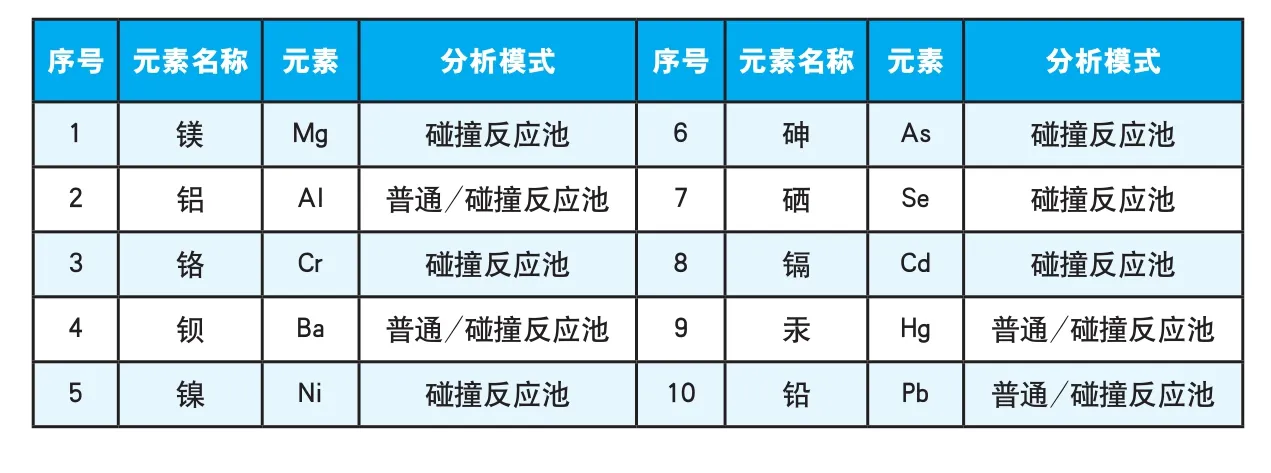
表5 电感耦合等离子体质谱仪操作参考条件Table 5 Inductively coupled plasma mass spectrometer operating reference conditions
2、结果与分析
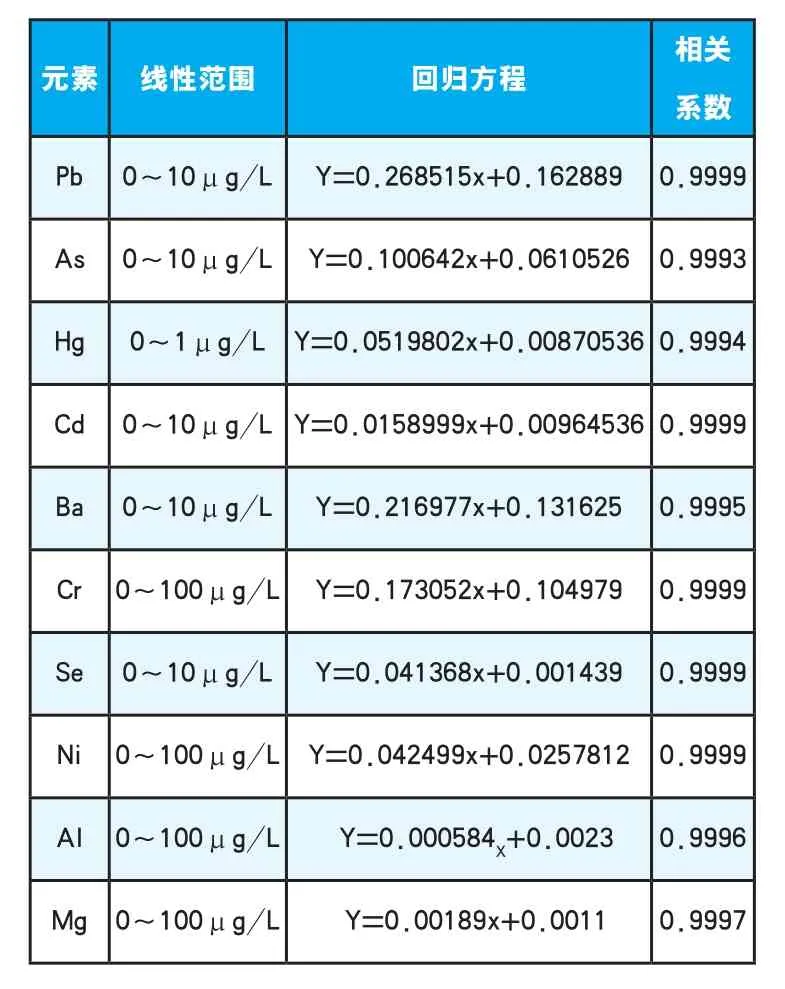
表6 方法的线性范围及相关系数Table 6 The linear range of the method and correlation coefficient
2.1 工作曲线
ICP-MS线性范围很宽,本文根据实际食品样品的元素浓度范围,确定了各元素的标准系列浓度。铅、砷、镉、钡、硒标准系列浓度范围为0~10μg/L,镁、铝、铬、镍为0~100μg/L,汞为0~1μg/L。在实际测定过程中,可根据样品的实际含量调整标准溶液的浓度范围,也可以对实际测定样品进行稀释,尽量使样品的测定浓度落在曲线的中间位置,这样可获得较为准确的结果。以上几种元素测定回归方程的相关系数均大于0.9993(见表5)[11-13]。
2.2 方法检出限和定量限
制备21份消化空白,上机测定,根据检出限的计算方法LOD=3sd/b和LOQ=10sd/b(b为工作曲线斜率),以仪器响应值的3倍和10倍标准偏差除以工作曲线斜率,同时考虑仪器背景相当浓度(BEC),再称取0.5g样量定容至25mL,计算出方法检出限、定量限1和定量限2(见表6)。
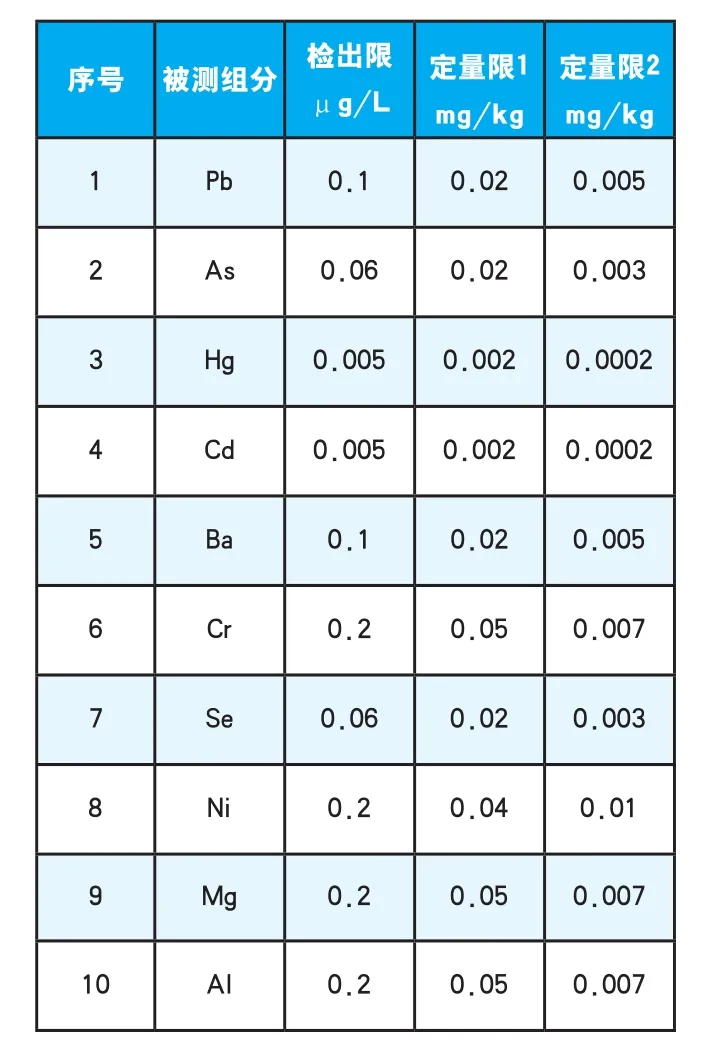
表7 各元素的检出限和定量限Table 7 Limit of detection and limit of quantification for each element
2.3 方法精密度、回收率及准确度
2.3.1 精密度:
实验室内重现性条件下的精密度选择不同基质的样品(含国家标准物质、实际样品),采用微波消解或压力罐消解法,对各类样品进行7次独立测试,计算7次相对标准偏差(RSD%),结果全部小于4.3%,完全达到欧盟委员会决议授权文件《贯彻执行96/23/EC关于分析方法和结果解释的决议》中对定量方法的精密度要求(数据见表7)。
长时间测定精密度实验 在近30h的实际样品测试过程中,每隔20个样品重复测测试同一低浓度标准溶液,共测试13次,其相对标准偏差均<5%。

表8 方法精密度及回收率Table 8 Precision and recovery of the method
2.3.2 回收率
对没有标准物质的其他基质类别样品(如蜂蜜、食用油、巧克力、调味品等)进行加标回收试验,将上述样品作为本底,同时向各样品中加入浓度50μg/L的混合标准溶液,采用高压密闭消解方法处理后,测定样品加标后各种元素的含量,计算加标回收率(数据见表8),结果除了少部分在定量限附近的加标样品外,各元素加标平均回收率均达到91.44%~100.20%,满足欧盟委员会决议授权文件《贯彻执行96/23/EC关于分析方法和结果解释的决议》中对定量方法的回收率的要求(白酒样品回收率数据见表7)[14-16]。

表9 样品回收率Table 9 Sample recovery rate
2.3.3 准确度:
标准参考物质 选择国内外各类有证标准参考物质,如、绿茶(GBW10052(GSW-30))、菠菜(GBW10015)、鸡肉(GBW10018)等共21种样品,每种平行制备3份样品,采用高压密闭消解后,测定样品中各元素的含量,除了少部分在定量限附近的数据,测定结果绝大多数在标准参考物质的证书参考值范围内,表明方法的准确度良好(数据见表9)[17]。
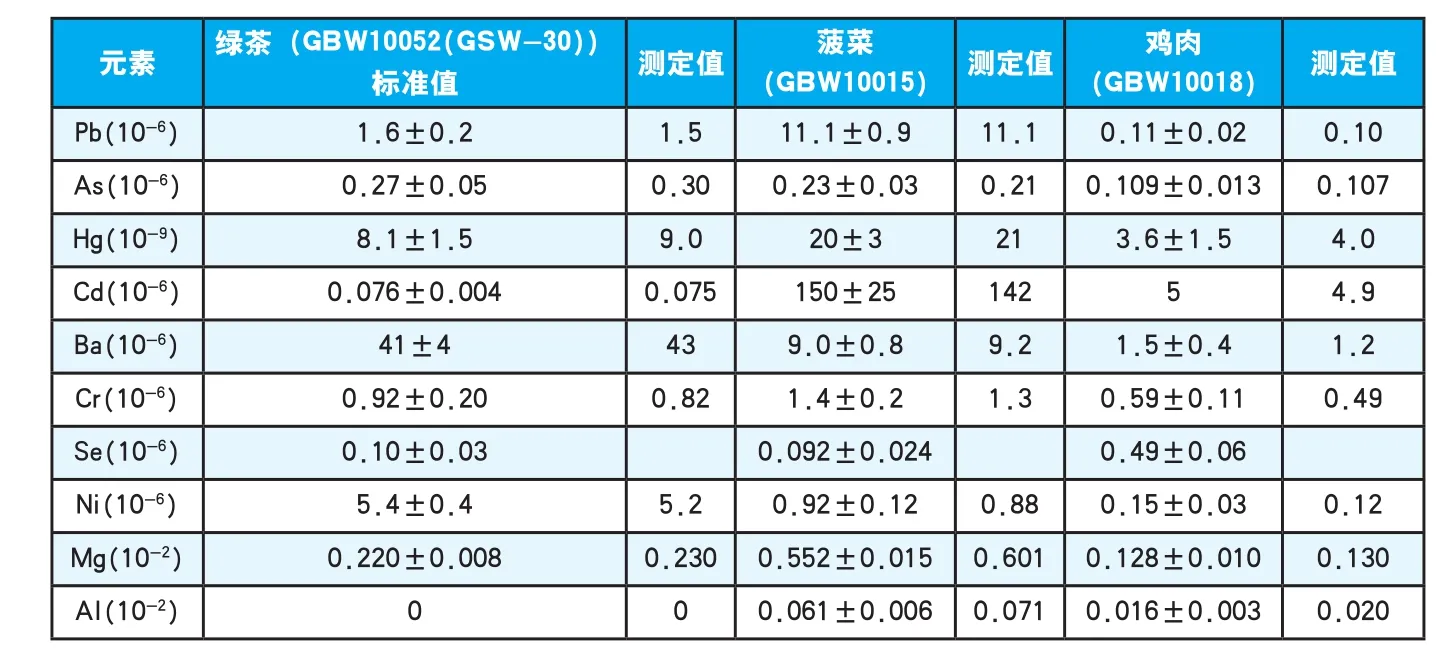
表10 方法准确度Table 10 Method accuracy
3、 讨论
本实验内标元素选择的原则为样品溶液中不含有该元素、与分析元素质量相近、电离电位与分析元素相近、与被测元素有相近的化学特性的物质作为内标。内标主要用来校正仪器的漂移。如果测定的元素对内标基本上没有同质量的干扰,内标的浓度与被测元素浓度相近即可。依据以上对方法验证的一系列数据,本实验对内标元素浓度的确定也满足检测的需求,使实验获得了成功,对今后食品中铅、砷、汞、镉、钡、铬、硒、镍、镁、铝10种有害元素ICP-MS法内标的选择提供了可行的方法[18-19]。
本实验方法10种待测元素标准曲线的线性相关性R2均大于0.9993,检出限均小于0.1μg/L,食品中10种元素的加标回收率均在91.44~100.20%,各元素的相对标准偏差(RSD)均小于5%,可以满足日常对食品中可能含有对人体有害8种元素筛查的需求。
ICP- MS分析技术的干扰主要有氧化物、双电荷、多原子离子、质量歧视效应、基体抑制、物理效应等干扰, 本研究采用最优化的仪器条件、选择合适的内标元素、干扰校正方程等方法加以消除,改善并提高了仪器的精密度。
4、结论
本方法采用单硝酸消解体系,经微波密闭消解或密闭高压消解食品样品,应用电感耦合等离子体质谱仪,标准曲线法定量,可以较好地测定铅、砷、汞、镉、钡、铬、硒、镍、镁、铝10种元素。方法快速、准确、具有较高的灵敏度。
[1] 刘虎生,邵宏翔.电感耦合等离子体质谱技术与应用[M].北京:化学工业出版社,2005, 18-29.
[2]VERSTRAETEN D. Elan DRC- e等离子体质谱仪在食品分析中的应用[J]. 岩矿测试, 2009, 27(1): 84-93.
[3] HAMMER D, NICOLAS M, ANDREY D. Improved chromium determination in various food matriced using DRC ICP-MS[J]. Atomic Spectroscopy, 2005, 26(6): 203-208.
[4] 汪地强, 赵振宇, 杨红霞, 等. ICP- MS测定茅台酒中32中微量元素[J]. 酿酒科技, 2008, 28(12): 104-105.
[5] 刘江晖.ICP-MS 测定海产品中汞含量[M].理化检验-化学分册,2006,42(6):207
[6] 倪张林, 汤富彬, 屈明华. 微波消解-电感耦合等离子体质谱法测定油茶籽油中的5种重金属元素[J]. 食品科学, 2013, 34(4): 165-167.
[7] 陈福北, 刘辉庭, 黄巧燕, 等. 微波消解ICP-MS/ICP-AES法测定广藿香中24种无机元素[J]. 食品科技, 2011, 36(10): 259-261.
[8] XIE Hualin, HUANG Kelong, LIU Jinchun, et al. Determination of traceelements in residual oil by high resolution inductively coupled plasma mass spectrometry[J]. Analytical and Bioanalytical Chemistry, 2009, 393(8): 2075-2080.
[9] NARDI E P, EVANGELISTA F S, TORMEN L, et al. The use of inductively coupled plasma mass spectrometry (ICP-MS) for the determination of toxic and essential elements in different types of food samples[J]. Food Chemistry, 2009, 112(3): 727-732.
[10] KE贾维斯. 著. 尹明, 李冰, 译. 电感耦合等离子体质谱手册[M ]. 北京: 原子能出版社, 1997:113-215.
[11] 刘奋, 戴京晶, 林奕芝, 等. ICPMS测定食品中多种金属元素[J]. 现代预防医学, 2002, 27(1): 43-45.
[12] 陈杭亭, 曹淑琴, 曾宪津. 电感耦合等离子体质谱方法在生物样品分析中的应用[J]. 分析化学评述与进展, 2001, 59(5): 592-600.
[13] 芮玉奎, 余庆泉, 金银花, 等. 应用ICP-MS快速测定葡萄酒中40种元素含量[J]. 光谱学与光谱分析, 2007, 26(5): 1015-1017.
[14]陈兰珍, 芮玉奎, 赵静, 等. 应用ICP-MS测定不同蜂蜜中微量元素和重金属[J]. 光谱学与光谱分析, 2008, 27(6): 403-1405.
[15]严冬, 姚继军. 动态反应池电感耦合等离子体质谱法分析膳食补充剂中的微量金属元素[J]. 岩矿测试, 2010, 28(2):Ⅰ0001- Ⅱ0002.
[16] 彭荣飞, 侯建荣, 黄聪. ICP-MS直接测定酱油中Pb和As的研究[J]. 中国卫生检验杂志, 2008, 18(7): 1315-1316.
[17] 林立, 陈玉红, 田艳玲, 等. 电感耦合等离子体质谱法直接测定酱油中的铅[J].环境化学, 2007, 26(7): 410-412.
[18] 中华人民共和国卫生部. GB 2762—2005 食品中污染物限量[S]. 北京: 中华人民共和国卫生部, 中国国家标准化管理委员会, 2005.
[19] 张建, 田志强, 卢垣宇,等. 电感耦合等离子体质谱法检测白酒中28种元素[J].食品科学, 2013, 34(22): 257-206.
ICP-MS detection of lead in food, arsenic, mercury, cadmium, barium, chromium, silver, nickel 8 harmful elements
ZHANG Jian1,2,TIAN Zhi-qiang*1,2,LU Yuan-yu1,2,SUN Zong-qi1,2,ZHOU Zhu-ping1,2,ZHU Li-bo1,2,LI Li1,2,SHAO Fei-long1,2
(1.China National Center for Alcoholic Beverage and Soft Drink Quality Supervision and Inspection 550004;2.China Institution of Supervision and Inspection Product Quality of Guizhou Province ,Guiyang 550004)
A method for determination of Pb、As、Hg、Cd、Ba、Cr、Se、Ni、Mg、Al in food by ICP-MS was established. The ten elements were detected simultaneously after the samples digested by microwave digestion. The detection limits of these elements range from 5 ng/ L to 200 ng/L, linear correlation r≥0.9993. The precision was RSD <4.3% , and recoveries of samples were of the range 91.44%~100.20%.The results showed close agreement with the reference values in different kinds of food standard materials of GBW 10052(GSW-30)、GBW 10015、GBW 10018, and the results was fne. This method is simple, fast, high sensitivity,which can meet the demand for element analysis in food.
microwave digestion; ICP-MS; food; Pb、As、Hg、Cd、Ba、Cr、Se、Ni、Mg、Al
基金项目:贵州省科学技术厅社会攻关计划项目(黔科学SY[2013]3111;2013GZ47387);2012年度贵州省质监系统科技计划项目(2012ZK005) ;2014年饮料类产品中重金属元素的风险评估研究(国家食品安全风险评估中心、中国食品发酵工业研究院国家重点项目)
TS 26

