腔内修复术治疗破裂性腹主动脉瘤的疗效及技巧探讨
张显岚, 郭建刚
(桂林医学院附属医院 血管乳腺外科, 广西壮族自治区 桂林, 541001)
腔内修复术治疗破裂性腹主动脉瘤的疗效及技巧探讨
张显岚, 郭建刚
(桂林医学院附属医院 血管乳腺外科, 广西壮族自治区 桂林, 541001)
摘要:目的观察腔内修复术(EVAR)治疗破裂性腹主动脉瘤(RAAA)的疗效,并探讨手术经验与技巧。方法2009年1月—2013年12月收治的RAAA患者12例,均于全身麻醉后行EVAR,经一侧股动脉穿刺置管造影,沿肾动脉下方通过输送器植入支架。结果12例患者中,8例(66.67%)植入分叉型人工血管内支架,4例(33.33%)植入直型支架;平均手术时间(170.35±15.34) min,平均出血量和输血量分别为(92.55±8.67) mL和(301.58±16.39) mL。术中无死亡病例,术后2例(16.67%)死亡;主要并发症为心律失常、肺部感染、肾功能损害等,并发症总发生率58.33%; 1例(10.00%)患者于术后26个月出现Ⅰa型内漏,再次行栓塞治疗。结论EVAR是RAAA的有效救治方式,术前血管造影检查对保证手术效果至关重要。
关键词:腔内修复术; 破裂性腹主动脉瘤; 计算机断层扫描血管成像; 血管内支架
腹主动脉瘤(AAA)是临床常见的血管疾病,多见于老年人,随着医疗水平的发展,AAA的治疗效果不断提高[1],但仍有少数患者存在瘤体自然破裂的风险,即发生破裂性腹主动脉瘤(RAAA)。RAAA死亡率可达80%,既往多采用开放手术治疗,但传统术式创伤大,围术期并发症及死亡率较高。近年来,主动脉腔内修复术(EVAR)在临床的应用逐步广泛,其在RAAA的治疗方面显示出微创、并发症发生率低等优势[2-3],成为临床关注的热点。本研究观察了EVAR治疗12例RAAA的临床疗效,并探讨其手术技巧,以期为RAAA的临床治疗提供参考,现报告如下。
1资料与方法
1.1 一般资料
选取2009年1月—2013年12月在桂林医学院附属医院血管乳腺外科治疗的RAAA患者12例为研究对象,所有患者均有腹部疼痛症状,经CT、彩超或主动脉计算机断层扫描血管成像(CTA)等影像学检查确诊。男8例,女4例;年龄65~81岁,平均(69.54±4.26)岁;腹主动脉直径5.00~9.20 cm, 平均(7.21±2.18) cm; 破口直径3.45~8.20 cm, 平均(4.93±2.07) cm; 瘤体最大直径3.50~9.85 cm, 平均(6.85±2.13) cm; 动脉粥样硬化性AAA 10例,腹主动脉假性动脉瘤2例;8例为肾下型, 4例为肾周型;12例患者均合并腹腔积液。
1.2 方法
1.2.1术前准备:12例患者均于术前评估并完善血、尿、粪常规、心电图、凝血功能等常规检查,10例生命体征平稳者行CTA检查确诊,2例失血性休克者经对症治疗,待生命体征平稳后行CTA检查。
1.2.2手术方法[4]:12例均行全身麻醉,经一侧股动脉穿刺置管造影,根据造影中所测的瘤颈长度、直径,瘤体、髂动脉钙化程度,腹腔内重要脏器动脉及髂动脉、股动脉的情况等,与CT等检查结果进行比较分析,选择合适的覆膜支架型号。沿肾动脉下方通过输送器植入支架,植入分叉型支架者,从对侧股动脉植入分支支架,确保其与支架主体紧密连接,并以球囊扩张连接部;植入单臂型支架者,结扎对侧股总动脉后,行股-股动脉人工血管转流。髂总动脉全长瘤样变者,可用弹簧圈预先栓塞患侧髂内动脉;髂动脉扭曲严重者应行超硬导丝拉伸纠正;动脉瘤累及重要脏器动脉时行开窗或“烟囱”技术重建受累内脏动脉[5]。手术完成后再次行CTA检查评估封闭情况,如有内漏应使用球囊进行扩张。最后修复股动脉,常规关闭切口。
1.2.3术后处理:术后严密监测患者生命体征,防止血压过高;给予水化治疗,防止发生造影剂肾病;给予阿司匹林进行抗凝治疗;鼓励患者尽早下床活动,适当给予促进肠蠕动或排便等处理,防止发生腹腔间隔室综合征。术后2周、3个月及1年复查腹主动脉CTA。所有患者均获得随访,末次随访时间2014年12月。
1.3 观察指标
观察患者的手术结果、围术期相关情况、术后并发症的发生及随访结果。
2结果
2.1 手术结果与围术期相关情况
12例患者中,8例(66.67%)植入分叉型人工血管内支架,4例(33.33%)植入直型支架。平均手术时间(170.35±15.34) min, 平均出血量(92.55±8.67) mL, 平均输血量(301.58±16.39) mL。平均总住院时间(14.47±3.92) d, 术后平均进食(6.25±2.38) h, 首次下地时间(22.83±4.06) h。3例术中造影发现Ⅰ型内漏,行球囊扩张后消失。术中无死亡病例,术后2周,1例死于严重肺部感染所致的呼吸衰竭,1例死于心功能衰竭。
2.2 并发症
12例患者中,发生心律失常2例,心力衰竭1例,肺部感染2例,呼吸衰竭1例,肾功能损害1例。并发症总发生率58.33%(7/12)。除2例死亡外,其余经对症处理后均好转。
2.3 随访结果
10例未死亡患者均获得随访,中位随访时间(48.56±7.36)个月。其中1例(10.00%)患者术后26个月出现Ⅰa型内漏,再次行腔内栓塞治疗。
2.4 典型案例
患者,男, 63岁。因“腹痛1月余,突发加重2 d,伴有腰部胀痛”入院,经CT、CTA检查确诊为腹主动脉下段动脉瘤破裂出血,见图1、图2。手术情况:取双侧腹股沟皮纹切口约5 cm,经左侧股总动脉穿刺置入5 F动脉鞘,再经右股动脉穿刺置入动脉鞘备用,经右侧动脉鞘内经交换导丝及眼镜蛇导管配合,将导管置入支架分腿内并手推,造影证实导管在主体支架内,引入超硬导丝退出动脉鞘,置入12×16×54 mm短腿覆膜支架并释放远端覆盖右侧髂内动脉开口,开放主体支架左侧短腿,再次引入12×16×37 mm锥形支架并释放远端位于髂内动脉开口上缘。见图3。
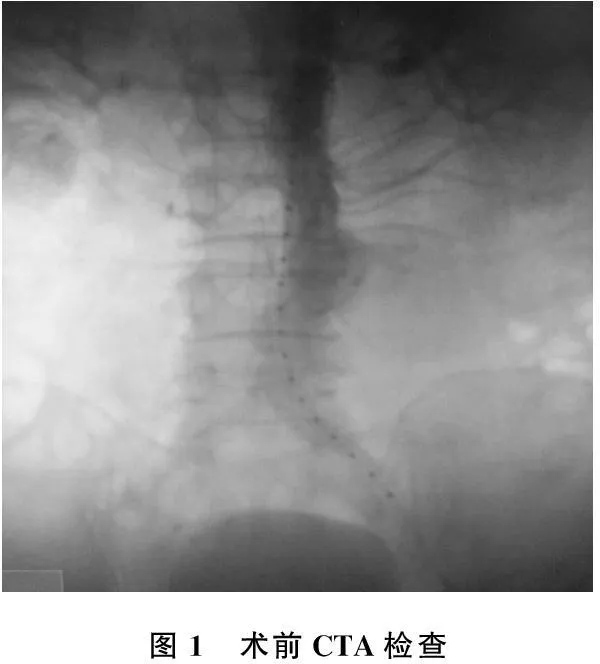
图1 术前CTA检查
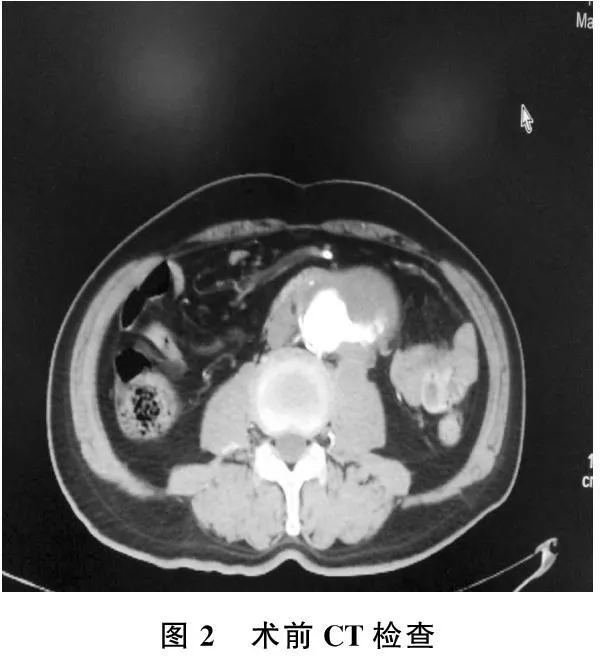
图2 术前CT检查
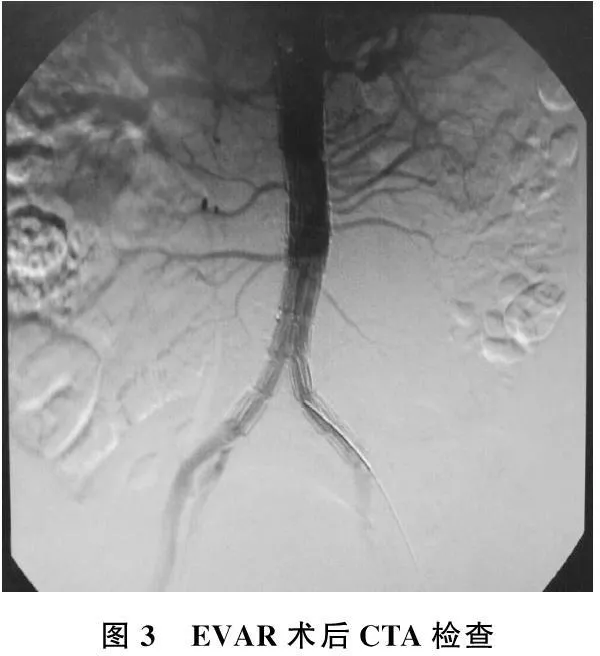
图3 EVAR术后CTA检查
3讨论
AAA是指腹主动脉的直径>正常直径的1.5倍以上,多见于60岁以上的男性患者,其发病与动脉粥样硬化、腹主动脉结构缺陷、高血压等多种因素相关。约1/3未经治疗的AAA有发生破裂的风险,RAAA是临床急重症,死亡率较高。传统开放手术治疗的死亡率约40%,而EVAR经过近20年的发展,其微创性、恢复快等优势得到了充分体现,也越来越多地应用于AAA的治疗[6-7]。一项荟萃分析显示, EVAR治疗RAAA的术后30 d死亡率[OR=0.47, 95%CI(0.39~0.57)]及并发症发生率[OR=0.59, 95%CI(0.43~0.81)]均低于开放手术(P<0.01)[8]。
术前评估及选择合适支架是EVAR的重点与难点,因此术前CTA对手术的顺利实施及手术结果的保证具有重要意义。通过术前CTA, 可以了解瘤体的长度、直径等基本特征、破裂情况及髂动脉、股动脉等是否有扭曲、狭窄、闭塞等情况[9]。本组中有2例出现失血性休克,经合理抢救、充分复苏后可进行CTA检查,这为全面评估患者病情,并选择合适支架提供了重要参考。需要指出的是,若抢救后患者生命体征依然不稳定,应立即行急诊手术,以免错失最佳救治时机。本组12例患者手术即刻成功率为100%,手术时间、出血量及输血量均较传统手术低,提示EVAR是RAAA的有效救治方法,与杨根欢[10]、Stokmans[11]等报道一致。
尽管EVAR创伤小,但仍无法避免相关并发症的发生,其中最常见的并发症是内漏,即有连续的血流进入支架移植物外的瘤腔。术中支架植入后应及时行CTA检查,观察是否有内漏出现[12],如出现Ⅰ型内漏,应使用球囊扩张或加用短袖套支架(Cuff),术后应遵医嘱定期复查,一旦发现内漏应及时进行二次栓塞治疗。本组3例患者于术中发现Ⅰ型内漏,行球囊扩张后消失;1例于术后26个月出现Ⅰa型内漏,再次行腔内栓塞治疗。本组还出现少数心律失常、肺部感染及肾功能损害等并发症,其中2例死亡,死亡率(16.67%)高于徐克等[13]报道的9.5%, 可能与样本数较小有关,同时, 2例死亡患者术前基础疾病均较多,在手术应激状态下极易发生器官衰竭,导致死亡。
通过总结临床案例,作者总结EVAR治疗RAAA的经验与技巧如下: ① 瘤体解剖学条件是RAAA患者能否行EVAR的主要因素,因此术前CTA检查,全面评估病情至关重要,若瘤颈严重钙化、瘤颈成角大,可能增加手术难度; ② 既往有腹部手术史、伴心肺等脏器疾病等患者,预计行开放手术风险较大者,可首先考虑EVAR治疗[14]; ③ 参考国外学者的报道,本组12例患者术中均注意控制血压,可减少术中出血及输血量,及术后凝血功能异常的发生[15]。
参考文献
[1]Mohan P P, Rozenfeld M, Kane R A, et al. Nationwide trends in abdominal aortic aneurysm repair and use of endovascular repair in the emergency setting[J]. J Vas Interv Radiol, 2012, 23(3): 338.
[2]Mehta M, Kreienberg P B, Roddy S P, et al. Ruptured abdominal aortic aneurysm: endovascular program development and results[J].Semin Vasc Surg, 2010, 23(4): 206.
[3]Park B D, Azefor N, Huang CC, et al. Trends in treatment of ruptured abdominal aortic aneurysm: impact of endovascular repair and implications for future care[J]. J Am Coll Surg, 2013, 216(4): 745.
[4]Ritter J C, Stanley B M. The “fenestrated inside fenestrated” stent graft solution for therapy-resistant type Ia endoleak after fenestrated endovascular aortic aneurysm repair[J]. J Vasc Surg, 2014, 59(3): 814.
[5]刘暴, 刘昌伟, 郑月宏, 等. 高危复杂腹主动脉瘤腔内修复术临床分析[J]. 中华外科杂志, 2011, 49(10): 878.
[6]刘杰, 葛阳阳, 贾鑫, 等. 腔内修复术治疗有症状性和无症状性腹主动脉瘤围术期结果比较[J]. 中华外科杂志, 2014, 52(5): 342.
[7]张宏鹏, 郭伟, 刘小平, 等. 高外科风险腹主动脉瘤腔内修复术的近远期结果[J]. 中华外科杂志, 2011, 49(10): 873.
[8]李晓勇, 李敏. 腹主动脉瘤破裂腔内治疗的荟萃分析[J]. 中华普通外科杂志, 2011, 26(11): 910.
[9]舒畅, 王暾. 破裂性腹主动脉瘤的治疗[J]. 国际外科学杂志, 2013, 40(12): 805.
[10]杨根欢, 刘昌伟, 李拥军, 等. 破裂性腹主动脉瘤患者腔内治疗的临床分析[J]. 中华医学杂志, 2014, 94(5): 344.
[11]Stokmans R A,Teijink J A,Cuypem P W,et a1.No differences inperioperative outcome between symptomatic and asymptomatic AAAs after EVAR:an analysis from the ENGAGE Registry[J].Eur J Vasc Endovase Surg, 2012, 43(6): 667.
[12]张宏鹏,郭伟,刘小平, 等. 高外科风险腹主动脉瘤腔内修复术的近远期结果[J]. 中华外科杂志, 2011, 49(10): 873.
[13]徐克, 钟红珊, 吴瑕, 等. 腔内修复术治疗腹主动脉瘤中远期疗效观察与探讨[J]. 中国医学影像技术, 2008, 24(4): 585.
[14]哈尔满·阿吉汗, 热衣汗古丽·买买提, 赛力克·马高维亚, 等. 传统开放手术与腔内修复术治疗腹主动脉瘤71例[J]. 中国现代普通外科进展, 2011, 14(6): 498.
[15]Morrison C A, Carrick M M, Norman M A, et al. Hypotensive resuscitation strategy reduces transfusion requirements and severe postoperative coagulopathy in trauma patients with hemorrhagic shock: preliminary results of a randomized controlled trial[J]. J Trauma, 2011, 70(3): 652.

Study on clinical efficacy and techniques of
endovascular aneurysm repair on ruptured
abdominal aortic aneurysm
ZHANG Xianlan, GUO Jiangang
(DepartmentofVascularBreastSurgery,GuilinMedicalUniversity,Guilin,Guangxi, 541001)
ABSTRACT:ObjectiveTo observe the clinical efficacy of endovascular aneurysm repair (EVAR) in the treatment of ruptured abdominal aortic aneurysm (RAAA) and to explore the surgical experiences and techniques. MethodsA total of 12 RAAA patients admitted from January, 2009 to December, 2013 were selected and given EVAR following general anesthesia. Unilateral femoral artery was punctured to indwell catheters for angiography, and stent was implanted through transporters under renal artery. ResultsOf the 12 patients, 8 cases (66.67%) were implanted with bifid artificial endovascular stents and 4 cases (33.33%) with straight-form stents. The average surgical time was (170.35±15.34) minutes and the average hemorrhagic volume and blood transfusion volume were (92.55±8.67) and (301.58±16.39) mL, respectively. No patient died during operation, but 2 cases (16.67%) died after operation. The main complications included arrhythmia, pulmonary infection and renal functional damage, etc, with rate of 58.33%. One (10.00%) patient had type Ⅰ a endoleak 26 months after operation, so embolization therapy was performed again. ConclusionEVAR is an effective therapy for RAAA, and preoperative angiography is critical in assuring the surgical efficacy in clinic.
KEYWORDS:endovascular aneurysm repair; ruptured abdominal aortic aneurysm; computed tomography angiography; endovascular stent
基金项目:中国高校医学期刊临床专项资金(11520845)
收稿日期:2015-03-01
中图分类号:R 543.1
文献标志码:A
文章编号:1672-2353(2015)09-055-04
DOI:10.7619/jcmp.201509016

