气相色谱法测定止汗搽剂中苯酚和乙醇的含量
段和祥 程奇珍 杨毅生 王晓青
1.江西省药品检验检测研究院,江西省药品与医疗器械质量工程技术研究中心,江西南昌 330029;2.解放军总医院第一附属医院药剂药理科,北京100048
止汗擦剂为医院制剂[1],具有消毒、杀菌作用,处方由5%甲醛、2%苯酚、3.75%乙醇组成的水溶液。它可使皮肤发赤,改善皮下血液循环,有利于药物的渗透与吸收,是临床使用较广的药物,主治手足多汗症。止汗擦剂由苯酚和乙醇等组成,原质量标准对苯酚采用紫外吸收系数法进行控制,未对乙醇含量进行控制,为更好的控制产品的质量,建立专属性好、准确度高的气相色谱法对止汗擦剂中苯酚[2-6]和乙醇[7-12]的含量进行控制,并进行方法学考察。结果表明,所建立的方法简便、快捷,灵敏度高,准确度好。
1 仪器与试药
Agilent 6890N 型气相色谱仪,氢火焰离子化检 测 器(FID),Sartorius BP211D 精 密 电 子 天 平(德国赛多利斯股份公司)。苯酚、乙醇对照品(中国食品药品检定研究院,批号100509-201203、130106-201202);止汗擦剂(某医院,批号130311、131108-1、131108-2、131108-3);N,N-二甲基甲酰胺为色谱纯。
2 方法与结果
2.1 色谱条件
色谱柱HP-5 石英毛细管柱(30mm×0.53mm,5.0μm);程序升温:初始柱温90℃,保持6min,以20℃/min 的速率升至170℃,保持7min。进样口温度220℃,检测器温度250℃,分流比为2 ∶1,氮气流速2mL/min,氢气的流速40mL/min,空气流速400mL/min。
2.2 溶液的制备
供试品溶液:精密量取本品1mL,置50mL 量瓶中,加N,N-二甲基甲酰胺稀释至刻度,摇匀,作为供试品溶液。
对照品溶液:精密称取对照品苯酚0.1986g、乙醇0.3013g,置50mL 量瓶中,加N,N-二甲基甲酰胺溶解并稀释至刻度,摇匀,作为对照品贮备溶液。精密量取对照品贮备溶液各1mL,置同一10 量瓶中,用N,N-二甲基甲酰胺稀释至刻度,摇匀,作为对照品溶液。
阴性样品溶液:按处方比例取甲醛溶液5mL,置100mL 量瓶中,用蒸馏水稀释至刻度,作为空白辅料;再精密量取空白辅料1mL,置50mL 量瓶中,加N,N-二甲基甲酰胺稀释至刻度,作为空白辅料溶液。
2.3 专属性试验
分别吸取“2.2”项下制备的供试品溶液、对照品溶液和阴性样品溶液,按“2.1”项下色谱条件,测定,记录色谱图。结果苯酚和乙醇色谱峰的理论板数均大于5000,分离度均大于2.0,阳性样品溶液对测定无干扰,见图1(A、B、C)。
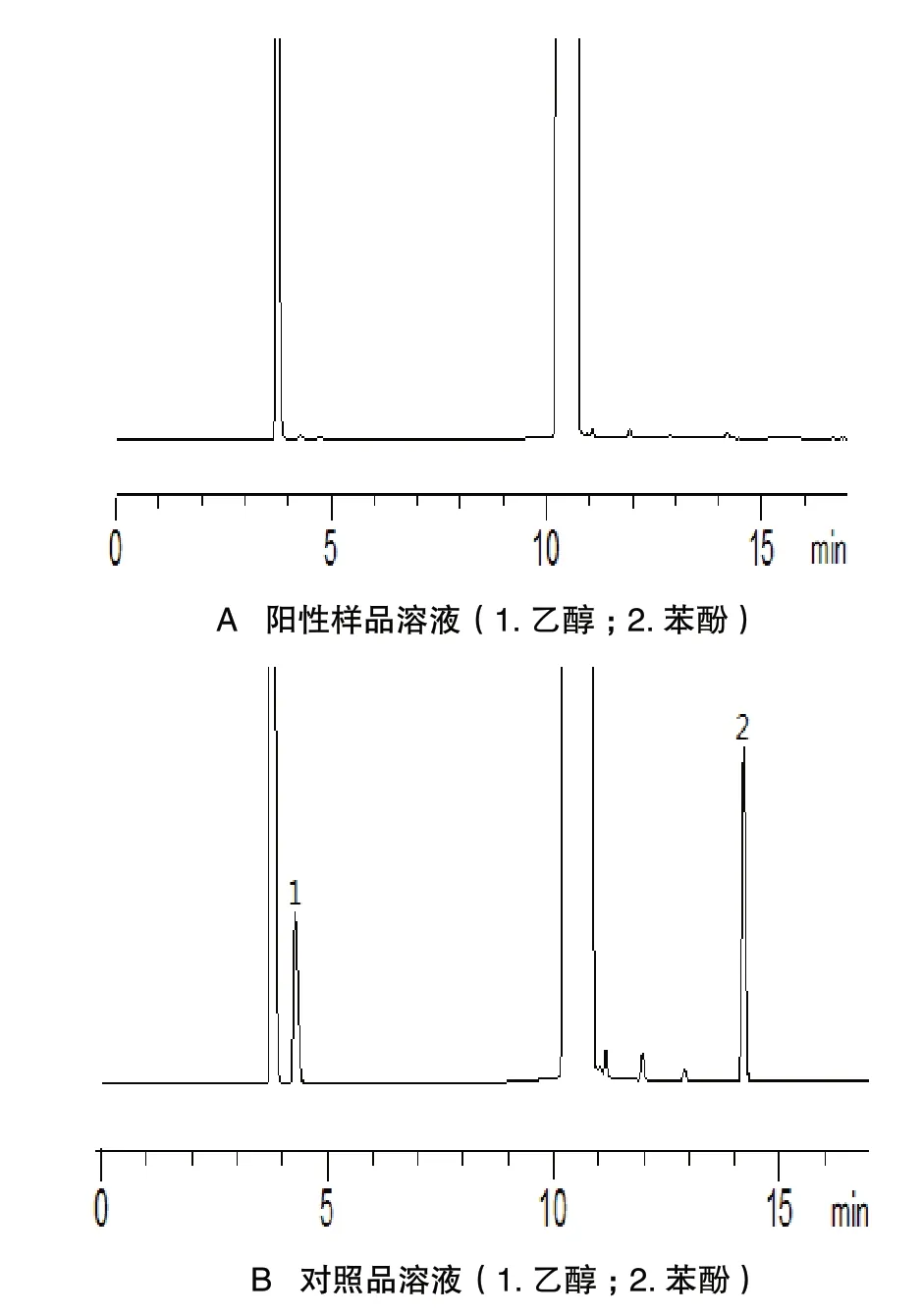
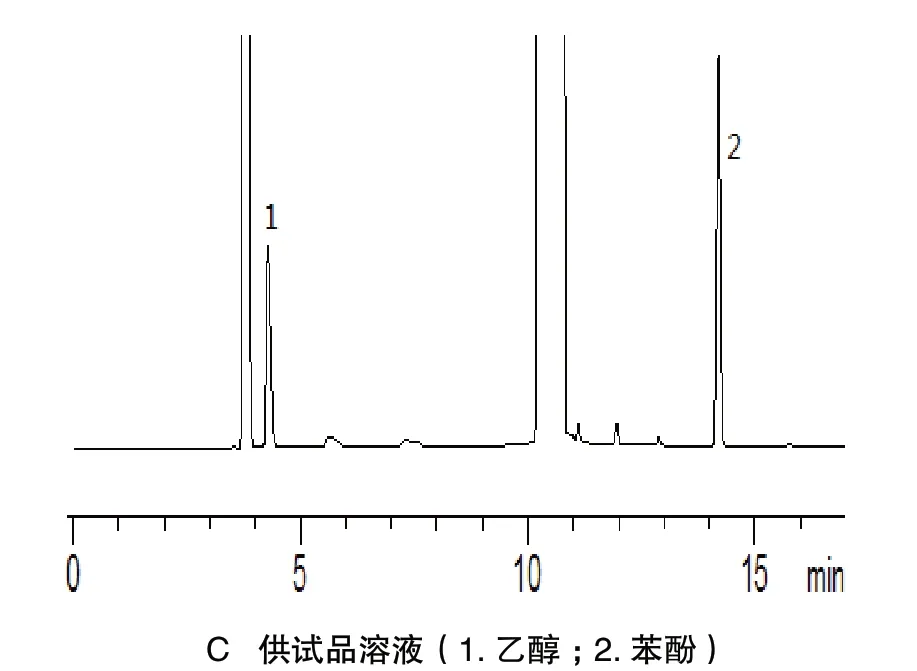
图1 气相色谱图
2.4 线性关系及检出限
精 密 量 取 对 照 品 贮 备 溶 液2.0、1.0、1.0、2.5、2.5、2.5mL,分别5、5、10、50、100、200mL 量瓶中,用N,N-二甲基甲酰胺稀释至刻度,摇匀,作为线性供试液。精密量取上述线性供试液各1μL,按“2.1”项下色谱条件测定,以各自测得的峰面积为纵坐标(A),浓度为横坐标(c)进行线性回归。苯酚、乙醇回归方程分别为:A=5861 c -73.487(0.9998)和A=2561.6 c -9.5617(0.9999)。结果表明苯酚在0.0497 ~1.59mg/mL 浓度范围内线性关系良好;乙醇在0.0753 ~2.41mg/mL 浓度范围内线性关系良好。另取对照品溶液,采用逐步稀释法,按上述色谱条件测定和方法进样分析,检测限以S/N=3 计算。结果苯酚、乙醇的检出限分别为0.32、0.61μg/mL。
2.5 精密度试验
取“2.2”项下对照品溶液6 份,照“2.1”项下色谱条件,分别进样,计算峰面积相对标准偏差(RSD)。结果苯酚、乙醇的RSD 分别为0.63%、0.94%。
2.6 重复性
取止汗擦剂(批号为130311)样品6份,按“2.2”项下方法制备供试品溶液,依法测定,按外标法以峰面积计算含量,结果苯酚和乙醇的RSD 分别为0.71%、1.47%。
2.7 稳定性试验
取“2.2”项下供试品溶液(批号130311),照“2.1”项 下 色 谱 条 件,分 别 于0、6、12、18、24h 进样,计算峰面积的RSD。苯酚、乙醇的RSD 分别为0.54%、0.82%。结果表明供试品溶液在24h 内,稳定性良好。
2.8 回收率试验
精密量取9 份按处方比例配制的空白辅料各1mL,分别置50mL 量瓶中,分别精密加入对照品贮备溶液4.0、5.0、6.0mL,用N,N-二甲基甲酰胺稀释至刻度,摇匀,进行回收率测定。苯酚、乙醇的平均回收率为102.8%(RSD=1.44%)、101.0%(RSD=1.45%)。结果表明方法的准确性良好,见表1。
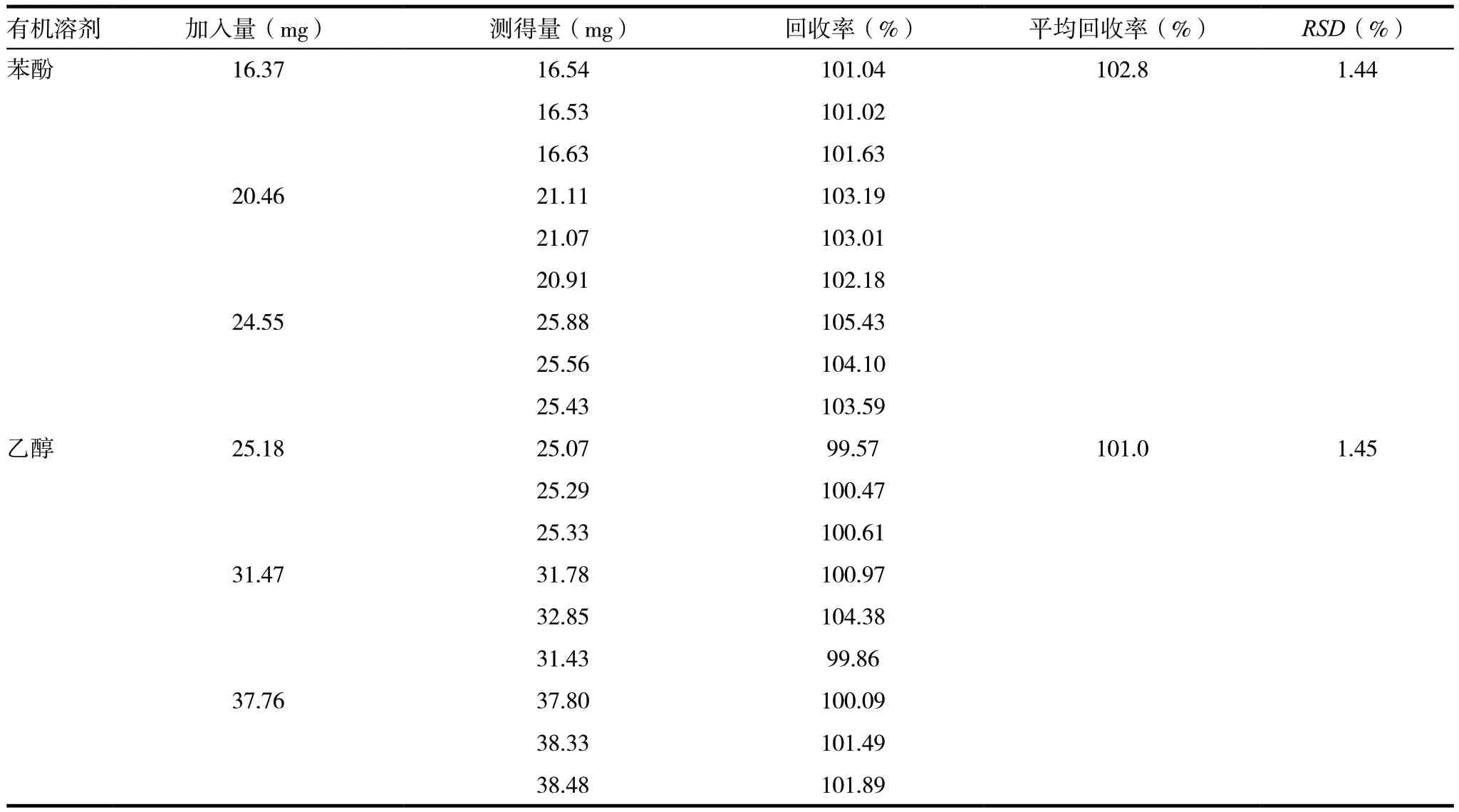
表1 回收率试验结果(n=9)
2.9 样品测定
取对照品溶液及供试品溶液,按上述色谱条件进样,记录色谱图,以外标法按峰面积计算,结果:批号130311、131108-1、131108-2、131108-3 的苯酚含量(g/mL)分别为1.64%、1.80%、1.81%、1.79%;乙醇含量(g/mL)分别为2.82%、3.05%、3.00%、3.00%。
3 讨论
3.1 溶剂的选择
乙醇与水、乙醚、氯仿、酯、烃类衍生物等有机溶剂混溶;苯酚微溶于冷水,可在水中形成白色混浊,易溶于65℃以上的热水,易溶于醇、醚等有机溶剂。N,N-二甲基甲酰胺与水、醇、醚、酮、不饱和烃、芳香烃烃等混溶,溶解能力强。考虑水与气相色谱柱的固定液反应或溶解造成柱流失,降低柱效,不宜用水作为溶剂,而选择N,N-二甲基甲酰胺作为溶剂。
3.2 色谱柱的选择
苯酚与乙醇均为弱极性分子,均含有羟基,当苯酚受到苯环π 键的影响,使氧和碳形成p-π 共轭,使得羟基强度减小,也能够电离,所以也呈酸性,乙醇不电离,所以它的羟基强度最大,而碳氧单键强度最小,故乙醇的极性强于苯酚。根据相似相溶原则-即待测组分与固定液极性匹配原则选择色谱柱:(1)选择DB-5 和HP-5 毛细管柱,从分离度和分离效果来分析,HP-5 的效果较好;(2)同时考察了非极性DB-1、HP-1 毛细管柱;中等极性毛细管柱DB-1701、DB-17;强极性毛细管柱DBWAX、DB-FFAP、HP-INNOWAX 共7 种色谱柱的分离效果,结果均不理想。
3.3 色谱条件的优化
常压下乙醇的沸点78.4℃,苯酚的沸点182℃,两组份的沸点相差较大,在恒温条件下,假如柱温较低,则低沸点组合分离得好,而高沸点组分的流出时间会太长,造成峰展宽,甚至滞留在柱中造成柱污染,反之柱温太高,低沸点组分又难以分离,故采用程序升温条件。
本实验方法简便、快捷,灵敏度高,结果准确。可用于止汗擦剂质量的有效控制。
[1] 中国医院制剂规范(西药制剂第二版)[S].北京:中国医院科技出版社,85-86.
[2] 国家药典委员会编.中华人民共和国药典(二部)[S].2010 年版.北京:中国医药科技出版社,2010:443.
[3] 马延慧,程丽萍,郇瑜,等.气相色谱法测定止痒洗剂中苯酚和薄荷脑的含量[J].中国药物与临床,2014,24(9):1162-1163.
[4] 王玉飞,金米聪,李继革.顶空固相微萃取-气相色谱法测定尿中苯酚[J].中国卫生检验杂志,2011,21(10):2401-2402.
[5] 徐道华,张红伟.气相色谱法测定复方薄荷脑苯酚酊中薄荷脑和苯酚的含量[J].西北药学杂志,2011,26(6):427-429.
[6] 兰文,刘雁鸣,石笑弋.气相色谱法测定樟酚酊中樟脑及苯酚的含量[J].中南药学,2013,11(12):931-934.
[7] 国家药典委员会编.中华人民共和国药典(二部)[S].2010 年版.北京:中国医药科技出版社,2010:10-11.
[8] 施俊辉,史亚军,唐梅,等.气相色谱内标法测定黄芩提取物亚微乳中的乙醇残留[J].中国实验方剂学杂志,2011,17(15):66-68.
[9] 王坤,翟宇,王英华.顶空毛细管气相色谱法测定苦参素中丙酮和乙醇残留量[J].药物分析杂志,2010,30(7):1258-1260.
[10] 赵美艳,徐琛,吕燕平,等.气相色谱法测定聚维酮碘溶液中乙醇和乙酸的残留量[J].中国临床药学杂志,2014,23(2):103-106.
[11] 姜姗,倪健,黄淑惠,等.毛细管柱气相色谱法测定10个厂家养阴清肺糖浆中乙醇的含量[J].中华中医药杂志,2011,26(7):1609-1611.
[12] 孔霁,臧恒昌,王彦厚.气相色谱法测定阿莫西林克拉维酸钾片中的乙醇残留量[J].食品与药品,2014,16(2):120-122.

