RP-HPLC法同时测定通窍鼻炎片中5种成分
张 倩,王世祥,陈勇勇,马晓毅,边六交,岳 俏,郑晓晖
(西北大学 生命科学学院, 陕西 西安 710069)
·生命科学·
RP-HPLC法同时测定通窍鼻炎片中5种成分
张 倩,王世祥,陈勇勇,马晓毅,边六交,岳 俏,郑晓晖
(西北大学 生命科学学院, 陕西 西安 710069)
建立RP-HPLC 法同时测定通窍鼻炎片中花椒毒酚、水合氧化前胡素、白当归素、欧前胡素和异欧前胡素的含量。Agilent TC-C18色谱柱(4.6 mm×250 mm,5 μm),流动相为0.2%甲酸水(A)—乙腈(B),梯度洗脱(0~42 min,22% B;43~72 min,50% B);柱温30℃;进样量50 μL,流速1.0 mL/min;检测波长为 254 nm。花椒毒酚在0.163~5.216 μg/mL (r2=0.999 8),水合氧化前胡素在0.699~22.356 μg/mL (r2=0.999 5),白当归素在0.375~11.988 μg/mL (r2=0.999 8),欧前胡素在1.617~51.744 μg/mL (r2=0. 999 3),异欧前胡素在0.869~27.784 μg/mL (r2=0.999 8)质量浓度范围内与峰面积具有良好的线性关系,平均回收率均大于95%。该方法准确可靠,可行性及重复性良好,可作为通窍鼻炎片的质量控制方法。
通窍鼻炎片;含量测定;RP-HPLC
通窍鼻炎片是由苍耳子、白芷、黄芪等7味中药组成,具有散风固表、宣肺通窍的作用,用于慢性鼻炎、过敏性鼻炎、鼻窦炎等疾病治疗[1]。本处方中白芷含有香豆素、挥发油和糖苷类有效成分[2],部分香豆素类组分及异欧前胡素、欧前胡素、水合氧化前胡素和白当归素等成分具有明显的抗炎、镇痛和解痉挛等作用,其镇痛机制可能与抑制NO的合成或释放有关[3-6]。目前对于通窍鼻炎片的质量控制仅集中于欧前胡素、异欧前胡素、5-O-甲基维斯阿米醇苷等一种或两种成分的含量测定[7-8],对花椒毒酚、水合氧化前胡素、白当归素、欧前胡素和异欧前胡素的同时测定未见报道。本实验采用 RP-HPLC法同时测定通窍鼻炎片中的花椒毒酚、水合氧化前胡素、白当归素、欧前胡素和异欧前胡素的含量,旨在为通窍鼻炎片质量控制提供参考方法。
1 材 料
1.1 仪 器
Agilent 1200 系列高效液相色谱仪(美国安捷伦公司);XS105DU 型电子天平(瑞士梅特勒-托利多公司);KQ 型数控超声波清洗器(昆山市超声仪器有限公司);Maxima 超纯水机(美国基因公司)。
1.2 药品与试剂
通窍鼻炎片(规格为12片/板,3板/盒,每片0.30 g。吉林吉春制药股份有限公司,批号:130503;四平市吉特药业有限公司,批号:20121104;修正药业集团股份有限公司,批号:130501;通化斯威药业股份有限公司,批号:130901;成都地奥集团天府药业股份有限公司,批号:130101);花椒毒酚、水合氧化前胡素、白当归素、欧前胡素、异欧前胡素对照品(成都普菲德生物技术有限公司,批号分别为:121121,130520,121102,120903,121209);色谱乙腈(美国 Fisher公司);其他试剂均为分析纯。
2 方 法
2.1 色谱条件
Agilent TC-C18色谱柱(4.6 mm×250 mm,5 μm),流动相为0.2%甲酸水(A)—乙腈(B),梯度洗脱(0~42 min,22% B;43~73 min,50% B);检测波长为254 nm;体积流量1.0 mL/min;柱温30℃;进样量50 μL。
2.2 对照品溶液的配制
精密称取花椒毒酚3.26 mg、水合氧化前胡素4.14 mg、白当归素1.11 mg、欧前胡素2.94 mg、异欧前胡素1.51 mg分别置于10 mL容量瓶,并以甲醇定容至刻度线,即得花椒毒酚326 μg/mL、水合氧化前胡素414 μg/mL、白当归素111 μg/mL、欧前胡素294 μg/mL和异欧前胡素151 μg/mL对照品溶液。分别精密量取各对照品溶液适量于25 mL容量瓶,并以甲醇定容。即得含花椒毒酚5.216 μg/mL、水合氧化前胡素22.356 μg/mL、白当归素11.988 μg/mL、欧前胡素51.744 μg/mL、异欧前胡素27.784 μg/mL的混合对照品溶液,经0.45 μm微孔滤膜滤过,4℃保存备用。
2.3 供试品溶液的制备
取本品10片,除去糖衣和粉衣,研成细粉,取粉末0.6 g,精密称定,至于50 mL具塞锥形瓶,向瓶中加入70%甲醇20 mL,超声提取20 min。提取液滤过,药渣用70%甲醇洗涤2次,每次2 mL,合并滤液并移至25 mL容量瓶中,并用70%甲醇定容,摇匀,经0.45 μm微孔滤膜滤过,4℃冷藏备用。
2.4 阴性供试品溶液的制备
花椒毒酚、水合氧化前胡素、白当归素、欧前胡素和异欧前胡素来源于白芷,按药典中通窍鼻炎片的生产工艺[1]制备缺白芷的阴性制剂,并按照2.3 项下所述方法制备阴性供试品溶液。
3 结 果
3.1 专属性
在拟定的色谱条件下对供试品溶液进行分析,花椒毒酚、水合氧化前胡素、白当归素、欧前胡素和异欧前胡素与其他组分的色谱峰均可基线分离 (分离度大于1.5),且阴性供试品无干扰。混合对照品、供试品和阴性供试品色谱图见图 1。
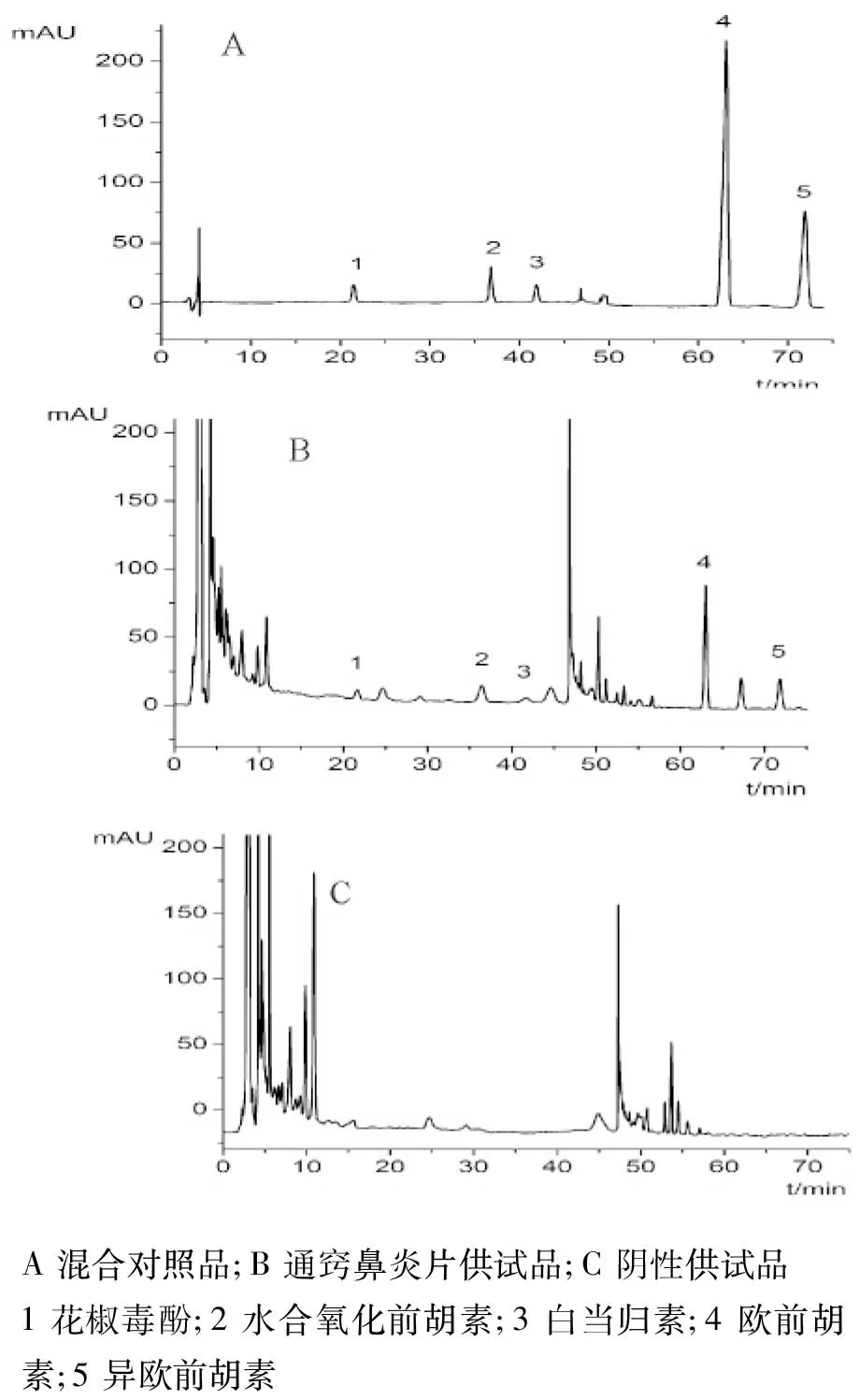
图1 高效液相色谱图Fig.1 HPLC chromatogram
3.2 线性关系考察
精密吸取2.2 项下混合对照品溶液,用甲醇配制成系列浓度的混合对照品溶液在拟定的色谱条件下对上述混合对照品溶液进行分析,以浓度(μg/mL)作为横坐标,相应色谱峰面积作为纵坐标,绘制标准曲线,得花椒毒酚、水合氧化前胡素、白当归素、欧前胡素和异欧前胡素的标准曲线分别为Y=183.42X-4.038 6(r2=0.999 8);Y=120.47X+17.103(r2=0.999 5);Y=70.514X+8.651(r2=0. 999 8);Y=157.65X+131.51(r2=0. 999 3);Y=128.04X+43.092(r2=0. 999 8)。结果表明,花椒毒酚在0.163~5.216μg/mL,水合氧化前胡素在0.699~22.356μg/mL,白当归素在0.375~11.988μg/mL,欧前胡素在1.617~51.744μg/mL,异欧前胡素在0.869 ~27.784μg/mL质量浓度范围内线性关系良好。
3.3 精密度试验
精密吸取混合对照品溶液50μL,连续进样 5 次,花椒毒酚、水合氧化前胡素、白当归素、欧前胡素和异欧前胡素的RSD值分别为2.12%,1.96%,2.38%,2.73%,1.39%,表明仪器精密度良好。
3.4 重复性试验
取通窍鼻炎片粉末(批号:130501)6份,分别依照 2.3 项下所述方法制备供试品溶液,并在拟定的色谱条件下分别进行分析。花椒毒酚、水合氧化前胡素、白当归素、欧前胡素和异欧前胡素峰面积的RSD值分别为2.25%,1.94%,2.37%,2.81%,2.19%,表明供试品重复性良好。
3.5 稳定性试验
精密称取通窍鼻炎片粉末(批号:130501)0.60028g,按照 2.3项下方法制备供试品溶液并在室温下放置0,2,4,6,8,10,12h,在拟定的色谱条件下分别进行测定。花椒毒酚、水合氧化前胡素、白当归素、欧前胡素和异欧前胡素面积的RSD值分别为2.03%,1.92%,2.86%,2.61%,2.25%,表明供试品溶液在12h内稳定性良好。
3.6 加样回收率试验
精密称取通窍鼻炎片粉末(批号:130501)0.3g,平行称取6份,分别加入2.2项下混合对照品溶液3.1mL,按照 2.3项下方法制备供试品溶液,在拟定的色谱条件下进样分析,并计算各组分加样回收率。显示花椒毒酚、水合氧化前胡素、白当归素、欧前胡素和异欧前胡素的平均回收率分别为97.81%±2.18%,96.95%±3.01%,98.47%±3.57%,100.48%±2.56%和97.95%±1.99%,表明该样品处理方法可靠。
3.7 样品的测定
取不同厂家生产的通窍鼻炎片粉末,分别按照2.3项下所述方法制备供试品溶液,在拟定的色谱条件下进样分析,每批样品平行测定3次并记录峰面积,根据标准曲线法计算各待测组分含量,结果见表1。
本实验从各药房购得 5 种不同厂家生产的通窍鼻炎片,并对其中各待测成份的含量进行了测定。结果显示,不同厂家生产的通窍鼻炎片中这 5 种成分含量存在差异(表1)。花椒毒酚、水合氧化前胡素和白当归素均为成都地奥生产的含量最高;欧前胡素和异欧前胡素均为四平吉药生产的含量最高。由于每片通窍鼻炎片所含白芷以欧前胡素含量计,且不得少于60μg[1],因此本实验所测的 5 个厂家和批号的样品均达到标准。
4 讨 论
根据国家和企业的相关标准,通窍鼻炎片的质量控制方法目前仅局限于对欧前胡素的含量测定,这对于复方制剂来说不能够全面的控制其质量。本实验采用RP-HPLC法同时测定通窍鼻炎片中的花椒毒酚、水合氧化前胡素、白当归素、欧前胡素和异欧前胡素的含量,该法不仅简便而且重复性良好,以期为提高和完善通窍鼻炎片的质量标准提供实验依据。

表1 通窍鼻炎片有效成分的测定Tab.1 Determination of components in TongqiaoBiyanTablets
4.1 提取方法的选择
本实验分别采用纯水、50%甲醇、70%甲醇作为提取溶剂,研究了不同提取溶剂对样品中各待测组分溶出的影响,结果显示,以70%甲醇超声提取时,各测定成份的含量最高。为了研究提取时间对药物中各待测组分溶出的影响,实验分别考察了15,20和30 min作为提取时间。结果表明,各组分在20 min与30 min的提取结果基本相同,因此最终选择70%甲醇超声提取20 min作为样品最佳提取方法。
4.2 色谱条件选择
实验过程中,对流动相的不同配比(15~75%乙腈)进行了研究。结果表明,乙腈-0.2%甲酸水溶液作为溶剂系统,以22%乙腈洗脱时,水合氧化前胡素和白当归素的峰形和分离度最好;以50%乙腈洗脱时,欧前胡素和异欧前胡素具有较好的峰形和最佳的分离度。因此,本实验采取上述梯度进行洗脱,以实现在分析周期内各待测成分尽可能达到最佳的分离度。
4.3 含量差异分析
本实验测定了不同厂家生产的通窍鼻炎片中5种成分含量,表1显示该5种成分含量存在差异。这可能与该制剂中的白芷是以生药粉末入药有关。因为各生产厂家用于生产该制剂的白芷生药产地不同,生长地域的温度、湿度、光照等条件也存在着差异,所以生长环境不同的白芷生药粉末中相应成分的含量可能存在差异。而这些生长条件如何影响白芷中相应成分的含量有待于进一步研究。
[1] 国家药典委员会. 中华人民共和国药典(一部)[S]. 北京:化学工业出版社, 2010: 1058.
[2] ZHANG H, GONG C G, LV L, et al. Rapid separation and identification of furocoumarins in Angelica dahurica by high-performance liquid chromatography with diode-array detection, time-of-flight mass spectrometry and quadrupole ion trap mass spectrometry[J]. Rapid Communication in Mass Spectrometry, 2009, 23(14): 2167-2175.
[3] 王梦月,贾敏如,马逾英,等. 白芷中四种线型呋喃香豆素类成分药理作用研究[J]. 天然产物研究与开发, 2010, 22: 485-489.
[4] NIE H, MENG L Z, ZHOU J Y, et al. Imperatorin is responsible for the vasodilatation activity of angelica dahurica var. formosana regulated by nitric oxide in an endothelium-dependent manner[J]. Chinese Journal of Integrative Medicine, 2009, 15(6): 442-447.
[5] SEO W D, KIM J Y, RYU H W, et al. Identification and characterisation of coumarins from the roots of Angelica dahurica and their inhibitory effects against cholinesterase[J]. Journal of Functional Foods, 2013, 5(3): 1421-1431.
[6] LIAO Z G, LIANG X L, ZHU J Y, et al. Correlation between synergistic action of Radix Angelica dahurica extracts on analgesic effects of Corydalis alkaloid and plasma concentration of dl-THP [J]. Journal of Ethnopharmacology, 2010, 129(1): 115-120.
[7] 温莉萍,王秀兰,郜宁. HPLC测定通窍鼻炎胶囊中欧前胡素的含量[J]. 华西药学杂志, 2003, 18(1): 65-66.
[8] 刘基柱,刘丹,龚红全,等. 毛细管电泳法测定通窍鼻炎片中欧前胡素和异欧前胡素的含量[J]. 中药材,2008,31(7): 1081-1082.
(编 辑徐象平)
Simultaneous determination of five components in Tongqiao Biyan Tablets by RP-HPLC
ZHANG Qian, WANG Shi-xiang, CHEN Yong-yong, MA Xiao-yi, BIAN Liu-jiao, YUE Qiao, ZHENG Xiao-hui
(College of Life Sciences, Northwest University, Xi′an 710069, China)
To establish a RP-HPLC method for simultaneously determining xanthotoxol, hydrate oxypeucedanin, byakangelicin, imperatorin and isoimperatorin in Tongqiao Biyan Tablets. The analysis was performed on Agilent TC-C18column (4.6 mm×250 mm, 5 μm), and the mobile phase consisted of acetonitrile-0.2% formic acid with step gradient elution. The flow rate was 1 mL/min and detection wavelengths was set at 254 nm. The samples showed a good relationship in the ranges of 0.163~5.216 μg/mL for xanthotoxol (r2=0.999 8), 0.699~22.356 μg/mL for hydrate oxypeucedanin (r2=0.999 5),0.375~11.988 μg/mL for byakangelicin (r2=0.999 8), 1.617~51.744 μg/mL for imperatorin (r2=0.999 3) and 0.869~27.784 μg/mL for isoimperatorin (r2=0.999 8). All of the average recoveries were more than 95%. The method is accurate, reliable and reproducible and can be used for quality control of Tongqiao Biyan Tablets.
Tongqiao Biyan Tablets; content determination; RP-HPLC
2014-03-11
陕西省自然科学基金资助项目(2010JM4047);西北大学大学生创新基金资助项目(2012099)
张倩,女,陕西西安人,从事中药代谢与分析研究。
王世祥,男,陕西杨凌人,西北大学副教授,从事中药物质基础研究。
R987
:ADOI:10.16152/j.cnki.xdxbzr.2015-02-016

