二氧化钛/碳纳米管复合催化剂的制备及生物法-光催化处理酒精废水研究
朱 军,李雪莲,许冬冬,李晓玲
宿州学院化学化工学院,安徽宿州,234000
二氧化钛/碳纳米管复合催化剂的制备及生物法-光催化处理酒精废水研究
朱 军,李雪莲,许冬冬,李晓玲
宿州学院化学化工学院,安徽宿州,234000
采用溶胶-凝胶法,以钛酸四丁酯为前驱体,通过调节TiO2/CNTs质量百分比(2%、3%、4%),制备二氧化钛/ 碳纳米管(TiO2/CNTs) 复合催化剂;在不同焙烧温度下处理复合催化剂,并利用X射线衍射仪(XRD)、红外光谱(FT-IR)、扫描电子显微镜(SEM)对复合催化剂进行表征。先用生物法处理酒精废水,然后在可见光照射下,考察复合催化剂在不同条件下对酒精废水降解效果的影响。结果表明:在500℃下,TiO2/CNTs质量百分比约3%时,复合催化剂锐钛矿相比例最高;在光照时间为50 min、pH=4、复合催化剂用量0.6 g时,复合催化剂对酒精废水COD降解率最高。
溶胶-凝胶法;二氧化钛/碳纳米管;生物法;光催化;酒精废水
现代生产和生活中酒精的使用十分广泛,推动了酒精工业的快速发展,但酒精生产过程中产生大量高温且含高浓度悬浮物的有机废水对环境带来较大的影响[1-3]。处理该类废水经常使用生物法去除有机物,但厌氧-好氧结合的传统工艺降解成本较高。
光催化氧化技术因催化效率高、价格低廉,在环境治理领域有着广阔的应用前景。在众多光催化剂中,纳米二氧化钛因具有化学性质稳定、易制备[4-6]以及催化活性高、稳定性好、对人体无毒、价格低廉等优点[7],已广泛应用于工业废水处理。但在现有研究中,因纳米二氧化钛颗粒细小,单独使用时回收困难,因此寻找合适的载体是解决回收问题的难点[8-9]。碳纳米管是一种具有稳定化学性能和独特吸附性能的一维纳米材料[10]。碳纳米管作为二氧化钛光催化剂的载体,不仅可以提高负载型催化剂的表面积,还可以提高对有机物的吸附和富集能力[11-12]。
本文采用溶胶-凝胶法,以钛酸四丁酯为制备原料,通过调节TiO2/CNTs不同质量百分比(2%、3%、4%),制备二氧化钛/ 碳纳米管(TiO2/CNTs)复合催化剂,在不同焙烧温度下处理复合催化剂,并利用XRD、FT-IR、SEM对复合催化剂进行表征。经生物法(活性污泥法)处理后,在可见光照射下,考察复合催化剂对酒精废水降解的影响。
1 实验部分
1.1 实验仪器及药品
仪器:DX-2600X射线衍射仪(丹东方圆仪器有限公司);TU-3310型紫外可见分光光度计(日本日立公司);2950纳米粒度仪(英国马尔文仪器有限公司);FTIR-370傅里叶变换红外光谱仪(ThermoNicolet);SU1510扫描电子显微镜(日本日立有限公司)。
药品:钛酸四丁酯(国药集团化学试剂有限公司);无水乙醇(安徽安特生物化学有限公司);>50 nm多壁碳纳米管(中国科学院成都有限公司);纳米TiO2(Aladdin Industrial Corporation);盐酸(上海振企化学试剂有限公司);乙酸(上海展云化工有限公司)。
1.2 实验步骤
1.2.1 TiO2/CNTs复合催化剂的制备
(1)将一定量的碳纳米管置于14 mL钛酸四丁酯、45 mL无水乙醇、3 mL乙酸中得A液并超声分散0.5 h。另取30 mL无水乙醇和15 mL去离子水均匀混合形成B液,将超声分散后的A液边搅拌边逐滴加到B液中,连续滴加2 h;待A液完全滴完后,将混合溶液在室温下陈化40 h即可得到凝胶,将凝胶在空气中、120℃下,干燥24 h后得到干燥凝胶,将其研碎后置于马弗炉内(450℃、500℃、550℃、600℃)下焙烧2 h,制得TiO2/CNTs的质量百分比约3%的复合催化剂[13]。
(2)用同样方法分别制备TiO2/CNTs质量百分比约2%和4%的复合催化剂。
1.2.2 TiO2/CNTs复合催化剂的表征
运用FT-IR、XRD、SEM和纳米粒度仪等对催化剂进行表征,探究上述不同条件下制备的TiO2/CNTs复合材料的微观特征。
1.2.3 采用生物法—光催化处理酒精废水
分别取10 mL酒精废水和240 mL的蒸馏水,置于500 mL烧杯中,向其中加入3.75 g活性污泥,调节废水的pH在6.5左右,水温控制在30℃;并向废水中不断通入空气,经过2 h之后测定处理后的酒精废水COD。
在可见光照射下,通过改变酒精废水的pH、复合催化剂用量和光照时间,探究复合催化剂对酒精废水降解的影响。酒精废水COD作为复合催化剂降解指标。
2 结果与讨论
2.1 不同焙烧温度下TiO2/CNTs复合催化剂表征
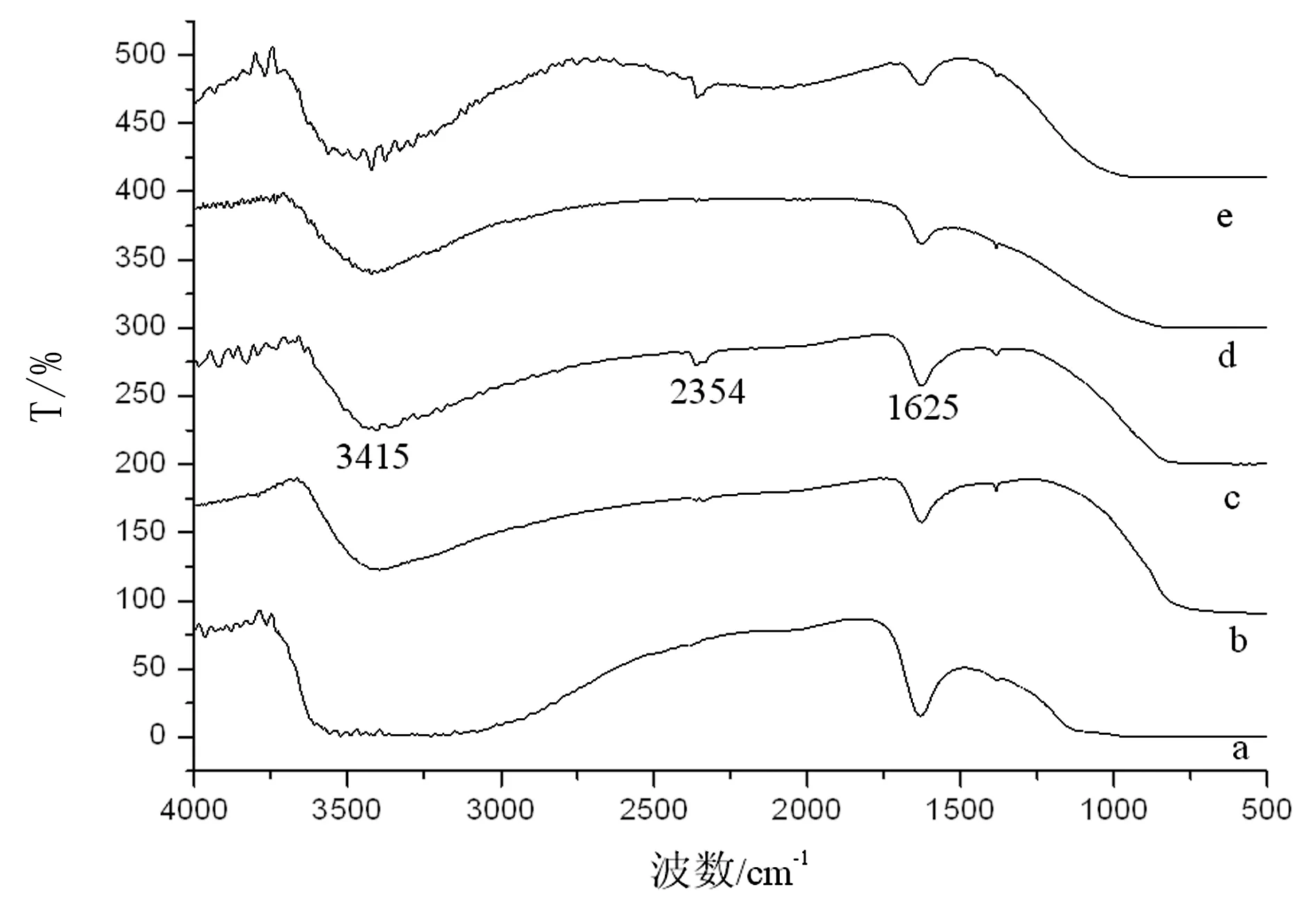
图1 不同焙烧温度处理TiO2/CNTs和TiO2的FT-IR
2.1.1 不同焙烧温度处理复合催化剂的FT-IR
参照红外谱图[10,14],由图1(a)至(e)可知:在3600~3200 cm-1处的宽吸收峰为TiO2表面和自由水-OH基团的伸缩振动引起的,1625 cm-1峰为吸附水的Ti-O的弯曲振动引起的。图3(c)在2354 cm-1处出现的吸收峰是亚甲基的对称伸缩振动吸收峰蓝移的结果。由各图比较看出,随着温度升高,图1(b)至(e)中这两个吸收峰强度在不断减弱,且图1(c)(即煅烧温度为500℃)中的吸收峰强度相对较高。
2.1.2 不同焙烧温度处理TiO2/CNTs复合催化剂的XR
用标准谱图JCPDS(1976)标准(21-1272)、(21-1276)[15-16]与图2相比,位于2θ为25.4°、38.2°、48.2°的衍射峰分别属于锐钛矿相的(101)、(004)、(200)特征晶面,其中2θ为54.3°,62.7°分别是金红石晶型的(220)、(310)的特征晶面。由图2(b)至(e)各图比较可知,图2(b)、(c)中锐钛矿相比例较高,金红石相比例少;图2(d)、(e)中金红石相比例上升。依据锐钛型计算公式可知:锐钛型%=1/(1+1.265IR/IA),计算出图2(c)(即煅烧温度为500℃)中锐钛矿相比例最大。
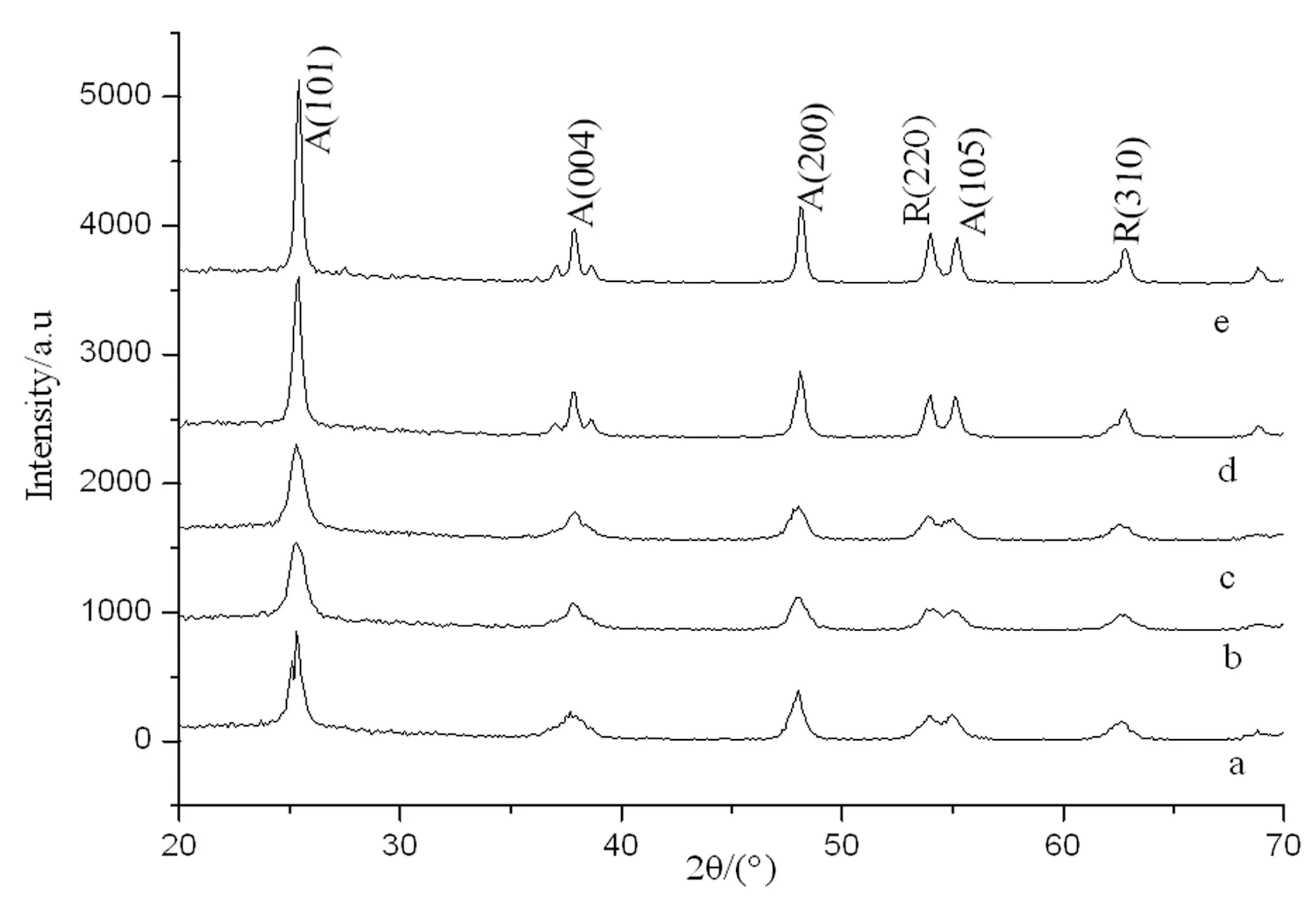
图2 不同焙烧温度TiO2/CNTs和纯TiO2的XRD

图3 不同焙烧温度处理下TiO2/CNTs的SEM
2.1.3 不同焙烧温度处理TiO2/CNTs复合催化剂的SEM
由图3可以看出,TiO2/CNTs复合催化剂都发生了不同程度的团聚,这可能是由于高温焙烧影响了复合催化剂表面电荷的分布而产生团聚。图3中(a)→(d)比较,(b)图的TiO2/CNTs复合催化剂团聚现象不明显,颗粒分布比较均匀,形状较好。
2.1.4 不同焙烧温度处理TiO2/CNTs复合催化剂的颗粒尺寸分析
由图4可观察到,不同焙烧温度处理复合催化剂,对其纳米粒径大小有一定影响。在450℃~600℃条件下,复合催化剂纳米粒径是先变小后变大,且在500℃时,处于最小值。结合前面SEM分析得出:在500℃焙烧的复合催化剂的纳米粒径最小。
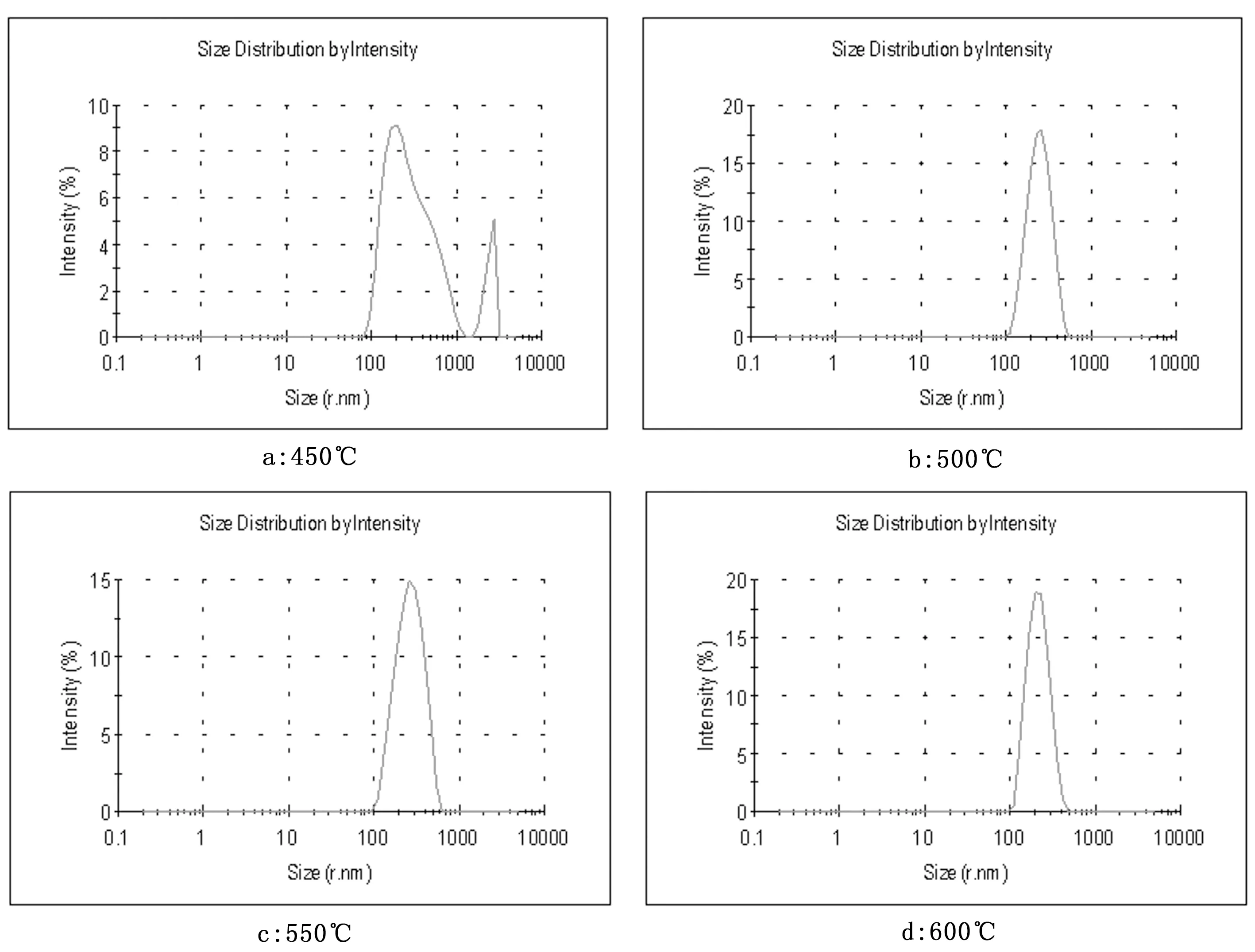
图4 不同焙烧温度处理下复合催化剂的纳米粒径
从以上分析可知,制备复合材料的最适煅烧温度为500℃,因此以下实验中材料煅烧的温度都设为500℃。
2.2 不同加入量碳纳米管的TiO2/CNTs复合催化剂表征
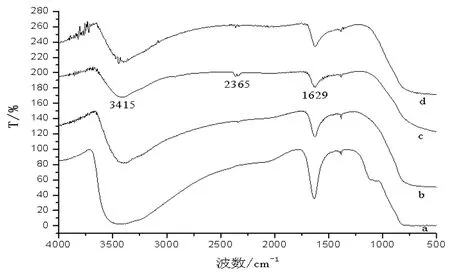
图5 不同加入量碳纳米管的TiO2/CNTs复合催化剂和纯TiO2的FT-IR
2.2.1 不同量碳纳米管的TiO2/CNTs复合催化剂的FT-IR
比较图5各曲线,(b)至(d)随温度的升高-OH基团的伸缩振动吸收峰逐渐变弱,研究表明在提高催化剂表面的羟基的浓度有利于光催化反应[18]。只有曲线(c)在2365cm-1处有比较好的亚甲基对称伸缩振动蓝移的吸收峰,同时曲线(c)在1629cm-1处Ti-O的弯曲振动也有较好的吸收带。
2.2.2 不同加入量碳纳米管的TiO2/CNTs复合催化剂的XRD
根据JCPDS(1976)标准(21-1272)、(21-1276)[16-17]和各种晶型的晶体在整个混合物中所占的比例A%=IA/(IA+IR)[19](A为锐钛矿型,R为金红石型,I为衍射峰的强度)分析,百分比为3%碳纳米管的TiO2/CNTs复合催化剂,锐钛矿相的衍射峰强度比较大,金红石的特征峰较弱(图6)。
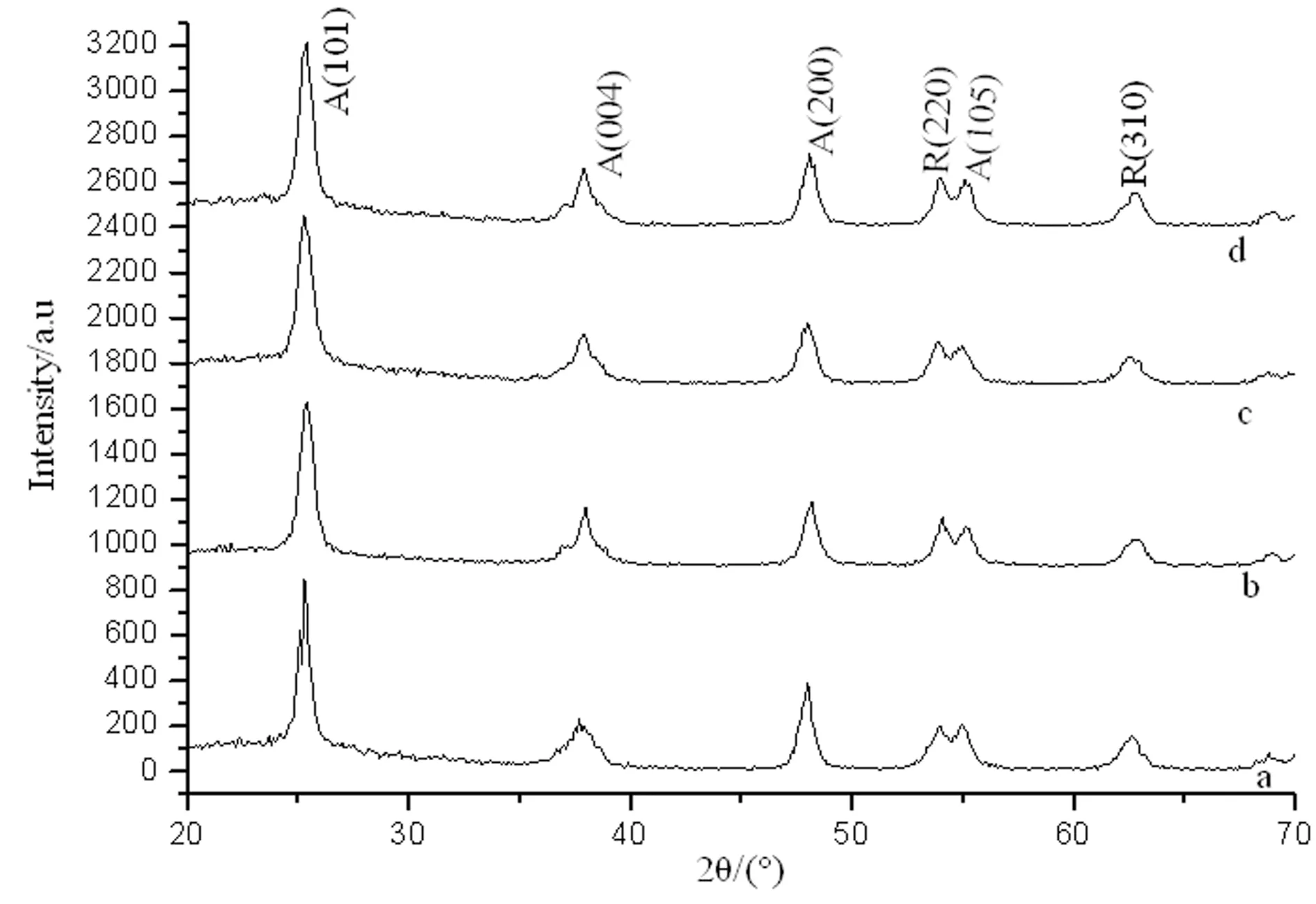
图6 不同加入量碳纳米管的TiO2/CNTs和纯TiO2的XRD
2.2.3 不同加入量碳纳米管的TiO2/CNTs复合催化剂的颗粒尺寸分析
由图7可以看出,碳纳米管与TiO2的加入量不同,对催化剂颗粒大小影响不同。TiO2/CNTs百分含量从2%~4%时复合催化剂的纳米粒径先变小后变大,TiO2/CNTs百分含量为3%时,复合催化剂的纳米粒径最小,推测该粒径范围可能具有较好的催化效率。
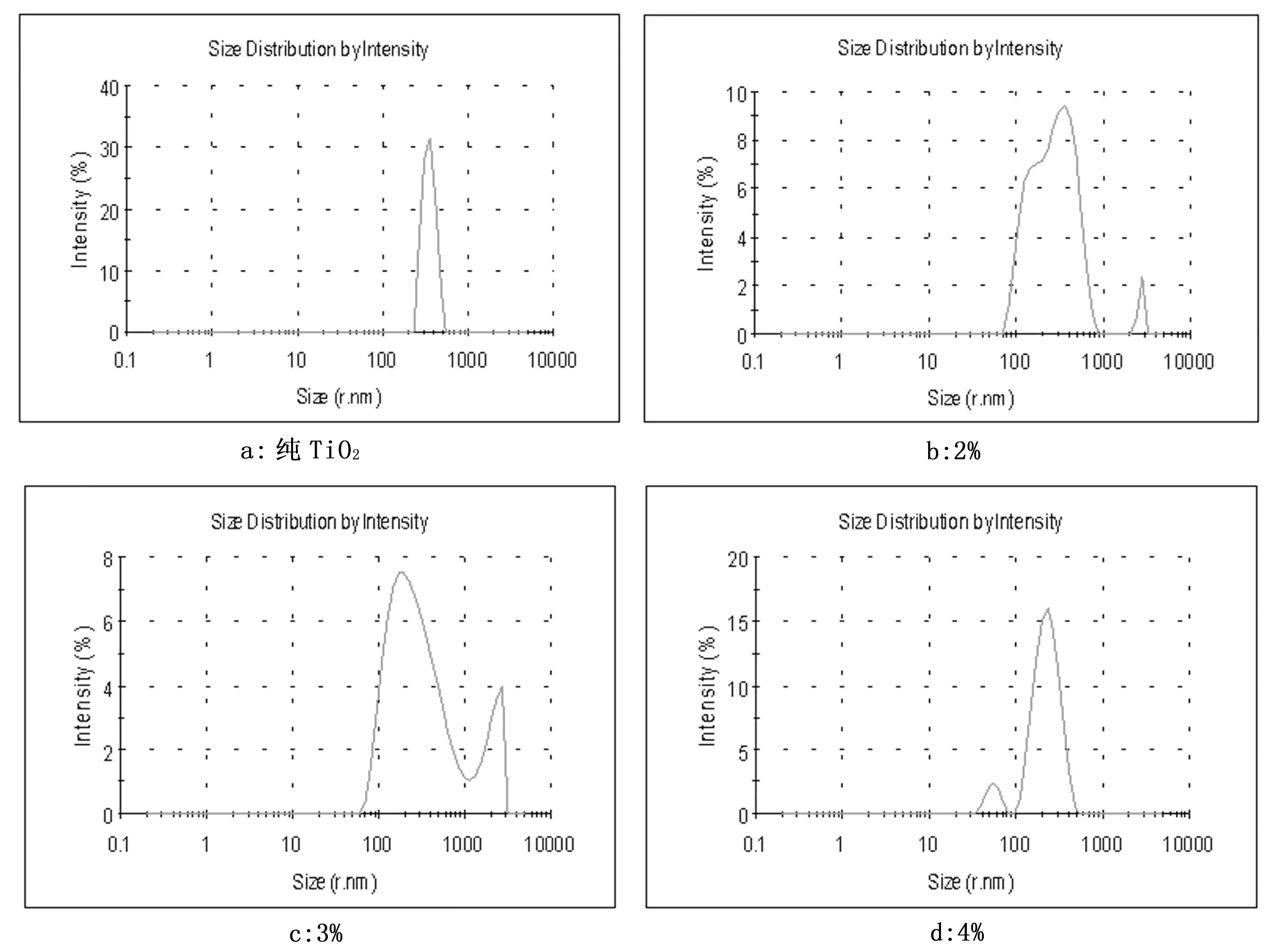
图7 不同加入量碳纳米管的TiO2/CNTs和纯TiO2的纳米粒径
由以上分析可知,复合材料碳纳米管的加入量为3%最适,因此以下实验复合材料碳纳米管的添加量均为3%。
2.3 不同因素对复合催化剂降解酒精废水COD的影响
2.3.1 好氧生物法处理酒精废水实验
由表1可知,通过好氧生物法处理之后的酒精废水COD降至1728 mg/L,经计算,COD降解率达到50.4%。

表1 好氧生物法处理酒精废水的水质分析
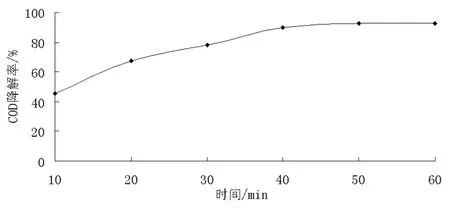
图8 不同光照时间对酒精废水COD降解率的影响
2.3.2 不同光照时间对酒精废水中COD降解率的影响
由图8可以看出,从10~60 min时间段,复合催化剂对酒精废水COD降解率逐渐升高至几乎不变,反应进行50 min时,COD的降解率最高为95.6%。60 min后,复合催化剂对酒精废水的降解率几乎不变。因此,选择50 min作为光照时间。
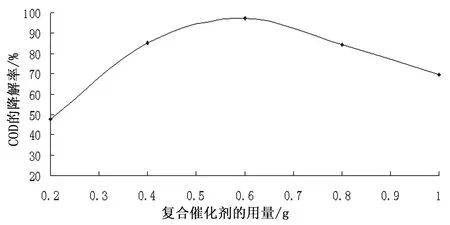
图9 不同复合催化剂用量对酒精废水COD降解率的影响
2.3.3 不同复合催化剂用量对酒精废水COD降解率的影响
由图9可知,当光照时间为50 min,复合催化剂用量在0.2~1 g时,复合催化剂对酒精废水COD降解率是先高后低;添加量为0.2、0.4、0.6、0.8、1.0 g时,对应COD降解率分别为49.5%、89.7%、98.5%、83.4%、72.6%,其中添加量约为0.6 g时,COD降解率最高,达到94.5%。可能的原因是:复合催化剂用量过大时,废水的浊度加大,阻碍可见光照射,从而引起反应体系对光的吸收减少,影响了复合催化剂的光催化效率[19]。
2.3.4 不同pH对酒精废水COD降解率的影响
由图10可知,当光照时间50 min、催化剂用量0.6 g、酒精废水pH在2~11时,复合催化剂对酒精废水COD降解率先高后低。pH在2~4时,复合催化剂对酒精废水COD逐渐升高;在pH=2时;对酒精废水COD降解率是65.6%;pH=4.0时,对酒精废水COD的降解率最高,达到96.4%;pH在4~11时,COD的降解率逐渐下降。可能的原因是:复合材料表面具有双亲性,当pH比较小时,其表面呈正电性,由于部分中间产物呈负电性,它们会占据数目有限的活性中心,使降解率下降;当pH比较大时,其表面呈负电性,与呈负电性的中间产物产生了排斥效果,影响了降解效果[20]。
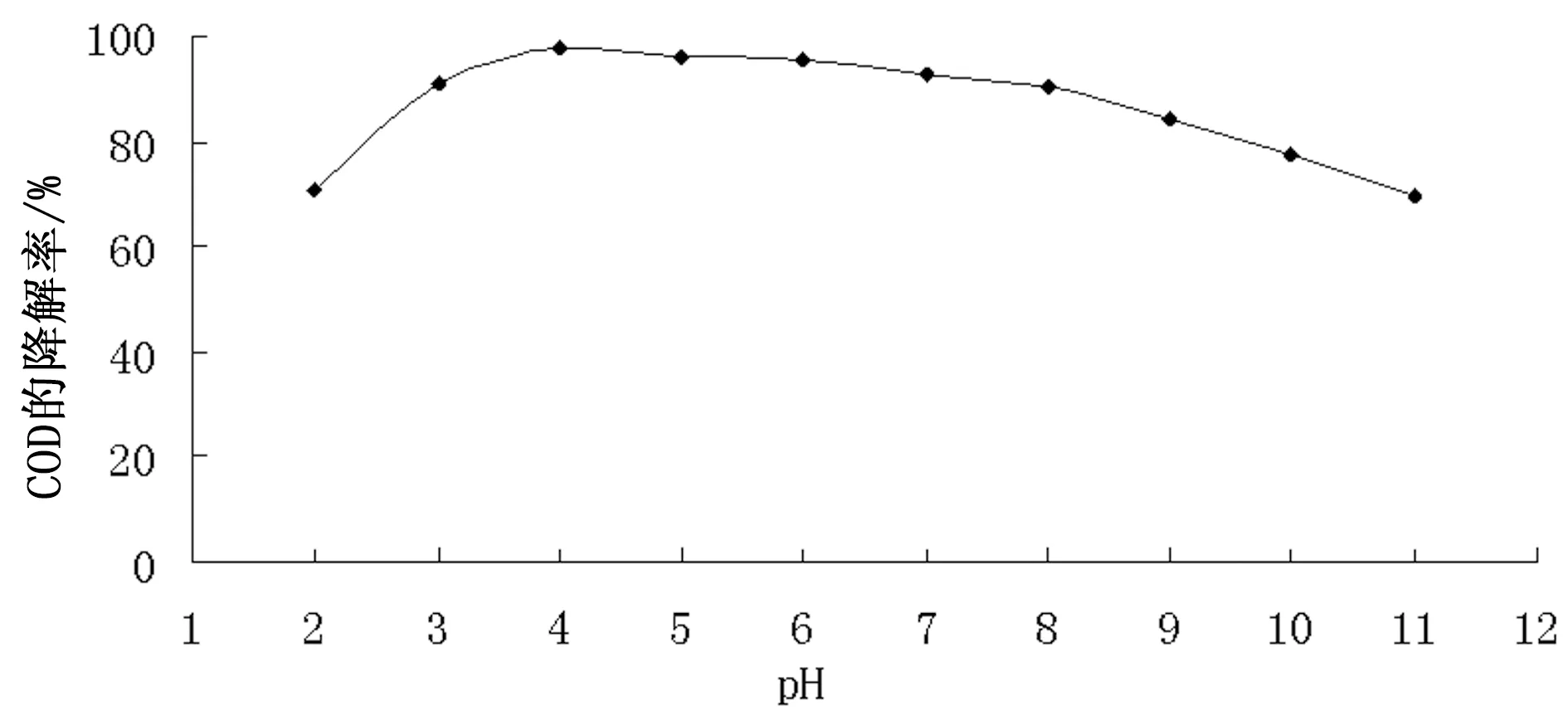
图10 不同pH对酒精废水COD降解率的影响
3 结束语
(1)采用溶胶-凝胶法,以钛酸四丁酯为前驱体,制备TiO2/CNTs复合催化剂,通过调节TiO2/CNTs质量百分比(2%、3%、4%),在不同焙烧温度下处理复合催化剂,并利用XRD、FT-IR、SEM对复合催化剂进行表征,结果表明:在500℃焙烧下,TiO2/CNTs质量百分比约3%的复合催化剂对酒精废水降解率最高。
(2)改变酒精废水的pH、反应时间、复合催化剂用量都会对复合催化剂光催化效率有一定影响。在光照时间50 min,复合催化剂用量0.6g,pH为4.0时,复合催化剂对酒精废水COD降解率最高。
[1]刘广亮,买文宁,赵雅光.酒精废水处理工程实例[J].工业用水与废水,2007,38(1):86-88
[2]寿栋华.酒精生产废水的处理研究[J].广州化工,2008,32(4):50-53
[3]沈连峰,田立江,陈荣平,等.酒精废水的处理和综合利用技术[J].水处理技术,2007(8):68-70
[4]刘洪涛,徐冠华,朱果逸.先进水处理技术研究进展[J].水处理技术,2008,34(4):1-7
[5]Jia Chenzhong,Liu Song.Research progress on TiO2photocatalytic oxidation technology and its application in water treatment[J].Guangzhou Chemical Industry,2012,40(4):5-7
[6]郑怀礼,张峻华,熊文强.纳米TiO2光催化降解有机污染物研究与应用新进展[J].光谱学与光谱分析,2004,24(8):1003-1008
[7]张丙华,李俊玲.纳米TiO2光催化降解技术在污水处理中的应用[J].四川环境,2006,25(5):56-60
[8]张婷婷,解强,姜勇,等.TiO2/AC光催化剂的制备及苯酚光催化降解性能研究[J].水处理技术,2011,37(2):18-22
[9]徐慧娟.光催化剂TiO2的发展与应用[J].廊坊师范学院学报:自然科学版,2009,9(1):77-82
[10]王韶华.改性纳米TiO2光催化剂的制备及其去除水中染料污染物的研究[D].广州:华南理工大学研究生院,2010:1-163
[11]Feng Guizhen. Photocatalytic degradation of methylene blue by the supported TiO2[J].Sichuan Environ,2009,28(1):8-10
[12]张万忠,乔学亮,邱小林,等.纳米二氧化钛的光催化机理及其在有机废水处理中的应用[J].人工晶体学报,2006,35(5):1026-1031
[13]吴俊明,姚俊杰,杨汉培,等.纳米二氧化钛/碳纳米管复合催化剂光催化性能及碳纳米管组分的作用[J].化学学报,2010,68(14):1349-1356
[14]王环颖,李文军,常志东,等.非共价修饰碳纳米管/二氧化钛复合材料的合成及性能[J].无机化学学报,2011,27(2):269-275
[15]彭鹏,柴春霞,李心田.低温水热合成金红石二氧化钛纳米棒[J].周口师范学院学报,2009,26(2):68-70
[16]张延伟,王培卿,张京,等.亚微型锐钛矿二氧化钛空心球的制备与表征[J].宁波大学学报:理工版,2009,22(4):533-538
[17]刘仁龙.纳米TiO2光催化氧化处理苯酚水溶液的研究[D].重庆:重庆大学化学化工学院,2004:1-120
[18]邹俐辉,张泉,曾丽萍,等.二氧化钛/碳纳米管/壳聚糖薄膜的制备及对苯的降解性能[J].环境工程学报,2012,6(1):270-274
[19]刘新育,张东升,张立华,等.TiO2光催化降解林可霉素废水的研究[J].工业水处理,2009,29(3):40-42
[20]赵宝顺,肖新颜,张会平.纳米二氧化钛光催化降解苯酚水溶液[J].精细化工,2005,22(5):339-341
(责任编辑:汪材印)
2015-10-08
安徽省教育厅自然科学研究项目“二氧化钛/碳纳米管/壳聚糖复合材料的制备及应用”(KJ2013Z315);宿州学院校科研平台开放课题“二氧化钛/碳纳米管/壳聚糖复合材料的制备及应用研究”(2012YKF02);宿州学院校平台开放课题“α-Fe2O3纳米功能材料的制备及应用研究”(2012YKF05);宿州学院一般科研项目“头孢类药物及纳米材料与蛋白质相互作用的研究”(2014yyb09)。
朱军(1973-),女,安徽宿州人,硕士,副教授,主要研究方向:环境化学。
TB383.1
:A
:1673-2006(2015)12-0102-05
10.3969/j.issn.1673-2006.2015.12.028

