Me-OMS-1s分子筛催化叔丁基过氧化氢分解制备叔丁醇
冯利利,卢书培,齐兴义,韩晓
(1北京建筑大学城市雨水系统与水环境教育部重点实验室,北京市应对气候变化研究及人才培养基地,北京 100044;2北京航空航天大学化学与环境学院,北京 100191)
Me-OMS-1s分子筛催化叔丁基过氧化氢分解制备叔丁醇
冯利利1,卢书培2,齐兴义2,韩晓1
(1北京建筑大学城市雨水系统与水环境教育部重点实验室,北京市应对气候变化研究及人才培养基地,北京 100044;2北京航空航天大学化学与环境学院,北京 100191)
采用静态水热法合成了Me-OMS-1s(Me=Mg,Co,Ni,Cu)分子筛催化剂,对合成的分子筛进行了X射线衍射和电感耦合等离子体发射光谱表征,并系统考察了反应温度(318~338 K)、反应时间(0.5~6 h)和催化剂用量(1.67~8.33 mg·ml−1)对Me-OMS-1s催化叔丁基过氧化氢分解制备叔丁醇反应性能的影响。研究结果表明,合成的分子筛均为钡镁锰矿型(todorokite)氧化锰;在选择的多相催化反应条件下,Me-OMS-1s均有催化叔丁基过氧化氢歧化分解的反应活性,反应物叔丁基过氧化氢具有较高的转化率,产物叔丁醇的选择性均为100%。Me-OMS-1s催化叔丁基过氧化氢歧化分解的反应活性顺序为:Cu-OMS-1 > Mg-OMS-1 > Ni-OMS-1 > Co-OMS-1。叔丁基过氧化氢的转化率随反应温度的升高、反应时间的延长和Me-OMS-1s用量的增大而显著增大。
合成;Me-OMS-1s分子筛;催化;叔丁基过氧化氢;制备;叔丁醇
引 言
叔丁醇(tert-butyl alcohol,TBA)是一种重要的精细化工产品,可用作内燃机的燃料添加剂、涂料和医药的溶剂、合成药物和香料的原料以及制取高纯度或聚合级异丁烯等[1],也有将其作为化学热泵的报道[2]。目前,叔丁醇的工业生产技术主要有3种[3]:异丁烯硫酸水合法 (间接水合)、异丁烯直接水合法和丙烯/异丁烷共氧化法 (哈康法)。异丁烯硫酸水合法需要消耗大量的硫酸和烧碱,对设备腐蚀严重,须使用高性能材质的设备,成本高,该方法已经逐渐被淘汰。异丁烯直接水合法采用强酸性离子交换树脂作为催化剂,在稍高压力条件下树脂会发生破裂造成催化剂的失活。哈康法由叔丁烷自氧化、丙烯催化环氧化和产物混合物(环氧丙烷 +叔丁醇)纯化分离3步组成,产品收率高,对设备无腐蚀,所需能耗小,生产成本低,是一种很重要的叔丁醇生产方法,但该反应主产品为环氧丙烷,叔丁醇只是副产品。
在哈康法制备叔丁醇的第1步中,叔丁烷自氧化反应产物为叔丁醇和叔丁基过氧化氢(tert-butyl hydroperoxide,TBHP)混合物。若将该产物混合物中的叔丁基过氧化氢在催化反应条件下以可控方式歧化分解成叔丁醇和氧气,则可使叔丁烷自氧化反应直接延伸为简单易行和绿色友好的叔丁醇制备过程,从而缩短哈康法的工艺流程和避免上述工艺缺陷。
根据文献报道,叔丁基过氧化氢歧化分解反应主要是由自由基引发完成[4-5]。由于第4周期过渡金属元素锰有多种价态,具有较好的氧化还原性质,易引发自由基活性中间体的产生,因此,本研究选择含有锰元素且具有孔道结构的OMS-1型锰氧化物为叔丁基过氧化氢多相歧化分解反应的催化剂。OMS-1为Todorokite型多孔状氧化锰(钡镁锰矿),其由3×3个[MnO6] 八面体连接而成并形成孔道结构[6]。因独特的多孔结构和骨架锰离子(Mn4+)可变价性,OMS-1有着广泛的应用,如用作可充电和不可充电电池的电极材料[7-10],作为高选择性的离子交换材料处理废水中的金属离子[11-13],作为选择性氧化反应的催化剂[14-19]等。
本文在合成的系列Me-OMS-1s(Me=Mg,Co,Ni,Cu)分子筛催化剂上考察反应温度、反应时间和催化剂用量等反应参数对叔丁基过氧化氢催化歧化分解反应活性的影响,旨在为实用型制备叔丁醇催化反应体系的设计与开发提供实验基础。
1 实验材料和方法
1.1 Me-OMS-1s分子筛的制备
选用过二硫酸钾 (K2S2O8) 为强氧化剂,一水合硫酸锰(MnSO4·H2O) 为锰源,加入Mg2+作为结构导向剂,在氢氧化钠 (NaOH) 强碱溶液中通过氧化还原反应制备Na-OL-1前驱物;Na-OL-1经过与硝酸镁 (Mg(NO3)2)溶液离子交换,形成Mg-OL-1;Mg-OL-1再经过与含有相应Me2+(Me = Co,Ni,Cu) 的溶液离子交换,形成Me-OL-1;将Me-OL-1在合适的条件下进行水热处理即可得到Me-OMS-1目标产物。实验所用化学试剂均为分析纯。具体制备过程如下。
(1)Na-OL-1的制备 在搅拌下将1.71 g (10.0 mmol) MnSO4·H2O溶于20 ml去离子水中,制备MnSO4·H2O溶液;将30 ml 6 mol·L−1NaOH溶液逐滴加入上述MnSO4·H2O溶液中,制备Mn(OH)2悬浮液;搅拌15 min后,将1.90 g (7.0 mmol) K2S2O8和0.35 g (1.4 mmol) MgSO4·7H2O固体混合物缓慢加入Mn(OH)2悬浮液中,搅拌1 h后,经3次过滤分离和洗涤得到棕褐色掺杂Mg2+的Na-OL-1。
(2)Me-OL-1的制备 取200 ml 1 mol·L−1Mg(NO3)2溶液,用其将湿润的Na-OL-1制成悬浮液,搅拌12 h制得Mg-OL-1;取200 ml 0.5 mol·L−1硝酸盐溶液 (Co(NO3)2,Ni(NO3)2和Cu(NO3)2溶液),用其将湿润的Mg-OL-1制成悬浮液,搅拌12 h进行第1次离子交换;再取200 ml 0.5 mol·L−1同一硝酸盐溶液,用其将经过第1次离子交换后的固体制成悬浮液,搅拌12 h进行第2次离子交换,制得Me-OL-1 (Me = Co,Ni,Cu)。
(3)Me-OMS-1的制备 取15 ml去离子水将湿润的Me-OL-1 (Me = Mg,Co,Ni,Cu) 制成悬浮液,并转移至有聚四氟乙烯内衬的反应釜中进行水热处理,反应温度为160℃,反应时间为24 h,将所得产物进行洗涤、干燥得到Me-OMS-1 (Me = Mg,Co,Ni,Cu)。
1.2 Me-OMS-1s分子筛的XRD和ICP-AES表征
采用日本Rigaku公司D/max 2200PC型自动X射线衍射仪测定合成的Me-OMS-1s试样的XRD谱图,Cu Kα靶,Ni滤光,扫描速率3 (°)·min−1,扫描范围(2θ) 5°~60°。采用美国Varian公司Vista-M PX型电感藕合等离子体发射光谱仪分析Me-OMS-1s试样的元素组成。
1.3 TBHP催化歧化分解反应性能测定
在配有气体计量装置的间歇式玻璃反应器(图1)中常压下考察Me-OMS-1催化TBHP歧化分解反应性能。在反应器中依次加入一定量的催化剂(25~50 μm)和5 ml乙腈(反应介质),用恒温水槽的恒温循环热水将反应体系加热升温至指定反应温度后,加入1 ml 65%(质量分数)的TBHP,随后立刻封闭反应体系,并开始记录反应时间t以及反应时间为t时量气管中的水面在反应前后的高度差,依据该高度差计算出氧气释放体积,并根据实验水温将其转化为标准状态下的体积,即得反应时间为t时TBHP 催化歧化分解释放的氧气体积Vt。在无副反应条件下,记录TBHP完全歧化分解(353 K反应温度下)时氧气释放体积并转化为标准状态下的体积,即得氧气释放总体积V∞,利用Vt/V∞可计算TBHP在t时刻的反应转化率。

图1 自建的间歇式反应装置Fig. 1 Self-built batch reaction device
反应完全后,通过离心分离除去反应母液中的固体催化剂颗粒,对采集的清液用气相色谱法分析其中的TBHP、叔丁醇和其他有机化合物的含量,采用装有25 m长SE-30毛细柱和FID检测器的Varian CP-3800型气相色谱仪。依据TBHP、叔丁醇和其他有机化合物的校正色谱峰面积,采用校正峰面积归一化法计算TBHP的反应转化率和叔丁醇的选择性。经验证,此方法计算的TBHP的反应转化率与Vt/V∞计算的转化率近似相等,本文给出的转化率数据源自色谱峰面积计算而得。
2 实验结果与讨论
2.1 Me-OMS-1s的XRD和ICP-AES表征
合成的Me-OL-1s和Me-OMS-1s样品的XRD谱图如图2所示,由图可见,合成的Me-OL-1s和Me-OMS-1s样品均有较高的物相纯度和结晶度,且在相应位置存在特征峰。二维层状结构的Na-OL-1在2θ为12.40°和25.02°处有两个特征峰,其对应的晶面间距分别为d1=0. 71 nm和d2= 0.36 nm,与JCPDS卡片库中的JCPDS 43-1456完全对应,并且可以判断其属于单斜晶系,空间群为C2/m,晶胞参数a= 0.5174 nm,b=0. 2850 nm,c=0.7336 nm,β= 103.18°,特征峰对应的晶面指数分别为 (001) 和(002)。Mg-OL-1在2θ为 9.24°、18.38°和27.64°处有3个特征峰,对应的晶面间距分别为d1= 0.96 nm、d2= 0.48 nm和d3= 0.32 nm,晶面指数为(100)、(102) 和 (300)。三维孔道结构的Mg-OMS-1的特征峰位置与Mg-OL-1相似,在2θ为 9.56°和18.96°处有两个特征峰,对应的晶面间距分别为d1= 0.96 nm和d2=0. 48nm,晶面指数为 (100) 和(102),相对应的JCPDS卡片序号为38-0475,属于单斜晶系,P2/m空间群,晶胞参数为a= 0.9757 nm,b=0. 2842 nm,c=0. 9560 nm,β= 94.07°。
Na-OL-1与Mg(NO3)2溶液离子交换后,分子层间距由0.71 nm增大至0.96 nm,相对于Na-OL-1的衍射峰,Mg-OL-1的衍射峰向小角度方向偏移。由Bragg方程可知,在波长λ确定情况下,随着分子层间距d的增大,θ变小,即向小角度方向偏移。实验结果与Bragg方程的理论吻合,从而表明锰氧化物的物相发生了转变,即由水钠锰矿 (birnessite,Na-OL-1) 转变为布塞尔矿 (buserite,Me-OL-1) 及钡镁锰矿 (todorokite,Me-OMS-1)。
表1为Me-OMS-1s (Me=Mg,Co,Ni,Cu) 样品的ICP-AES元素分析结果。ICP-AES分析结果表明所有Me-OMS-1试样均含有Na、Mg和Mn 3种元素,Mg-OL-1经过两次离子交换和水热合成得到的Co-OMS-1、Ni-OMS-1和Cu-OMS-1试样分别含有相应的金属阳离子(Co2+、Ni2+和Cu2+)。依据元素组成数据和文献[20]报道的方法计算的Me-OMS-1s的分子式分别为:Na0.04Mg2.00Mn10O20.13·3.52H2O,Na0.02Mg1.21Mn10Co1.82O21.13·2.36H2O,Na0.02Mg1.07Mn10Ni1.45O20.63·3.07H2O,Na0.01Mg0.84Mn10Cu2.26O21.21·2.90H2O。

图2 Me-OL-1s和Me-OMS-1s的XRD 谱图Fig. 2 XRD spectra of Me-OL-1s and Me-OMS-1s

表1 Me-OMS-1s分子筛的ICP-AES元素分析结果Table 1 ICP-AES elemental analysis of Me-OMS-1s molecular sieves/%(mass)
2.2 反应温度对Me-OMS-1s催化TBHP歧化分解反应性能的影响
反应温度对Me-OMS-1s催化TBHP歧化分解反应性能的影响如图3所示。由图3可见,所有Me-OMS-1s均可催化TBHP歧化分解成叔丁醇和氧气,且无任何其他副产物生成,即产物叔丁醇的选择性为100%。比较各反应温度下TBHP的转化率可以看出,TBHP的转化率随反应温度的升高而增大,在338 K下所有Me-OMS-1s催化叔丁基过氧化氢发生歧化分解反应1 h后叔丁基过氧化氢转化率均高于80%。
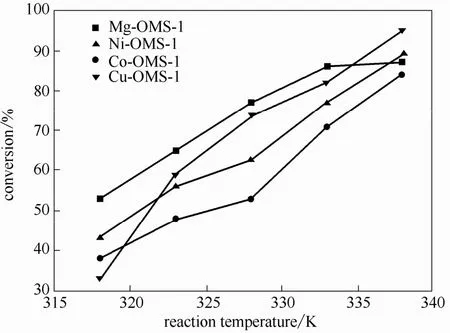
图3 反应温度对Me-OMS-1s催化TBHP歧化分解反应性能的影响Fig. 3 Effect of reaction temperature on disproportionation decomposition of TBHP catalyzed by Me-OMS-1s
2.3 反应时间对Me-OMS-1s催化TBHP歧化分解反应性能的影响
反应时间对Me-OMS-1s催化TBHP歧化分解反应性能的影响如图4所示。由图可见,所有Me-OMS-1s的TBHP转化率均随反应时间的延长而升高。当反应时间为2 h时,Cu-OMS-1催化叔丁基过氧化氢分解反应中,叔丁基过氧化氢转化率已为100%,即TBHP全部歧化分解成叔丁醇和氧气,此时Me-OMS-1 (Me = Mg,Co,Ni) 催化叔丁基过氧化氢分解反应中,叔丁基过氧化氢转化率均在90%以上。

图4 反应时间对Me-OMS-1s催化TBHP歧化分解反应活性的影响Fig. 4 Effect of contact time on disproportionation decomposition of TBHP catalyzed by Me-OMS-1s
2.4 Me-OMS-1s形式浓度对TBHP歧化分解反应性能的影响
催化剂不能改变化学平衡,但是可以加快化学反应的速率,即增加催化剂用量,通常会大幅提高化学反应的速率。Me-OMS-1形式浓度([Me-OMS-1])对TBHP歧化分解反应性能的影响见图5。如图5所示,随着Me-OMS-1形式浓度(催化剂用量)的增加,TBHP转化率也随之增大。Cu-OMS-1具有最高的催化叔丁基过氧化氢发生歧化分解反应的性能,且催化剂形式浓度的变化对催化剂的性能影响不大,在所选用的形式浓度范围内(1.67~8.33 mg·ml-1),Cu-OMS-1催化叔丁基过氧化氢发生歧化分解反应中,叔丁基过氧化氢转化率均高于90%。对其他Me-OMS-1 (Me = Mg,Co,Ni)试样,催化剂形式浓度的变化对叔丁基过氧化氢的转化率有较显著的影响,但当选用最高形式浓度(8.33 mg·ml-1) 时,叔丁基过氧化氢转化率均在80%以上。
2.5 Me-OMS-1s的催化反应活性寿命
对Me-OMS-1催化叔丁基过氧化氢歧化分解反应活性寿命进行考察。第1轮称取70 mg Me-OMS-1样品用于催化叔丁基过氧化氢歧化分解反应,实验结束后,将反应所得混合物离心分离,分别得到Me-OMS-1和上层清液。利用气相色谱对上层清液进行定性和定量分析,确定出反应产物中叔丁基过氧化氢和叔丁醇的质量分数,从而计算出叔丁基过氧化氢的转化率。再将离心所得的Me-OMS-1用乙腈洗涤3次,在空气中自然干燥后,用于下一轮催化反应活性寿命实验。在之后的催化活性寿命实验中 (第2~6轮实验),所用的催化剂Me-OMS-1依次来自于上一轮寿命实验离心所得,实验结果如表2所示。重复6轮的活性寿命实验显示Cu-OMS-1的活性基本不变,Mg-OMS-1、Co-OMS-1和Ni-OMS-1的活性则有不同程度的下降。此外,反应母液的ICP-AES分析未检测出相关金属离子,即在反应过程中,无金属离子流失现象。

图5 Me-OMS-1s形式浓度 ([Me-OMS-1]) 对TBHP歧化分解反应性能的影响Fig. 5 Effect of [Me-OMS-1] on disproportionation decomposition of TBHP catalyzed by Me-OMS-1
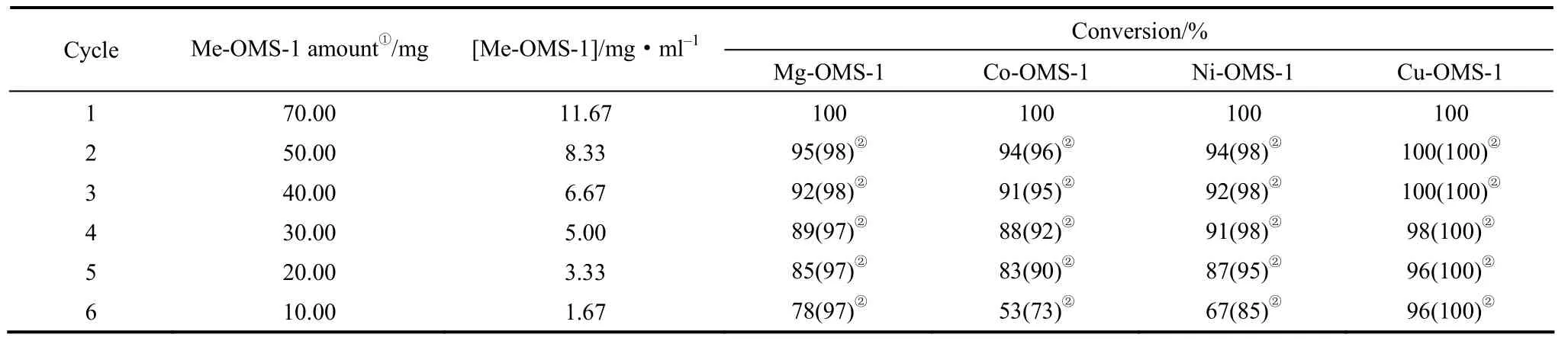
表2 Me-OMS-1s催化反应活性寿命数据Table 2 Catalytic reactivity life data of Me-OMS-1s
3 结 论
(1)合成的Me-OMS-1s样品均为钡镁锰矿型(todorokite)氧化锰。
(2)在温和反应条件下 (318 ~338 K),Me-OMS-1s均有催化叔丁基过氧化氢歧化分解的反应活性,其活性高低顺序为:Cu-OMS-1 >Mg-OMS-1 > Ni-OMS-1 > Co-OMS-1。
(3)在选择的多相催化反应条件下,Me-OMS-1s催化叔丁基过氧化氢歧化分解反应中叔丁醇的选择性均为100%。
(4)叔丁基过氧化氢的转化率随反应温度的升高、反应时间的延长和Me-OMS-1s用量的增大而增大。
[1] Qi L, Qi X Y, Wang L L, Feng L L, Lu S P. Decomposition oftert-butyl hydroperoxide intotert-butyl alcohol and O2catalyzed by birnessite-type manganese oxides: kinetics and activity [J].Catalysis Communication, 2014, 49(4): 6-9.
[2] Zhao Guosheng (赵国胜), Yang Bolun (杨伯伦). Dehydration oftert-butyl alcohol in reactive distillation on adapted to chemical heat pump [J].Journal of Chemical Industry and Engineering(China) (化工学报), 2004, 55(3): 384-389.
[3] Cui Yunzi (崔云梓), Fu Jing (付静), Wang Xizheng (王喜正). Production technology oftert-butyl alcohol and its application market [J].Qilu Petrochemical Technology(齐鲁石油化工), 2004, 32(4): 294-297.
[4] Hiatt R R, Mill T, Mayo F R. Homolytic decompositions of hydroperoxides(Ⅰ): Summary and implications for autoxidation [J].Journal of Organic Chemistry, 1968, 33(4): 1416-1420.
[5] Turrà N, Neuenschwander U, Baiker A, Peeters J, Hermans I. Mechanism of the catalytic deperoxidation oftert-butyl hydroperoxide with cobalt(Ⅱ) acetylacetonate [J].Chemistry-A European Journal, 2010, 16(44): 13226-13235.
[6] De Guzman R N, Shen Y F, Shaw B R, Suib S L, OʼYoung C L. Role of cyclic voltammetry in characterizing solids: natural and synthetic manganese oxide octahedral molecular sieves [J].Chemistry of Materials, 1993, 5(10): 1395-1400.
[7] Ghodbane O, Pascal J L, Favier F. Microstructural effects on charge-storage properties in MnO2-based electrochemical supercapacitors [J].ACS Applied Materials and Interfaces, 2009, 1(5): 1130-1139.
[8] Cui X L, Liu G D, Lin Y H. Amperometric biosensors based on carbon paste electrodes modified with nanostructured mixed-valence manganese oxides and glucose oxidase [J].Nanomedicine -Nanotechnology, 2005, 1(2): 130-135.
[9] Sun Z J, Chen H Y, Shu D, He C, Tang S Q, Zhang J. Supercapacitive behavior and high cycle stability of todorokite-type manganese oxide with large tunnels [J].Journal of Power Sources, 2012, 203(1): 233-242.
[10] Li Shengjuan (李生娟), Wang Shulin (王树林), Xu Bo (徐波). Preparation and properties of activated carbon nano-particles/ Zn-MnOxcomposite electrode material [J].CIESCJournal(化工学报), 2010, 61(1): 223-227.
[11] Dyer A, Pillinger M, Newton J, Harjula R, Möller T, Amin S. Sorption behavior of radionuclides on crystalline synthetic tunnel manganese oxides [J].Chemistry of Materials, 2000, 12(12): 3798-3804.
[12] Laatikainen K, Pakarinen J, Laatikainen M, Koivula R, Harjula R, Paatero E. Preparation of silica-supported nanoporous manganese oxides [J].Separation and Purification Technology, 2010, 75(3): 377-384.
[13] Peng Changjun (彭昌军), Jiang Xiuli (姜秀丽), Ji Hongfang (计红芳), Wang Yuanpeng (王远鹏), Ouyang Tong (欧阳通), Li Qingbiao (李清彪). Adsorption behavior of Fe-Mn binary oxide towards As(Ⅲ) and As(Ⅴ) and its application in biogas slurry [J].CIESCJournal(化工学报), 2014, 65(5): 1848-1855.
[14] Brock S L, Duan N G, Tian Z R, Giraldo O, Zhou H, Suib S L. A review of porous manganese oxide materials [J].Chemistry of Materials, 1998, 10(10): 2619-2628.
[15] Miyake T, Koike K, Aoki I, Murayama N, Sano M. Synthesis of Al-containing octahedral molecular sieves and oxidation of cyclohexane with them [J].Applied Catalysis A:General, 2005, 288(1/2): 216-219.
[16] Katranas T K, Godelitsas A C, Vlessidis A G, Evmiridis N P. Propane reactions over natural todorokite [J].Microporous Mesoporous Materials, 2004, 69(3): 165-172.
[17] Fuertes A, Costa-Serra J F Da, Chica A. New catalysts based on Ni-birnessite and Ni-todorokite for the efficient production of hydrogen by bioethanol steam reforming [J].Energy Procedia, 2012, 29: 181-191 .
[18] Chen T, Dou H Y, Li X L, Tang X F, Li J H, Hao J M. Tunnel structure effect of manganese oxides in complete oxidation of formaldehyde [J].Microporous Mesoporous Materials, 2009, 122(1/2/3): 270-274.
[19] Zhang Q, Cheng X D, Zheng C, Feng X H, Qiu G H, Tan W F, Liu F. Roles of manganese oxides in degradation of phenol under UV-Vis irradiation: adsorption, oxidation, and photocatalysis [J].Journal of Environmental Sciences, 2011, 23(11): 1904-1910.
[20] Ma Y, Luo J, Suib S L. Syntheses of birnessites using alcohols as reducing reagents: effects of synthesis parameters on the formation of birnessites [J].Chemistry of Materials, 1999, 11(8): 1972-1979.
Catalytic decomposition oftert-butyl hydroperoxide intotert-butyl alcohol over Me-OMS-1s molecular sieves
FENG Lili1, LU Shupei2, QI Xingyi2, HAN Xiao1
(1Key Laboratory of Urban Stormwater System and Water Environment of Ministry of Education,Beijing Climate Change Response Research and Education Center,Beijing University of Civil Engineering and Architecture,Beijing100044,China;2School of Chemistry and Environment,Beihang University,Beijing100191,China)
A series of Me-OMS-1s (Me=Mg, Co, Ni, Cu) molecular sieves was synthesized by the static hydrothermal method. The as-synthesized Me-OMS-1s were characterized by means of XRD and AES-ICP. The effects of reaction temperature (318—338 K), reaction time (0.5—6 h) and formal catalyst concentration (1.67—8.33 mg·ml−1) were investigated in detail on catalytic decomposition oftert-butyl hydroperoxide intotert-butyl alcohol over the as-synthesized Me-OMS-1s. The results showed that the synthetic Me-OMS-1s belonged to todorokite-type manganese oxides. All the Me-OMS-1 catalysts bore the activity for the catalytic disproportionation decomposition oftert-butyl hydroperoxide under the selected heterogeneous catalytic reaction conditions. The conversion of the reactanttert-butyl hydroperoxide under various reaction conditions was found to be high and the selectivity towards the producttert-butyl alcohol was 100%. The activity of Me-OMS-1s followed the order of: Cu-OMS-1 > Mg-OMS-1 > Ni-OMS-1 > Co-OMS-1. The conversion level oftert-butyl hydroperoxide was markedly enhanced with increasing reaction temperature, contact time and formal Me-OMS-1concentration.
synthesis; Me-OMS-1s molecular sieves; catalysis;tert-butyl hydroperoxide; preparation;tert-butyl alcohol
QI Xingyi, sharpfl@buaa.edu.cn
10.11949/j.issn.0438-1157.20150053
TQ 426.94; TQ 223.1
:A
:0438—1157(2015)10—3965—06
2015-01-13收到初稿,2015-06-24收到修改稿。
联系人:齐兴义。
:冯利利(1980—),女,博士,副教授。
国家自然科学基金项目(51206009);北京市青年英才项目(YETP1663)。
Received date: 2015-01-13.
Foundation item: supported by the National Natural Science Foundation of China (51206009) and the Beijing Higher Education Young Elite Teacher Project (YETP1663).