扶正抗毒丸稳定性研究
陆宇惠+刘因华+马克坚+俞永琼+赵景云+郭世民
摘要:目的 探讨扶正抗毒丸质量稳定规律。方法 按稳定性方法对其质量标准进行跟踪考察。结果 经3年的稳定性实验证明扶正抗毒丸质量稳定各项指标均符合扶正抗毒丸标准。结论 在现行的包装材料、工艺、质量标准下,经3年考察扶正抗毒丸质量稳定。
关键词:扶正抗毒丸;质量追踪;薄层鉴别
中图分类号:R284 文献标志码:A 文章编号:1007-2349(2014)12-0061-03
扶正抗毒丸系云南省中医中药研究所附属医院研制,2009年获得省食品药品监督管理局批准医疗机构制剂生产批件,批准文号为:滇药制字(Z)20090003A,该制剂为云南省中医药治疗艾滋病试点项目的用药。因使用广泛,我们对其质量进行3年的考察,结果报道如下。
1 扶正抗毒丸的一般情况
处方:10味药(药味略)。制法:以上10味,人参粉碎成细粉备用。其余黄芪等九味用乙醇加热回流提取2次,每次2 h,滤过,滤液回收乙醇,并浓缩至相对密度为1.4~1.5(50℃)的稠膏,80℃以下干燥为干浸膏;药渣加水煎煮2次,每次1 h,滤过,滤液浓缩至相对密度为1.4~1.5(50℃)的稠膏,80℃以下干燥为干浸膏,与上述干浸膏和人参细粉混合,制丸成1000 g,即得。性状:本品为黄棕色至黑色的小丸;气微,味苦。功能主治:益气养阴,滋肾健脾,清热解毒。用于治疗HIV感染潜伏期,证属气阴两虚,脾肾不足,邪毒内蕴者。
2 研究方法及结果:
2.1 试验供试品 扶正抗毒丸(浓缩丸),规格:每袋装3 g;剂型:浓缩丸;批号:20091201、20100401、20110101;批产量:大规模生产,每批成品量:3000kg(400件);生产者:云南省中医中药研究院附属医院制剂室;生产日期2009年12月20日;2010年4月26日;2011年1月29日;试验开始时间:2009年12月22日;2010年4月28日;2011年2月1日。结束试验时间:2012年12月22日;2013年4月28日;2014年2月1日。
2.2 稳定性试验的条件 加速试验:将待考察3批供试品在温度(40±2)℃,相对湿度(75±5)%条件下放置6个月。
长期稳定性试验:将待考察3批供试品在室内常温阴凉条件放置36个月。内包装:为密封银白色长方形铝塑袋。
2.3 质量检测方法、指标限度要求 质量检测方法,按《中国药典》2010年版一部丸剂项下进行;指标限度要求为:性状:为棕绿色至黑色的浓缩丸;气微,味苦、微甜。鉴别:照薄层色谱法(《中国药典》一部附录Ⅵ B)及扶正抗毒丸质量标准,符合要求。水分:<9%。溶散时限:<120 min。重量差异:重差范围为±6%。微生物限度:细菌数<10000个,霉菌数<100个,大肠菌群<100个,大肠埃希菌<0个,活满<0个。
主要检测设备:(1)分析天平 Sartorius BT 224S 美国赛多力斯;(2)三用紫外分析仪 ZF-I型 上海顾村电光仪器厂;(3)电热恒温水浴锅 DZKW-9-4 北京永光明医疗仪器厂;(4)超净工作台 SCB-1360北京东联哈尔仪器制造有限公司;(5)药品稳定性试验箱 LHH-250SDP上海蓝豹。
2.4 考察方法 加速试验:将待考察的每批扶正抗毒丸全检量的四倍量取样,以外包装即20袋/盒,每批12合,在温度(40±2)℃,相对湿度(75±5)%条件下,以最大面积暴露于环境中的方式堆码在药品稳定性试验箱中,放置6个月,定期检测各考察项目。分别于0、1、2、3、6月取样,进行检测。长期稳定性试验:将待考察的3批扶正抗毒丸全检量的十倍量,以外包装即20袋/盒,每批30合分批号堆码放置,在室内常温阴凉条件下放置36个月,定期检测各考察项目。分别于0、3、6、9、12、18、24、36月取样,进行检测[1-3]。
3 考察结果
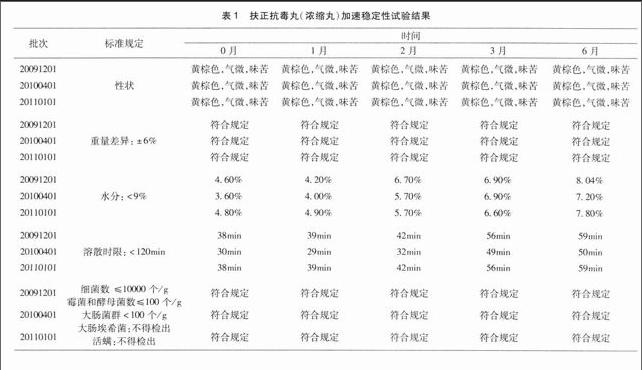
3.1 加速实验结果 性状:1、2、3、6月与0月比较,均为黄棕色的小丸;气微,味苦。3批扶正抗毒丸无变化,符合规定。鉴别:紫花地丁、黄芩、人参、姜黄的薄层鉴别,1、2、3、6月与0月比较,均检出与对照品或对照药材相对应的斑点。3批扶正抗毒丸无明显变化,符合规定。水分:1、2、3、6月与0月比较,3批扶正抗毒丸的水分均呈上升趋势,但6个月时最高的1个批号为8.04%,3批均<9%的指标限度。符合规定。溶散时限:1、2、3、6月与0月比较,3批扶正抗毒丸的溶散时限均呈上升趋势,但6个月时最高的1个批号为59 min,3批均<120 min指标限度。符合规定。重量差异:1、2、3、6月与0月比较,3批扶正抗毒丸重差范围为均在±6%以内。符合规定。微生物限度:1、2、3、6与0月比较,3批扶正抗毒丸均细菌数<30000个/g,霉菌数<100个/g,大肠菌群<100个/g,大肠埃希菌未检出。无霉变、长螨者。符合规定。数据见表1。
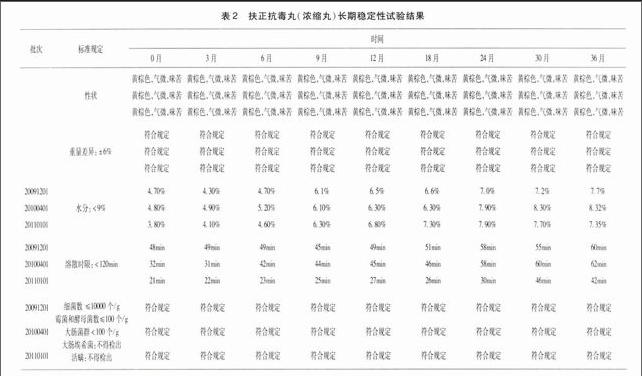
3.2 长期实验结果 性状:3、6、9、12、18、24、30、36月与0月比较,均为黄棕色的小丸;气微,味苦。3批扶正抗毒丸无明显变化,符合规定。鉴别:紫花地丁、黄芩、人参、姜黄的薄层鉴别,3、6、9、12、18、24、30、36月与0月比较,均检出与对照品或对照药材相对应的斑点。3批扶正抗毒丸无明显变化,符合规定。水分:3、6、9、12、18、24、30、36月与0月比较,3批扶正抗毒丸的水分均呈上升趋势,但36个月时最高的1个批号为8.32%,3批均<9%的指标限度。符合规定。溶散时限:3、6、9、12、18、24、30、36月与0月比较,3批扶正抗毒丸的溶散时限均呈上升趋势,但36个月时最高的1个批号为62 min,3批均<120min指标限度。符合规定。重量差异:3、6、9、12、18、24、30、36与0月比较,3批扶正抗毒丸重差范围为均在±6%以内。符合规定。微生物限度:3、6、9、12、18、24、30、36与0月比较,3批扶正抗毒丸均细菌数<30000个/g,霉菌数<100个/g,大肠菌群<100个/g,大肠埃希菌未检出。无霉变、长螨者。符合规定。数据见表2。
表2 扶正抗毒丸(浓缩丸)长期稳定性试验结果
4 实验结果分析
本品先醇提后水提,含大量糖分,极易吸潮,故随时间推移,水分、溶散时限呈缓慢上升趋势。
本品不含大量油性及挥发性成分且包装为铝塑复合膜,遮光性能较好,故性状变化不大。本品在成品微生物限度检验合格后,变化不大。
加速试验6个月和长期试验36个月结果比较显示:水分、溶散时限呈缓慢上升趋势,加速试验比长期试验上升稍快。因为昆明长年气温及湿度变化不很大,故长期试验与0月比差距不太大,9个月后水分、溶散时限上升较明显可能由于制剂吸湿所致。其他检测项目显示加速试验和长期试验比较变化不大。
5 结论
加速试验6个月和长期试验36个月结果表明,在现有生产工艺、规格、包装材料和包装工艺条件下制成的扶正抗毒丸,在室内常温阴凉条件下质量稳定。可保证临床用药质量的稳定。
参考文献:
[1]国家药典委员会.原料药与药物制剂稳定性试验指导原则,见《中国药典》2005年版二部.北京:化学工业出版社,2005:附录176.
[2]国家食品药品监督管理局注册司.化学药物稳定性研究的技术指导原则.2005.
[3]国家药品监督管理局中药新药质量稳定性研究的技术要求,见《中药新药研究的技术要求》.1999.endprint

