脱硫剂羟基氧化铁中硫磺的回收研究
吕诗淇,赖君玲,罗根祥
(辽宁石油化工大学 化学化工与环境学部, 辽宁 抚顺 113001)
脱硫剂羟基氧化铁中硫磺的回收研究
吕诗淇,赖君玲,罗根祥
(辽宁石油化工大学 化学化工与环境学部, 辽宁 抚顺 113001)
以四氯乙烯为溶剂,采用溶剂法从脱硫剂羟基氧化铁中回收硫磺。考察了浸取温度、浸取时间、液-固比和溶剂重复使用等因素对硫磺回收率的影响,并对羟基氧化铁和产物硫磺进行了XRD表征。结果表明:在羟基氧化铁20 g、浸取温度为80 ℃、浸取时间60 min、液-固比8∶1的条件下,硫磺的回收率为97.5%;XRD表征结果证实了该产物为硫磺。
溶剂法; 羟基氧化铁; 四氯乙烯; 硫回收
近年来,脱硫剂羟基氧化铁应用十分广泛[1]。羟基氧化铁脱硫过程中,吸收H2S气体使其通过再生以单质硫的形式存在,与羟基氧化铁结合在一起,难以分离。本研究通过回收单质硫以实现羟基氧化铁吸收剂循环使用,以期废物资源化。
硫磺的回收方法有很多,其中浮选法[2]、热过滤法[3]和溶剂法,其中溶剂法脱硫效果较好。常用的溶剂法有硫化铵法[4]、煤油法[5]、二甲苯法[6]和二硫化碳法等。其中硫化铵法工艺复杂,硫磺的纯度不能达到99.5%;煤油法设备安全性要求高[7],脱硫后的残渣中仍然有煤油,必须燃烧处理;二甲苯易挥发,实验设备要求密闭;二硫化碳对硫的溶解量少并且毒性很大。因此本实验中选择了四氯乙烯作为化学溶剂,与煤油、二甲苯相比,四氯乙烯的性质稳定、毒性小且不容易挥发,来考察其作为化学溶剂对羟基氧化铁中硫磺回收情况的考察,以达到废料羟基氧化铁的重复使用。
1 实验部分
1.1 仪器及试剂
山东华鲁电热仪器有限公司DF-101S集热式恒温加热磁力搅拌器,上海力箭有限公司YB-150粉碎机,上海精宏实验设备有限公司DZF-6050真空干燥箱,山东华鲁电热仪器有限公司SHZ-D循环水式多用真空泵,日本理学公司D/max RB X射线衍射仪。
脱硫剂羟基氧化铁(其中含硫磺质量分数为25.0%,其余为羟基氧化铁),北京三聚公司,四氯乙烯,分析纯,上海凌峰化学试剂有限公司,无水乙醇,分析纯,国药集团化学试剂有限公司。
1.2 实验原理
化学溶剂法回收硫磺是利用可以溶解硫的溶剂从含硫物料中溶解硫再经提取得到硫磺产品。使用的溶剂有一个显著特点,就是随着温度升高后对硫磺的溶解度会大幅增加。
实验中选择四氯乙烯作为溶剂,表1中给出了在不同温度下四氯乙烯的溶硫能力[8]。根据这种特性,实验中将羟基氧化铁在四氯乙烯中加热,待硫磺溶解,固液分离后,再降低温度使硫磺析出,同时四氯乙烯溶剂可重复使用。

表1 不同温度下硫在四氯乙烯中的溶解Table 1 The solubility of sulfur at different temperatures in tetrachlorethylene
1.3 实验步骤
在圆底烧瓶中加入研磨并烘干的羟基氧化铁和四氯乙烯,磁力搅拌下回流加热,一段时间后将溶液趁热过滤,将滤液冷却至室温,继续用冰水浴冷却45 min后,接着把滤液减压抽滤,并用无水乙醇洗涤,将得到的产品在60 ℃条件下烘干后得到样品。
1.4 硫磺回收率
硫磺的回收率记作W0,根据公式(1):

式中: m2—产品硫磺的质量, g;
m1—羟基氧化铁的质量, g。
1.5 实验步骤
使用D/max RB型XRD测定脱硫前后的羟基氧化铁实验原料以及浸出的硫磺产物的物相,Cu Kα辐射(λ=0.154 18 nm)管压:40 kV,管流:100 mA,采用连续扫描方式,步长0.02 °,扫描速率4 °(2θ)/min。
2 结果与讨论
2.1 硫磺回收率的考察
2.1.1 反应温度的影响
在羟基氧化铁20 g,四氯乙烯的体积和羟基氧化铁质量的比值为液-固比(以下简称液固比)为8∶1、反应时间60 min的条件下考察温度对羟基氧化铁中硫磺回收率的影响,实验结果见图1。

图1 反应温度对硫磺回收率的影响Fig.1 Effect of the reaction temperature on sulfur recovery
由图1可以观察到,反应温度小于 80 ℃时,硫磺的回收率随着温度的升高而增大,硫磺回收率达到 97%;当浸取温度接着升高到 110 ℃时,硫磺的回收率变化较平缓;当温度高于110 ℃后,硫磺回收率反而下降,究其原因主要是因为在常压下四氯乙烯的沸点为121 ℃,当温度大于110℃后四氯乙烯溶剂逐渐开始沸腾,使液-固比降低,硫磺的回收率也因此降低。因此实验选择 80 ℃为最佳反应温度。
2.1.2 反应时间的影响
在羟基氧化铁 20 g、液-固比 8∶1、反应温度80 ℃条件下考察反应时间对硫磺回收率的影响,实验结果见图2。
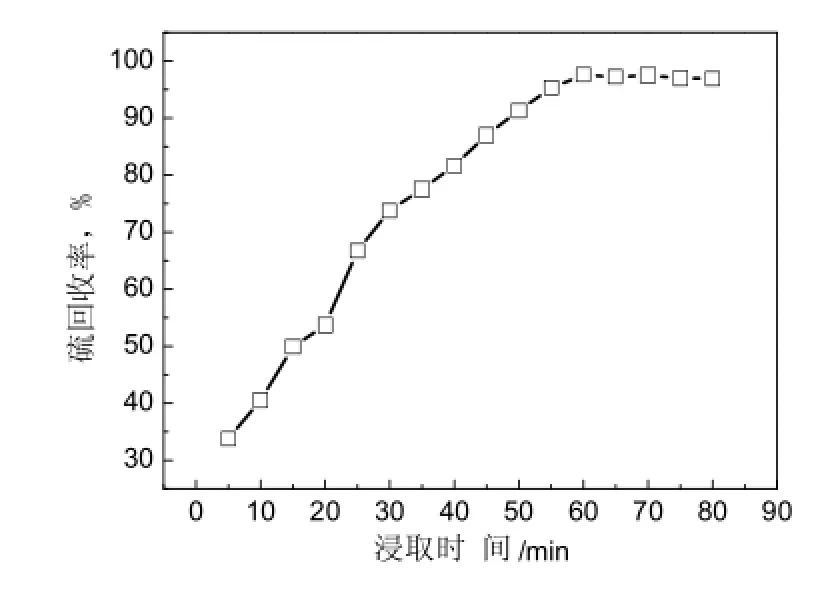
图2 反应时间对硫磺回收率的影响Fig.2 Effect of the reaction time on sulfur recovery
如图2所示,反应时间为60min时,硫磺回收率达到最大值,此后随着反应时间的增加,硫磺回收率再无明显变化;反应时间过短,硫磺溶解不完全,导致硫磺回收率偏低,因此最佳反应时间为60 min。
2.1.3 液-固比的影响
在羟基氧化铁20 g、反应温度为80 ℃、反应时间60 min的条件下考察液-固比对硫磺回收率的影响,实验结果见图3。

图3 液-固比对硫磺回收率的影响Fig.3 Effect of the solid - liquid ratio on sulfur recovery
如图3所示,当液-固比大于8∶1时,硫磺回收率数值趋于稳定,硫磺回收率达到95%以上;液-固比过低时硫磺浸出不完全,硫磺回收率很低。因此实验选择最佳液-固比为8∶1。
2.1.4 溶剂重复使用的影响
在羟基氧化铁20 g、液-固比为8∶1、反应温度80 ℃、反应时间60 min和四氯乙烯溶剂160 mL(回收硫磺后分离得到的溶剂四氯乙烯)的条件下考察四氯乙烯溶剂重复使用对硫磺回收率的影响,实验结果见图4所示。
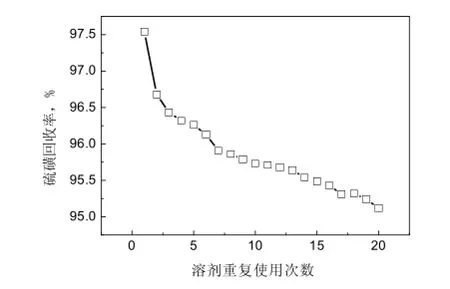
图4 溶剂重复使用对硫磺回收率的影响Fig.4 Effect of the solvent reusing times on sulfur recovery
由图4可以看出,四氯乙烯溶剂可以直接重复使用,在重复使用20次之后,硫磺的回收率从97.5%下降到95%,由此表明四氯乙烯溶剂可循环使用。
2.2 表征
2.2.1 羟基氧化铁的表征
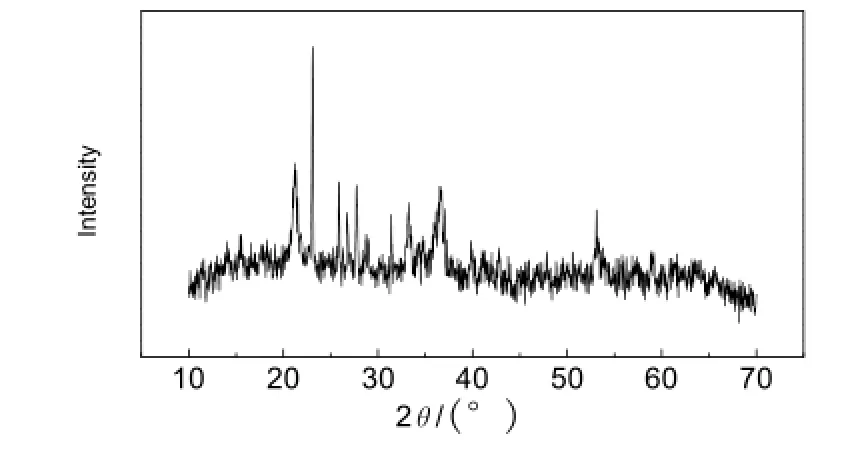
图5 羟基氧化铁的XRD图谱Fig.5 XRD pattern of hydroxyl iron oxide
脱硫前羟基氧化铁的XRD图如图5所示。和标准谱图进行对比,在2θ =23.2°处明显出现硫磺的主峰,在2θ =25.98°, 27.86°,28.8°,29.06°处也有一定强度的单质硫的衍射峰,表明该羟基氧化铁中含有单质硫磺,同时羟基氧化铁中除了含有针铁矿和赤铁矿,还有纤铁矿[γ-FeO(OH)],与针铁矿同质多象(即有共同的化学组成但晶体结构不同):针铁矿中氧和氢氧根离子的排列呈现六方最密堆积,而纤铁矿为立方堆积,两者的铁离子都分布与一个八面体空隙中。此外还有白铁矿(FeS2),是FeS2的不稳定变体,高于350 ℃即转变为黄铁矿。
脱硫后的羟基氧化铁的XRD图如图6所示。从图6中可以看出,和硫磺的标准谱图对比,未见硫磺的特征峰,表明硫磺从羟基氧化铁中已经被完全分离;从谱图中可以看出,脱硫后的羟基氧化铁中主要含针铁矿,一种黄棕色的羟基氧化铁矿物(α -FeOOH)和赤铁矿(α-Fe2O3),在2θ =33.3°和35.76°处有较弱的赤铁矿的衍射峰。
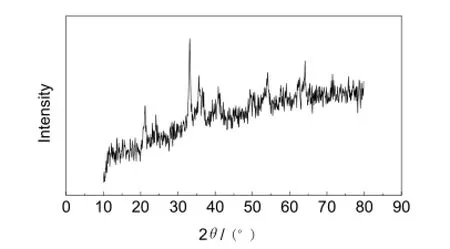
图6 脱硫后的羟基氧化铁的XRD图谱Fig.6 XRD pattern of hydroxyl iron oxide after the desulfurization
2.2.2 硫磺产品的表征
在温度为80℃、时间为60 min、液-固比为8:1的条件下得到的产品的XRD如图7所示。由图7可以看出,和硫磺的标准谱图相一致,在2θ =23.2°处明显出现硫磺的主峰,在 2θ=25.98°、27.86°、28.8°、29.06°处也有一定强度的单质硫的衍射峰,表明所得到的产品为硫磺,并且没有杂质峰,表明所得产品的纯度好。
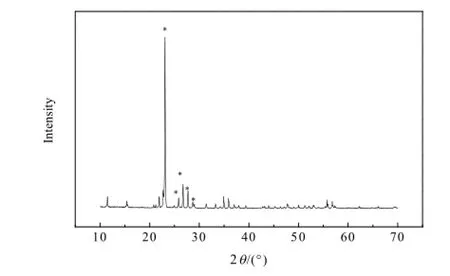
图7 硫磺的XRD图谱Fig.7 XRD pattern of sulfur
3 结 论
本文利用四氯乙烯溶剂回收含单质硫 25.0%的羟基氧化铁废脱硫剂中的元素硫,通过对各个条件的单因素试验研究,得出了如下结论:
(1)用四氯乙烯提取羟基氧化铁中元素硫是完全可行的。四氯乙烯是溶硫能力很强的一种良好溶剂。考虑浸出成本,取得最大回收率的最佳硫磺回收方案为∶ 液-固比 8∶1、浸取温度 80 ℃、浸取时间60 min,此时硫磺浸出率可达97.5%。
(2)四氯乙烯有机溶剂可以多次循环使用,在重复使用20次后硫磺回收率仍能保持在95%以上。
[1]王立贤, 赵刚, 吴志强. 常温脱硫剂羟基氧化铁的制备与性能评价[J]. 气体净化, 2010, 10(2)∶ 4-7.
[2]邱冠周, 伍喜庆, 王毓华. 近年浮选进展[J]. 金属矿山, 2006 (1)∶41-52.
[3]邓孟俐. 硫化锌精矿加压浸出元素硫的形成机理及硫回收工艺的研究[J]. 工程设计与研究 (长沙), 2009 (2)∶ 14-18.
[4]龙小艺, 龙凯. 硫化锌精矿浸出渣硫磺回收工艺[J]. 无机盐工业, 2008, 40(10)∶ 53-54.
[5]李竟菲, 王宝璐, 徐敏. 含铜金精矿中单质硫的煤油浸取回收工艺[J]. 化学工程, 2009, 37(8)∶ 75-78.
[6]杨天足, 赵天从. 用二甲苯从湿法冶金残渣中提取元素硫[J]. 中南矿冶学院学报, 1990, 21(2)∶ 171-176.
[7]姚淑华, 石中亮, 宋守志. 有色金属矿物中硫资源的回收及综合利用[J]. 中国资源综合利用, 2003 (8)∶ 14-18.
[8]李振华, 王吉坤. 闪锌矿氧压酸浸渣中硫的回收研究[J]. 矿业工程, 2011, 6 ( 6 )∶ 31-33.

图6 地达诺辛分子前线轨道图Fig.6 Photo of dideoxyinosine molecular
4 结 论
对标题新药分子地达诺辛, 基于量子化学理论及方法,本文在 6-311+G(d,p)水平上进行了模拟和计算。对抗艾滋病新药的5大吸收光谱比如UV-Vis,IR,1HNMR ,13CNMR以及Raman等进行了标注和拟合,获得了与其分子标准品光谱基本相合的较好结果。自然原子轨道电荷和前线轨道图表明,杂环官能团氮及氢原子(-NH)最有可能是该分子发挥其药理(毒理)性的作用位点。
参考文献:
[1]刘晓园. 治疗 A I D S 的新药双脱氧肌昔[J]. 国外医药—合成药、生化药、制剂分册, 1993, 14(1)∶ 33-34.
[2] 杨蓓, 郁颖佳, 陶芸莺, 邵路平, 段更利. 国产去羟肌苷散剂与进口去羟肌苷片剂的人体生物等效性[J]. 中国新药与临床杂志, 2005, 24 (9)∶ 701-703.
[3]陈炜,仲平,张军霞. HPLC法测定去羟肌苷咀嚼片中阿斯巴甜的含量[J]. 中国药房, 2015, 26(3)∶ 371-373.
[4]李建军, 郑 伟, 屈凌波, 杨 冉.化学发光法测定去羟肌苷[J].分析试验室, 2009, 28(11)∶ 17-19.
[5] 杨世华, 王秀萍. 高效液相色谱法测定2, 3-双脱氧肌昔的含量[J]. 中国药师, 2005, 8(8)∶ 640-641.
Research on Recovery of Sulfur From Hydroxyl Iron Oxide Desulfurizer
LV Shi-qi, LAI Jun-ling, LUO Gen-xiang
(College of Chemistry, Chemical Engineering and Environmental Engineering,Liaoning Shihua University,
Liaoning Fushun 113001, China)
Sulfur was recovered from hydroxyl iron oxide desulfurizer containing 25.0% sulfur by solvent method in tetrachloroethylene solvent. The influence of reaction temperature,reaction time,liquid-solid ratio and reusing times of organic solution on sulfur recovery was investigated. The hydroxyl iron oxide desulfurizer and the product were characterized by X-ray diffraction (XRD) technology. The results show that, when the liquid-solid ratio of tetrachloroethylene to desulfurizer hydroxyl iron oxide containing 25.0% sulfur is 8:1, leaching temperature is 80 ℃, leaching time is 60 min, hydroxyl iron oxide is 20 g, the recovery of sulfur can be over 97.5%. The XRD characterization result has proved that recovered product is sulfur.
solvent method; hydroxyl iron oxide; tetrachloroethylene; sulfur recovery
TQ 028
A
1671-0460(2015)09-2090-04
2015-04-16
吕诗淇(1989-),女,内蒙古人,在读研究生,研究方向:材料的合成和应用研究。邮箱:83694168@qq.com。
罗根祥(1965-),男,教授,硕士,研究方向:无机新材料的合成。邮箱:gxluo1965@163.com。

