罗布麻双层漂浮型脉冲释药片的制备
冉茂莲, 李小芳, 余 琳, 罗丽佳, 罗 丹, 李 平, 周 维
(成都中医药大学中药标准化教育部重点实验室中医药资源及开发利用国家重点实验室培育基地,四川成都611137)
罗布麻双层漂浮型脉冲释药片的制备
冉茂莲, 李小芳*, 余 琳, 罗丽佳, 罗 丹, 李 平, 周 维
(成都中医药大学中药标准化教育部重点实验室中医药资源及开发利用国家重点实验室培育基地,四川成都611137)
目的制备用于节律性高血压治疗的罗布麻提取物漂浮型脉冲释药片。方法以崩解时间和溶出度为指标,筛选罗布麻提取物速释片芯的崩解剂,用混料设计优选最佳漂浮层处方,体外释药试验考察对时滞的影响。结果优选的处方和工艺条件为:交联聚维酮 (PVPP)作为片芯崩解剂;包衣处方中羟丙甲基纤维素 (HPMC K4M)作为凝胶材料,乳糖用量为20%;漂浮层以30%卡波姆 (carbopol)、36.3%羟丙甲基纤维素、33.7%碳酸氢钠组合最优。体外释放试验表明,罗布麻双层漂浮型脉冲片在经6 h滞期后药物脉冲释放。结论罗布麻双层漂浮型脉冲片达到瞬间起漂并持续到预定的时滞期脉冲释药,满足节律性疾病的治疗要求。
罗布麻;漂浮型脉冲释药系统;片剂;交联聚维酮 (PVPP);羟丙甲基纤维素 (HPMC K4M);卡波姆 (carbopol);制备
漂浮型脉冲释药系统(floating pulsatile drug delivery system,FPDDS)[1]是集漂浮与脉冲于一体旨在提高制剂的胃滞留,使其在一定的时滞相后于胃或小肠远端完全释放的释药系统。特别适用于夜间酸突破[2-3]、 关节痛症[4]、 心血管[5-6]等具有昼夜节律性疾病的治疗。该系统的优势为:在特定时间段内没有药物释放,最后在上消化道完全释放;可以在睡觉时服用而释药却在清晨,是一个很有前途的时间治疗系统;利用胃液充分的优势,延长制剂在消化道的滞留时间,提高体内释药时滞控制的稳定性,避免出现制剂脉冲释放发生时已通过药物吸收部位的问题,保证药物的吸收[7]。病人在方便时服药,药物在病发前释放,提高疗效和病人用药顺应性[8],减少用药次数从而提高患者的依从性,能使药物的疗效和毒性进一步分离[9-10]。罗布麻为夹竹桃科Apocynaceae植物,学名Apocynum venetum L,为 《中国药典》收载的降压中药。2010年版 《中国药典》记载其功能主治为平肝安神、清热利水,用于肝阳眩晕,心悸失眠,浮肿尿少[11]。罗布麻叶中含有黄酮类、生物碱类等成分。现代药理研究表明罗布麻总黄酮是其降血压、降血脂和抗血小板聚集、镇静、利尿的主要有效成分[12]。本研究拟采用压制包衣法制备罗布麻双层漂浮型脉冲释药片,通过体外溶出试验优选处方,并探讨其释药机理。
罗布麻双层漂浮型脉冲释药片主要由三部分组成:a含药速释片芯,是为了加快脉冲释药完全的关键;b包衣层,外层包衣材料采用亲水性凝胶材料HPMC,HPMC不但具有一定漂浮能力,而且具有生物黏附性,有利于制剂的胃滞留。HPMC吸水形成凝胶层可减少时滞期前的药物释放量,在包衣层中加入致孔剂乳糖,调节释药时滞长短及释药速率;c漂浮层,为保证制剂用药后在胃部可迅速起漂,有利于其在胃内滞留,有效控制漂浮时滞,以卡波姆(Carbopol)、碳酸氢钠(NaHCO3)和HPMC K4M制备了漂浮层。
1 仪器与试药
DP-I型单冲压片机(上海中药机械厂);UV-6100型紫外可见分光光度计;ZRS-8G智能溶出试验仪 (天大天发科技有限公司制造)。罗布麻叶提取物 (实验室自制,罗布麻叶饮片购于四川新荷花中药饮片股份有限公司,批号1303085,产地辽宁,经提取精制得到的罗布麻提取物,总黄酮含有量为80%以上);金丝桃苷对照品购于成都曼思特生物科技有限公司 (批号 MUST-13080201)。HPMC K4M(上海卡乐康包衣技术有限公司));Carbopol 934P(美国诺誉化工有限公司);乳糖(AR) (成都市科龙化工试剂厂);其他试剂均为分析纯。
2 方法
2.1 罗布麻双层漂浮型脉冲释药片的制备
2.1.1 速释片芯的制备 将罗布麻提取物与崩解剂、微晶纤维素、微粉硅胶混合均匀,采用6 mm冲模粉末直接压片制备速释片芯 [0.1 g/片,含提取物60 mg,硬度40 N]。
2.1.2 衣层的制备 将HPMC与乳糖充分混匀,备用。
2.1.3 漂浮层的制备 将Carbopol、HPMC和NaHCO3按一定比例混合均匀,备用,0.1 g/片。
2.1.4 双层漂浮型脉冲片的制备 将处方量漂浮层填充于10 mm的冲模里,轻压使其平整,将半量的外层包衣衣料置冲模中,铺平,置罗布麻速释片芯于衣料中央,再将半量外层衣料加入冲模中,调整压片力,压片 [0.3 g/片,硬度40~50 N]。
2.2 体外测定方法
2.2.1 对照品溶液、供试品溶液及空白辅料溶液的配制 精密称取金丝桃苷对照品0.001 92 g于50 m L量瓶中,以0.1 mol/L盐酸液为介质定容至刻度,摇匀,制得质量浓度为0.038 4 mg/mL的对照品溶液;精密称取罗布麻提取物适量至50mL量瓶中,用0.1 mol/L盐酸液溶解并稀释至刻度,摇匀,配制成供试品溶液;按处方配比,称取各种辅料适量,用0.1 mol/L盐酸液配制成不含罗布麻提取物的空白辅料溶液。
2.2.2 测定波长的选择 精密移取对照品溶液、供试品溶液及空白辅料溶液2 mL分别于10 ml量瓶中,定容至刻度,并分别置紫外分光光度计中在200~800 nm间进行扫描,扫描结果为:对照品液、供试品液吸收光谱基本相似,且都在360 nm和258 nm处有最大吸收峰,而空白辅料溶液在此处无吸收,但258 nm处有多种物质存在紫外吸收,因此选择360 nm波长处测定罗布麻提取物的吸收度。
2.2.3 标准曲线的制备 分别精密吸取对照品溶液1.5、2、2.5、3、3.5、4 mL于10 mL量瓶中,定容至刻度。在360 nm波长处测定吸光度,绘制标准曲线,得标准曲线方程A=5.694 9C-0.050 6,r=0.999 4。表明在人工胃液中,金丝桃苷在0.057 6~0.153 6 mg/mL质量浓度范围内线性关系良好。
2.2.4 精密度考察 精密移取金丝桃苷对照品溶液2 mL于10 mL量瓶中,用0.1 mol/L盐酸液定容至刻度,于360 nm处连续6次测定吸收值,RSD为0.72%,表明该仪器精密度良好。
2.2.5 回收率试验 分别取线性范围内高、中、低3种质量浓度的罗布麻溶液按处方比例加入辅料进行回收率的测定,平行3份。计算回收率值为98.2%,RSD为1.1%。
2.2.6 体外释放度测定 取双层漂浮型脉冲释药片,按 《中国药典》2010年版释放度测定法项下第二法(桨法)操作,释放介质为0.1 mol/L HCl 900 mL,温度为 (37 ±0.5)℃,转速为 100 r/min[13-15],于规定时间取样5 mL,微孔滤膜滤过,同时补充同温等量的新鲜介质,采用紫外分光光度法测定光密度,计算药物的累积释放百分数。
2.3 速释片芯用崩解剂的筛选 分别以交联羧甲纤维素钠(CCNa)、交联聚维酮(PVPP)、低取代羟丙纤维素(L-HPC)和羧甲淀粉钠(CMS-Na)作为崩解剂 (每片用量均为8%),制备片芯,按“2.2.6”项下操作测定片芯溶出度,评价片芯的释药情况。
2.4 包衣处方因素及水平对制剂体外释药的影响采用单因素试验,按 “2.2.6”项下操作测定释放度,优选包衣处方,处方因素和水平主要为:乳糖占衣膜的比例 (10%、20%、30%、40%、50%)和衣膜用量 (80、100、120、140、160 mg)。
2.5 漂浮层处方的筛选及漂浮性能考察 采用混料设计优选漂浮层中HPMC、Carbopol和NaHCO3的最佳配比,并以起漂时间和漂浮时滞为考察指标。漂浮性能以药片投入0.1 mol/L HCl介质中起漂时间小于1 min,持续漂浮时间大于12 h为宜。实验过程中,各因素固定水平分别为以HPMC K4M与乳糖比4:1为包衣材料,衣重为0.1 g;漂浮层NaHCO3用量为20%,Carbopol用量40%,HPMC用量40%,0.1 g/片。按“2.1”项下操作制备双层漂浮型脉冲片,片剂硬度为40~50 N。
2.6 处方和工艺重复性试验 按照确定的最佳处方和工艺,制备3批罗布麻双层漂浮型脉冲释药片,按 “2.2.6”项下操作测定释放度,考察其处方和工艺的重复性。
3 结果
3.1 片芯崩解剂的筛选 CMS-Na、PVPP、CCNa和L-HPC的崩解时间分别为21、4.45、11.3、34 min。PVPP不同用量(6%、8%、10%)制得片芯的崩解时间分别为7.01、4.6、6.95 min。体外释药测定结果分别见图1,以8%PVPP崩解时间最短,溶出速率最快。
3.2 包衣处方的筛选 不同包衣处方及用量对制剂体外药物释放结果见图1。由图知,当衣膜中乳糖含有量小于或等于20%,衣膜用量为100 mg以上时,释药时滞均能大于6 h。乳糖有含量对释药速率有较大影响,因为乳糖为亲水性辅料,随着乳糖量的增加,衣层溶蚀越快,当衣层变薄时,由于乳糖溶解,衣层形成大量孔道,有利于介质进入片芯,加速片芯吸水膨胀,并加速释药。
3.3 漂浮层处方筛选 混料设计要求所有因素所占比例之和为1,所以A、B、C之和要等于1,通过采用单因素试验优选出Carbopol、HPMC、NaHCO3的较优配比为2:2:1,在此基础上,采用混料设计优选漂浮层的最佳配比,即A、B、C分别的取值范围定为0.3~0.7、0.3~0.7、0~0.4。将起漂时间和漂浮时滞数值标准化为0~1间的归一值(desirability),并以各指标“归一值”求算几何平均数,得到总评 “归一值”OD。对取值越小越好的因素和取值越大越好的指标,可分别采用Hassan法进行数学转换求 “归一值”dmin和dmax,公式如下[16]:
dmin=(Ymax-Yi)/(Ymax-Ymin)(Y为评价指标);
dmax=(Yi-Ymin)/(Ymax-Ymin);
OD=(d1d2…dk)1/K(K为指标数)。
本研究所用指标起漂时间取最小值,漂浮时滞取最大值 (由于存在未起漂和漂浮时滞超过12 h的情况,未起漂或起漂时间超过5 min,均视为5 min,漂浮时滞超过12 h,均视为12 h)。因素水平及结果见表1和图2~图4。
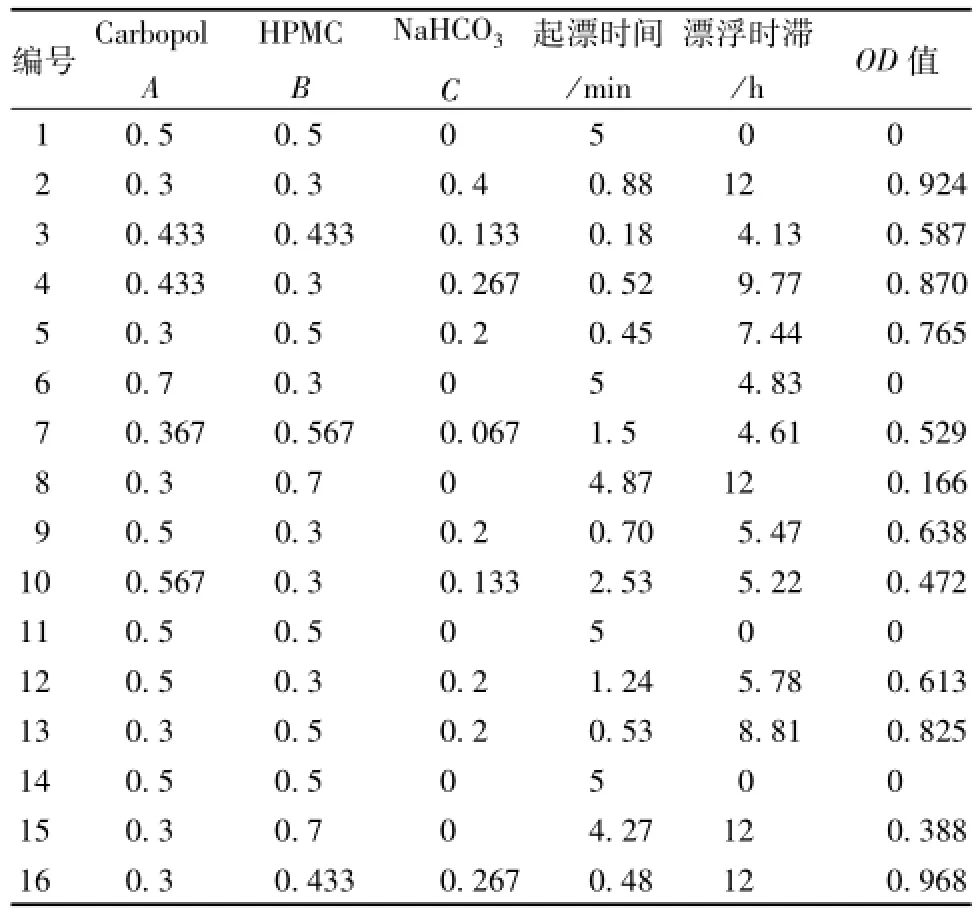
表1 混料实验设计及结果Tab.1 Experimental design and results form ixtures
二项式拟合方程为:
OD=0.307 32A+1.083 12B-1.469 30C-2.694 80AB+5.301 09AC+5.916 25BC(r= 0.984 7,P<0.000 1)根据回归方程、三维图和平面图,可以看出二项式拟合较好,得到漂浮层最佳处方Carbopol为30%,HPMC K4M为36.3%,NaHCO3为33.7%。预测值OD值为0.956 6。为检验试验方法的可靠性,按优选工艺条件进行3次验证试验,结果与拟合方程预测的最大值比较,偏差=[(预测值-实测值)/预测值]×100%,所得OD均值为0.941 7,与预测值偏差为1.58%,说明本实验建立的数学模型能用于预测漂浮层的最佳配比。

图2 HPM C与NaHCO3交互作用三维图Fig.2 Three-dimensional figure for interaction of HPMC w ith NaHCO3
4 处方和工艺重复性试验

图3 Carbopol与NaHCO3交互作用三维图Fig.3 Three-dimensional figure for interaction of Carbopol w ith NaHCO3
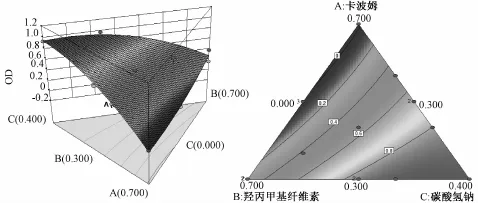
图4 Carbopol与HPMC交互作用三维图Fig.4 Three-dimensional figure for interaction of Carbopolwith HPMC
高血压发作的节律性以凌晨6点左右最为明显,因此本制剂的释药前的时滞应控制在6~7 h。由上述研究结果可知,罗布麻双层胃滞留型脉冲释药片的最佳处方和工艺条件为:以PVPP作为片芯崩解剂,每片用量为8%;包衣处方中HPMC K4M与乳糖用量比为4:1,以100 mg/片为宜;漂浮层最佳处方Carbopol为30%,HPMC K4M为36.3%,NaHCO3为33.7%;工艺采用干法压制包衣,控制制剂硬度为40~50 N。按以上优选的处方和工艺条件进行3批验证试验,通过体外释放度研究,结果为起漂时间均小于1 min,大量释药均在6 h后开始,且释药在2 h释药约90%,结果见图5。由图中释药曲线可见,3批罗布麻双层漂浮型脉冲释药片的体外释药情况,包括起漂时间、时滞期和时滞后的药物释放均 (P>0.05)无显著性差异,重复性良好。
5 讨论
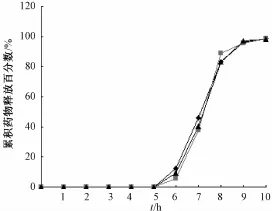
图5 3批罗布麻双层漂浮型脉冲片的体外释药曲线Fig.5 In vitro drug release curve for three batches of gogbane tablets
漂浮型脉冲片的制备是为了在疾病症状出现的高峰期使血浆中的药物浓度达到最大,且应在方便时服用,病发前提供最大的释药。初期 (即时滞期)为少量或无释药阶段,时滞后药物脉冲释放完全为第二阶段,保证稳定重现的时滞和时滞后药物的脉冲释放是此类给药系统制备的关键和难点,而其时滞长短与制剂所处胃、肠道环境的体液量有关。普通脉冲释药系统在体内受胃、肠道转运及胃、肠道不同部位消化液量的影响,存在释药时滞变异大等问题,同时胃排空过程的高可变性质会导致其在体内的变异性和生物利用度问题。为了克服这个问题,提出了漂浮型脉冲释药系统[17]。双层漂浮型脉冲释药系统是根据疾病的昼夜节律性发作特点而设计的,即在一定时滞期后脉冲释放药物,以达到时辰治疗学的要求。本研究以罗布麻提取物为模型药物,制备双层漂浮型脉冲片,使其在时滞后脉冲释放完全,以满足高血压病症发作时的治疗需要。
本研究通过体外释放度和崩解时间测定,确定采用PVPP作为片芯崩解剂,PVPP具有很强的膨胀性能及较高的毛细管活性,因而能迅速地将水吸收到药片中,由于内部压力 (溶胀压力)超过了药片的强度,以至药片瞬间崩解,以满足迅速释药,但PVPP黏结性较强,用量越多,有可能不利于其崩解,所以用量以8%为宜;外层衣膜以HPMC为主,配合使用致孔剂乳糖来调节衣层的溶蚀速率及释药速率;采用干粉末直接压制法包衣。体外释放研究发现,衣膜与人工胃液接触后,水化形成凝胶层,控释药物的释放;漂浮层中NaHCO3与胃液反应生成的CO2滞留于凝胶层中,双层片的漂浮层迅速膨胀,漂浮层带着脉冲片达到液面上部,由于漂浮层溶蚀较慢,能保证一定的漂浮时滞。同时HPMC吸水溶胀后具有一定的漂浮能力及生物黏附性,均能延长制剂在胃中的滞留。时滞期内以制剂释药量少于10%为佳,随着时间的推移,脉冲释药片的外包衣不断溶蚀,使衣膜凝胶层变薄,介质扩散通过衣膜与速释片芯接触,片芯吸水膨胀到一定程度时会胀破薄的衣膜凝胶层,加快药物的释放,达到在预定的时滞期即6 h后脉冲释药的目的,脉冲释药片释药完毕,剩下上层的漂浮部分在胃的蠕动作用下,经过一定时间后也会经消化道排出体外,而其在体内的释药情况还需进一步研究。
[1]Patel J,DalvadiH,Shah D.Time and/or site specific drug delivery of floating pulsatile release delivery system[J].Sys Reviews Pharm,2011,2(1):59-65.
[2]Saitoh T,Watanabe Y,Kubo Y,et al.Intragastric acidity and circadian rhythm[J].Biomed Pharmacother,2001,55(1):138s-141s.
[3]Moore JG,Englert E.Circadian rhythm of gastric acid secretion in man[J].Nature,1970,226(5252):1261-1262.
[4]Maharastra.Pulsatile drug delivery:current scenario[J].Int J Pharma Bio Sci,2011,2(3):332-343.
[5]Pickering T G,James G D.Determinants and consequences of the diurnal rhythm of blood pressure[J].Am J Hypertens,1993,6(6):166S-169S.
[6]Massin M M,Maeyns K,Withofs N,et al.Circadian rhythm of heart rate and heart rate variability[J].Arch DisChild,2000,83(2):179-182.
[7]Bodmeier R,Krogel I.Floating or pulsatile drug delivery systems based on coated effervescent cores[J].Int J Pharm,1999,187(2):175-184.
[8]张 瑜,武亚玲,耿燕娜,等.盐酸青藤碱胃滞留型择时释药片的研制[J].中国中药杂志,2009,34(5):554-559.
[9]邹 豪.口服脉冲和定时释药系统[J].国外医学药学分册,1999,26(1):33-38.
[10]刘璧玉,陈燕忠,吕 竹.脉冲释药技术在中药制剂中的应用[J].中国药师,2011,14(12):1816-1817.
[11]国家药典委员.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010:196-197.
[12]盛 萍,王新铃,杨学斌,等.罗布麻总黄酮提取工艺的优选[J].时珍国医国药,2006,17(4):587-588.
[13]Efentakis M,KoligliatiS,Vlachou M.Design and evaluation of a dry coated drug delivery system with an impermeable cup,swellable top layer and pulsatile release[J].Int J Pharm,2006,311(1-2):147-156.
[14]Zou Hao,Jiang Xuetao,Kong Lingshan,et al.Design and evaluation of a dry coated drug delivery system with floating-Pulsatile release[J].JPharm Sci,2008,97(1):263-273.
[15]Jessy S,Vishal P.Novel floating pulsatile approach for chronotherapeutic release of indomethacin[J].Dhaka Univ JPharm Sci,2007,6(1):37-41.
[16]吴 伟,崔光华,陆 彬.实验设计中多指标的优化:星点设计和总评 “归一值”的应用[J].中国药学杂志,2000,35(8):532.
[17]Chawla G,Gupta P,Koradia V,et al.Gastroretention:a means to address regionalvariability in intestinal drug absorption[J].Pharm Tech,2003,27(7):50-68.
Preparation of bilayer floating gogbane tablets for pulsatile release
RAN Mao-lian, LIXiao-fang*, YU Lin, LUO Li-jia, LUO Dan, LIPing, ZHOUWei
(Chengdu University of Traditional ChineseMedicine,Ministry of Education Key Laboratory for Standardization of Chineseherbalmedicines,System of Traditional Chinese Medicine Resources and Development Utilization of Ministry of State Key Laboratory Breeding Base,Chengdu 611137,China)
AIMTo develop a floating godbane leaf(Apocynum venetum L.)extract tablets with pulsatile drug delivery system for circadian rhythmic hypertension treatment.M ETHODSThe disintegration time and dissolution rate were taken as indexes for selection of the disintegrating agent for a quick release tablet core and the mixing design to screen the optimal formula for the bilayer.The in vitro testwas applied to evaluating the lag time of tablet release.RESULTSThe optimum prescription and process conditionsweremade up by PVPP as the disintegrate agent for core materiel,HPMC K4M with 20%lactose for gelmaterial,30%carbopol,36.3%HPMC K4M,and 33.7%sodium bicarbonate were employed for the pulsatile layer.In vitro release test showed that the release from bilayer floating pulsatile gogbane tablets began after six-hour time lag.CONCLUSIONThe bilayer floating godbane tablets for pulsatile release reach the target for instant floating and start the release at the expected time after the designed lag,and this qualifies the treatment of rhythmic diseases.
godbane leaf(Apocynum venetum);floating pulsatile drug delivery system;tablets;PVPP;HPMC K4M;carbopol;preparation
R944
A
1001-1528(2015)04-0752-06
10.3969/j.issn.1001-1528.2015.04.013
2014-07-03
四川省教育厅项目 (12ZA042)
冉茂莲 (1988—),女,硕士生,研究方向为中药新剂型及中药新技术。Tel:15828508177,E-mail:1948440664@qq.com
*通信作者:李小芳,女,教授,博士生导师,研究方向为中药新剂型及新技术。Tel:13808195110,E-mail:lixiaofang918@163.com

