水溶性高分子基H2S供体的合成及其光释放H2S的研究
王 林,李钟玉,兰云军
(浙江省碳材料温州大学化学与材料工程学院皮革技术研究重点实验室,浙江 温州 325027)
水溶性高分子基H2S供体的合成及其光释放H2S的研究
王 林,李钟玉,兰云军
(浙江省碳材料温州大学化学与材料工程学院皮革技术研究重点实验室,浙江 温州 325027)
硫化氢(H2S)是继NO和CO后新发现的一种信号分子,对细胞具有保护作用。近些年来,H2S在生物学和药理学领域的研究取得了一些重大进展,但仍然有大量的基本问题有待解决。本研究结合高分子药物传输理念和光释放药物的方法合理地设计了一种包含偕取二硫醇型基本结构单元的高分子H2S释放源。
硫化氢;信号分子;光释放
硫化氢(H2S)气体最先在1777年被瑞典无机化学家卡尔·威廉·舍勒(Carl Wilhelm Scheele)发现,它现在已经被人们所熟知是一种拥有臭鸡蛋气味的有毒气体。但是,最近的研究表明它与一氧化氮(NO)和一氧化碳(CO)一样被认为是气体递质家族的一员[1-3]。研究表明哺乳动物体内合成硫化氢至少有3种必需的酶:胱硫醚β-合酶(CBS)、胱硫醚γ-裂解酶(CES)和巯基丙酮酸转移酶(MPST)(图1)。CBS主要存在于大脑、神经系统和肝脏中,而CSE则主要存在于主动脉、门静脉和其他血管组织中[4]。CES主要负责脉管系统中的硫化氢产生以及心脏通过L-硫脲醚和胱氨酸合成L-半胱氨酸、丙酮酸酯和氨的反应,MPST主要局限于线粒体中。Kimura和他的同事们证明在α-酮戊二酸存在下MPST和半胱氨酸氨基转移酶共同作用半胱氨酸产生硫化氢[5]。也有报道称MPST可以在D-氨基酸氧化酶存在条件下将D-半胱氨酸转化成硫化氢。虽然这些酶的表达都有其组织特异性,但是它们都是将半胱氨酸或者半胱氨酸衍生物转化为硫化氢[6]。这些酶共同精确地调节组织内的硫化氢含量,因此它们对硫化氢的体内平衡非常重要。
在2014年Foster和他的同事通过共聚FBEMA和MEO2MA合成水溶性无规共聚物Poly(FBEMA-co-MEO2MA),然后通过FBEMA上的醛基与SATHA上的硫胺基点反应,合成具有半胱氨酸敏感的H2S供体。Foster课题组首次合成了可控型高分子硫化氢供体,这种聚合物释放硫化氢与小分子SATOs一样都要受到半胱氨酸和谷胱甘肽的调节[7]。同年Hasegawa和他的同事利用PEG与ADT-OH偶联,合成一种高分子H2S供体PEGADT[8]。他们利用老鼠的巨噬细胞的内吞作用,进入细胞质,并研究了PEG-ADT加强脂多糖感应的抗炎作用。

图1 水溶性硫化氢供体的合成方程式
1 实验部分
1.1 主要试剂
2,2’-偶氮二异丁腈 (AIBN)、聚乙二醇甲醚甲基丙烯酸酯(Mn=500)、五氧化二磷、磷酸氢二钠、磷酸一氢钠全部为分析纯。
1.2 水溶性H2S供体的合成及其共释放H2S的检量
1.2.1 水溶性无规共聚物P(AEMA10-co-OEGMA60)的合成
2-(4-氧代戊酸乙酯)甲基丙烯酸酯(AEMA)(0.40g,1.75×10-3mol)、聚乙二醇甲醚甲基丙烯酸酯(Mn=500)(8.76g,1.75×10-2mol)、二硫代苯甲酸-2-(乙氧甲酰基)-2-丙酯(ECPDB)(47mg,1.75×10-4mol)和2,2’-偶氮二异丁腈AIBN(5.8 mg,3.5×10-5mol)溶解在4mL DMF的安瓿瓶中。将安瓿瓶放入液氮中冻实后用油泵抽气10min,然后放入水中解冻,连续3次,去除反应体系中的氧气。将安瓿瓶放入70℃的油浴中反应3h,再放入水中冷却,与空气接触,终止反应。将反应混合物溶解在100mL的高纯水中,在超滤瓶中经100kDa的超滤膜超滤1次,将滤液再放入超滤瓶中经4000Da的超滤膜超滤48h。将超滤瓶中的残留液冷冻干燥得到浅红色黏稠液体。经GPC检测数均分子量Mn=34200,PDI=1.31。1H NMR (500MHz,CDCl3),δ:4.28×10-6,4.09× 10-6,3.85×10-6~3.45×10-6,3.38×10-6,2.80×10-6,2.63×10-6,2.22×10-6,1.10×10-6~0.75×10-6。
1.2.2 水溶性无规共聚物P(TK10-co-OEGMA60)的合成
将聚合物 P(AEMA10-co-OEGMA60) (1.026g,3×10-5mol,Mn=34200,PDI=1.31)和2-硝基苄硫醇 (0.112g,6.6×10-4mol) 混合后加入P2O5(0.09g,6×10-4mol),反应48h。将反应混合物溶解在100mL水中用超滤瓶经过100kDa的超滤膜超滤1次,得到的滤液冷冻干燥得到浅黄色黏稠物。经GPC检测数均分子量Mn=38700,PDI=1.28。1H NMR (500 MHz,CDCl3),δ:7.59×10-6,7.50×10-6,7.38× 10-6,4.25×10-6~3.90×10-6,3.75×10-6~3.40× 10-6,3.31×10-6,0.48×10-6,2.03×10-6,1.46×10-6,1.10×10-6~0.75×10-6。
1.2.3 亚甲基蓝H2S水溶液的最大紫外吸收波长
首先配置80μM的Na2S标准溶液和2mg·mL-1的聚合物pH=7.4的磷酸缓冲溶液,量取45mL的聚合物缓冲溶液于40mm×40mm的石英比色皿中,在光强为200 mW·cm-2条件下照射反应。每隔1min取2mL的反应液于甲基蓝混合液(30mM FeCl3在1.2M HCl水溶液400 μL,20mM N,N-二甲基-1,4-苯二胺硫酸盐在7.2M的HCl水溶液400 μL,质量分数为1%的醋酸锌水溶液200 μL,以下同)。对照样品为量取2mL的80 μM的Na2S标准溶液于甲基蓝混合液。静止20min,在550~750nm之间进行全波长扫描。得到最大吸收峰为695nm。
1.2.4 亚甲基蓝标准曲线绘制
首先配置20mM,pH=7.4的磷酸缓冲溶液1L。然后称取120.20mg Na2S· 9H2O 溶解在100mL的容量瓶中,用pH=7.4磷酸缓冲溶液定容,配置出5mM的Na2S标准溶液。分别量取5mM的Na2S标准溶液50、100、200、400、600、800、1000 μL于50mL的容量瓶中,并分别用pH=7.4磷酸缓冲溶液定容。最终分别得到浓度梯度为5、10、20、40、60、80、100 μM的Na2S标准溶液。将梯度标准溶液分别量取2mL加入甲基蓝混合液,空白样品为量取2mL的pH=7.4的磷酸缓冲溶液于甲基蓝混合液。静止20min,分别在695nm波长下测量吸光度,绘制吸光度与Na2S浓度的标准曲线。
1.2.5 H2S释放的动力学研究
量取45mL 2mg·mL-1的聚合物pH=7.4的磷酸缓冲溶液于40mm×40mm的石英比色皿中,在波长为365nm光强为200mW·cm-2照射反应。每隔1min取2mL的反应液于甲基蓝混合液。对照样品为量取2mL的pH=7.4的磷酸缓冲溶液于甲基蓝混合液。
2 结果与讨论
2.1 核磁共振氢谱(1H NMR)表征

图2 聚合物Poly(AEMA10-co-OEGMA60)和Poly(TK10-co-OEGMA60)核磁氢谱(1H NMR)
如图2所示,水溶性无规共聚物P(AEMA10-co-OEGMA60)和P(TK10-co-OEGMA60)核磁图谱对比,g氢从2.20移动到1.45,e氢和f氢分别从2.80和2.63移动到2.49和2.04,可以看出羰基在变化为缩硫酮键时拉电子能力减弱,使羰基周围的e、f、g氢核外电子变多,从而令其向高场移动。除此之外,分别在4.08、7.38、7.51、7.89处出现了o、l、m、n氢。因此,从核磁氢谱可以看出,羰基已经完全与邻硝基苄硫醇偶联。通过k氢与g氢的积分面积得出TK∶OEGMA=1∶6。
2.2 傅立叶变换红外光谱(FT-IR)表征
如图3所示,虚线代表水溶性无规共聚物Poly(AEMA10-co-OEGMA60)的红外吸收谱图,实线代表水溶性无规共聚物Poly(AEMA10-co-OEGMA60)与2-硝基苄硫醇偶联后的红外吸收谱图。从图3中可以看出酮羰基的吸收出在1728cm-1,偶联前后明显减弱。偶联后在1528cm-1出现1个新的吸收峰为芳香硝基的N-O伸缩振动。红外图谱表明羰基已经偶联。
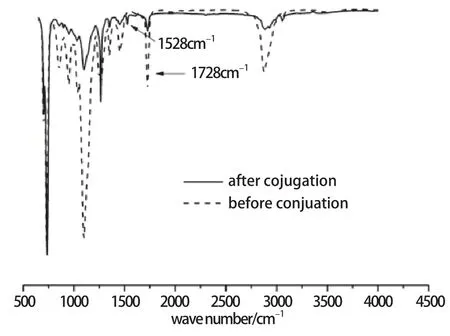
图3 水溶性无规聚合物与邻硝基苄硫醇偶联前后的红外吸收
2.3 凝胶渗透色谱(GPC)表征

图4 水溶性无规聚合物偶在与邻硝基苄硫醇联前后的凝胶色谱(GPC)
如图4所示,实线代表水溶性无规共聚物Poly(AEMA10-co-OEGMA60)的GPC图谱,虚线代表水溶性无规共聚物Poly(AEMA10-co-OEGMA60)与2-硝基苄硫醇偶联后的GPC图谱,从图4中可以看出偶联后,GPC峰值偏移并不是很明显,但是还是向左偏移,而且分布变窄。这从侧面进一步证明羰基与邻硝基苄硫醇偶联。
如图5所示,水溶性H2S供体聚合物的磷酸缓冲溶液在经过UV (365nm)光照后与亚甲基蓝混合液混合的紫外吸收与Na2S标准溶液与亚甲基蓝混合溶液混合的紫外吸收相同,最大吸收峰都在695nm处。并且随着光照时间的延长紫外吸收的强度变强,因此可以利用Na2S标准溶液作为H2S的标准溶液,做Na2S浓度与吸光度的标准曲线。

图5 亚甲基蓝H2S水溶液的紫外吸收
如图6所示,通过不同标准浓度的Na2S,及其亚甲基蓝紫外吸收绘制出一条H2S浓度与吸光度相关的直线y=0.01894x+0.0231, 相关系数为0.99779。
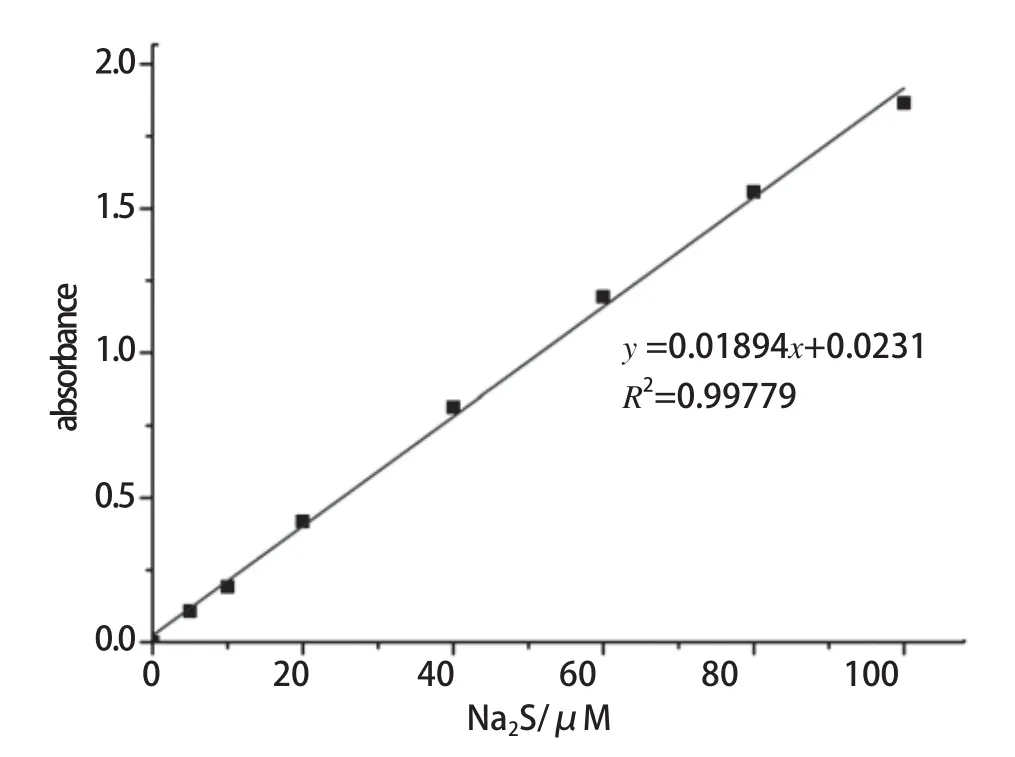
图6 Na2S亚甲基蓝法标准曲线
如图7所示,2mg·mL-1聚合物Poly(AEMA10-co-OEGMA60)的pH=7.4的磷酸缓冲溶液在紫外光365nm、200 mW·cm-2的光强下在12min时达到峰值,最大释放量达到50μM。没有光照的聚合物不能释放硫化氢。

图7 2 mg·mL-1聚合物mPEG-TK的胶束在pH=7.4的磷酸缓冲溶液H2S光释放与时间的关系
3 结论
通过RAFT无规共聚单体AEMA和OEGMA合成水溶性无规聚合物Poly(AEMA10-co-OEGMA60),然后P2O5无溶剂催化与邻硝基苄硫醇反应合成了偕取二硫醇型H2S供体聚合物Poly(TK10-co-OEGMA60),通过不同的表征方法证明了目标产物,通过亚甲基蓝法考察了聚合物的H2S释放。
[1] Vandiver M S, Snyder S H. Hydrogen sulfide: a gasotransmitter of clinical relevance[J]. Journal of molecular medicine, 2012, 90(3): 255-263.
[2] Wang R. Physiological implications of hydrogen sulfide: a whiff exploration that blossomed[J]. Physiological reviews, 2012,92(2): 791-896.
[3] Li L, Rose P, Moore P K. Hydrogen sulfide and cell signaling[J]. Annual review of pharmacology and toxicology, 2011(51): 169-187.
[4] Martelli A, Testai L, Breschi M C, et al. Hydrogen sulphide: novel opportunity for drug discovery [J]. Medicinal research reviews, 2012, 32(6): 1093-1130.
[5] Shibuya N, Mikami Y, Kimura Y, et al. Vascular endothelium expresses 3-mercaptopyruvate sulfurtransferase and produces hydrogen sulfide[J]. Journal of biochemistry, 2009, 146(5): 623-626.
[6] Shibuya N, Koike S, Tanaka M, et al. A novel pathway for the production of hydrogen sulfide from D-cysteine in mammalian cells[J]. Nature communications, 2013(4): 1366.
[7] Foster J C, Matson J B. Functionalization of Methacrylate Polymers with Thiooximes: A Robust Postpolymerization Modification Reaction and a Method for the Preparation of H2S-Releasing Polymers[J]. Macromolecules, 2014, 47(15): 5089-5095.
[8] Hasegawa U, van der Vlies A J. Design and synthesis of polymeric hydrogen sulfide donors[J]. Bioconjugate chemistry, 2014, 25(7): 1290-1300.
Synthesis and Investigation of Water-soluble and Photocontrollable Polymeric Hydrogen Sulfide
WANG Lin, LI Zhong-yu, LAN Yun-jun
(Zhejiang Key Laboratory of Biomass Materials, College of Chemistry and Materials Engineering, Wenzhou University, Wenzhou 325027, China)
Hydrogen sulf de (H2S) was a newly recognized signaling molecule with very potent cytoprotective actions. Although the f elds of H2S physiology and pharmacology had rapidly growing in recent years, a number of fundamental issues still need to be addressed to advance our understanding of the biology and clinical potential of H2S in the future. Herein, we rationally designed and synthesized a new ideal H2S donor using the concept of polymeric drug delivery and stimuli-responsiveness.
hydrogen sulf de; signaling molecule; photoresponse
TQ 251.1+2
A
1670-9905(2015)05-0029-04
王林(1988-),男,硕士,研究方向:应用高分子化学,E-mail:dzwl1115@163.com
2015-03-16

