液相色谱-高分辨质谱测定动物源性食品中均三嗪类药物残留
宫小明, 杨丽君, 王洪涛, 马荣桧, 丁葵英, 郭礼强, 孙 军
(1.潍坊出入境检验检疫局,山东潍坊 261041;2.威海出入境检验检疫局,山东威海 264200)
液相色谱-高分辨质谱测定动物源性食品中均三嗪类药物残留
宫小明1, 杨丽君2, 王洪涛1, 马荣桧1, 丁葵英1, 郭礼强1, 孙 军1
(1.潍坊出入境检验检疫局,山东潍坊 261041;2.威海出入境检验检疫局,山东威海 264200)
[目的]建立动物源性食品中均三嗪类药物及其代谢物残留的液相色谱-高分辨质谱分析方法。[方法] 采用QuEChERS技术进行样品前处理,利用Exactive液相色谱-高分辨质谱联用系统进行检测,建立了动物源性食品中地克珠利、妥曲珠利、妥曲珠利砜、妥曲珠利亚砜等4种均三嗪类药物及其代谢物残留的分析方法。[结果] 地克珠利、妥曲珠利、妥曲珠利砜、妥曲珠利亚砜4种均三嗪类药物在2.0~50.0 μg/L范围内线性关系良好(r2>0.99)。牛粉基质中4种化合物在5、10和20 μg/kg加标水平的回收率为74.5%~90.1%,相对标准偏差(RSD)为 15.4%~17.5%。[结论] 该方法稳定、可靠,可用于动物源性食品中均三嗪药类物残留的检测。
动物源性食品;均三嗪类药物;QuEChERS;液相色谱-高分辨质谱
20世纪80年代出现的均三嗪类抗球虫药因其高效、广谱、毒性低,在畜牧业生产中受到了广泛重视。目前,生产中使用的均三嗪类药物主要有地克珠利和妥曲珠利,地克珠利和妥曲珠利可以有效杀灭包括球虫在内的多种原虫,属于高效抗球虫药物,妥曲珠利在动物体内主要代谢产物为妥曲珠利砜和妥曲珠利亚砜。
均三嗪类药物的检测主要有气相色谱-电子捕获法、液相色谱-紫外检测法[1-3]。近年来,均三嗪类药物残留的高效液相色谱-串联质谱分析方法国内外有较多的研究报道[4-7],由于分子结构的原因,妥曲珠利和妥曲珠利砜无论在何种碰撞能量下都无法得到合适的子离子,因此只能选择其母离子,利用SIM方式对其进行检测,根据欧盟2003/181/EC 法规,低分辨质谱母离子只能算1分,远低于确证4分的要求[8-9],因此低分辨质谱只用于进行筛查,在遇到阳性结果时,必须进行进一步确证。轨道阱高分辨质谱仪具有较高的分辨率、扫描速度和灵敏度,可以有效去除基质干扰,实现高通量的目标物或非目标物筛选和高可靠性的确证定量分析[10-12]。笔者采用QuEChERS[13-15]技术进行样品前处理,利用Exactive液相色谱-高分辨质谱联用系统进行检测,建立了动物源性食品中地克珠利、妥曲珠利、妥曲珠利砜、妥曲珠利亚砜等4种均三嗪类药物及其代谢物残留的分析方法。通过与低分辨质谱检测结果的比较,有效避免了假阳性结果的出现。
1 材料与方法
1.1 仪器、试剂与材料
1.1.1仪器。静电场轨道阱高分辨质谱仪(Thermofisher Exactive);万分之一天平(Mettler AE163);均质器(IKA T25);振荡器(IKA MS1);离心机(Eppendorf 5810);氮吹仪(N-EVAP-111)。
1.1.2试剂与材料。地克珠利、妥曲珠利、妥曲珠利砜、妥曲珠利亚砜标准品,其化合结构式见图1,均购自于Sigma-Aldrich公司;乙睛、甲醇、甲酸(色谱纯),水为Milli-Q超纯水,使用前过0.45 μm滤膜;氯化钠、中性氧化铝(分析纯);N-丙基乙二胺粉(PSA)、二甲基十八碳硅烷粉(ODS),均购自于Agela Technologies公司。
1.2 标准溶液的配制准确称取10 mg地克珠利、妥曲珠利、妥曲珠利砜、妥曲珠利亚砜,用乙腈溶解,准确定容至100 ml,得到浓度为100 μg/ml的标准储备液,避光于4 ℃下保存。使用时用基质空白提取液稀释成适当浓度的标准工作液。为避免分析物分解,应当用棕色器皿保存,现用现配。
1.3 样品处理准确称取5.0 g样品,置于100 ml塑料离心管中,加入5.0 g无水硫酸镁,加入乙腈15 ml,在均质机上高速均质2 min左右,10 000 r/min高速离心10 min,取上清9 ml氮吹浓缩,乙腈定容到1.5 ml,加入150 mg ODS吸附剂玻璃试管中,1 400 r/min涡混2 min,离心后取1 ml上清液,氮吹,1 ml初始流动相定容,上机检测。
1.4 液相色谱串联质谱
1.4.1液相色谱条件。色谱柱:Agilent ZORBAX SB-C18柱(3.0 mm ×100 mm,1.8 μm);柱温为35 ℃;流速为0.3 ml/min,进样量为10 μl;流动相:A为0.1%甲酸水,B为甲醇;梯度洗脱程序:0~2.0 min(10% B),2.5~6.0 min(10%B~90%B),6.0~9.0 min(90%B),10.0~12.0 min(10%B)平衡3 min。

注:A.地克珠利;B.妥曲珠利;C.妥曲珠利亚砜;D.妥曲珠利砜。图1 4种化合物的分子结构

表1 4种化合物的质谱参数
1.4.2质谱条件。全扫描正/负离子模式,扫描质量范围m/z200~1 000;分辨率为25 000;扫描速度为4 Hz;自动增益控制(AGC)目标值为10 e6;喷雾电压为3 500 V;离子传输管温度为320 ℃;鞘气气压为35 Au;辅助气压为10 Au;离子源温度为300 ℃。4种化合物的质谱参数如表1所示。
2 结果与分析
2.1 提取条件的选择均三嗪类药物属于弱极性物质,易溶于甲苯、乙酸乙酯、丙酮、甲醇、乙腈等有机溶剂,微溶于正己烷和石油醚,在水中的溶解度极低。笔者分别考察了甲醇、乙酸乙酯、乙腈作为提取溶剂,均可以得到良好的提取效果,乙腈能更有效地沉淀蛋白,减少杂质干扰,同时乙腈也有利于下一步使用QuEChERS技术进行净化,因此选择乙腈作为提取溶剂。
2.2 各种吸附剂粉对回收率的影响QuEChERS技术是2003年由美国化学家Steven J.Lehotay和德国的Michelangelo Anastassiadas[13-14]提出的一种快速、简单、低成本的样品处理方法。该方法采用分散固相萃取(Dispersive-SPE)净化法,即提取液直接加入吸附剂粉进行净化,经离心后上清液上机检测。
为了选择合适的吸附剂,首先考察各种吸附剂粉对回收率的影响,取2 ml乙腈溶解的浓度为0.05 μg/ml的4种药物的混标溶液,分别加入150 mg不同的吸附剂,经振荡、离心后,取上清液1 ml,上机,试验重复6次,计算平均回收率。从表2可以看出,ODS对目标物的吸附较少,同时又可以很好地吸附脂肪酸、维生素、色素、甾醇等杂质,因此选择ODS作为最终的吸附剂。

表2 不同吸附剂对目标化合物回收率的影响
2.3 牛粉样品高分辨质谱与低分辨质谱检测结果的比较由于分子结构的原因,妥曲珠利和妥曲珠利砜无论在何种碰撞能量下都无法得到合适的子离子,因此只能利用选择离子扫描(SIM)模式对母离子进行检测,QuEChERS技术的优点是简单、快速,缺点是净化效果差,此前利用低分辨三重四级杆质谱在(SIM)模式对样品进行检测,可以满足筛查的要求,但是在遇到复杂基质干扰的情况下,就必须进行进一步确证。轨道阱高分辨质谱仪具有较高的分辨率和灵敏度,可以有效去除基质干扰。从图2可以看出,在妥曲珠利4.3 min左右的出峰时间,牛粉样品有一个明显的峰;从图3可以看出,在5.79 min左右妥曲珠利的出峰时间,牛粉样品既提取不到妥曲珠利的精确质量数也得不到对应的色谱峰,因此可以判断牛粉为阴性样品,低分辨质谱下样品的峰应该为杂质干扰,为假阳性结果。
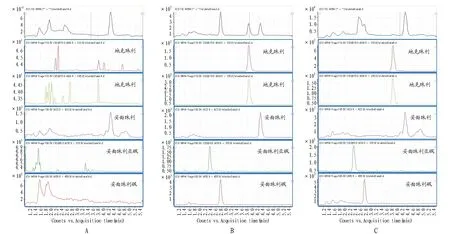
注:A.牛粉样品;B.各类药物标准品;C.牛粉加标样品。图2 牛粉样品、各类药物标准品和牛粉加标样品的低分辨色谱图

注:A.牛粉样品;B.各类药物标准品;C.牛粉加标样品。图3 牛粉样品、各类药物标准品和牛粉加标样品高分辨色谱图和在5.79 min的高分辨质谱图
2.4 线性范围、定量限、回收率和精密度用基质提取液配制一系列不同浓度的4种药物混合标准溶液,依次进样,以峰面积为纵轴,以浓度为横轴,绘制校准曲线,由工作站可直接计算回归方程及相关系数。由表3可知,4种分析物在2.0~50.0 μg/L范围内线性关系良好。以20 μg/kg空白牛粉添加色谱图,根据10倍信噪比计算定量限,4种化合物的定量限均为2 μg/kg,能满足日本、欧盟等国家规定的最大残留限量。
用空白样品加标方法进行回收率和精密度试验。分别对牛粉进行3个不同水平的加标,每个水平平行测定7次,计算回收率和相对标准偏差。由表3可知,4种化合物在2、10、20 μg/kg加标水平的回收率为74.5%~90.1%,相对标准偏差(RSD)为15.4%~17.5%。
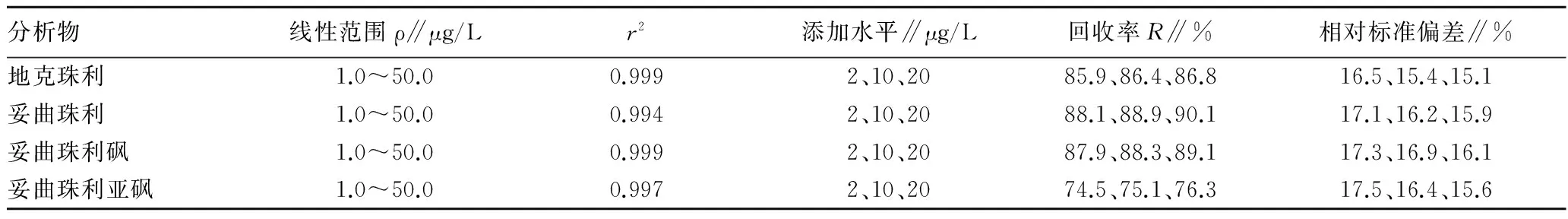
表3 4种药物的回归方程、相关系数、回收率与相对标准偏差
3 小结
笔者将最先应用于农药多残留分析的QuEChERS技术引入地克珠利、妥曲珠利、妥曲珠利砜、妥曲珠利亚砜等4种均三嗪类药及其代谢物残留分析的样品前处理过程,针对妥曲珠利、妥曲珠利砜无法得到碎片离子,只能采用SIM模式检测母离子的特点,借助静电场轨道阱高分辨质谱仪分辨率、出色的质量精度、高灵敏度和宽动态范围的特点对样品进行检测,与高效液相色谱法-串联四极杆质谱法相比可以更好地去除基质干扰,灵敏度大大提高。该方法具有适用性强、简单快速、经济等特点,各项技术指标均能满足日常检测分析的要求,应用于实际样品检测,取得了满意的效果。
[1] 施祖灏,朱良强,卢运站,等.鸡组织中地克珠利和妥曲珠利残留HPLC检测方法的建立[J].中国兽医学报,2009,29(1):79-81.
[2] 祁克宗,施祖灏,彭开松,等.质固相分散萃取-高效液相色谱法检测鸡组织中均三嗪类药物残留[J].分析化学,2007,35(11):1601-1606.
[3] 施祖灏,葛庆联陆俊贤,等.同时检测2种均三嗪类抗球虫药物残留的样品前处理方法的比较[J].色谱,2009,27(3):303-306.
[4] KIMIHIKO Y,SUSUMU I,YASUHIDE T,et al.Simultaneous determination of Emmamectin,its metabolites,Milbemectin,Ivermectin and Abamectin in tomato,Japanese radish and tea by LC/MS[J].J Health Sci,2004,50(1):17-24.
[5] 高华鹏,张健玲,李永夫,等.超高效液相色谱-串联质谱法快速测定鳗鱼中阿维菌素类农药残留[J].质谱学报,2008,29(6):337-342.
[6] 徐颖洁,韩航如,郭永刚,等.液质联用方法测定鸡血浆中妥曲珠利及其代谢产物[J].南京农业大学学报,2006,29(1):127-130.
[7] 宫小明,孙军,董静,等.高效液相色谱-串联质谱法测定猪肉中的阿维菌素类、地克珠利、妥曲珠利及其代谢物残留[J].色谱,2011,29(3):217-222.
[8] 孙雷,张骊,徐倩,等.超高效液相色谱-串联质谱法检测猪肉和猪肾中残留的10种镇静剂类药物[J].色谱,2010,28(1):38-42.
[9] 董静,潘玉香,朱莉萍,等.果蔬中54种农药残留的QuEChERS/GC-MS快速分析[J].分析测试学报,2008,27(1):66-69.
[10] GRIMALT S,SANCHO J V,POZO O J,et al.Quantification,confirmation and screening capability of UHPLC coupled to triple quadrupole and hybrid quadrupole time-of-flight mass spectrometry in pesticide residue analysis[J].J Mass Spectrom,2010,45(4):421-436.
[11] KRAUSS M,SINGER H,HOLLENDER J.LC-high resolution MS in environmental analysis:From target screening to the identification of unknowns [J].Anal Bioanal Chem,2010,397(3):943-951.
[12]KELLMANN M,MUENSTER H,ZOMER P,et al.Full scan MS in comprehensive qualitative and quantitative residue analysis in food and feed matrices:how much resolving power is required [J].J Am Soc Mass Spectrom,2009,20(8):1464-1476.
[13] KLINSUNTHORN N,PETSOM A,NHUJAK T.Determination of steroids adulterated in liquid herbal medicines using QuEChERS sample preparation and high-performance liquid chromatography [J].J Pharm Biom Anal,2011,55:1175-1178.
[14] STUBBINGS G,BIGWOOD T.The development and validation of a multiclass liquid chromatography tandem mass spectrometry(LC-MS/MS)procedure for the determination of veterinary drug residues in animal tissue using a QuEChERS(QUick,Easy,CHeap,Effective,Rugged and Safe)approac[J].Anal Chim Acta,2009,637:68-78.
[15 ]LEHOTAY S J,MASTOVSKA K,LIGHTFIELD A R,et al.Multi-analyMulti-analyst,multi-matrix performance of the QuEChERS approach for pesticide residues in foods and feeds using HPLC/MS/MS analysis with different calibration techniques [J].J AOAC Int,2010,93(2):355-367.
Determination of Diclazuril, Toltrazuril and Metabolite Residues in Animal-derived Food by Liquid Chromatography—High Resolution Mass Spectrometry
GONG Xiao-ming1, YANG Li-jun2, WANG Hong-tao1et al
(1.Weifang Entry-Exit Inspection and Quarantine Bureau, Weifang, Shandong 261041;2.Weihai Entry-Exit Inspection and Quarantine Bureau,Weihai,Shandong 264200)
[Objective] The research aimed to establish the detecting method of liquid chromatography—high-resolution mass spectrometry for detecting the residues of diclazuril,toltrazuril and its metabolites in animal-derived food. [Method] The samples were pre-treated by using QuEChERS technology and detect by using Exactive liquid chromatography—high resolution mass spectrometry. The detecting method of liquid chromatography—high-resolution mass spectrometry for detecting the residues of diclazuril,toltrazuril and its metabolites in animal-derived food was established. [Result] Diclazuril,toltrazuril and its metabolites showed a good linear correlation in the range of 2.0-50.0 μg/L(r2>0.99). The average recoveries of these four compounds in beef power at the spiked levels of 2,10,20 μg/kg was 74.5%-90.1%, and the relative standard deviations(RSD)was 15.4%-17.5%. [Conclusion] This method was stable and reliable, and so it could be used for detecting diclazuril, toltrazuril and its metabolites.
Animal-derived food; 1,3,5-triazine; QuEChERS; Liquid chromatography—high-resolution mass spectrometry
国家质检总局科研项目(201310143)。
宫小明(1976- ),男,山东莱西人,高级工程师,硕士,从事兽药残留、真菌毒素及添加剂研究。
2015-08-13
S 851.347
A
0517-6611(2015)28-114-04

