CaO基脱硫剂中TCa、CaO、CaF2、SiO2、P的联合测定
王俊秀,薛明浩,侯俊坤,马清文,魏文升
(山东鲁丽钢铁有限公司,山东 寿光 262724)
试验研究
CaO基脱硫剂中TCa、CaO、CaF2、SiO2、P的联合测定
王俊秀,薛明浩,侯俊坤,马清文,魏文升
(山东鲁丽钢铁有限公司,山东 寿光 262724)
试样用含有硼酸的混合熔剂熔融,稀盐酸酸化后定容。通过控制测定时各元素的酸度,分别用硅钼蓝光度法测定SiO2,铋磷钼蓝光度法测定P、EGTA滴定法测定TCa;利用CaO易溶解于稀乙酸,而CaF2不溶解于稀乙酸的特性,试样用稀乙酸溶解处理过滤分离后,用EGTA滴定法测定CaO;计算出CaF2量。测定结果满意,方法可行,适合冶金工厂日常生产需要。关键词:CaO基脱硫剂;TCa;CaO;光度法;EGTA滴定法
1 前言
CaO基脱硫剂主要用于炼钢脱硫,与硅钙合金具有同样的脱硫、脱氧、去气等净化钢液的作用,但CaO基脱硫剂价格低,可降低炼钢成本。脱硫剂化学成分决定其价格和用量。为了保证进厂脱硫剂的质量,快速分析其成分,有效控制原材料采购成本,参考有关文献[1-6],实验制定了用EGTA滴定法与分光光度法联合快速测定CaO基脱硫剂中TCa、CaO、CaF2、SiO2、P的测定方法,获得了满意的结果。
2 实验部分
2.1 试剂
混合熔剂:无水碳酸钠+硼酸+无水碳酸钾(3+ 2+1);盐酸(ρ约1.19 g/mL);3.5%钼酸铵溶液;草硫混合酸:4份草酸(4%)与1份硫酸(1+3.5)混合,搅拌均匀;6%硫酸亚铁铵溶液:称取60 g硫酸亚铁铵,溶解于预先加有8 mL硫酸的水中,以水稀释至1 000 mL;5%酒石酸钾钠溶液;1%硝酸铋溶液:称取1 g硝酸铋溶解于100 mL硝酸(1+9)中;2%抗坏血酸溶液:称取2 g抗坏血酸溶解于100 mL乙醇(1+1)中;硫代硫酸钠溶液:称取0.2 g硫代硫酸钠与0.1 g无水碳酸钠溶解于100 mL水中,混匀;三乙醇胺(1+3);1%硫酸镁溶液;20%氢氧化钾溶液;1%半胱氨酸溶液;钙黄绿素混合指示剂:称取0.2 g钙黄绿素及0.1 g百里香酚酞与20 g氯化钾于研钵中混匀研细,在105℃烘干箱内干燥1 h,冷却后,盛于棕色磨口瓶备用;乙酸(1+9);EGTA标准溶液(0.010 mol/L):称取3.900 g EGTA(基准试剂),于400 mL烧杯中,加200 mL水,低温加热溶解,在不断搅拌下,滴加氢氧化钾溶液(2%)至EGTA完全溶解,冷却至室温,移入1 000 mL容量瓶,用水稀释至刻度,摇匀。
2.2 操作步骤
1)试样溶液的制备。称取0.250 0 g试样于预先盛有4 g混合熔剂的铂金坩埚中,混匀,并覆盖1 g混合熔剂,盖上坩埚盖,于1 000~1 050℃的高温炉内熔融8 min,取出稍冷却,置于盛有100 mL热水的250 mL烧杯中,加20 mL盐酸,在低温电炉上加热浸取至熔融物全部溶解后,用水洗净坩埚,移入500 mL容量瓶,以水洗净烧杯,冷却至室温,用水稀释至刻度,摇匀为母液,用于测定SiO2、P、TCa(实际为CaO与CaF2合量)。
2)硅钼蓝光度法测定SiO2。移取5 mL母液[1)]于100 mL容量瓶中,加10 mL钼酸铵溶液,摇匀,置于沸水浴中加热30 s,取出以流水冷却至室温,加25 mL草硫混酸,摇匀,立即加入5 mL硫酸亚铁铵溶液,用水稀释至刻度摇匀。用1~2 cm比色皿于波长680 nm处,以水为参比液测定吸光度。用含SiO2量相近的萤石标样,按同样分析方法操作,测定吸光度,换算SiO2含量。
3)铋磷钼蓝光度法测定P。移取50 mL母液[1)]于100 mL容量瓶中,加3 mL高氯酸混匀,加5 mL硝酸铋溶液,2 mL硫代硫酸钠溶液,10 mL抗坏血酸溶液,5 mL钼酸铵溶液,5 mL酒石酸钾钠溶液,用水稀释至刻度,摇匀。放置8~10 min,用3 cm比色皿于波长650 nm处,以水为参比液测定吸光度,用含P量相近的萤石标样,按同样分析方法操作,测定吸光度,换算P含量。
4)EGTA滴定法测定TCa。移取50 mL母液[1)]于250 mL烧杯中,加80 mL水,10 mL三乙醇胺,2 mL半胱氨酸溶液,2 mL硫酸镁溶液,摇匀,加20 mL氢氧化钾溶液,少量钙黄绿素混合指示剂,用EGTA标准溶液滴定,在玻璃棒搅拌下,由下而上观察至试液绿色荧光消失变为红色为终点(杯底需垫一块黑色纸)。
按下式计算TCa及TCaO的质量分数(%):

式中:C为EGTA标准溶液的浓度,mol/L;V1、V2分别为测定TCa及TCaO时滴定消耗EGTA标准溶液的体积,mL;40.08为Ca的摩尔质量,g/mol;56.08为CaO的摩尔质量,g/mol;m为称取试样量,g。
5)EGTA滴定法测定CaO。称取0.250 0 g试样于150 mL锥形瓶中,加40 mL乙酸(1+9),在沸水浴中加热25 min,取出,用中速定量滤纸过滤于500 mL容量瓶中,用热水洗涤6~8次。加15 mL盐酸于盛滤液的500 mL容量瓶中,冷却至室温,用水稀释至刻度,摇匀。移取50 mL上述试液于250 mL烧杯中,加80 mL水,10 mL三乙醇胺,2 mL半胱氨酸,2 mL硫酸镁溶液,搅匀,加20 mL氢氧化钾溶液,少量钙黄绿素指示剂,用EGTA标准溶液滴定,在玻璃棒搅拌下,由上而下观察至试液绿色荧光消失变为红色为终点(杯底需垫一块黑色纸)。
按下式计算CaO的质量分数(%):

式中V为滴定CaO消耗EGTA标准溶液体积,mL。6)氟化钙的质量分数(%)按下式计算:

3 实验结果与讨论
按实验方法测定CaO基脱硫剂中的TCa、CaO、CaF2、SiO2、P,结果见表1、表2。
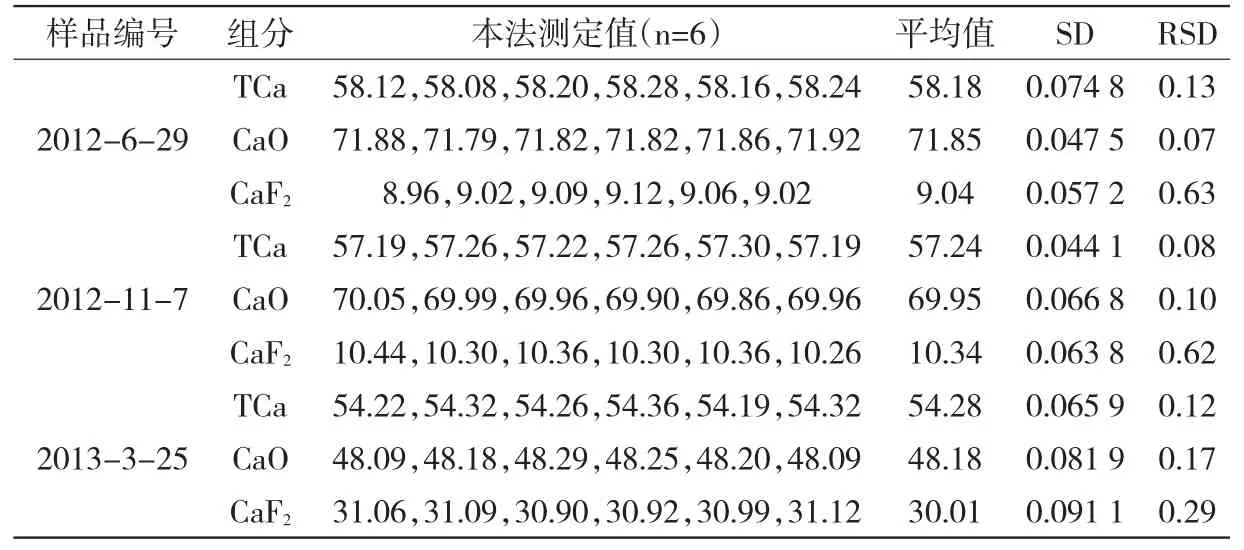
表1 CaO基脱硫剂中TCa、CaO、CaF2测定结果%
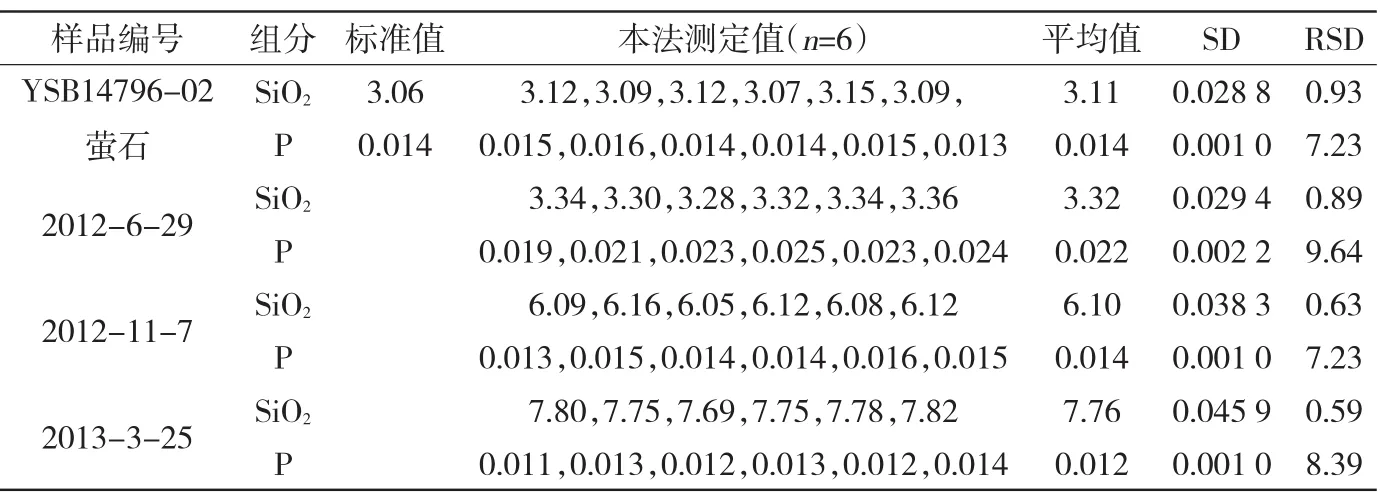
表2 CaO基脱硫剂中SiO2、P测定结果%
由表1、表2可知,该方法的分析结果误差完全在国标要求误差范围内,精密度较高,TCa、CaO、CaF2、SiO2、P的RSD分别为:0.13%、0.07%、0.29%、0.59%、7.21%。满足质量检验需要。
3.1 溶解试样条件的选择
CaO基脱硫剂是由石灰与萤石按一定比例混合制成的产品。如用混合熔剂在高温熔融试样,以稀盐酸浸取熔融物制成的试液,只能分析CaO和CaF2的总量,不能分别测定其含量。为此,利用CaO和CaF2的特性,先用稀乙酸溶解处理试样,CaO被稀乙酸溶解,而CaF2不被溶解,以定量滤纸过滤,而达到CaO与CaF2分离的目的。将滤液定容,移取部分试液,调节试液pH值≥13,用EGTA滴定法测定CaO的含量,取得了较好的效果。
试样中的碳酸钙,同时也被稀乙酸溶解使CaO结果偏高,但因CaO基脱硫剂中萤石分量少,因而含CaCO3量很少,可以忽略不计。在用稀乙酸(1+9)溶解试样时,CaO先生成Ca(OH)2,再被稀乙酸溶解生成乙酸钙,所以要用温热稀乙酸洗涤,以防止Ca(OH)2吸附在CaF2沉淀物上使CaO结果偏低。以每次用8 mL稀乙酸洗涤6~8次为宜。
3.2 EGTA滴定法测定Ca分析
1)干扰元素的消除。EGTA滴定法测定Ca时,三乙醇胺是掩蔽剂,因三乙醇胺与Fe、Al等金属离子形成的络合物比Ca离子与EGTA生成的络合物更稳定,因而起掩蔽作用,能消除对Ca滴定时的干扰[3]。少量重金属离子封闭钙指示剂,使滴定终点拖长或滴定不出终点,可加半胱氨酸掩蔽消除之[5]。
2)加硫酸镁的作用。由于CaO基脱硫剂中含少量Mg,以钙黄绿素指示剂用于EGTA滴定Ca时,看不到突变终点的变化,表明Ca2+离子单独存在时,钙黄绿素指示剂变色由绿色荧光消失变红色,终点不敏锐。若有Mg2+离子存在时,当试液pH值≥13时,Mg2+离子将形成Mg(OH)2沉淀,Mg2+不干扰Ca的测定,反而使终点比Ca2+离子单独存在时更加敏锐。因此本法测定Ca时,加入适量硫酸镁溶液,利用置换滴定原理来提高Ca终点变化的敏锐性,使分析Ca结果更加准确[6]。
3)钙黄绿素指示剂用量的选择。Ca指示剂用量对分析Ca结果有影响,用量太多,试液颜色深,终点提前到达,使Ca结果偏低,用量太少,试液颜色浅,到达终点拖长,使结果偏高,所以指示剂要适量。
3.3 硅钼蓝光度法测定SiO2分析
1)显色条件的选择。硅钼蓝光度法测定SiO2时,实验证明当室温低于10℃时,即使放置30 min也不能发色完全,最好用沸水浴中加热30 s显色。
2)P、As干扰的消除。硅钼蓝光度法测定SiO2时,P、As也能与钼酸铵生成络合物被还原成钼蓝,当加入草硫混酸后,P、As、络合物首先被破坏,但随着时间过长硅钼络合物也能被破坏。所以,通常在草硫混酸加入1 min内加入硫酸亚铁铵,否则Si结果偏低。
3.4 铋磷钼蓝光度法测定P分析
1)显色酸度的选择。铋磷钼蓝络合物的形成酸度各说不一,本方法采用正交实验法进行选择,并实验了试剂的加入顺序,结果表明,酸度为0.51~0.7 mol/L的高氯酸介质中是最佳条件。在氧化性酸介质中,磷铋钼三元络合物被较弱的还原剂抗坏血酸在室温条件下迅速还原成铋磷钼蓝,借此进行光度法测定P。
2)干扰元素的消除。试液中大量Ca元素不影响P的测定,Si、As等元素均能形成钼蓝,本方法用酒石酸钾钠和硫代硫酸钠掩蔽Si、As。由于Si的室温显色酸度在0.08~0.4 mol/L盐酸或硝酸介质中,本操作是在0.51~0.70 mol/L高氯酸介质中显色,使硅钼蓝的形成非常慢,因此改为8~10 min显色后测定吸光度,可消除Si的干扰。
4 结论
利用CaO易溶解于稀乙酸而CaF2不溶解于稀乙酸的特性,将CaO基脱硫剂试样用稀乙酸溶解处理,达到CaO与CaF2分离的目的,用EGTA滴定法测定CaO量;计算出CaF2量;另称取一份试样用混合熔剂在高温条件下熔融,以稀盐酸浸取酸化,定容后,用EGTA滴定法测定TCa量;剩余试液用分光光度法测定SiO2和P。实现了CaO基脱硫剂中TCa、CaO、CaF2、SiO2、P的联合快速测定。平行样品分析结果的误差,完全在国标允许误差范围内,满足炼钢生产质量要求及进厂CaO基脱硫剂原材料质量检验把关工作的需要。
[1]陈寿椿.重要无机化学反应[M].上海:上海科学技术出版社,1983:374.
[2]R·浦希比.实用络合滴定法[M].广州:中山大学出版社,1987:420-421.
[3]国家机械工业委员会.工业分析[M].北京:机械工业出版社,1988:258-260.
[4]鞍钢钢研所.实用冶金分析[M].沈阳:辽宁科学技术出版社,1990:561.
[5]王际祥,马淑华.石灰石、白云石中氧化钙和氧化镁的分析EGTA—CYDTA容量法的试验[J].山东冶金,1993,15(1):42-45.
[6]曹玉红,高卓成,王慧卿,等.碳镁球团复合脱氧脱硫剂中CaO、MgO、SiO2的测定[J].山东冶金,2013,35(4):41-43.
United Determination of the TCa,CaO,CaF2,SiO2and P in CaO Based Desulfurizer
WANG Junxiu,XUE Minghao,HOU Junkun,MA Qingwen,WEI Wensheng
(Shandong Luli Iron and Steel Co.,Ltd.,Shouguang 262724,China)
The sample was melted in the mixed solvent containing boric acid,and then constant volume was fixed after acidification by dilute hydrochloric acid.Now,a part of test solution was taken to determine silicon dioxide,phosphorus and TCa respectively by silicon molybdenum blue method,bismuth phosphorus molybdenum blue method and EGTA titrimetric method through controlling their acidity during the determination of each elements.Using the characteristics of the calcium oxide is easy to be dissolved in dilute acetic acid,while the calcium fluoride is insoluble in dilute acetic acid,another sample was taken and dissolved by dilute acetic acid solution.And the constant volume of solution was fixed after filtration and separation.A part of solution was taken to determine CaO by EGTA titrimetric method.The content of CaF2was calculated.The determination results were satisfied,the method was feasible and suitable for the daily production need in metallurgy factory.
CaO based desulfurizer;TCa;CaO;spectrometry;EGTA titrimetric method
O657.3;O655.22
A
1004-4620(2015)04-0045-03
2015-03-18
王俊秀,女,1973年生,1994年毕业于潍坊学院化学分析专业。现为山东鲁丽钢铁有限公司质检科科长,高级工程师,从事材料测定方法的试验研究修订及质量管理工作。

