石墨烯/炭黑杂化材料:新型、高效锂离子电池二元导电剂
李 用 ,吕小慧,苏方远,3,贺艳兵,李宝华,杨全红,,康飞宇
(1.清华大学深圳研究生院,深圳炭功能材料工程实验室,深圳市石墨烯重点实验室,广东 深圳 518055;2.天津大学 化工学院,天津 300072;3.中国科学院山西煤炭化学研究所,炭材料重点实验室,山西 太原 030001;)
1 前言
电动汽车、规模化储能及电动工具等新型应用领域的兴起对锂离子电池的性能提出了更高要求[1]。为了保证快速能量存储的性能,锂离子电池电极必须兼具良好的电子导电性和离子传导性。然而常用的锂离子电池正极材料(钴酸锂、锰酸锂及磷酸铁锂等)和负极材料(钛酸锂等)都具有较低的电子导通特性,严重制约了锂离子电池材料的容量发挥。为了提高倍率和循环性能,锂离子电池电极需要添加导电剂以构建有效的导电网络[2]。然而过多添加不参与能量存储的导电剂会降低电极的能量密度,因此需要寻求添加量较少的高效导电添加剂[3]。石墨烯纳米片(GN)是高导电率的二维柔性材料,在能源领域已被广泛研究[4-7]。笔者所在课题组较早开展了石墨烯作为LiFePO4正极材料导电剂的应用研究,提出了石墨烯与正极材料颗粒的“点-面”接触导电模型,证明石墨烯是一种高效的锂离子电池导电剂;同时发现用于商品化电池时,石墨烯的存在对锂离子传输过程产生一定的阻碍,在大倍率下充放电时性能迅速降低[2,8]。Zhang 等通过探究石墨烯导电剂在钛酸锂负极中的作用,同样发现过多的GN 将阻碍锂离子的传输过程[9]。为了解决该问题,本课题组在商品化电池中使用石墨烯与炭黑共混作为二元导电剂,减少石墨烯用量,在改善电池功率性能的同时并发现了二者的协同作用,同时使用质量分数1%石墨烯和1%炭黑的电池时不论在输出电压还是容量性能都优于使用2%石墨烯的电池[8]。Jiang 等采用不同比例石墨烯与炭黑(CB)作为锰酸锂的二元导电剂,也发现能更加有效地构建导电网络[10]。
目前文献报道的石墨烯/炭黑二元导电剂都是在电极制备过程中通过物理混合而成,难以保证二者的良好分散与接触。为了进一步提高导电效果,笔者将二元导电剂中的石墨烯/炭黑在电极制备之前通过化学作用结合到一起,利用水热自组装方法制备新型杂化材料作为锂离子电池正极二元导电剂,考察其对LiFePO4正极材料倍率性能的提升作用。
2 实验
2.1 材料制备
采用改进的Hummers 方法制备氧化石墨[11]。将所制氧化石墨与去离子水1∶1质量比强超声分散(细胞粉碎机,功率300 W)2 h,形成氧化石墨烯溶液,以氧化石墨烯与炭黑的质量比例(4∶1,8∶1,18∶1)加入炭黑,为了增加炭黑的分散性,同时加入表面活性剂CTAB,超声分散2 h,制备出氧化石墨烯/炭黑的均匀混合液。移入100 mL 水热反应釜中180 ℃反应12 h,过滤后冷冻干燥,分别在300 ℃和900 ℃氩气气氛下进行热处理2 h,所得样品即为石墨烯/炭黑杂化材料。对所得的材料通过质量比和热处理温度进行标记,如4GN/CB-300 表示水热前氧化石墨烯与炭黑的质量比为4∶1,随后经300 ℃热处理的样品。
2.2 表征方法
采用X 射线衍射(XRD,日本理学RigakuD/max 2500 Cu 靶衍射仪,测试电流100 mA,电压40 kV,扫描速度5°/min)对样品进行结构表征,采用扫描电子显微镜(SEM,日本日立Ultra-high Resolution SEM S-4800 HITACH S4800,测试电压为10 kV)和透射电子显微镜(TEM,日本电子株式会社JEOL-2011,测试电压为200 kV)对样品进行形貌分析表征。
2.3 电池组装与测试
采用LiFePO4(深圳德方纳米公司)作为活性物质,聚偏氟乙烯(PVDF)作为粘结剂,将各种导电剂、LiFePO4及粘结剂加入 N-甲基吡咯烷酮(NMP),超声、搅拌分散后得到均匀电池浆料。为了避免PVDF 对电池测试结果的影响,PVDF 的使用质量分数都固定为8%,导电剂添加量为5%和10%的电极中导电剂与LiFePO4的质量比分别为5∶87 和10∶82。将所得电池浆料使用涂膜器涂覆在铝箔上,涂覆间隙为90 μm,80 ℃真空中12 h 烘干后冲片称量,然后在氩气气氛下的手套箱中装配成CR2032 型扣式电池。电池倍率性能和循环性能采用蓝电(Land 2001A,武汉市蓝电电子股份有限公司)对电池进行恒流充放电测试,电压范围为2.0~4.2 V(vs Li+/Li);采用电化学工作站(ZAHNER Im6ex,德国)对电池进行交流阻抗表征。
3 结果与讨论
图1 为GO、CB、300 ℃和900 ℃热处理后的石墨烯/炭黑杂化材料的XRD 谱图。可以看出,GO的XRD 曲线在2θ=12°处存在一个尖锐的衍射峰(层间距d=0.754 nm),此处衍射峰是因为氧化石墨中的石墨片层间被引入了含氧官能团和水分子,而使石墨片层间距增大(理想石墨的层间距为0.34 nm)[12]。在2θ=24.8°处炭黑衍射谱有一个较宽的衍射峰(d=0.366 nm),这主要是因为炭黑内部的杂乱结构所导致。从GN/CB-300 和GN/CB-900 样品XRD 谱图可以看出,GO 的特征峰消失,表明水热过程和热处理过程石墨片层间的官能团脱除[13]。

图1 GO,CB,GN/CB-300 和GN/CB-900 的XRD 谱图Fig.1 XRD patterns of GO,CB,GN/CB-300 and GN/CB-900.
GN/CB-300 和GN/CB-900 分别在2θ=25.2°和2θ=26°处有一个较宽的衍射峰,层间距分别为0.36、0.35 nm,并且热处理温度升高,峰位右移,层间距逐渐变小,说明900 ℃热处理后官能团进一步脱除。
图2 为GN/CB-900 的SEM 和TEM 照片。由图2a 可以看出,水热自组装法制备的GN/CB-900材料的CB 颗粒与石墨烯片层结合,CB 颗粒均匀分布于GN 片层的边缘和表面,由于CB 颗粒的引入,GN 片层表面褶皱,片层不易团聚。由图2b 可以清楚看到GN/CB-900 中的GN 片层是透明薄片,表面均匀分布着链状的炭黑颗粒。样品在做TEM 之前经过了强超声处理,但仍可以明显看到CB 颗粒与GN 片层的紧密结合,表明CB 颗粒与GN 在水热过程中能够形成较强的结合,稳定性高于简单的物理混合。
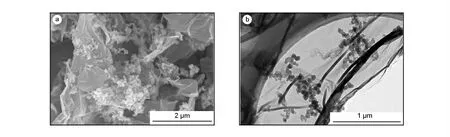
图2 GN/CB-900 的(a)SEM 和(b)TEM 照片Fig.2 (a)SEM and (b)TEM images of GN/CB-900.
图3 为使用不同导电剂的LiFePO4材料的高倍率性能对比。图3a 是使用300 ℃热处理后的GN/CB 杂化材料作为导电剂时LiFePO4倍率性能。可以看出,没有使用导电剂时,LiFePO4容量性能非常低,添加所制二元导电剂后容量性能有明显提升,0.5 C时比容量由95 mAh/g 提高到了153 mAh/g。然而随着放电电流持续增加,容量性能迅速降低,5 C 时已降到60 mAh/g 以下,10 C 时部分样品的容量已低于10 mAh/g,此时与没有使用导电剂的LiFePO4性能没有区别。这主要是因为GN 处理温度较低,大量存在的表面含氧官能团及缺陷结构导致其电导率不够理想。炭黑含量的不同对LiFePO4也有不同的影响,炭黑含量越多,使用二元导电剂的LiFePO4倍率性能越好,并且倍率越高效果越明显:5 C 倍率下,使用4GN/CB-300、8GN/CB-300、18GN/CB-300 的LiFePO4的比容量分别为60 mAh/g、50 mAh/g及5 mAh/g,进一步说明300 ℃处理的GN 导电性较差,LiFePO4电化学性能的提高主要归因于炭黑颗粒的存在。
为了进一步提高所得二元导电剂的性能,对GN/CB 杂化材料在900 ℃条件下进行了热处理。图3b 为GN/CB-900 作为LiFePO4导电剂的倍率性能与单独使用GN 和CB 导电剂的对比。经900 ℃热处理后GN/CB 二元导电剂性能有了较大的提升,使用不同GN 与CB 配比的二元导电剂的各电极中LiFePO4在低倍率下的比容量无差别。在0.5 C 倍率下的比容量都在150~153 mAh/g 之间,然而随着放电倍率增加,容量差别变得越来越明显,在10 C 倍率下,8GN/CB-900 的导电剂效果优于4GN/CB-900 和18GN/CB-900。该规律与300 ℃热处理的二元导电剂不同,主要是因为900 ℃热处理后GN 电导率大幅度提高所致。此时二元导电剂的电导率不再需要依靠增加CB 的配比来保证,导电剂效果的发挥主要依靠二者的协同作用。CB 含量太少时,GN 量较多,此时过多的GN 将会对锂离子的传输过程产生阻碍,电池倍率性能变差;而CB 含量太多时,GN 含量过少,不能保证较好的协同作用。在本实验条件下,8GN/CB-900 表现出了最优的结果,既可以构筑一个有效的导电网络,又能提供快速的离子传输通道。
图3b 为GN 和CB 单一导电剂和二元导电剂的性能对比,可以明显看出所制二元导电剂具有良好的性能优势。使用5%GN-900 的LiFePO4在5 C和10 C 的放电倍率下容量分别为85 和51 mAh/g(与商品化电池中使用GN 导电剂的倍率性能具有一定的差别,这主要是因为在扣式电池制备过程中电极涂覆厚度较薄,活性物质的面密度显著低于商品化电池)。在所有导电剂中性能下降最快,这说明在该条件下GN 导电剂仍会影响锂离子在高电流密度条件下的传输行为,导致电极内部电解液浓度不均匀,降低了LiFePO4材料的性能发挥。5%8GN/CB-900-LFP 和10% CB-LFP 电极在10 C 倍率下的比容量分别为:73 和62 mAh/g,前者比后者的容量性能提高了17.7%。考虑到电极中LiFePO4含量不同(两个电极中粘结剂用量都为8%,故前者LiFePO4为87%,后者为82%),则按照整个电极质量考虑容量发挥,前者为63.5 mAh/g,后者为50.8 mAh/g,前者比后者提高了近25%。由图3c和d 中使用10%CB 和5%8GN/CB-900 导电剂的LiFePO4的充放电曲线可以看出,随着倍率提高,虽然两者的电压平台持续降低,但后者放电平台明显高于前者,进一步揭示了二元导电剂的突出性能。
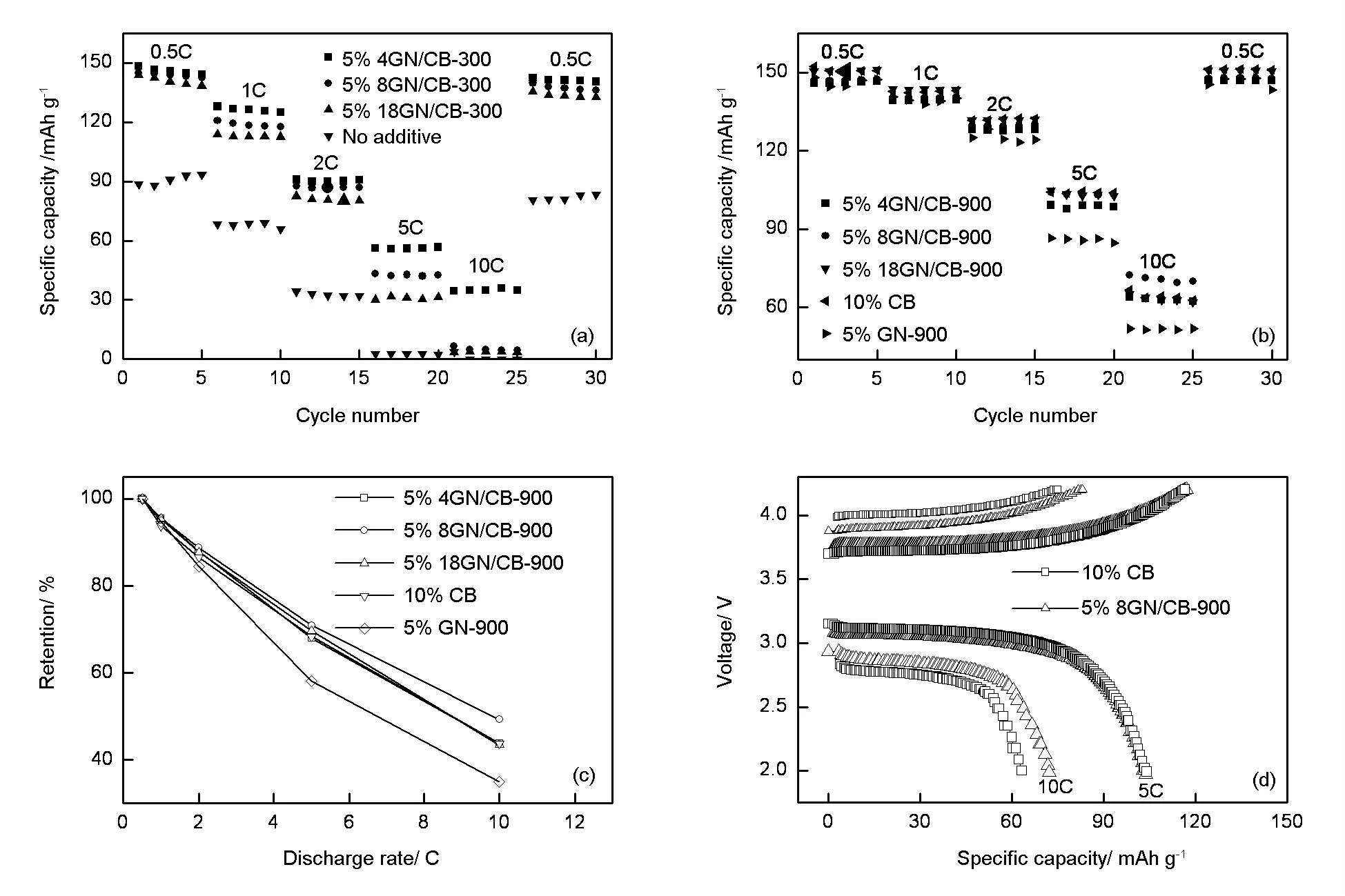
图3 使用不同导电剂的LiFePO4倍率性能对比:(a)300 ℃处理的二元导电剂,(b)900 ℃处理的二元导电剂及石墨烯与炭黑导电剂,(c)容量保持率,(d)使用炭黑和二元导电剂的LiFePO4充放电曲线Fig.3 Rate performance comparison of LiFePO4with different conductive additives.(a)Binary conductive additive treated at 300 ℃,(b)binary conductive additive treated at 900 ℃,GN and CB,(c)retention of specific capacity and(d)the charge/discharge profile of LiFePO4using CB and binary conductive additive,respectively.
图4 为使用5% 二元导电剂和10% CB 的LiFePO4电极的EIS 和循环性能图。从图4a 可以看出,两电极的EIS 曲线都包括中高频区域的弧形部分以及低频区域的斜线两个部分。通过内部插图的等效电路图拟合可以得到5% 8GN/CB-900 二元导电剂和10% CB 导电剂的电极的电化学反应电阻(Rct)值分别为58 Ω 和80 Ω,前者具有较小的阻抗。同时,使用二元导电剂的电极在低频区的扩散直线具有较大的斜率,表明电极内部锂离子具有较快的扩散系数,这都与图3 中的倍率性能的结果相一致。图4b 为两个LiFePO4电极的1 C 倍率下循环曲线,由图可知,与使用10%CB 导电剂的电极相比,使用5% 8GN/CB-900 的电极循环100 圈后的容量保持率98%以上,表现出良好的循环稳定性。
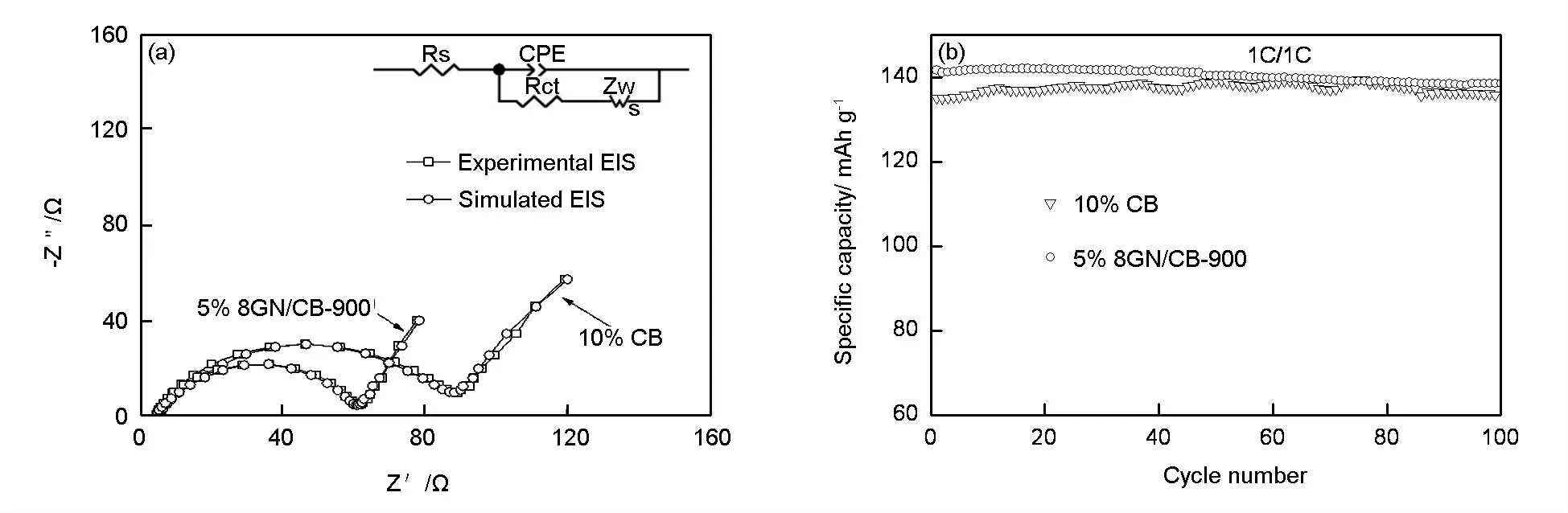
图4 二元导电剂与CB 导电剂性能对比:(a)交流阻抗,(b)循环稳定性Fig.4 Comparison of binary conductive additive and CB additive:(a)EIS and (b)cycle performance.
4 结论
石墨烯/炭黑杂化材料二元导电剂可以有效改善石墨烯导电剂阻碍锂离子传输过程的问题,使用5% 900℃热处理之后的二元导电剂的LiFePO410 C 时比容量比为73 mAh/g,优于使用10%炭黑导电剂时的LiFePO4。按照整个电极质量计算,前者的比容量性能比后者提高了近25%,同时也表现出了更好的循环性能。
[1]Pumera M.Electrochemistry of graphene,graphene oxide and other graphenoids:Review[J].Electrochemistry Communications,2013,36:14-18.
[2]Su F Y,You C,He Y B,et al.Flexible and planar graphene conductive additives for lithium-ion batteries[J].Journal of Materials Chemistry,2010,20(43):9644-9650.
[3]Dominko R,Gaberscek M,Drofenik J,et al.The role of carbon black distribution in cathodes for Li ion batteries[J].Journal of Power Sources,2003,119-121:770-773.
[4]Ak Geim K N.The rise of graphene[J].Nature Materials,2007,6:183-191.
[5]Tan Y B,Lee J M.Graphene for supercapacitor applications[J].Journal of Materials Chemistry A,2013,1(47):14814-14843.
[6]Venkateswara Rao C,Leela Mohana Reddy A,Ishikawa Y,et al.LiNi1/3Co1/3Mn1/3O2-graphene composite as a promising cathode for lithium-ion batteries[J].ACS Applied Materials &Interfaces,2011,3(8):2966-2972.
[7]Chang H,Wu H.Graphene-based nanocomposites:preparation,functionalization,and energy and environmental applications[J].Energy &Environmental Science,2013,6(12):3483.
[8]Su F-Y,He Y-B,Li B,et al.Could graphene construct an effective conducting network in a high-power lithium ion battery[J].Nano Energy,2012,1(3):429-439.
[9]Zhang B,Yu Y,Liu Y,et al.Percolation threshold of graphene nanosheets as conductive additives in Li4Ti5O12anodes of Li-ion batteries[J].Nanoscale,2013,5(5):2100-2106.
[10]Jiang R,Cui C,Ma H.Using graphene nanosheets as a conductive additive to enhance the capacitive performance of alpha-MnO2[J].Electrochimica Acta,2013,104:198-207.
[11]Lv W,Tang D M,He Y B,et al.Low-temperature exfoliated graphenes:vacuum-promoted exfoliation and electrochemical energy storage[J].ACS Nano,2009,3(11):3730-3736.
[12]Wang Q,Yan J,Fan Z,et al.Mesoporous polyaniline film on ultra-thin graphene sheets for high performance supercapacitors[J].Journal of Power Sources,2014,247:197-203.
[13]Zhao B,Liu P,Jiang Y,et al.Supercapacitor performances of thermally reduced graphene oxide[J].Journal of Power Sources,2012,198:423-427.
[14]Xu J,Gai S,He F,et al.A sandwich-type three-dimensional layered double hydroxide nanosheet array/graphene composite:fabrication and high supercapacitor performance[J].Journal of Materials Chemistry A,2014,2(4):1022-1031.
[15]Giri S,Ghosh D,Das C K.In situ synthesis of cobalt doped polyaniline modified graphene composites for high performance supercapacitor electrode materials[J].Journal of Electroanalytical Chemistry,2013,697:32-45.
[16]Varzi A,Taeubert C,Wohlfahrt-Mehrens M,et al.Study of multi-walled carbon nanotubes for lithium-ion battery electrodes[J].Journal of Power Sources,2011,196(6):3303-3309.

