乙醇-水共沸物系新型分离工艺研究进展
朱 炜,刘 斌,司 倩,马涛涛,蔡信彬,樊增禄
(1.西安工程大学 环境与化学工程学院,陕西 西安710048;2.西安工程大学 纺织与材料学院,陕西 西安710048)
0 引 言
无水乙醇作为一种性能优良的有机溶剂,被广泛用于化妆品、制药、电子航天工业等行业.有些国家已将无水乙醇与汽油混合而成的汽油醇作为动力燃料[1-4].但当乙醇浓度达到95.57%时,乙醇与水将形成共沸物导致普通精馏无法继续进行分离.一直以来,乙醇-水物系的分离都是化工领域的一个研究热点.传统的共沸精馏和萃取精馏因在分离过程中耗能大,会使用对人身体有害的第三组分,所以这样技术必将逐渐被淘汰,进而被清洁的新工艺所替代,如加离子液体萃取精馏,膜技术和吸附法等.
1 精馏工艺
1.1 共沸精馏
共沸精馏就是向共沸物中添加第三种组分,与欲分离组分形成二元最低恒沸物或三元最低恒沸物,恒沸物的沸点较原共沸物要低很多,从而使溶液变成“恒沸物-纯组分”的蒸馏.加入的第三种组分称为夹带剂或恒沸剂.
夹带剂是共沸精馏的核心,理想的夹带剂应满足下述要求:①与欲分离组分形成恒沸物,其沸点与另一组分的差别至少10℃;②尽量与组分中含量少的组分形成恒沸物,且夹带的量尽可能高;③恒沸物冷凝后可分为轻、重两相,使夹带剂易于回收;④满足工业要求,如来源广、价格低、热稳定、无腐蚀、无毒等.
可用作乙醇-水分离的共沸剂有:苯,正戊烷[5],二乙醚[6],环己烷[7],正己烷[8],正庚烷[9],异辛烷,丙酮[10],聚合物[11]等.其中,苯和环己烷是使用最多的两种共沸剂.
1.2 萃取精馏
萃取精馏也是向共沸物中加入第三组分,通过第三组分与原溶液中各组分的相互作用,改变了原组分间的相对挥发度,从而打破共沸物系的共沸点.所加第三种组分称为萃取剂.
整个萃取精馏的关键是萃取剂的选择.根据所加萃取剂的不同萃取精馏可分为普通萃取精馏、溶盐萃取精馏、复合萃取精馏和加离子液体萃取精馏.
1.2.1 普通萃取精馏 普通萃取精馏的萃取剂是有机溶剂,其需满足的条件有:选择性强,溶解度大,沸点适当,满足工业要求(同夹带剂)等.可用于乙醇-水分离的有机溶剂萃取剂有:乙二醇,二乙醚,甲苯和呋喃等.
1.2.2 溶盐萃取精馏 溶盐萃取精馏用盐溶液作萃取剂,利用溶盐的“盐效应”打破组分间的共沸点来实现精馏.溶盐萃取精馏的最大优点是盐对组分间相对挥发度的改变程度大,但固体盐的结晶会引起设备堵塞、腐蚀问题.
可用 于 溶 盐 萃 取 精 馏 的 盐 有:CaCl2[12],CoCl2[13],CuCl2,NiCl2[14],SrBr2[15],NaAc/KAc[16],Ca(NO3)2,NaI/KI[17],葡萄糖[18],HgCl2/LiCl[19]等.其中 HgCl2和 LiCl是上述盐中最有效的.
1.2.3 复合萃取精馏 复合萃取精馏采用将盐与有机溶剂形成混合物的方式提取萃取剂,如乙二醇+CaCl2[20]等.它是溶盐萃取精馏和普通萃取精馏的结合,并综合了各自的优点.与普通萃取精馏相比,复合萃取精馏能减少溶剂循环量,减少能耗和设备投资.
1.2.4 加离子液体萃取精馏 由于传统有机溶剂萃取剂易挥发,再生能耗大,固体盐会腐蚀、堵塞设备.因此选择或开发“绿色”萃取剂将势在必行.离子液体具有低蒸汽压、无毒、无腐蚀性等独特优点,因此有望作为“绿色“萃取剂而取代传统的有机溶剂和固体盐类[21-23].可作为萃取剂用于乙醇-水分离过程的离子液体如表1所示[24-34].
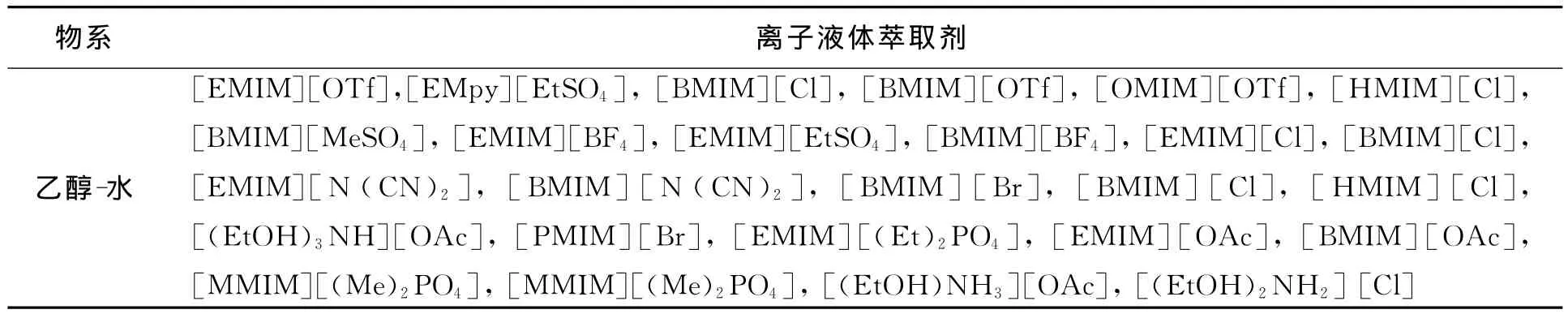
表1 可用于乙醇-水分离的离子液体Table 1 The ionic liquid used for separation of ethanol and water
2 膜分离工艺
膜分离技术是近年发展起来的一项高新技术,它以膜为分离介质,并在膜的两侧施加推动力(如压力差、电位差等),使预分离组分中的某一组分优先通过膜,从而达到分离的目的.目前应用于乙醇-水体系分离的膜分离技术主要有两种,分别是渗透汽化和膜接触器.
2.1 渗透汽化及蒸汽渗透
渗透汽化是液体混合物在膜下侧负压的作用下,利用膜对被分离混合物中某种组分有优先透过的特点,使该组分渗透通过膜,在膜的下侧汽化除去,实现分离的膜技术.蒸汽渗透与渗透汽化原理相似,唯一区别就是蒸汽渗透为气相进料,相变过程通常发生在进入装置之前,而在该过程中为蒸汽相渗透通过膜.表征渗透汽化的两个基本参数是渗透通量和分离因子.
渗透汽化的关键是选用合适的膜.用于醇-水渗透汽化分离的膜主要分为亲水性膜(优先透过水,适宜分离低水量的醇水溶液)和亲醇性膜(优先透过醇,适宜分离低醇量的醇水溶液)两类.但不管是亲水性膜还是亲醇性膜都很难同时满足渗透通量和分离因子两个要求.因此,除对原有两种膜进行改性外,还出现了共混膜,如聚乙烯醇-壳聚糖共混膜和硅橡胶-壳聚糖共混膜.可用于乙醇水分离的渗透汽化膜有:磺化聚砜膜[35],光化聚合复合膜[36],芳香酰胺膜[37],锂化聚砜膜[38],壳聚糖复合膜[39]等.
渗透汽化透水膜最早实现工业化.GFT,Kalsp,Lurgi等公司已经建立起采用平板膜的工业化渗透汽化或蒸汽渗透工艺工厂[40].但是这些装置的尺寸很大,操作不便,因而效率不高.Tsuyumoto[40]等在实验工厂进行了采用中空纤维膜组件生产无水乙醇的渗透汽化实验:用6m2膜处理流率为100kg/h的含水量为6%(质量分数)的乙醇水溶液,持续两个月,乙醇损失极低.Mulder和Smolder[41-42]对渗透汽化法分离乙醇-水的机理进行了研究.Nguyen[43]等使用聚丙烯腈/聚乙烯吡咯烷酮共混膜进行了渗透汽化分离实验.Wenzlaff[44]等表征了三醋酸纤维素和苯乙烯-丁二烯膜交联化的性能.Sander和Soukup[45]报道了他们设计和运行的乙醇脱水的渗透汽化工厂.
唐俏瑜[46]等将聚二甲基硅氧烷/聚偏氟乙烯复合膜应用于乙醇-水的渗透汽化分离,考察了膜交联温度、操作温度、物料浓度和膜下侧压力对分离性能的影响,最终分离因子为8.23,渗透通量为281.36g/(m2·h).曾小雅[47]等采用BPPO(溴代聚苯醚)非对称膜考察了添加剂含量、BPPO浓度、进料组成和温度对乙醇-水渗透汽化分离性能的影响.结果当进料温度为60℃,乙醇含量为50%,添加剂浓度为9.9%,BPPO含量为10%时,渗透通量为236.4g/m2·h,分离因子达16.74.纪树兰[48]等研究了聚苯醚含量、进料乙醇含量、进料温度对聚苯醚/聚砜复合膜分离乙醇水的渗透汽化性能的影响,结果当复合膜中聚苯醚含量为14%,进料温度为60℃且含乙醇10%时,渗透通量为157.2g/m2·h,乙醇的选择系数为15.6.Xia[49]等利用聚乙烯醇/陶瓷复合膜渗透汽化工艺来分离乙酸乙酯/乙醇/水三元共沸物系,考察了操作温度、进料水含量和流率对于分离性能的影响,并用Flory-Huggins理论研究膜与渗透剂间的相互作用,用UNIFAC模型描述膜中渗透剂的活度.牛洪金[50]等使用PDMS(聚二甲基硅氧烷)-PPO(聚苯醚)嵌段共聚物非对称渗透汽化膜渗透汽化来分离乙醇-水,分别研究了铸膜液浓度、膜后侧压、进料流速对分离性能的影响.结果当嵌段共聚物质量分数为11%,进料流速为0.267L/min,乙醇含量为5%,温度为60℃,膜后侧压为10kPa时,渗透通量达850.7g/m2·h,乙醇的选择系数为8.78.
2.2 膜接触器
膜接触器是以多孔的疏水膜作为传质接触界面,并与吸收、萃取等单元操作相耦合的一种膜分离技术.膜接触器能提供比传统的接触设备大500倍的接触面积(液—液接触),两流体的流速也可独立控制.
Cussler[51-52]提出一种可用于精馏操作的膜接触器,该膜接触器采用非选择性的微孔聚乙醚(内涂聚二甲基硅氧烷)中空纤维膜代替传统的精馏填料,并将之应用于异丙醇-水体系的分离.2007年,林兰[53]开发了非选择性的微孔聚醚砜膜(内有甲基硅氧烷涂层)的膜接触器,并将其用于乙醇-水体系的分离.研究结果表明,将新型中空纤维膜接触器作为精馏填料,在操作弹性、产能以及分离效率等方面均具有明显优势.2011年,李娜[54]将经PDMS(聚二甲基硅氧烷)涂覆改性的PVDF(聚偏氟乙烯)复合膜组件作为结构填料用于乙醇-水体系分离.结果表明,膜的孔隙率为28.7%,溶胀度为84%,精馏效率提高了59%,液相总传质系数为5.815×10-3cm/s.
3 吸附工艺
由于固体存在表面力,当流体与固体接触时,流体中的某些物质有附着于固体表面的趋势,这种现象称为吸附.被吸附的流体叫吸附质,固体叫吸附剂.吸附的逆过程称为脱附.吸附法就是利用吸附剂对流体混合物中不同组分的选择性吸附实现分离的方法.
吸附剂的性能对吸附分离的技术经济指标起着决定性作用.工业吸附剂的要求有:表面积大,选择性高,机械强度好,化学稳定性和热稳定性好,廉价易得等.可用于乙醇-水分离的吸附剂主要有分子筛和生物质两大类.
3.1 分子筛吸附
分子筛是具有均匀微孔结构的硅铝酸盐化合物.分子筛能把比其直径小的分子吸附到孔腔内部,并对极性分子和不饱和分子进行优先吸附.对于乙醇-水物系而言,水和乙醇的临界分子直径分别是2.7A和4.7A.因此,水分子可进入3A分子筛内部,加之分子筛对强极性水的吸引作用被吸附在分子筛内部,而乙醇分子则被阻挡在外,从而实验水与乙醇的吸附分离.
Ishikawa[55]等最先报道用沸石分子筛分离乙醇/水的研究,结果表明,在352.15~362.15K下,分离因子达到1 633,渗透通量为0.1kg/m2·h.工业规模的乙醇脱水中,钾和钠沸石也被用到[56].Carmo[57]将3A沸石作为吸收剂用于乙醇-水的变压吸附工艺中,考察了进料量、吸附压力和温度、解吸压力和温度对于浓缩效果、回收率、产率及总循环时间的影响,并将实验结果用经验方程进行了拟合,最后得到了该工艺的最佳操作条件.李浩[58]采用分子筛吸附法制取无水乙醇,得到了水在3A分子筛上的吸附等温曲线模型,并对吸附过程、脱附过程的工艺条件,以及整个工艺流程进行了探讨.范荣玉[59]研究了3A,4A,5A分子筛对乙醇中微量水的吸附性能,结果表明4A分子筛的吸附效果最好,由此测定了不同温度下乙醇中微量水在4A分子筛上的静态吸附平衡数据,并用Langmuir和Freundlic两个吸附等温式分别进行拟合,还采用固定床测定了不同粒径、初始浓度、床层高度,流量下的动态穿透曲线.
3.2 生物质吸附
生物质吸附是将有机生物质作为吸附剂.生物质吸附剂除了拥有同分子筛一样的低吸附能耗以外,还有很多其自身特有的优势.比如生物质吸附剂的成本比较低廉(大量存在于自然界、废弃材料或农作物中),分离效果较好且再生能耗要小于分子筛.有时当所用吸附剂与生产燃料乙醇的原料相同时,可不需再生处理.
为使生物质吸附剂的比表面积更大,吸附效果更好,就必须对其进行改性.改性的方法主要有3种[60]:物理法、化学法和生物法.物理法主要是机械研磨、湿热处理等;化学法可分为两种:一种是使大分子变为小分子,如酸水解,另一种是使其变为大分子,如交联等;生物法则是利用酶的改性水解作用.由于物理方法改性效果不佳,浪费较大,目前研究主要侧重于酸水解和酶水解.与酸水解相比,酶水解工艺有着非常明显的优势:第一,酶水解可破坏淀粉的中心区域,形成较深的明显孔洞;第二,酶水解后的废料处理成本低且可再利用.所以,目前生物质吸附剂的改性主要采用酶水解法.
Ladisch[61]等分别研究了淀粉(玉米和马铃薯),木聚糖,纯纤维素和玉米渣作为气相分离乙醇-水混合物吸附剂的吸附效果,得到吸水能力的顺序为玉米淀粉>玉米渣>木聚糖>纯纤维素,并指出以上结果是由生物质中支链淀粉浓度不同造成,支链淀粉的浓度越大,吸附剂的吸水能力就越大.Benson和George[62]用一根变热吸附柱来评价三种木质素基吸附剂(漂白木浆,橡木木屑,红麻秆芯)的除水效率,绘制了临界点曲线来表征吸附剂的效率,并和淀粉基吸附剂进行了对比,还得到了水分子在吸附剂多孔基质中扩散的传质性能和传质区的速度和长度.Sowerby[63]等开发了一个用来描述在短小直径柱中的乙醇-水共沸物的气相吸附干燥过程的非等温非绝热模型,并将用模型计算出来的临界点曲线和温度曲线与实验结果进行了比较,还讨论了吸附和解吸过程中两层膜各自阻力的相对大小.韩秀丽[64]等研究了生物质复合物吸附剂对水和乙醇的气相吸附性能,测定了生物质复合物吸附剂吸附乙醇溶液中水的穿透曲线,考察了进料流速、进料浓度和床层高度对吸附穿透曲线的影响,也测定了再生后吸附剂的穿透曲线,找出了最佳再生条件.结果表明,吸附剂对水的最大吸附量可达20%,且再生后的吸附剂对水仍有很好的吸附能力.Wang[65]等通过比较五种淀粉基吸附剂的乙醇脱水穿透曲线,发现ZSG-1的效果最优(可得到99.7wt%的无水乙醇),成本和能耗低,可回收.还采用Bohart-Adamns方程描述了ZSG-1的吸附动力学,并计算了吸附热.李清明[66]等采用固定床吸附柱研究了马铃薯吸附剂对乙醇-水的气相吸附过程.结果表明,生产能力和透过时间随着时间的降低、粒径的变小、进料流量的降低和床层高度的增大而增大,每1千克吸附剂制得无水乙醇205.1g.张琳叶[67]等研究了甘薯吸附剂制备燃料乙醇的过程,重点考察了吸附过程中床层温度、进床气速、床层高度、甘薯粒度等因素对透过曲线的影响,并给出了吸附波移动速度、传质区长度的计算方法.
4 其他方法
Fullarton和Schlunder[68-69]提出了一种新型分离共沸物的工艺:扩散蒸馏.该工艺中液体在低于沸点下蒸发,然后在惰性气通道中扩散和冷凝.因此分离效果不仅与各组分的相对挥发度相关,还与它们在惰性气中的扩散有关.他们将该工艺用于乙醇-水的分离,发现所有实验结果可以用汽液相平衡和Stefan-Maxwell方程(稳态分子扩散)进行描述,他们还提出了扩散精馏的单点行为概念.McDowell和Davis[70]通过对积分柱的计算机模拟扩展了扩散精馏过程行为的描述和研究,所建立的模型比Fullarton和Schlunder的模型有所改进,尤其是对于模型参数的认知上.Taylor和Krishna[71]建议将扩散蒸馏工艺用于无水乙醇的生产.Chung[72]等在湿壁柱中用扩散蒸馏法生产无水乙醇,并观察了蒸发和冷凝温度、环形部分、惰性气的选择性和总通量对过程的影响.Kim[73]等为Chung的工艺过程建立了一个模型(考虑到显热的传递),并提出一种算法,它可以使冷凝液膜界面温度的计算更准确.此外,还有许多其他分离乙醇-水的方法:变压工艺,精馏工艺[74],精馏和渗透汽化相结合的工艺[75-76],超临界CO2萃取工艺[77],用汽油做萃取剂的萃取精馏[78],用汽油做萃取剂的液液萃取[79-81]和通过化学络合作用进行分离的方法[82]等.
5 几种工艺的比较
从工艺而言,上述几种无水乙醇的生产方法各具特点:精馏工艺作为传统工艺已沿用几十年,工艺成熟、易于产业化,但其能耗大,操作要求高,发展方向主要集中于降低能耗和研发新型第三种组分.就两种特殊精馏生产工艺来说,萃取精馏比恒沸精馏更具发展潜力,因其能耗相对较低;膜分离技术能耗低、易操作、易批量生产,因此具有很好的工业化应用前景.但由于膜的造价较高,若要使其在工业上得到广泛应用,还需要在膜和膜组件研发,工艺参数优化及吸附剂性能提高等方面进行大量的研究;吸附法能耗同样相对较低.具有发展潜力,但仍处实验研究阶段.值得一提的是,生物质吸附是继分子筛吸附后一种满足可持续发展战略的清洁工艺:一方面,生物质既是发酵法生产乙醇的原料,又是吸附剂;另一方面,用作吸附剂的生物质再生失效后可直接再用作发酵原料.
从能耗而言,精馏法的能耗最大,而非精馏法工艺(如膜分离,吸附法)的能耗相对则较低,因此经济效益也较好.表2比较了几种无水乙醇生产工艺的能耗情况.
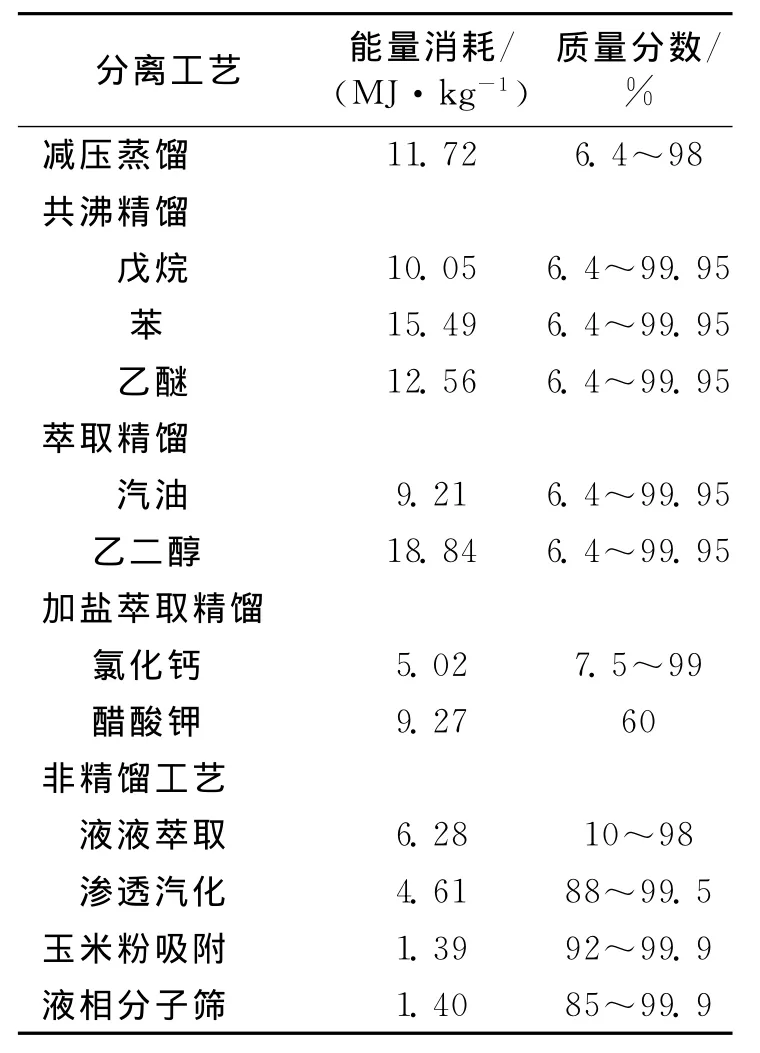
表2 不同无水乙醇生产工艺的能耗Table 2 Energy consumption of various processes for anhydrous ethanol production
6 结束语
随着世界能源危机的加剧和环保意识的增强,人们对乙醇-水物系分离工艺的要求越来越高.精馏法虽然工艺成熟,但能耗较大,设备投资大,因此现在涌现了很多新兴的节能精馏技术,如多效精馏,热泵精馏等.这些新兴精馏技术现已用于工厂的技改过程中.非精馏法能耗较低,经济效益显著,但无论是膜材料还是吸附剂现在还存在各种各样的问题,严重阻碍了其工业化,有待于进一步的研究.况且对于低醇量的醇水溶液分离,非精馏法优势不再明显.综上,工业上合理的乙醇-水分离方法应该是精馏法与非精馏法的结合,如萃取精馏+膜分离或萃取精馏+吸附法等.因此有理由相信,随着节能精馏技术,膜技术与吸附剂法的不断完善和进步,乙醇-水物系分离工艺中存在的问题将一定得到有效解决,从而实现乙醇-水分离工艺的绿色化.
[1] MALHOTRA R K,DAS L M.Biofuels as blending components for motor gasoline and diesel fuels[J].J Sci Ind Res,2003,62(2):90-96.
[2] SANTOSH K,NEETU S,RAM P.Anhydrous ethanol:A renewable source of energy[J].Renew Sust Energ Rev,2010,14:1830-1844.
[3] JACKSON M,MORALES M M.Ethanol fuel use:Promising prospects for the future[J].Renewable Energy for Development,2004,17(1):1-4.
[4] YU S,TAO J.Energy efficiency assessment by life cycle simulation of cassava-based fuel ethanol for automotive use in Chinese Guangxi context[J].Energy,2009,34(1):22-31.
[5] TREYBAL R E.Mass-transfer operations[M].3rd ed.Singapore:McGraw-Hill Book Co.,1980.
[6] BLACK C.Distillation modeling of ethanol recovery and dehydration processes for ethanol and gasohol[J].Chem Eng Prog,1980,76(3):78-85.
[7] GOMIS V,FONT A,PEDRAZA R,et al.Isobaric vapour-liquid and vapour-liquid-liquid equilibrium data for the system water+ethanol+cyclohexane[J].Fluid Phase Equilib,2005,235(4):7-10.
[8] GOMIS V,FONT A,PEDRAZA R,et al.Isobaric vapor-liquid and vapor-liquid-liquid equilibrium data for the waterethanol-hexane system[J].Fluid Phase Equilib,2007,259(1):66-70.
[9] GOMIS V,FONT A,SAQUETE MD.Isobaric vapour-liquid and vapour-liquid-liquid equilibrium data for the system water+ethanol+n-heptane at 101.3kPa[J].Fluid Phase Equilib,2006,248(43):206-210.
[10] GOMIS V,PEDRAZA R,FRANCES O,et al.Dehydration of ethanol using azeotropic distillation with isooctane[J].Ind Eng Chem Res,2007,46(13):4572-4576.
[11] Al-AMER A.Investigating polymeric entrainers for azeotropic distillation of the ethanol/water and MTBE/methanol systems[J].Ind Eng Chem Res,2000,39(10):3901-3906.
[12] NISHI Y.Vapor-liquid equilibrium relations for the system accompanied by hypothetical chemical reactions containing salts[J].J Chem Eng Jpn,1975,8(7):187-191.
[13] JAQUES D,GALAN MA.Isobaric LVE data for alcohol-water systems saturated with a salt which appear to contradict the Gibbs-Konovolov theorem[J].Chem Eng Sci,1980,35(8):1803-1804.
[14] BURNS J A,FURTER W F.Effects of salts having large organic ions on vapor-liquid equilibrium[J].Adv Chem Ser,1976,155(2):85-98.
[15] GALAN M,LABRADOR M,ALVAREZ J.Salt effect in liquid-vapor equilibrium:Ethanol-water system saturated with strontium bromide,barium nitrate,and strontium nitrate[J].J Chem Eng Data,1980,25(1):7-9.
[16] MERANDA D,FURTER WF.Vapour-liquid equilibrium data for system:Ethanol-water saturated with potassium acetate[J].Can J Chem Eng,1966,44(3):298-300.
[17] VMERANDA D,FURTER WF.Vapor-liquid equilibrium in alcohol-water systems containing dissolved halide salts and salt mixtures[J].AIChE J,1972,18(1):111-116.
[18] TAN T C,TEO W K,TI H C.Vapour liquid equilibria of ethanol-water system saturated with glucose at subatmospheric pressures[J].Chem Eng Res Des,1988,66(2):75-83.
[19] TAN T C,NG B H.Effect of mixed dissolved solutes on the vapour liquid equilibrium of the ethanol-water system:Prediction and experimental verification[J].Chem Eng Res Des,1993,71(3):53-61.
[20] LEI Z,WANG H,ZHOU R,et al.Influence of salt added to solvent on extractive distillation[J].Chem Eng J,2002,87(4):149-156.
[21] MARSH K N,BOXALL J,LICHTENTHALER R.Room temperature ionic liquids and their mixtures——a review[J].Fluid Phase Equilib,2004,219(1):93-98.
[22] HAN X X,ARMSTRONG D W.Ionic liquids in separations[J].Acc Chem Res,2007,40(11):1079-1086.
[23] LEI Z,CHEN B,LI C,et al.Predictive molecular thermodynamic models for liquid solvents,solid salts,polymers,and ionic liquids[J].Chem Rev,2008,108(4):1419-1455.
[24] ORCHILLES A V,MIGUEL P J,VERCHER E,et al.Using 1-ethyl-3-methylimidazolium trifluoromethanesulfonate as an entrainer for the extractive distillation of ethanol+water mixtures[J].J Chem Eng Data,2010,55(4):1669-1674.
[25] CALVAR N,GOMEZ E,GONZALEZ B,et al.Experimental vapor-liquid equilibria for the ternary system ethanol+water+1-ethyl-3-methylpyridinium ethylsulfate and the corresponding binary systems at 101.3kPa:Study of the effect of the cation[J].J Chem Eng Data,2010,55(8):2786-2791.
[26] GENG W,ZHANG L Z,DENG D S,et al.Experimental measurement and modeling of vapor-liquid equilibrium for the ternary system water+ethanol+1-butyl-3-methylimidazolium chloride[J].J Chem Eng Data,2010,55(4):1679-1683.
[27] MOKHTARANI B,GMEHLING J.(vapour+liquid)equilibria of ternary systems with ionic liquids using headspace gas chromatography[J].J Chem Thermodyn,2010,42(8):1036-1038.
[28] ZHANG L Z,GE Y,JI D X,et al.Experimental measurement and modeling of vapor-liquid equilibrium for ternary systems containing ionic liquids:A case study for the system water+ethanol+1-hexyl-3-methylimidazolium chloride[J].J Chem Eng Data,2009,54(8):2322-2329.
[29] CALVAR N,GONZALEZ B,GOME Z,et al.Vapor-liquid equilibria for the ternary system ethanol+water+1-butyl-3-methylimidazolium methylsulfate and the corresponding binary systems at 101.3kPa[J].J Chem Eng Data,2009,54(3):1004-1008.
[30] CALVAR N,GONZALEZ B,GOME Z,et al.Vapor-liquid equilibria for the ternary system ethanol+water+1-ethyl-3-methylimidazolium ethylsulfate and the corresponding binary systems containing the ionic liquid at 101.3kPa[J].J Chem Eng Data,2008,53(3):820-825.
[31] GE Y,ZHANG L Z,YUAN X C,et al.Selection of ionic liquids as entrainers for separation of(water+ethanol)[J].J Chem Thermodyn,2008,40(8):1248-1252.
[32] CALVAR N,GONZALEZ B,GOMEZ E,et al.Study of the behaviour of the azeotropic mixture ethanol-water with imidazolium-based ionic liquids[J].Fluid Phase Equilib,2007,259(1):51-56.
[33] CALVAR N,GONZALEZ B,GOMEZ E,et al.Vapor-liquid equilibria for the ternary system ethanol+water+1-butyl-3-methylimidazolium chloride and the corresponding binary systems at 101.3kPa[J].J Chem Eng Data,2006,51(6):2178-2181.
[34] JORK C,SEILER M,BESTE Y A,et al.Influence of ionic liquids on the phase behavior of aqueous azeotropic systems[J].J Chem Eng Data,2004,49(4):852-857.
[35] CHEN S H,LIN S S,CHANG D J,et al.Pervaporation separation of water/ethanol mixture by sulfonated polysulfone membrane[J].J Membr Sci,2001,183(1):29-36.
[36] DOGUPARTHY S P.Pervaporation of aqueous alcohol mixtures through a photopolymerised composite membrane[J].J Membr Sci,2001,185(2):201-205.
[37] LEE K R,WANG Y H,TENG H Y,et al.Preparation of aromatic polyamide membrane for alcohol dehydration by pervaporation[J].Eur Polym J,1999,35(5):861-866.
[38] SHIHHSIUNG C,REYMAY L,CHINGSHAN H,et al.Pervaporation separation water/ethanol mixture through lithitated polysulfone membrane[J].J Membr Sci,2001,193(1):59-67.
[39] WANG X P,SHEN Z Q,ZHANG F Y.A novel composite chitosan membrane for the separation of alcohol-water mixtures[J].J Membr Sci,1996,119(2):191-198.
[40] TSUYUMOTO M,TERAMOTO A,MEARES P.Dehydration of ethanol on a pilot-plant scale,using a new type of hollow-fiber membrane[J].J Membr Sci,1997,133(1):83-94.
[41] MULDER M,SMOLDERS C.On the mechanism of separation of ethanol/water mixtures by pervaporation.I.Calculation of concentration profiles[J].J Membr Sci,1984,17(3):289-307.
[42] MULDER M,FRANKLIN A,SMOLDERS C.On the mechanism of separation of ethanol/water mixtures by pervaporation.II.Experimental concentration profiles[J].J Membr Sci,1985,23(3):451-458.
[43] NGUYEN Q T,LE B L,NEEL J.Preparation of membranes from polyacrylonitrile-polyvinylpyrrolidone blends and the study of their behaviour in the pervaporation of water-organic liquid mixtures[J].J Membr Sci,1985,22(2-3):245-255.
[44] WENZLAFF A,BODDEKER K W,HATTENBACH K.Pervaporation of water-ethanol through ion-exchange membranes[J].J Membr Sci,1985,22(2-3):333-344.
[45] SANDER U,SOUKUP P B.Design and operation of pervaporation plant for ethanol dehydration[J].J Membr Sci,1988,36:463-375.
[46] 唐俏瑜,王莉,展侠,等.高选择性PDMS/PVDF复合膜渗透汽化分离乙醇/水混合物[J].膜科学与技术,2011,31(6):1-5.TANG Qiaoyu,WANG Li,ZHAN Xia,et al.Pervaporation of ethanol/water mixtures by PDMS/PVDF composite membranes with high permeability[J].Membrane Science and Technology,2011,31(6):1-5.
[47] 曾小雅,纪树兰,秦振平,等.溴化聚苯醚渗透汽化非对称膜的制备及其乙醇/水分离性能[J].膜科学与技术,2011,31(6):30-33.ZENG Xiaoya,JI Shulan,QIN Zhenping,et al.Preparation of BPPO asymmetric membrane and its pervaporation for ethanol/water solution[J].Membrane Science and Technology,2011,31(6):30-33.
[48] 纪树兰,曾小雅,秦征平,等.聚苯醚/聚砜复合膜对乙醇/水混合体系的渗透汽化分离[J].北京工业大学学报,2011,37(6):893-897.JI Shulan,ZENG Xiaoya,QIN Zhenping,et al.Pervaporation separation of ethanol/water mixture by PPO/PSF composite membrane[J].Jounal of Beijing University of Technology,2011,37(6):893-897.
[49] XIA S,WANG W,LIU G,et al.Pervaporation properties of polyvinyl alcohol/ceramic composite membrane for separation of ethyl acetate/ethanol/water ternary mixtures[J].Korean J Chem Eng,2012,29(2):228-234.
[50] 牛洪金,刘威,刘吉达,等.PDMS-b-PPO非对称渗透汽化膜对乙醇/水的分离性能[J].膜科学与技术,2013,33(1):66-70.NIU Hunjin,LIU Wei,LIU Jida,et al.Pervaporation of water/ethanol binary mixtures by PDMS-PPO asymmetric membrane[J].Membrane Science and Technology,2013,33(1):66-70.
[51] ZHANG G,CUSSLER E L.Distillation in hollow fibers[J].AIChE J,2003,49(9):2344-2351.
[52] ZHANG G,CUSSLER E L.Hollow fibers as structured distillation packing[J].J Membr Sci,2003,215(1-2):185-193.
[53] 林兰,张国亮,孟琴.新型中空纤维膜接触器用于乙醇/水体系分离的探索[J].化工学报,2007,58(11):2822-2827.LIN Lan,ZHANG Guoliang,MENG Qin.Ethanol-water separation in hollow fiber membrane contactor[J].Journal of Chemical Industry and Engineering(China),2007,58(11):2822-2827.
[54] 李娜.PDMS/PVDF中空纤维复合膜接触器用于醇/水体系分离的性能研究[D].杭州:浙江工业大学,2011,21-49.LI Na.PDMS/PVDF hollow fiber composite membrane for alcohol-water[D].Hangzhou:Zhejiang University of Technology,2011,21-49.
[55] ISHIKAWA A.CHIANG T H,TODAF F.Separation of water-alcohol mixtures by permeation through a zeolite membrane on porous glass[J].J Chem Soc Chem Commun,1989,22(3):764-768.
[56] GUAN J,HU X.Simulation and analysis of pressure swing adsorption:Ethanol drying process by the electrical analogue[J].Sep Purif Technol,2003,31(4):31-35.
[57] CARMO M J,GUBULIN J C.Ethanol-water separation in the PSA process[J].Adsorption,2002,8:235-248.
[58] 李浩.分子筛吸附法制无水乙醇的机理及工艺[J].山东化工,2009,38(11):29-33.LI Hao.The mechanism and technics of the absolute alcohol made by the molecular sieve adsorption method[J].Shangdong Chemical Industry,2009,38(11):29-33.
[59] 范荣玉,吴方棣.分子筛吸附脱除乙醇中微量水的研究[J].武夷学院学报,2013,32(2):60-64.FAN Rongyu,WU Fangdi.Study on purification of small amount of water from ethanol on molecular sieves by adsorption[J].Journal of Wuyi University,2009,38(11):29-33.
[60] 刘一鸣,高鑫,李洪,等.生物质吸附剂在制备燃料乙醇中应用的研究进展[J].化工进展,2013,32(10):2336-2342.LIU Yiming,GAO Xin,LI Hun,et al.Research progress in development of adsorbents in the producing biomass-based fuel ethanol[J].Chemical Industry and Engineering Process,2013,32(10):2336-2342.
[61] LADISCH M,VOLOCH M,HONG J,et al.Cornmeal adsorber for dehydrating ethanol vapors[J].Ind Eng Chem Process Des Dev,1984,23(3):437-443.
[62] BENSON T,GEORGE C.Cellulose based adsorbent materials for the dehydration of ethanol using thermal swing adsorption[J].Adsorption,2005,11:697-701.
[63] SOWERBY B,CRITTENDEN B.A vapour phase adsorption and desorption model for drying the ethanol-water azeotrope in small columns[J].Trans IChemE,1991,69(1):3-13.
[64] 韩秀丽,刘金盾,马晓建,等.乙醇脱水吸附剂吸附-脱附性能的研究[J].高校化学工程学报,2008,22(6):1059-1064.HAN Xiuli,LIU Jindun,MA Xiaojian,et al.Research on adsorption performance of ethanol dehydration adsorbent[J].Journal of Chemical Engineering of Chinese Universities,2008,22(6):1059-1064.
[65] WANG Y,GONG C,SUN J,et al.Separation of ethanol/water azeotrope using compound starch-based adsorbents[J].Bioresource Technol,2010,101(8):6170-6176.
[66] 李清明,谭兴和,苏小军,等.乙醇-水体系在马铃薯粉吸附剂上的吸附过程研究[J].生物质化学工程,2012,46(4):42-45.LI Qingming,TAN Xinhe,SU Xiaojun,et al.Study on vapor adsorption process of ethanol-water system on potato powder[J].Biomass Chemical Engineering,2012,46(4):42-45.
[67] 张琳叶,微光涛,陈砺.甘薯吸附剂固定床吸附脱水制燃料乙醇及技术思考[J].可再生资源,2012,30(2),42-49.ZHANG Linye,WEI Guangtao,CHEN Li.Preparation of fuel alcohol by adsorption dehydration in fixed bed using sweet potato as adsorbent and thoughts on its technology[J].Renewable Energy Resources,2012,30(2),42-49.
[68] FULLARTON D,SCHLUNDER E.Diffusion distillation——a new separation process for azeotropic mixtures[J].Chem Eng Fundam,1983,2(3):53-58.
[69] FULLARTON D,SCHLUNDER E.Diffusion distillation——a new separation process for azeotropic mixtures.Part I:Selectivity and transfer efficiency[J].Chem Eng Process,1986,20(2):255-263.
[70] MCDOWELL J,DAVIS J.A characterization of diffusion distillation for azeotropic separation[J].Ind Eng Chem Res,1988,27(11):2139-2148.
[71] TAYLOR R,KRISHNA R.Multicomponent mass transfer[M].New York:JohnWiley &Sons,Inc,1993:79-89.
[72] CHUNG I,SONG K,HONG W,et al.Ethanol dehydration by evaporation and diffusion in an inert gas layer[J].HWAHAK KONGHAK,1994,32(4):734-741.
[73] KIM S,LEE D,HONG W.Modeling of ethanol dehydration by diffusion distillation in consideration of the sensible heat transfer[J].Korean J Chem Eng,1996,13(5):275-281.
[74] TEGTEMEIER U.Process design for energy saving ethanol production[J].Biotechnol Lett,1985,7(2):129-134.
[75] GOODING C,BAHOUTH F.Membrane aided distillation of azeotropic solutions[J].Chem Eng Commun,1985,35(6):267-279.
[76] ISHIDA M,NAKAGAWA N.Exergy analysis of a pervaporation system and its combination with a distillation column based on energy utilization diagram[J].J Membr Sci,1985,24(3):271-283.
[77] HARTLINE F.Lowering the cost of alcohol[J].Science,1979,206(4414):41-42.
[78] CHAMBERS R,HERENDEEN R,JOYCE J,et al.Gasohol:Does it or doesn′t it produce positive net energy[J].Science,1979,206(4420):789-795.
[79] LEEPER S,WANKAT P.Gasohol production by extraction of ethanol from water using gasoline as solvent[J].Ind Eng Chem Proc Des Dev,1982,21(2):331-334.
[80] LEE F,PAHL R.Use of gasoline to extract ethanol from aqueous solution for producing gasohol[J].Ind Eng Chem Proc Des Dev,1985,24(2):250-255.
[81] GRAMAJO D,BONATTI C,SOLIMO H.Liquid-liquid equilibrium of water+ethanol+reformate[J].Fluid Phase Equilib,2005,230(1-2):45-50.
[82] ROUSSEAU R.Handbook of separation process technology[M].New York:John Wiley &Sons,1987:45-85.

