超高效合相色谱法快速检测纺织品中的8 种荧光增白剂
汤 娟, 丁友超 , 曹锡忠, 齐 琰, 钱 凯
(江苏出入境检验检疫局工业产品检测中心,江苏 南京210001)
荧光增白剂(FWAs)是一种能激发入射光线产生荧光,使所染物质获得类似荧石效应的荧光染料,广泛应用于纺织纤维、纸张、塑料、涂料和合成洗涤剂,其中应用于纺织纤维的FWAs 种类最多。经FWAs 处理过的纺织品,不仅改善外观,提高品质和档次,同时提升了商业价值,因而FWAs 的消费量越来越高。目前,我国纺织品中常用FWAs 的品种主要包括双三嗪氨基二苯乙烯类型、二苯乙烯联苯类型、双苯并唑类型、二苯乙烯基苯类型、吡唑啉类型、香豆素类型等[1]。
FWAs 中含有一些特别活跃的分子,较易迁移至角质层或血液里,且不易分解,其可大大削减人体免疫力,甚至会造成血液系统受损;FWAs 对皮肤黏膜有强烈的刺激作用,使人体出现皮肤起皱、汗液减少、红肿瘙痒、感染出血或紫斑溃烂等症状,甚至会引发变态反应性皮炎或接触性皮炎等疾病[2];乌鲁木齐市疾病预防控制中心报道FWAs 能与伤口外的蛋白质结合,阻碍伤口愈合;被人体吸收后能使人体细胞出现变异性倾向,其毒性聚集在肝脏或其他重要器官,成为潜在的致癌因素[3]。因此建立快速检测纺织品中FWAs 的方法非常紧急和必要。
目前,FWAs 的检测方法主要包括高效液相色谱-荧光法(HPLC-FLD)[4]、高效液相色谱-二极管阵列检测法(HPLC-DAD)[5]和液相色谱-质谱联用法(LC-MS)[6,7],研究基质主要集中于纸[8,9]、洗涤剂[10]、食品材料[11,12]、水[13-15]等。这些方法涉及的FWAs 不仅种类少,溶剂使用量大,更重要的是不符合开发绿色环保分析方法的发展趋势。
超高效合相色谱(ultra performance convergence chromatography,UPC2)技术是一种以超临界流体色谱技术原理为基础,以CO2为主要流动相的最新分离技术。该技术具有有机溶剂使用量少、黏度低、传质性能好、分离效率高、绿色环保等优点[16]。本研究利用UPC2技术建立了纺织品中8 种FWAs(见表1)的快速、简单的检测方法。
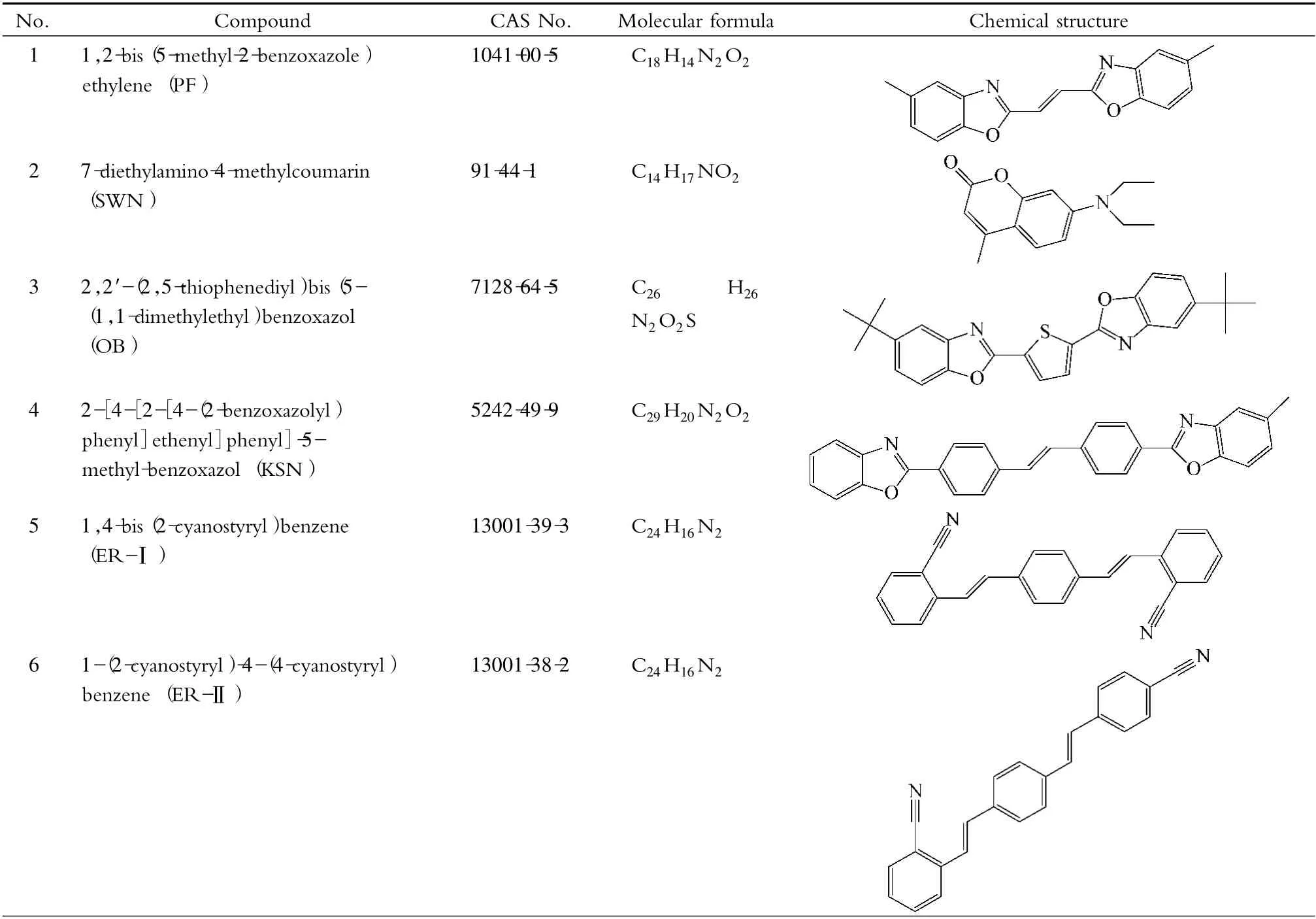
表1 8 种FWAs 的化学信息Table 1 Chemical information of the eight FWAs
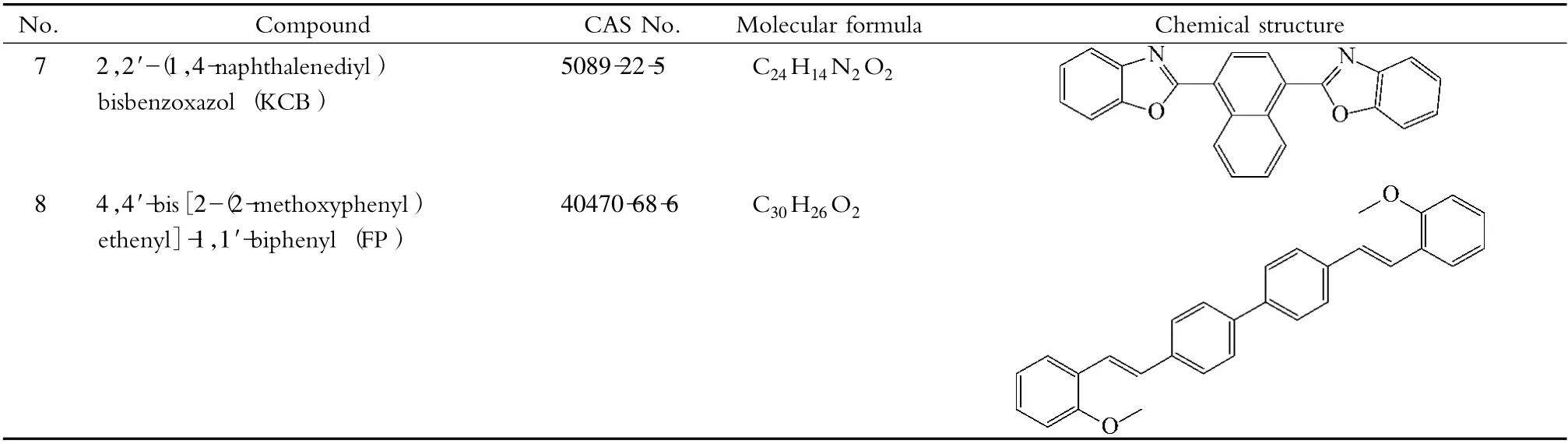
表1 (续)Table 1 (Continued)
1 实验部分
1.1 仪器与试剂
ACQUITY UPC2系统(美国Waters 公司),配ACQUITY UPC2PDA 检测器。ACQUITY UPC2HSS C18 SB 色谱柱(100 mm×3.0 mm,1.8 μm);ACQUITY UPC2CSH Fluoro-phenyl 色谱柱(100 mm×3.0 mm,1.7 μm);ACQUITY UPC2BEH色谱柱(100 mm ×3.0 mm,1.7 μm)(美国Waters公司)。PL602-L 和ML54 型电子天平(感量分别为0.01 g 和0.000 1 g,梅特勒-托利多仪器上海有限公司);KQ-250DB 型数控超声波清洗器(昆山市超声仪器有限公司);0.22 μm 有机相针式过滤器(上海安谱科学仪器有限公司)。
FWAs 标准品:FP(纯度>90.0%)、KCB(纯度>98.0%)、OB(纯度>98.0%)和KSN(纯度>95.0%)购于TCI 化成工业发展有限公司;SWN(纯度99%)购于J&K 公司;DT(纯度>85%)和ER-Ⅱ(纯度>85%)购于浙江珊瑚化工有限公司;ER-Ⅰ(纯度>65%)购于江苏格罗瑞化学有限公司。甲醇、乙腈、乙醇和异丙醇(色谱纯,德国Merck 公司)。三氯甲烷、N,N-二甲基甲酰胺和二甲苯(分析纯,南京化学试剂有限公司)。二氧化碳(纯度≥99.99%,南京天泽气体有限公司)。
1.2 实验方法
1.2.1 色谱条件
ACQUITY UPC2HSS C18 SB 色谱柱(100 mm×3.0 mm,1.8 μm);系统背压为13.10 MPa;色谱柱温度为60 ℃;进样量为2 μL;分析时间为12 min;流动相分别为超临界CO2(A 相)和甲醇(B相);梯度洗脱程序:0.0 ~0.5 min,95% A;0.5 ~9.0 min,95%A ~85%A;9.0 ~10.0 min,85%A ~95% A;10.0 ~12.0 min,95% A。流 速 为1.5 mL/min;检测波长为350 nm。
1.2.2 标准溶液的配制
分别准确称取50 mg 各种荧光增白剂(精确至0.1 mg)于10 mL 棕色容量瓶中,用乙醇溶解并定容至刻度,配成质量浓度为5 g/L 的单一标准储备液,于-4 ℃下避光保存。
分别吸取1 mL 单一标准储备液至50 mL 棕色容量瓶中,用乙醇定容至刻度,配成100 mg/L 的混合标准工作液,逐级稀释成所需的系列标准工作液。
1.2.3 样品前处理
将样品剪成5 cm × 1 cm 的碎片,准确称取(1.00 ±0.01)g 样品,用不含FWAs 的白色细线扎紧,在25 mL 沸腾的二甲苯上方垂直放置30 min,使冷凝溶剂从样品上流过,提取液冷却至室温后,于70 ℃旋转蒸发至干,用1 mL 乙醇溶解,用0. 22 μm有机相针式过滤器过滤至进样小瓶中,供超高效合相色谱仪测定。
2 结果与讨论
2.1 色谱柱的选择
8 种FWAs 中含有同分异构体和结构类似物,分离难度较大。色谱柱的选择是色谱分离方法的核心,本实验首先考察了具有明显差异的不同固定相色谱柱对8 种荧光增白剂分离的影响,即:ACQUITY UPC2HSS C18 SB 色谱柱(100 mm×3.0 mm,1.8 μm);ACQUITY UPC2CSH Fluoro-phenyl 色谱柱(100 mm × 3.0 mm,1.7 μm);ACQUITY UPC2BEH 色谱柱(100 mm ×3.0 mm,1.7 μm)。从图1 可见,在相同条件下,ACQUITY UPC2HSS C18 SB 色谱柱的分离效果明显好于其他两者。
2.2 流动相中辅助溶剂的选择

图1 不同色谱柱对8 种荧光增白剂的分离效果Fig.1 Effect of different columns on the separation of the eight FWAs
UPC2系统中少量的有机溶剂对分析物的分离具有重要影响。不同的有机溶剂具有不同的选择性和洗脱能力,超临界CO2作为UPC2的主要流动相,可与全部有机溶剂互溶,因而为辅助溶剂的选择提供了很宽的范围。本实验主要讨论了4 种常用有机溶剂(甲醇、乙腈、乙醇、异丙醇)对8 种FWAs 分离的影响。从图2 可以看出,4 种有机溶剂对8 种FWAs 的洗脱能力大小顺序为甲醇>乙醇>异丙醇>乙腈,且选择差异性明显,其中甲醇和异丙醇的分离效果较好,但异丙醇黏度较高,柱压偏高,且峰形较宽;乙腈和乙醇对8 种FWAs 的分离效果较差,乙腈使峰形展宽严重,且峰形较差;乙醇不能将SWN与杂质分开,且KCB 与ER-Ⅰ为共同出峰。因此实验选择甲醇作为辅助有机溶剂。
2.3 柱温及系统背压的优化
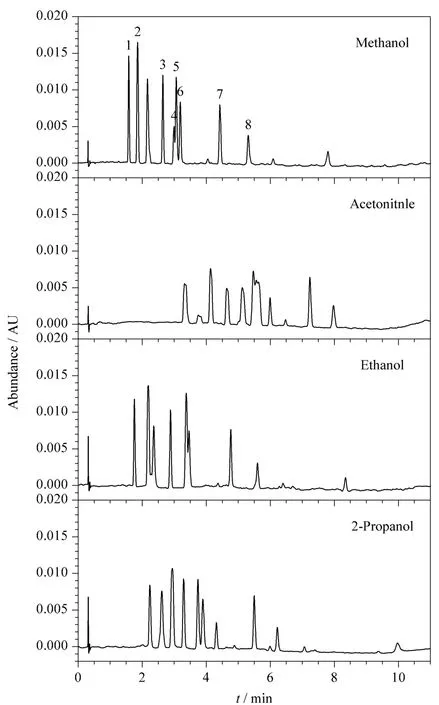
图2 不同有机溶剂对8 种FWAs 分离效果的影响Fig.2 Effect of different organic solvents on the separation of the eight FWAs
UPC2与一般液相色谱相比,分离温度和压力的改变能够更为显著地改变流动相的密度,从而改变其分离能力。较高的柱温导致流动相的密度变小而增加保留时间,较高的压力导致流动相的密度变大而缩短保留时间,因此温度和压力是建立UPC2方法中的两个重要参数。通常UPC2可设置的柱温为35 ~65 ℃,压力为11.72 ~24.14 MPa,但压力低于12.41 MPa 时,CO2会从超临界态转变为更接近气态的状态,影响其极性和密度,最终影响分析物的分离效果。综合考虑,实验考察了不同柱温(40、50、60 ℃)和不同系统背压(13.10、13.79、14.48 MPa)对8 种FWAs 分离的影响。从图3 可以看出,随着柱温的升高,保留时间延长,60 ℃时待测物均达到基线分离。而由图4 可见,系统背压的升高仅缩短了保留时间,对分离效果影响较小,但过高的背压会使系统压力过高。因此实验将柱温设为60 ℃,系统背压设为13.10 MPa。
2.4 紫外检测波长的选择

图3 不同温度对8 种FWAs 分离的影响Fig.3 Effect of different temperatures on the separation of the eight FWAs
采用三维(3D)检测模式,分别对8 种FWAs 单一标准溶液进行紫外扫描,扫描范围为210 ~500 nm,8 种FWAs 的最大吸收波长见表2。结合工作效率和检测灵敏度,采用350 nm 对8 种FWAs 同时进行扫描检测。

表2 8 种FWAs 的最大吸收波长Table 2 Maximum wavelengths (λmax)of the eight FWAs
2.5 样品前处理条件的优化
有关染料检测的文献及本实验室常用的前处理方法有甲醇[17,18]、三氯甲烷[4,7]或N,N-二甲基甲酰胺超声提取和N,N-二甲基甲酰胺或二甲苯循环提取。本研究比较了上述几种提取方法的提取情况,图5 显示了每种提取方法对8 种FWAs 的提取总量。对于同一自制阳性样品,二甲苯循环提取的提取效率最高,甲醇超声和N,N-二甲基甲酰胺超声的提取效率最低,仅为二甲苯循环提取效率的1.7%和3.3%。实验研究的8 种FWAs 均应用于化学纤维,此类纤维的生产需经高温高压,因而超声提取率不如循环提取,因此实验采用二甲苯循环提取作为样品前处理方法。

图4 不同系统背压对8 种FWAs 分离的影响Fig.4 Effect of auto back pressure regulators ()on the separation of the eight FWAs

图5 不同提取方法的提取效果Fig.5 Extraction efficiencies of different extraction methods
2.6 方法的线性范围和定量限
配制8 种FWAs 的质量浓度分别为1.0、2.0、5.0、10.0 和20.0 mg/L 的系列混合标准溶液,按1.2.1 节所述方法进行超高效合相色谱分析,以FWAs 的峰面积(y)为纵坐标,质量浓度(x,mg/L)为横坐标,建立标准曲线,得到FWAs 的线性回归方程。以信噪比为10(S/N =10)计算得到分析方法的定量限(LOQ)。从表3 可见,8 种FWAs 在1.0~20.0 mg/L 范围内线性良好(r≥0.999 1),LOQ在0.70 ~0.95 mg/L 之间。
2.7 回收率及精密度
以阴性涤纶样品为基质,采用标准添加法进行回收率和精密度测定,在2.0、5.0 和10.0 mg/kg 添加水平下的平均回收率在90.9% ~96.5%之间,相对标准偏差(RSD,n =6)在2.8% ~4.2% 之间(见表4),可见本方法的实验精密度能够满足分析要求。
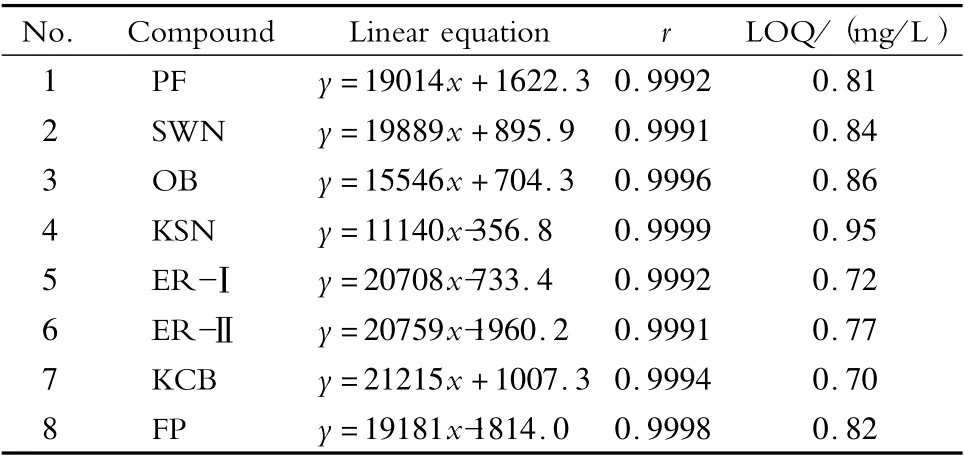
表3 8 种FWAs 的线性方程、相关系数(r)及定量限(LOQ)Table 3 Linear equations,correlation coefficients (r)and limits of quantification (LOQs)of the eight FWAs
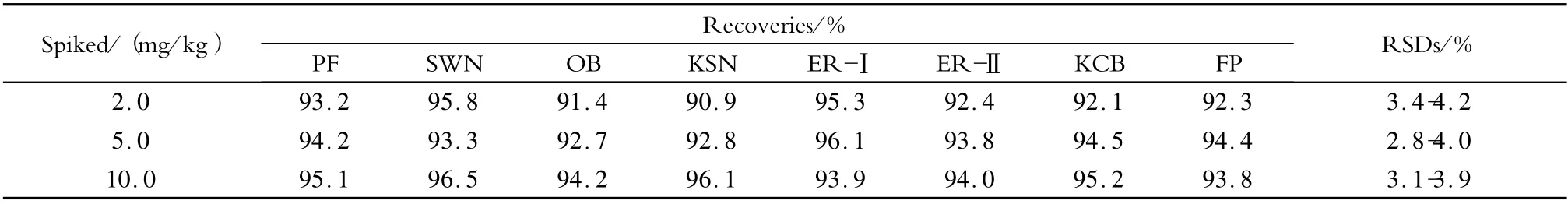
表4 不同添加水平下8 种FWAs 的回收率及精密度(n =6)Table 4 Recoveries and relative standard deviations (RSDs)of the eight FAWs at different spiked levels (n =6)
2.8 实际样品检测
采用本方法检测8 块含FWAs 的纺织品,结果表明,8 块纺织品中均检出ER-Ⅰ和ER-Ⅱ,含量分别为189.4 ~424.3 mg/kg 和193.5 ~603.4 mg/kg。典型阳性样品的超高效合相色谱图见图6。
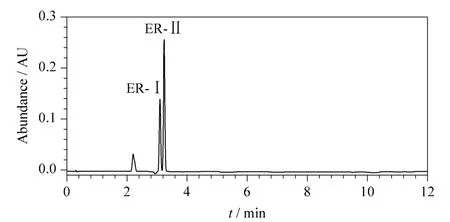
图6 一个阳性样品的色谱图Fig.6 Chromatogram of a positive sample
3 结论
通过优化辅助有机溶剂、柱温及系统背压等条件,建立了纺织品中8 种FWAs 的超高效合相色谱法。本方法分析时间短,能够在12 min 内使8 种FWAs 达到有效分离。仪器分析中使用的流动相以CO2为主,与普通液相色谱法相比,大大降低了有机试剂的使用,能够满足建立绿色环保分析方法的需求,同时也降低了检测成本。
[1] Chen R Q. Textile Auxiliaries (陈荣圻. 印染助剂),2005,22(7):1
[2] Zhang L S,Lu W T,Zhang Y Y. China Science and Technology Review (张丽莎,卢婉婷,张永勇. 中国科技博览),2013(21):602
[3] Guo H P,Zhang M Y,Liu Y H. Hunan Papermaking(郭惠萍,张美云,刘亚恒. 湖南造纸),2007(4):43
[4] Jiao Y N,Ding L,Zhu S H,et al. Chinese Journal of Chromatography (焦艳娜,丁利,朱绍华,等. 色谱),2013,31(1):83
[5] Xian Y P,Guo X D,Luo H Y,et al. Chinese Journal of Chromatography (冼燕萍,郭新东,罗海英,等. 色谱),2013,31(2):162
[6] Liu J,Li J,Li J Z,et al. China Pulp &Paper (刘峻,李军,李建中,等. 中国造纸),2013,32(3):30
[7] Du Z F,Xian Y P,Liu F J,et al. Chinese Journal of Analytical Chemistry (杜志峰,冼燕萍,刘付建,等. 分析化学),2014,42(5):636
[8] Chen H C,Ding W H. J Chromatogr A,2006,1108:202
[9] Chen L S,Jiang D G,Fu W S. Journal of Hygiene Research(陈立松,蒋定国,傅武胜. 卫生研究),2014,43(1):152
[10] Ma H J,Ma Q,Bai H,et al. Chinese Journal of Analysis Laboratory (马会娟,马强,白桦,等. 分析试验室),2014,33(5):569
[11] Wu Z L,Chen S D,Lin X J,et al. Modern Food Science and Technology (吴钟玲,陈树东,林晓佳,等. 现代食品科技),2013,29(11):2757
[12] Du Z F,Xian Y P,Liu F J,et al. Modern Food Science and Technology (杜志峰,冼燕萍,刘付建,等. 现代食品科技),2013,29(12):3014
[13] Aziz A,Steve P,Marie-Noelle P. Chemosphere,2014,100:27
[14] Shu W C,Ding W H. J Chromatogr A,2005,1088:218
[15] Chen H C,Wang S P,Ding W H. J Chromatogr A,2006,1102:135
[16] Li Z H,Wu S B,Liu S S,et al. Chinese Journal of Analytical Chemistry (李中皓,吴帅宾,刘珊珊,等. 分析化学),2013,41(12):1817
[17] Huang F,Huang X L,Lin X S,et al. Journal of Instrumental Analysis (黄芳,黄晓兰,林晓珊,等. 分析测试学报),2006,25(4):78
[18] Chen M J,Li Y M,Zhang R,et al. Dyestuffs and Coloration(陈美娟,李亚明,张蓉,等. 染料与染色),2006,43(4):51

