二维离子色谱法测定海水中的铵离子
林奇,林红梅,包洋鸣
(1.国家海洋局海洋–大气化学与全球变化重点实验室,福建厦门 361005;2.国家海洋局第三海洋研究所,福建厦门 361005;3.厦门大学海洋与地球学院,福建厦门 361005)
海洋中的含氮无机离子(NO3–,NH4+和NO2–)是海洋中最为重要的营养盐种类,其中NH4+是开阔大洋三氮中含量第二位的含氮离子,它在生物地球化学循环过程中扮演十分重要的角色。首先,NH4+与NO3–一样,均可被生物直接吸收利用;其次,由于NH4+主要循环过程在上层海洋(约400 m以浅),及其参与生物地球化学循环过程的特殊性,NH4+成为研究区分新生产力和再生生产力的关键形态[1]。
在近岸区域,由于人为活动的影响,NH4+浓度远远高过开阔大洋,尤其在网箱养殖区等区域,其高浓度的存在将对海洋生物产生毒害作用[2–3],因此测量海洋中的NH4+具有十分重要的意义。近年来,人们不断开发新的分析方法用于海洋中NH4+的检测[4–9]。
海水样品中的阳离子种类很多,且彼此间的浓度差异非常大。笔者曾对海水中阳离子采用高容量柱IonPac CS16进行等度淋洗分离,抑制电导法测定,建立了海水阳离子精密分析方法[10],样品经稀释后进样,可在30 min 内同时检测Li+,Na+,K+,Ca2+,Mg2+,Sr2+6种阳离子,但该法无法同时测定海水中的NH4+。笔者尝试采用二维色谱法测量海水中的NH4+,取得了较满意的结果。
1 实验部分
1.1 主要仪器与试剂
离子色谱仪:ICS–90A型,配IonPac CS16分离柱/CG16 5 mm保护柱、CSRS–300 4 mm阳抑制器、RFC–30淋洗液发生器(EGC–MSA)、PC10 PCR加压容器,美国戴安公司;
离子色谱仪:ICS–2500型,配GP50梯度泵、EG50淋洗液发生器(EGC–MSA)、CD25A电导检测器、IonPac CS12A分离柱/CG12A–4 mm保护柱、SC–CSRS–300 4 mm盐转换器、Chromeleon色谱工作站、LC25色谱单元(用于40℃恒温),美国戴安公司;
电子分析天平:CP224S型,感量为0.1 mg,瑞士赛多利斯公司;
甲基磺酸(MSA)淋洗液:由EGC ⅢMSA 试剂包自动生成,美国戴安公司;
Na+标准溶液:1 000 mg/L,编号为GBW(E)080127,国家标准物质研究中心;
NH4+标准溶液:1 000 mg/L,编号为GBW(E)080525,中国兵器工业集团第五三研究所;
实验用水为超纯水(电阻率18.2 MΩ·cm)。
1.2 色谱条件
1.2.1 一维色谱
色谱柱:IonPac CS16分离柱/CG16 5 mm保护柱;CSRS–300 4 mm抑制器:外加水模式,112 mA;淋洗液:30 mmol/L MSA溶液,等度淋洗;流量:1 mL/min;色谱柱和抑制器温度:40℃;进样体积:25 μL。
1.2.2 二维色谱
色 谱 柱:IonPac CS12A/CG12A 4 mm柱;SC–CSRS–300 4 mm抑制器:自循环模式,抑制电流为32 mA;淋洗液:8 mmol/L MSA溶液,等度淋洗;流量:1 mL/min;色谱柱和电导池温度:40℃;进样体积:1 300 μL。
2 结果与讨论
2.1 样品的前处理
IonPac CS–16色谱柱具有8 000 μeq/柱的高容量柱,可分离10 000∶1以上比例的Na+与NH4+,但仍不能用来直接进样分离海水中的Na+和NH4+,需要将海水适度稀释才能有效分离。分别选择10%,20%,50%的海水样品,以30 mmol/L MSA溶液等度淋洗,取25 μL进样,观察分离效果。结果只有10%和20%的海水样品可以将Na+与NH4+分开,50%的海水样品色谱图中Na+的色谱峰已经将NH4+色谱峰掩盖。选择经10倍稀释的海水进样,样品中的Na+,NH4+保留时间与标准溶液的保留时间基本一致。
2.2 阀切换时间窗口的选择
阀切换时间窗口的确定是关键的步骤之一,在第一维色谱中,选择抑制器出口与连接第二维色谱相同距离的管线直接接至电导池,观察Na+,NH4+的出峰变化,10%海水样品中Na+的保留时间为7.34 min,结束时间为8.5 min;而NH4+的出峰开始时间为8.4 min,保留时间为8.78 min,结束时间随浓度的增加而延长。在二维色谱中,高浓度NH4+的整个出峰时间达到1.1 min,因此采用大体积定量环1 300 μL进样,二维色谱阀切换装样的时间窗口设为8.3~9.6 min,以保证在IonPac CS16分离的NH4+组分能全部进入二维色谱的定量环中。仪器的淋洗程序列于表1。

表1 淋洗程序
2.3 淋洗液对二维色谱NH4+分离的影响
分别采用4,6,8,12,16,20 mmol/L MSA溶液作为淋洗液,考察使用IonPac CS12A柱时MSA淋洗液浓度对NH4+色谱峰高及其与Na+分离效果的影响。结果表明淋洗液浓度越低,Na+与NH4+之间的分离度越好,但同时NH4+的色谱峰高越来越小,虽然对峰面积影响不大,但对灵敏度却有影响。选择了8 mmol/L MSA溶液淋洗,抑制电流选择为32 mA,色谱分离效果与信噪比都较为理想,分析时间与一维色谱的时间同步完成,Na+与NH4+保留时间分别为8.98 min和10.53 min。图1为海水样品在8 mmol/L MSA淋洗液条件下的二维色谱图。
2.4 标准工作曲线与方法检出限
分别配制质量浓度为1,10,20,40,60,80,100,500,1 000,5 000,10 000 μg/L的系列NH4+标准溶液,将装有样品的PP瓶放于PC10 PCR加压容器罐中,以特氟隆管接触样品加压装样,按1.2色谱条件及表1仪器淋洗程序运行,采用1.0 μg/L NH4+标准溶液连续进样7次,计算方法检出限,依据色谱峰3倍信噪比(S/N)确定仪器的检出限(LOD)。线性范围、回归方程、相关系数和检出限如表2。
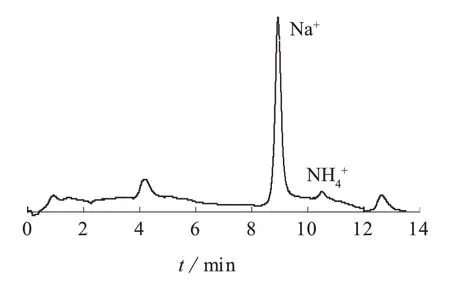
图1 海水样品的二维色谱图
2.5 方法精密度和加标回收试验
采用10 μg/L NH4+标准溶液连续进样7次,计算方法精密度,见表3。同时采用陈化的海水进行加标回收试验,对稀释10倍的海水样品分别加标20 μg/L和100 μg/L后连续测定5次,加标回收试验结果见表4。由表3、表4可知,方法的相对标准偏差为2.7%,加标回收率为80.8%~105.8%,表明本法测量精密度和准确度良好。
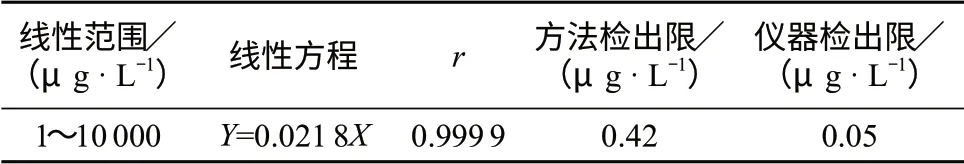
表2 线性范围、相关系数及检出限

表3 方法精密度试验结果

表4 海水样品中NH4+的加标回收试验结果
2.6 样品测定
海水样品在现场用洁净的PP瓶取样,分析时将样品经重量法稀释10倍后,用经洁净处理的0.2 μm水性PTFE微孔滤膜器(Lot Number:00153196,美国热电公司)过滤进样,采用该方法对近岸海水样品进行分析,测量结果见表5。
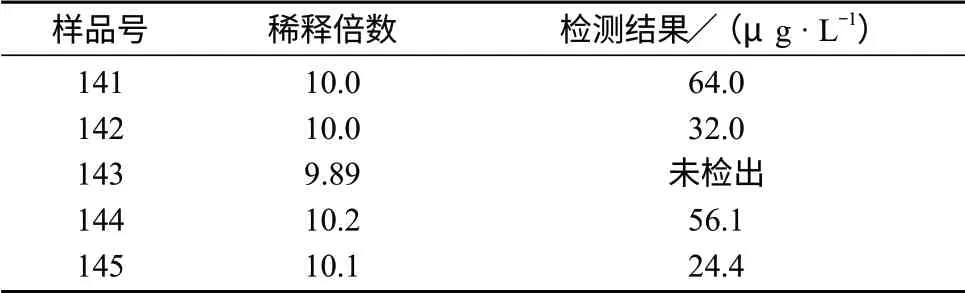
表5 海水样品铵离子分析结果
3 结语
采用二维色谱电导检测法测定了海水中的铵离子含量,方法较简单,容易实现自动进样分析,每个样品分析时间约25 min,检出限(LOD)可达到0.05 μg/L,采用SC–CSRS–300盐转换器,NH4+的线性范围可以从0.001~10 mg/L。但由于样品需要稀释后进样,方法的灵敏度对于近岸海水勉强够用,不适合大洋表层海水中NH4+的检测,有待于继续开发更灵敏的方法并开展海水中多种有机胺同步测定,目前这部分工作正在进行之中。
[1]Cotner J B,Biddanda B A. Small players,large role:microbial influerce on biogeochemical processes in pelagic aquatic ecosystems[J]. Ecosystems,2002,5(2): 105–121.
[2]Wu R,S S. The environmental impact of marine fish culture:towards a sustainable future[J]. Marine Pollution Bulletin,1995,31(4): 159–166.
[3]Barton J R. Environment,sustainable and regulation in commercial aqauaculture:the case of chilean salmonid production [J].Geoforum,1997,28(3–4): 313–328.
[4]Kuo C T,Wang P Y,Wu C H. Fluorometric determination of ammonium ion by ion chromatography using postcolumn derivatization with o-phthaldialdehyde[J]. J Chromatography A,2005,1085(1): 91–97.
[5]Meseguer-Lloret S,Molins-Legua C,Campins-Falco P. Selective determination of ammonium in water based on HPLC and chemiluminescence detection [J]. Anal Chim Acta,2005,536(1–2): 121–127.
[6]Watson R J,Butler E C V,Clementson L A,et al. Flow-injection analysis with fluorescence detection for the determination of trace levels of ammonium in seawater[J]. J Environ Monit,2005,7(1): 37–42.
[7]Wang P Y,Wu J Y,Chen H J,et al. Purge-and-trap ion chromatography for the determination of trace ammonium ion in high-salinity water samples [J]. J Chromatography A,2008,1 188(2): 69–74.
[8]Takahashi M,Nakamura K,Jin J. Study on the indirect electrochemical detection of ammonium ion with in situ electrogenerated hypobromous acid[J]. Electroanalysis,2008,20(20): 2 205–2 211.
[9]Oliveira S M,Lopes T,Toth I V,et al. Determination of ammonium in marine waters using a gas diffusion multicommuted flow injection system with in-line prevention of metal hydroxides precipitation[J]. J Environ Monit,2009,11(1):228–234.
[10]林红梅,林奇,徐国杰,等.离子色谱法测定海水中的阳离子[J].化学分析计量,2011,20(2): 27.

