硫酸氢氯吡格雷片包装材料对药品质量影响研究
吴路民 刘伟芬 李禄辉
(1.辅仁药业集团有限公司,河南 鹿邑477293;2.河南省医药学校,河南 开封475004)
0 背景
心血管疾病尤其是冠心病等是严重威胁人类健康的主要疾病。为了防止急性冠脉综合征患者PCI 术后由于血小板激活而引起的心血管不良事件,术后必须采用抗血小板治疗。 硫酸氢氯吡格雷是抗血小板治疗的有效药物之一。 硫酸氢氯吡格雷为血小板聚集抑制剂,能选择地抑制ADP 与血小板受体的结合, 随后抑制激活ADP 与糖蛋白GPⅡb/Ⅲα 复合物,从而抑制血小板的聚集。
本文通过影响因素试验分别对以普通包装片和避光包装片的两种硫酸氢氯吡格雷片中的有关物质进行研究和检测,旨在提供一种可靠的包装保证药品生产、流通和使用中的安全有效。
1 仪器与材料
高效液相色谱仪(LC-15C 泵;紫外检测器SPD-15C;自动进样器;SIL-10AF 色谱工作站,日本岛津);硫酸氢氯吡格雷片(自制);干燥箱(北京中兴伟业仪器有限公司);KQ-250 型超声波清洗器(昆山市超声仪器有限公司);光照试验箱。
硫酸氢氯吡格雷对照品(纯度质量分数为99.9%,中国药品检验所); 硫 酸 氢 氯 吡 格 雷 对 照 品 杂 质A (CAT.NO.1140586 USP ROCKVILLE MD LOT GOH250 118%); 硫酸氢氯吡格雷对照品B(CAT.NO.1140597 USP ROCKVILLE MD LOT G1H047 110%);硫酸氢氯吡格雷对照品杂质C (CAT.NO.1140600 USP ROCKVILLE MD LOT F2H215 99%);甲醇(色谱纯,J&K SCIENTIFIC LTD);乙腈(色谱纯,J&K SCIENTIFIC LTD);磷酸二氢钾(优级纯,国药集团化学试剂有限公司);水为纯净水。
2 方法与结果
2.1 试验样品的放置
将硫酸氢氯吡格雷片Ⅰ(普通包装)和Ⅱ(避光包装)分别于60℃,相对湿度75%、92.5%及4500 lx 光照条件下放置10 d, 分别于第5 天和第10 天取样分析。
2.2 有关物质的测定
采用HPLC 法测定硫酸氢氯吡格雷片有关物质。
2.3.1 有关物质检查溶液的配制
系统适用性溶液的制备:精密称取硫酸氢氯吡格雷约2.5mg,杂质B 5mg,置100ml 量瓶中,加流动相稀释至刻度,摇匀,即得。
供试品溶液的制备:取细粉适量(约相当于氯吡格雷75mg),精密称定,置200ml 量瓶中,配制供试品溶液。
对照品溶液1 的配制:用硫酸氢氯吡格雷对照品、氯吡格雷杂质A 对照品和氯吡格雷杂质C 对照品, 按照中国药典2010 年版二部第二增补本的方法配制对照品溶液1(用作系统适用性色谱柱实验)。
对照品溶液2 的配制:用硫酸氢氯吡格雷对照品,氯吡格雷杂质A 对照品,氯吡格雷杂质C 对照品,杂质B 对照品,按照中国药典2010 年版二部第二增补本的方法配制对照品溶液2(用作供试品测定)。
2.3.2 色谱条件和系统适用性色谱柱[1]
色谱条件和系统适用性: 按照中国药典2010 年版二部第二增补本的方法进行色谱条件和系统适用性色谱柱实验, 应符合以下规定。供试品溶液氯吡格雷杂质A 不得过0.5%, 氯吡格雷杂质C 不得过1.0%,杂质B 不得过0.3%,其它单个杂质不得过0.2%,杂质总量不得过1.5%。
2.3.3 测定方法
有关物质检查:精密量取各溶液10 ul,注入高效液相色谱仪,以外标法计算。
2.3.4 测定结果
按规定取样时间点取样,研成细粉,按“2.3.1”制备待测对照品和各供试品溶液,检测各溶液中硫酸氢氯吡格雷有关物质的含量,考察两种硫酸氢氯吡格雷片的稳定性,结果如下。
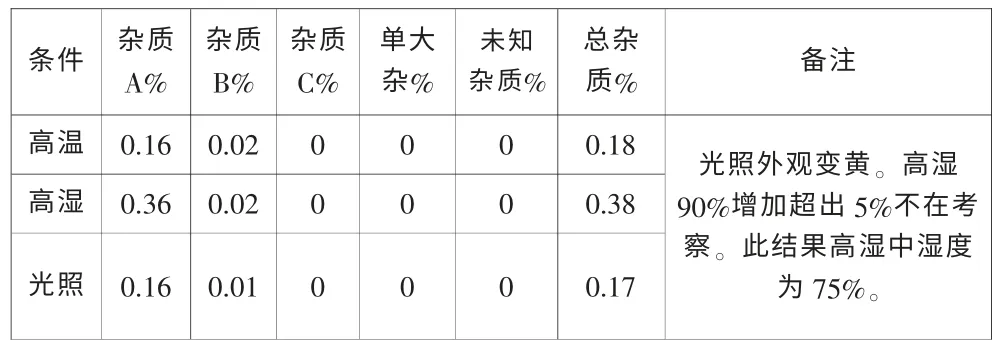
表1 5 天测定结果:普通包装片
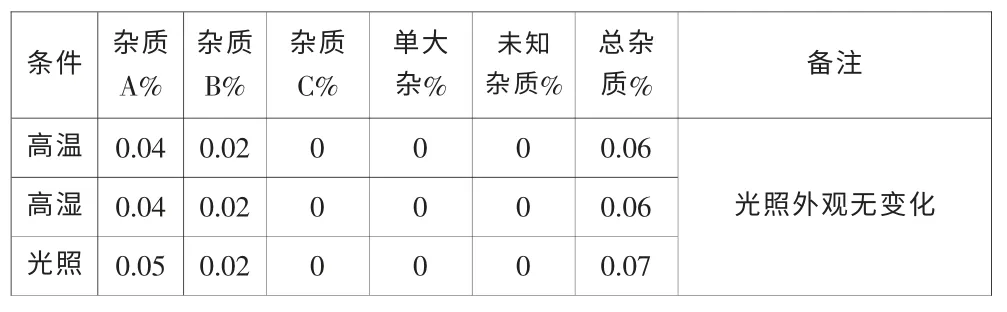
表2 5 天测定结果:遮光包装片
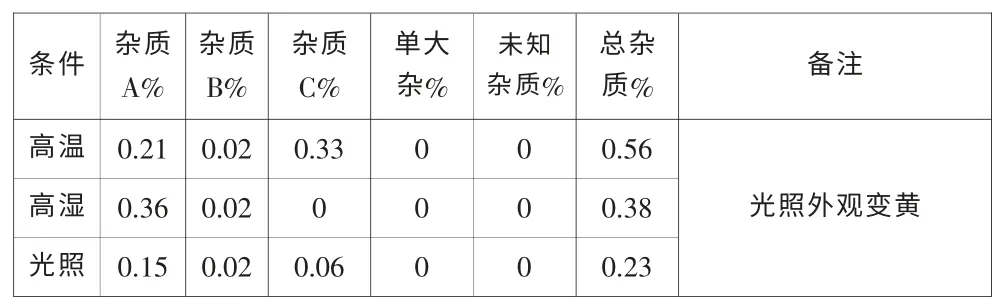
表3 10 天测定结果:普通包装片

表4 10 天测定结果:遮光包装片
由测定结果可知:普通包装片不稳定,杂质A、B、C 都递增,受光照影响会变色,易吸潮,不方便储存,质量影响比较大。避光光包装片比较稳定,杂质A、B、C 没有明显变化,质量较好,所以采用避光密封保存。
3 讨论
本文通过对普通包装片和避光光包装片在一定条件下放置后的有关物质考察研究,结果发现普通包装片有关物质都有所增加,外观亦发生明显变化。 所以推荐硫酸氯吡格雷片用遮光密封保存。
[1]Ch.P(2010)VolⅡthe second supplement[S].2010:Appendix 325.

