丙烯酸酯工业制备方法的研究进展
梁西良,郑力威,王 旭*,王文博
(1.黑龙江省科学院 高技术研究院,黑龙江 哈尔滨150020;2.黑龙江省科学院 石油化学研究院,黑龙江 哈尔滨150040)
前 言
丙烯酸酯(CH2=CHCOOR)分子中含有被羰基活化了的α、β 不饱和双键结构,因而可以构筑成千上万的具有各种性能的聚合物配方,可以乳液聚合、溶液聚合,可以与其它聚合单体共聚,可以是塑型聚合物,也可以是交联聚合物,得到黏度、硬度、耐久性、玻璃化温度各不相同的产物,因而使其产物具有多种多样的用途。丙烯酸酯类被广泛用于涂料、织物、胶黏剂和塑料,丙烯酸酯聚合或共聚可以在高吸水材料、洗涤剂、分散剂、絮凝剂和增稠剂等方面得到应用。
丙烯酸酯生产的唯一重要途径是醇和丙烯酸的直接酯化法。丙烯酸是最简单的脂肪族不饱和羧酸。1843年JosephRedtenbach以丙烯醛为原料,用氧化银为催化剂进行液相氧化时,第一次制得了丙烯酸。1873年CasparyandTollens制备了甲基、乙基和烯丙基丙烯酸酯,并观察到烯丙基丙烯酸酯在常温下,特别是在阳光下,即可发生固化,得到透明的固化物,从而发现了丙烯酸酯的聚合作用。1880年Kahlbaum首先对甲基丙烯酸酯进行了聚合,该聚合物完美的透光性以及优异的物理性能促使其对甲基丙烯酸酯及其聚合物进行了更加深入的研究。其建立了与甲基丙烯酸酯完全一致的经验式,并测定了甲基丙烯酸酯聚合物的溶解性、比重折射率和热稳定性,令人惊讶的是甲基丙烯酸酯聚合物直到升温320℃时才发生解聚。尽管在高温稳定性上具有不可思议的发现,但由于缺乏对其性能的了解,丙烯酸酯长期停留在试验室研究阶段。直到1901年,OttoRohm对丙烯酸酯的制备和聚合性能进行了详细和广泛的研究之后,发现其聚合物具有极其重要的工业用途,自此开始探索可能用于工业生产的方法[1]。由于缺乏令人满意的工业生产方法,使丙烯酸酯的早期商业开发受到限制。丙烯酸酯的实验室制备方法是通过氧化溴与烯丙醇的加成产物,得到α,β-二溴丙酸再与适当的醇进行酯化,最后脱溴制备而成。从原材料成本以及收率上来考虑,采用该方法大规模地制备丙烯酸酯显然是不切实际的。因此,找到一种方便价廉地生产丙烯酸的方法是工业开发丙烯酸酯的重要步骤。在其发展历程上,丙烯酸及酯类工业生产有多种方法,如氯乙醇法、氰乙醇法、Reppe法、烯酮法、甲醛-乙酸法、丙烯腈水解法、乙烯法、环氧乙烷法和丙烯氧化法等[2~5]。
1 丙烯酸酯生产工艺的发展
1.1 氯乙醇法
氯乙醇法是最早的丙烯酸工业生产方法。1927年和1931年,罗门哈斯(Rohm&Haas)公司先后在德国和美国建立生产装置,采用氯乙醇和氰化钠为原料,在碱性催化剂存在下进行反应得到氰乙醇,氰乙醇在硫酸存在下脱水生产丙烯腈,再经水解(或醇解),从而在工业规模上得到丙烯酸(酯)。
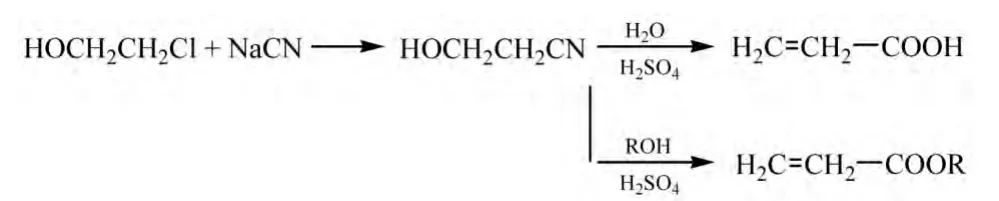
但由于反应过程会生成各种聚合物,因此丙烯酸收率较低,仅为60%~70%,故采用此法的生产装置早在20世纪50年代就已关闭。
1.2 氰乙醇法
氰乙醇法由氯乙醇法发展而来,随着石油化学工业的发展,改用环氧乙烷为原料,使其与由氰化钠和硫酸作用而得的氰化氢反应而得氰乙醇。1948年左右又用由天然气制得的氰化氢代替原来的氰化钠,使生产成本大幅度下降,1949年美国联合碳化物公司(UCC)亦用此法投入生产。
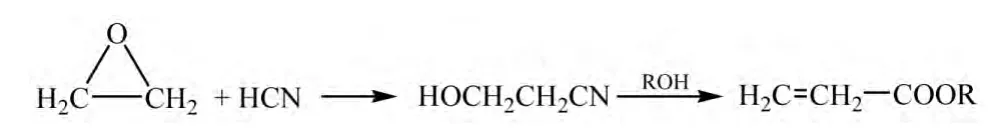
氯乙醇法及其改进方法在以后较长时间内成为各国生产丙烯酸及其酯的主要方法[6]。但此类方法丙烯酸收率仅为60%~70%,且氰化物剧毒,严重污染环境,投资和生产成本高,Rohm&Haas公司和UCC公司先后于1954年和1957年改用Reppe法和丙烯直接氧化法生产丙烯酸。
1.3 Reppe法
1939年,德国化学家WalterJuliusReppe在研究乙炔生产丙烯酸和丙烯酸酯时,发现有两种方法能使乙炔、一氧化碳与水或醇反应生成上述产品。
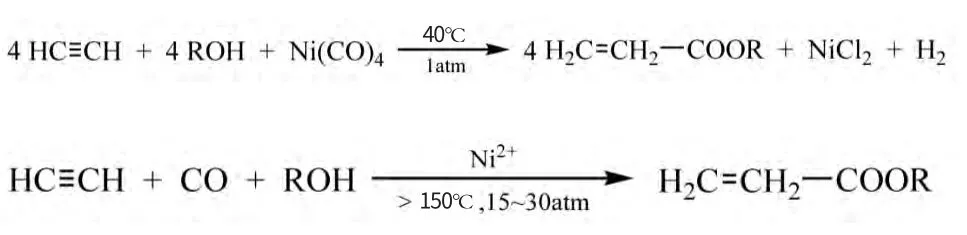
上述两种方法在反应中会使用到(或生成得到)大量毒性物质羰基镍,而且高温高压下,乙炔又有分解倾向,丙烯酸酯与乙炔亦可能发生聚合,容易造成危险后果,因此对工业生产来说存在一定问题。后来,美国Rohm&Haas公司和德国巴斯夫(BASF)公司分别改进了Reppe法,克服了上述缺点。
1956年德国BASF公司作了进一步改进,形成高压Reppe法,使生产能力达到了30万吨/年。它用四氢呋喃作溶剂,使反应中所需的大部分乙炔溶于四氢呋喃中,减少了高压处理乙炔的危险性。同时以溴化镍作催化剂、溴化铜作促进剂,不使用羰基镍,于200~225℃和80~100MPa的条件下,与含循环乙炔的一氧化碳和水反应,停留30min以后生成丙烯酸,然后再与醇反应生产相应的酯。
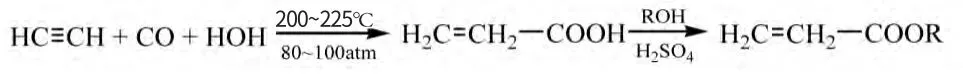
1960年,BASF公司和美国道公司组成DOWBadische公司采用高压Reppe法建立了丙烯酸的工业化生产装置。
Rohm&Haas公司基于Reppe的发明,将两种方法进行了结合,形成了改良Reppe法,在反应中通入一氧化碳,使合成丙烯酸所需的60%~80%的羰基来源于一氧化碳,这样镍的回收和羰基镍的再生可以大大减少,反应收率也得到了提高,如果停止输入一氧化碳即可停止反应。
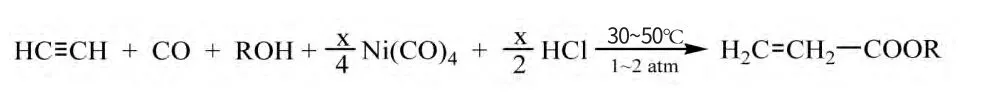
当x=1,即为Reppe法;当x<1,即为改良Reppe法,通常x可取0.2。
BASF公司也采用过改良Reppe法进行丙烯酸生产,其催化剂采用CuBr2和NiCl2体系。
1.4 烯酮法(β-丙内酯法)
该法采用乙烯酮(由丙酮和乙酸为原料制得)与无水甲醛反应生成β-丙内酯,β-丙内酯与热磷酸接触异构化生成丙烯酸,与醇和硫酸处理则生成丙烯酸酯。

乙烯酮法生产的产品纯度高、产品收率高,但用此法生产丙烯酸和丙烯酸酯的工厂很少,只有美国塞拉尼斯(Celanese)和B.F.Goodrich两家公司在20世纪60、70年代进行过工业生产,这主要是因为原料价格高,β-丙内酯为高毒性物质,同时生成的乙烯酮性质活泼,易于聚合,生产中对过程控制要求较高,所以当今工业上已不用此法生产。
1.5 甲醛-乙酸法
20世纪70年代因石油价格高涨,人们寻找以非石油原料路线合成丙烯酸,甲醛-乙酸法应运而生。甲醛和乙酸皆可由甲醇生产,甲醇来自合成气。乙酸及其酯在催化剂存在下与甲醛缩合可生成β-羟基丙酸及其酯,再经脱水即生成丙烯酸及其酯。

催化剂主要是一些金属盐类和金属氧化物,担载 在SiO2和Al2O3-SiO2载体上, 反应温度350~400℃、常压,依不同的催化剂和物料比,反应物转化率为30%~70%。该法技术上可行,但工艺比较复杂,且投资高,因而难以被工业界所接受。
1.6 丙烯腈水解法
丙烯腈化学水解合成丙烯酸的方法实际上是早期氰乙醇法的发展。20世纪60年代,丙烯氨氧化生产丙烯腈得到了发展,丙烯腈来源丰富,因此,在一定的条件下,可由丙烯腈路线来合成丙烯酸。该方法是法国UgineKuhlmann公司在1955年左右开发的,在硫酸作用下丙烯腈首先水解生成丙烯酰胺,后者进一步水解或醇解,生产丙烯酸或丙烯酸酯。

丙烯腈化学水解法工艺简单,反应条件相对温和,产品的分离和精制比较容易,投资较少,缺点是副产物酸性硫酸铵处理困难,污染严重。日本旭化成公司、CibaSpecialtyChemicals公司、Celanese公司曾使用此法生产丙烯酸,后于20世纪90年代分别停产或转为其他方法生产。
研究人员也尝试采用生物催化丙烯腈合成丙烯酸的方法[7~9],从而解决丙烯腈化学水解法的污染问题,并得到收率较高的丙烯酸,目前,该方法已初步达到工业化应用水平,但尚未进行工业化生产。
1.7 乙烯法
乙烯法是以乙烯为原料,以PdCl2和CuCl2复合体系为催化剂,通过乙烯的羰基化和氧化相结合来合成丙烯酸。
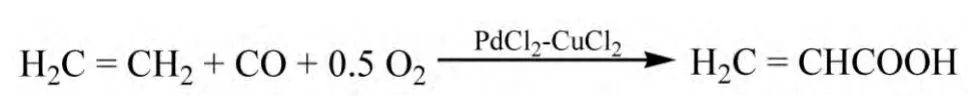
美国联合石油(Unionoil)公司于1973年使用该方法建成工业化装置。后期,又有研究人员开发了二氧化碳与乙烯通过偶联反应制备丙烯酸的方法[10~12]。目前,乙烯法生产丙烯酸尚处在开发当中,工艺尚不成熟。
1.8 丙烯氧化法
丙烯氧化法有一步法和两步法之分。
(1)一步氧化法的反应为:
(2)两步法的反应为:
第一步,丙烯氧化生成丙烯醛。
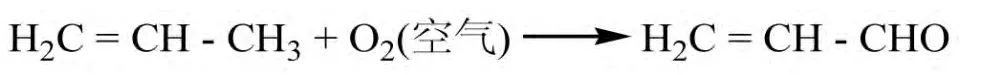
第二步,丙烯醛进一步氧化生成丙烯酸。

丙烯二步氧化法工艺路线是1960年开发的合成工艺,1969年UCC公司在美国建成第一套生产装置,接着日本触媒化学(NSKK)公司(1970年)、三菱化学(MCC)公司(1973年)以及美国Celanese公司(1973年)相继建厂。
除以上介绍的几种丙烯酸及酯的合成方法之外,近年来研究人员还开发了丙烷氧化[13]、环氧乙烷羰基化[14~16]等方法来制备丙烯酸,但这些方法工艺尚不成熟,尚未有大规模的生产装置。时至今日,丙烯氧化法是世界上工业合成丙烯酸的主流工艺方法,几乎所有的工业化大型丙烯酸生产装置全部采用丙烯两步氧化法进行生产。
2 结束语
由于丙烯酸酯所具备的独特的物理、化学和力学等性能,使其应用领域不断被开拓。随着市场需求的持续增长,丙烯酸酯的新产品以及高效、节能、绿色、环保的新生产工艺必将得到进一步的开发。
[1]上海市石油化学研究所情报组.丙烯酸和丙烯酸酯[J].石油化工, 1973(2): 163~170.
[2]陶子斌.丙烯酸生产与应用技术[M].北京: 化学工业出版社,2007 .
[3]陶子斌.世界通用丙烯酸及其酯类发展概况[J].丙烯酸化工与应用,2000, 13(1): 1~9.
[4]杨华.国内外丙烯酸(酯)市场现状与发展趋势[J].精细化工原料及中间体, 2006(8): 14~20.
[5]薛建萍.丙烯酸合成、应用及市场前景, 2007 中国玉米化工国际论坛论文集[C].北京,2007: 179~187.
[6]NEHER, H T.Acrylic Resins [J].Industrial & Engineering Chemistry, 1936,28(3): 267~271.
[7]NAGASAWA, T, NAKAMURA T , YAMADAH..Production of acrylic acid and methacrylic acid using Rhodococcus rhodochrous J1 nitrilase[J].Applied Microbiology and Biotechnology, 1990,34(3): 322~324.
[8]ARMITAGE, Y C , HUGUEHS J, WEBSTER N A.Nitrilase from Rhodoccus rhodochrous for converting acrylonitrile directly to acrylic acid: US, 5998180A[P].1999-12-07.
[9]DICOSIMO, R,FALLON R,JOHN E.Method for producing methacrylic acid acrylic acid with a combination of enzyme catalysts: US, 667015[P].2003-12-30.
[10]HOBERG H D.SCHAEFER.Nickel (0)-induzierte c-cverknüpfung zwischen alkenen und kohlendioxid[J].Journal of Organometallic Chemistry, 1982, 236(1): 28~30.
[11]GRAHAM D C.Production of Acrylic Acid through Nickel-Mediated Coupling of Ethylene and Carbon Dioxide-A DFT Study[J].Organometallics, 2007, 26(27): 6784~6792.
[12]BRUCKMEIER, C.Formation of Methyl Acrylate from CO2and Ethylene via Methylation of Nickelalactones[J].Organometallics,2010,29(10):2199~2202.
[13]王鉴, 郭丽,孟祥龙,等.丙烷直接氧化制丙烯酸的研究进展及展望[J].化工进展, 2008,27(8): 1170~1174.
[14]EIT D,ERIC K.Carbonylation of epoxides: US,5310948A[P].1994-05-10.
[15]DRENT E, KRAGTWIJK E.Carbonylation of epoxides: US,5359081[P].1994.
[16]SLAUGH L.H., T.C.Forschner.Method to prepare .α-β unsaturated carboxylic acids from epoxides using a cobalt and tin catalyst system: US,6084124[P].2000 -07-04.

