基于CONSORT的心血管疾病临床随机对照试验报告质量评价
张晔,黄亚明,赵玉虹
随机对照试验(randomized controlled trial,RCT)是采用随机分配的方法,将合格的研究对象分别分配到试验组和对照组,然后接受相应的试验措施,在一致的条件下或环境中,同步地进行研究和观测试验的效应,并用客观的效应指标对试验结果进行科学的测量和评价[1]。1996年,临床试验报告统一规范—CONSORT(Consolidated Standards of Reporting Trials)声明出版,并于2001、2010年进行了两次修订。目前国内RCT呈逐年增多的趋势,但质量参差不齐,部分研究有待进一步提高。近几年有学者开始应用CONSORT声明评价RCT报告质量,但多数针对中医药或中西医结合方面,且仅使用某一版CONSORT声明评价。
本研究采用1996年、2001年、2010年三个版本的CONSORT声明,尝试构建新的指标赋权方案,对样本中各条目报告的情况酌情赋分(采用10分制),然后依据各条目加权得分对心血管疾病RCT报告质量进行评价。
1 材料与方法
1.1 文献检索 计算机检索万方数据库、中国知网(CNKI)及PubMed收录的1997年1月至2012年12月国内期刊上公开发表的有关心血管疾病的RCT。筛选出符合标准的文献。检索时间为2013年3月8日。
1.2 方法
1.2.1 评价报告的工具 CONSORT 2010声明:报告平行对照随机临床试验指南的更新[2]、CONSORT 2010说明与详述:报告平行对照随机临床试验指南的更新[3]、CONSORT 1996声明:提高随机对照试验报告的质量[4]和CONSORT 2001说明与详述:报告随机对照试验指南的更新[5]。
1.2.2 纳入标准 1997年1月至2012年12月发表于国内期刊上的文献;所作研究属于心血管(循环系)疾病范畴;文献中有说明是随机对照试验;全文报告信息或数据完整。
1.2.3 排除标准 非随机对照试验、半随机对照试验及非干预性临床研究;同一样本的重复研究结果;会议论文;无法获取全文;中医药、细胞生物学研究或评价医疗器械疗效(如:介入器材)研究等。
1.2.4 RCT报告质量评价指标赋权、赋分原则 比对三版CONSORT声明条目[2,4,5],三版都有的一级或二级条目,予以权值1;出现在两版中的一级或二级条目,予以权值0.9;出现在一版中的一级或二级条目,予以权值0.7;赋予2010版新加入的“其他信息”条目(条目23、24、25)权值0.5。具体赋权方案见表1。
采用十分制对各条目进行酌情赋分。具体赋分方案见表2。不以报道形式为第一准则,以条目指标相应数据或信息报告的完整性(科学研究设计或方法的完善性)为基准。
1.2.5 资料提取和评价 由两名研究者逐篇阅读纳入RCT中对CONSORT各条目信息的报告情况,按描述明细程度记分,并标识统计各条目内容在文章中出现的具体位置。若有异议,则交叉核对。
1.3 统计学方法 ①采用Microsoft Excel2003计算各RCT质量加权得分,雷达图法分析RCT报告各组成部分质量平均分的变动情况。②采用SPSS 16.0进行统计学分析。分层分析报告质量加权得分均数比较采用t检验。P<0.05为差异具有统计学意义。
2 结果
2.1 文献检索结果 共检出879篇RCT文献,其中万方数据库149篇,CNKI 314篇,PubMed 416篇。依纳入排除标准,阅读文题、摘要及全文后最终纳入RCT文献368篇。
2.2 RCT报告质量评价结果
2.2.1 RCT报告总质量评价结果 368篇RCT报告质量平均134.96分(满分329)。换算成百分制后,为41.02,其中最高分为62.25,最低分为21.49。各分数段(百分制)篇数百分比分布见图1。各条目平均分见图2。
2.2.2 RCT报告各组成部分质量评价结果 RCT报告共分为六部分,文题和摘要、引言、方法、结果、讨论和其他信息。本研究中,RCT报告文题和摘要部分平均得分5.46,引言部分平均得分9.44,方法部分平均得分3.50,结果部分平均得分4.14,讨论部分平均得分3.79,其他信息部分平均得分0.02。RCT设计的核心为如何随机分配受试者,随机分配受试者包括3个步骤:分配序列生成、分配隐藏和分配实施。就本研究样本所示,随机方法部分平均得分仅为1.07。
发表时间不同的RCT报告各组成部分质量平均分(满分10分)及变动范围如图3、图4示。
2.2.3 RCT对应各评价条目信息描述位置不当 条目3a(方法),32篇在摘要、9篇在引言中描述;条目13a(结果),15篇在方法、1篇在讨论描述;条目13b(结果),16篇在方法、1篇在讨论描述;条目14a(结果),28篇在引言、4篇在摘要描述;条目15(结果),58篇在方法描述;条目16(结果),1篇在摘要、16篇在方法描述。条目19(结果),1篇在方法、10篇在讨论描述。
2.3 依数据库收录与否的RCT报告质量分层分析结果 分别按是否被PubMed数据库收录、是否被中国科学引文数据库(CSCD)收录、是否被中国科技核心期刊刊载、是否被中华医学会期刊刊载划分RCT报告,共得到8个分层子集。“是否被PubMed数据库收录”分层子集RCT报告质量加权平均分(“是” vs. “否”):[(40.87±7.23) vs. (41.48±7.90),P=0.499];“是否被CSCD收录”分层子集RCT报告质量加权平均分:[(41.38±7.43) vs. (39.48±7.10),P=0.056];“是否被中国科技核心期刊刊载”分层子集RCT报告质量加权平均分[(41.27±7.28)vs. (38.78±8.11),P=0.052];“是否被中华医学会期刊刊载”分层子集RCT报告质量加权平均分:[(42.56±7.10) vs. (39.04±7.31),P=0.000]。
3 讨论
3.1 RCT报告质量评价分析 国内RCT报告质量处于中等或中下等水平,与同类报道一致[7,8],还需进一步提高。其中,未报告条目24、25原因可能是大部分临床试验研究者还没有公开临床试验方案或资助来源的意识。极少数文献报告具体的国际注册号。这可能与中国目前对临床试验注册制度的宣传和教育不够,及大部分杂志尚未对注册制度进行强制要求有关,与目前报道较一致[9]。
RCT核心部分为试验的随机化过程。本研究中,随机方法部分各条目平均得分仅为1.07,其中,仍有64.4%的文献未报告产生随机分配序列的方法,仅6篇(1.63%)文献对随机方法的类型或限定的细节进行了说明,即使用何种程序或软件来生成随机序列,与Süt N等[10]研究所得出的结论较一致。仅4.08%的文献不同程度地对分配隐藏机制或过程进行了说明。盲法的正确实施,能够减少偏倚。而本研究中,仅9篇对试验盲法以及实施进行了说明;另有50篇仅提到试验中使用了双盲法,22篇提到试验中使用了单盲法,26篇提到该研究为开放性试验;70.92%的文献未对盲法的实施进行说明。

表1 CONSORT条目[6]赋权方案
37条评价条目中,报告条目信息位置或内容也存在不规范问题。存在方法或结果条目信息在摘要、引言或讨论中描述的情况,只简单描述、提到条目信息。
3.2 依数据库收录与否的RCT报告质量分层处理结果分析 “是否被中华医学会期刊刊载”分层子集RCT报告质量具有显著差异,且中华医学会期刊所刊载的RCT报告质量较非中华医学会期刊所刊载的RCT报告质量要好;而其他分层子集RCT报告质量都无显著差异,这与Smith BA等[10]研究所得出的结论较相似。
总而言之,我国RCT报告质量距CONSORT声明关于RCT报告标准的规定依旧相差甚远,尤其是方法学部分、RCT三大关键特征方面,仍有很大的提升空间。在将来的研究中,研究者应尽量采用CONSORT声明作为RCT报告写作的指导工具,依据CONSORT声明清单各条目严格设计出高质量的RCT。

表2 各条目具体赋分及相关定义(采用10分制赋分)

条目 分值 解释C:0 未说明所用附加分析的方法且该文为非多中心试验13a A:10能够说明随机分配到各组的受试者例数及各组接受已分配治疗的例数B:7 只说明随机分配受试者的总例数及接受已分配治疗的总例数C:0 未说明随机分配到各组的受试者例数及各接受已分配治疗的例数13b A:10能够说明各组失访和被剔除的例数及原因B:8 文中直接或间接说明未出现失访或被剔除的情况C:7 只说明试验失访和被剔除的总例数及原因D:5 能够说明各组失访和被剔除的例数但未说明原因E:0 未说明各组失访和被剔除的例数及原因14a A:10能够说明招募期和随访时间的长短,并说明具体日期B:7 只提到随访时间C:0 未说明招募期和随访时间的长短及具体日期14b A:10提及且解释试验中断或停止的原因B:0 未提及试验中断或停止的信息15 A:10能够列出每一组受试者的基线数据,包括人口学资料和临床特征B:5 能够简单说明每一组受试者的基线数据,包括人口学资料和临床特征或没有对各组进行分别说明C:3 只简单提及每一组受试者的基线数据,包括人口学资料和临床特征,如:“……无统计学意义。”D:0 未提及每一组受试者的基线数据或基线数据中未包括人口学资料或未包括临床特征16 A:10能够说明各组纳入每一种分析的受试者数目,及能够直接或间接说明分组分析的方法(ITT还是PP)B:7 能够说明各组纳入每一种分析的受试者数目但未提及分组分析的方法C:0 未说明各组纳入每一种分析的受试者数目且未提及分组分析的方法17a A:10能够列出各组每一项主要和次要结局指标的结果,效应估计值及其精确性(所列结果全部有95%可信区间)B:9 能够列出各组每一项主要和次要结局指标的结果,效应估计值及其精确性(所列结果部分有95%可信区间)C:8 能够列出各组每一项主要和次要结局指标的结果,效应估计值及其精确性(所有结果无95%可信区间,但有P值)D:3 能够列出各组每一项主要和次要结局指标的结果,效应估计值但未列出其精确性E:0 各组每一项主要和次要结局指标的结果17b A:10提及二分类结局,且同时提供相对效应值和绝对效应值B:0 未提及二分类结局18 A:10能够说明所做辅助分析的结果且能够指出哪些是预先设定的分析,哪些是新尝试的分析B:5 能够说明所做辅助分析的结果,但未指出哪些是预先设定的分析,哪些是新尝试的分析C:0 未提及所做辅助分析的结果或12b未说明所用附加分析的方法19 A:10能够介绍各组出现的严重危害或不良事件B:5 简单介绍各组出现的严重危害或不良事件C:3 简单提及各组出现的严重危害或不良事件D:0 未提及各组出现的严重危害或不良事件20 A:10能够介绍试验的局限性(有“局限性”或“不足”字样),报告潜在偏倚和不精确的原因B:0 未提及试验的局限性(无“局限性”或“不足”字样),报告潜在偏倚和不精确的原因21 A:10有说明试验结果被推广的可能性B:0 未提及试验结果被推广的可能性22 A:10能够对试验结果进行相对应的解释,权衡试验结果的利弊,并且考虑其他相关证据B:7 能够对试验结果进行相对应的解释,权衡试验结果的利弊,但未提及其他相关证据C:0 未对试验结果进行相对应的解释23 A:10有临床试验注册号和注册机构名称B:0 无临床试验注册号和注册机构名称24 A:10有说明在哪里可以获取完整的试验方案B:0 未说明在哪里可以获取完整的试验方案25 A:10有说明资助和其他支持(如提供药品)的来源,及提供资助者所起的作用B:0 未说明资助和其他支持(如提供药品)的来源,及提供资助者所起的作用
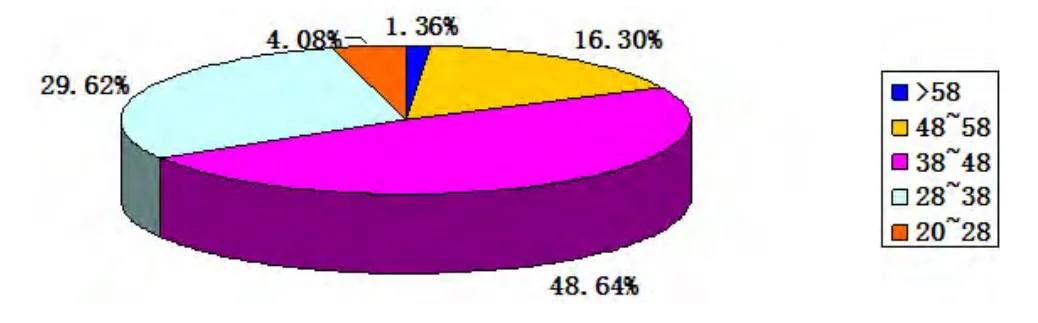
图1 RCT报告质量各分数段(百分制)篇数所占百分比

图2 RCT报告质量各评价条目平均分

图3 RCT报告各组成部分质量评价

图4 RCT报告各组成部分质量评价波动范围
[1] 王家良,王滨有. 临床流行病学[M]. 第三版. 北京:人民卫生出版社.2008:88.
[2] Schulz KF,Altman DG,Moher D,et al. CONSORT 2010 Statement:updated guidelines for reporting parallel group randomized trials[J].BMJ,2010,340:698-702.
[3] Moher D,Hopewell S,Schulz KF,et al. CONSORT 2010 explanation and elaboration: updated guidelines for reporting parallel group randomized trials[J]. BMJ,2010,340:869.
[4] Begg C,Cho M,Eastwood S,et al. Improving the Quality of Reporting of Randomized Controlled Trials. The CONSORT Statement[J].JAMA,1996,276(8):637-9.
[5] Altman DG,Schulz KF,Moher D,et al. The Revised CONSORT Statement for Reporting Randomized Trials: Explanation and Elaboration[J]. Ann Inter Med,2001,134(8):663-94.
[6] 周庆辉译. 随机临床试验应报告的信息CONSORT 2010对照检查清单(Checklist)[EB/OL]. http://www.consort-statement.org.
[7] 王吉林,林艳伟,陆嵘. 世界主要消化病杂志上随机对照试验报告质量比较分析[J]. 循证医学,2011,11(3):176-81.
[8] 张小利,贾万年,胡全兵,等. 七种军队医学期刊临床随机对照试验的报告质量评价[J]. 中国循证医学杂志,2010,10(4):501-4.
[9] 林小婷,李海民,齐国卿,等. 中国儿科领域随机对照试验报告质量横断面调查[J]. 中国循证儿科杂志,2012,7(3):210-5.
[10] Süt N,Senocak M,Uysal O. Assessing the quality of randomized controlled trials from two leading cancer journals using the CONSORT statement[J]. Hematol Oncol Stem Cell Ther,2008,1(1):38-43.
[11] Smith BA,Lee HJ,Lee JH. Quality of reporting Randomized Controlled Trials (RCTs) in the nursing literature: Application of the Consolidated Standards of Reporting Trials (CONSORT)[J]. Nursing Outlook,2008,56(1): 31-7.

