用亚硫酸钠从分银渣中浸出银
陈小红,赵祥麟,楚广,周兆安,杨天足,苏莎
(1. 中南大学 冶金与环境学院,湖南 长沙,410083;2. 金川镍钴研究设计院,甘肃 金昌,737100;3. 深圳市危险废物处理站有限公司,广东 深圳,518049 4. 湖南有色金属研究院,湖南 长沙,410015)
分银渣是指铜阳极泥经硫酸化焙烧,稀酸分铜,碱浸分碲,氯化分金,亚钠分银处理工艺的最后残渣,其主要成分是硫酸铅、硫酸钡,同时还含有少量Ag,Au,Pt和Pd等贵金属,具有一定的综合利用价值[1]。但是,由于分银渣成分复杂,贵金属含量相对又比较低,提取难度较大,过去大多数冶炼厂往往把分银渣放置或者直接返回阳极泥处理工序,加大阳极泥处理工序的负担。随着资源的日益匮乏,分银渣中有价金属的提取逐渐引起重视。目前,分银渣的处理工艺主要分为火法和湿法工艺。孙文达[2]采用火法还原熔炼富集金银工艺处理分银渣,而铜阳极泥中贵金属的提取技术也一直采用火法冶金,其主要缺点是投资大、工艺流程冗长,同时对环境造成污染[3]。分银渣的湿法处理方法主要有硫酸煮浸法[4]、硝酸浸出法[4−5]、硫代硫酸盐浸出法[1,6−7]、氨浸出法[8]和亚硫酸钠浸出法[9−10]。硫酸浸煮法主要适用于银以银单质或氧化银形式存在的废料,虽然流程简单、设备少、易操作,浸出液中除银外还存在大量贱金属硫酸盐,需进一步分离,针对以氯化银为主的分银渣效果并不是太理想。硝酸浸出银是化学上常用的快速提取银的有效方法,特点是溶解能力强、浸出率高,但贱金属与银一起被浸出,同时产生大量NO2气体,操作环境差。硫代硫酸盐浸出法以铜离子作氧化剂和催化剂,采用该法浸出速度快、浸出率高、无毒、贱金属浸出率低、选择性好,适用于浸出Ag,Ag2O,Ag2S和AgCl等多种形式存在的银,还可浸出金,但操作控制要求较严格。氨浸出法主要用于浸出AgCl,其特点是浸出速度快,但同时浸出铜等贱金属,适用的原料较少,同时产生NH3,造成环境污染。亚硫酸钠浸出法是目前工业中较常用的浸银的方法,主要用于浸出以 AgCl形式存在的银[10−12],常用于阳极泥分金后含银渣的浸出。李义兵等[13]研究用亚硫酸钠浸出分银渣中的银,浸出率达到90%以上,但需要进行焙烧预处理,工艺流程加长,也大大增加能耗。本文作者旨在寻找一种更加简便、节能的分银渣处理工艺。
1 亚硫酸钠浸出分银渣中银的反应原理
亚硫酸钠浸出分银渣银的机理主要是利用亚硫酸钠中的亚硫酸与银可以形成较为稳定的配合物[14],以达到浸出的目的,反应方程如下:
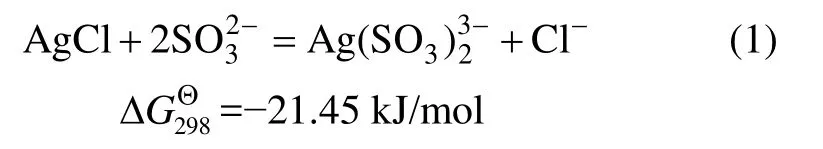
综上分析可知,理论上若想得到较高 AgCl浸出率,不仅需要增加浸出剂Na2SO3的质量浓度,还要保证较高的 pH,使其有足够的,与此同时要适当保持低的Cl−浓度。
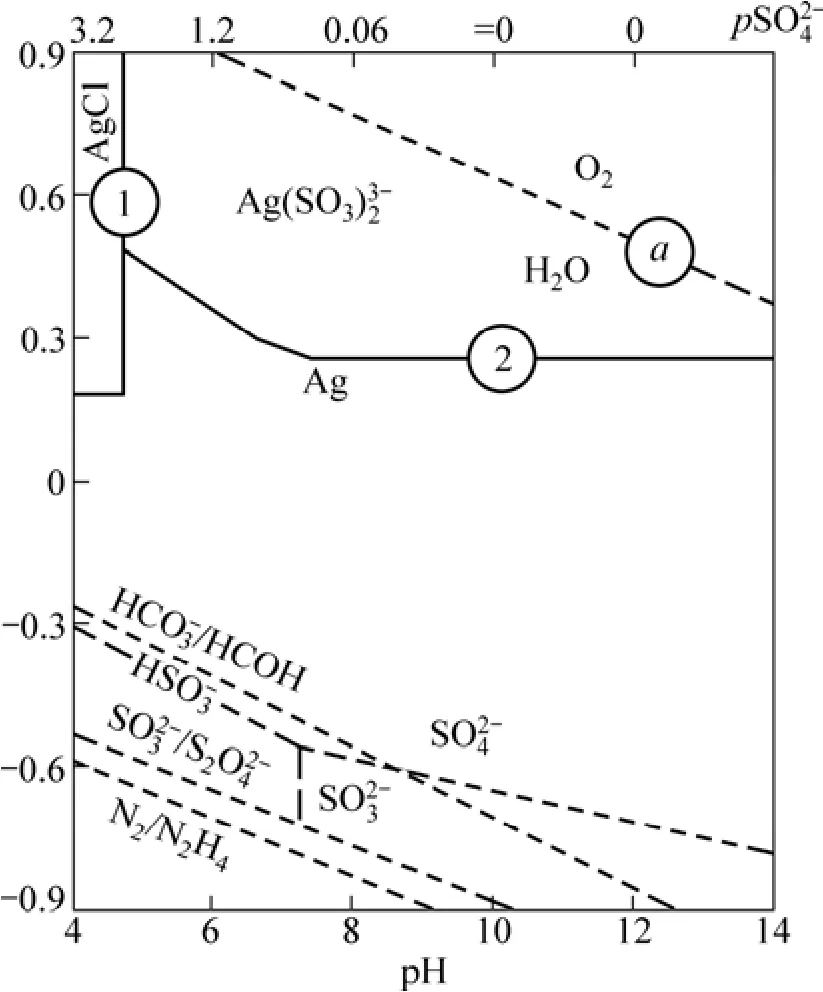
图1 25 ℃时AgCl--H2O系电位−pH图Fig. 1 E-pH diagram for AgCl--H2O system at 25 ℃=0.25 mol/L, c[Cl−]=0.5 mol/L, =1 mol/L, P O 2 =PH 2=1×105 Pa)
2 实验
2.1 实验原料
本研究所用的分银渣样品是某公司贵金属车间阳极泥分金分银后的渣样,渣样含水质量分数为30%~40%。先预先将渣样在烘箱中经90 ℃左右的温度烘干,分样。对干渣样进行XRF和XRD分析,其结果如表1和图2所示。
由表1可知:分银渣中主要元素组成为铅、钡、硫和氧。结合图2中XRD分析结果可知:分银渣中的主要成分是硫酸钡和硫酸铅,此批分银渣中银的质量分数为 2.19%,具有相当可观的回收价值。此外,Sb和Ni质量分数均近4%,也具有较高的回收价值。
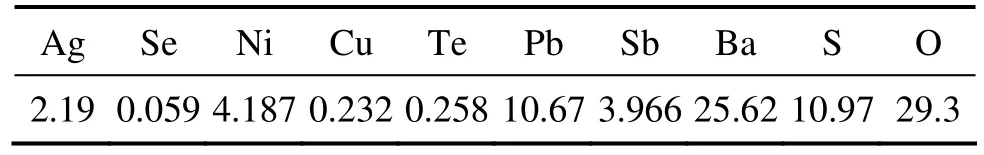
表1 分银渣主要元素组成(质量分数)Table 1 Composition of silver separating residue %
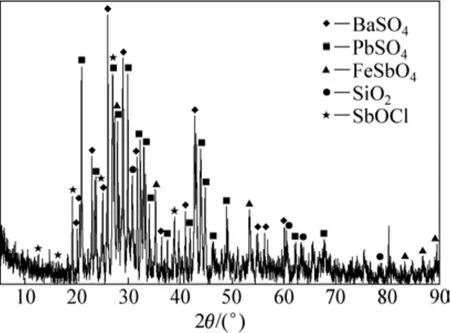
图2 分银渣的XRD图谱Fig. 2 XRD patterns of silver separating residue
2.2 实验仪器
实验过程用到的除普通玻璃器皿外的主要仪器如表2所示。

表2 实验主要仪器Table 2 Main instruments of experiment
2.3 实验方法
分银渣的活化及浸出反应在恒温水浴锅中进行。首先,称取10 g分银渣加入到容积为100 mL的缩口烧杯;然后,加入一定体积的水和磁力搅拌子及一定浓度的稀硝酸,反应一定时间,进行预处理;预处理结束后,按实验浸出液固比加入适量水,并用冰醋酸和醋酸钠缓冲液调节 pH至要求的范围,加入适量的亚硫酸钠,密封后放入恒温水浴锅中升温到指定温度,反应一定时间;反应结束后,将浸出液转移至外置容器并进行真空抽滤,滤液直接送分析,分析其中的银含量。
3 实验结果与讨论
3.1 亚硫酸钠浓度及活化的影响
活化过程:称取10 g分银渣,分别加入20 mL蒸馏水和10 mL质量分数为 2%稀硝酸配成固液比1:3的浆液,在50 ℃下,搅拌、活化1 h。
浸出实验条件:分银渣为 10 g,固液比为 1:8,pH=8,反应温度为30 ℃,反应时间为2 h,实验结果如图3所示。
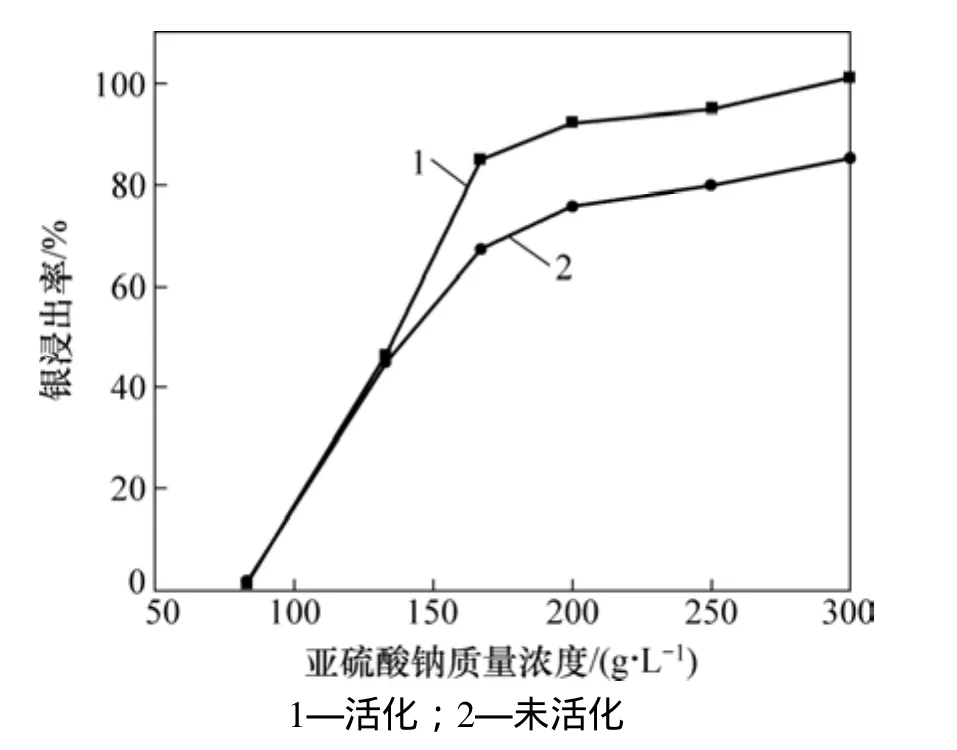
图3 亚硫酸钠浓度及活化对银浸出率影响Fig. 3 Effect of sodium sulfite concentration and activation on leaching rate of silver
从图3可见:随着亚硫酸钠浓度的增大银的浸出率先急剧增大,而后渐渐趋缓。当亚硫酸钠质量浓度达到170 g/L以上时,银的浸出率可以达到90%以上;当亚硫酸钠质量浓度大于200 g/L以后,随着亚硫酸钠质量浓度的升高,银的浸出率变大不太明显。综合考察选定亚硫酸钠的质量浓度为200 g/L。
硝酸活化和未活化两者浸出率的变化趋势都一样,在亚硫酸钠质量浓度小于125 g/L时,此时的浸出率较低且二者差别并不明显,但是随着亚硫酸钠质量浓度的增大,到达175 g/L之后,经硝酸活化后的分银渣的浸出率始终比未活化的浸出率高出约15%,这说明硝酸活化非常有利于银的浸出,能显著提高其浸出率,因此,在浸出反应之前进行硝酸活化是非常有必要的。
3.2 浸出时间及活化剂浓度的影响
实验条件:分银渣为10 g,固液比为1:8,pH为8,反应温度为30 ℃,亚硫酸钠质量浓度为200 g/L;反应时间对银浸出率的影响如图4所示。
由图4可见:反应时间过短、反应不完全、浸出率低;随着反应时间的延长,浸出率有显著的提高,而后继续延长反应时间不仅没能增加浸出率,反而有所降低,经分析觉得可能是存在以下2点原因:(1) 因为过长的反应时间,可能会使浸出剂亚硫酸钠被氧化,从而导致浸出反应逆向进行,浸出率有所下降;(2) 因为过长的反应时间可能会使得反应生成的被氧化而沉淀,从而表现出银的浸出率有所降低,因此,控制反应时间为1~3 h为佳。另外,从图4可见:稀硝酸浓度不同对银浸出率影响不大,在银浸出率最好的1~3 h期间,二者基本相近;在反应时间延长至3 h之后,经过4.5%稀硝酸活化的银浸出率更低些。据此可以得出,使用2%的稀硝酸活化更为合适。
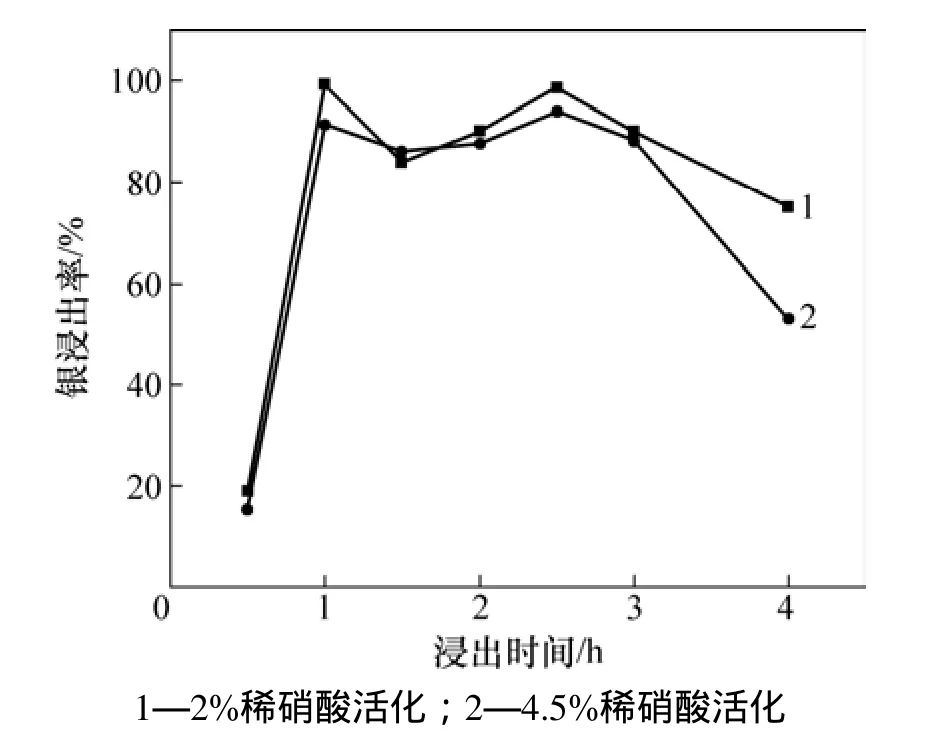
图4 浸出时间及活化剂浓度对银浸出率影响Fig. 4 Effect of leaching time and the activator concentration on leaching rate of silver
3.3 浸出液pH的影响
实验条件:分银渣为10 g,固液比为1:8,反应温度为30 ℃,亚硫酸钠质量浓度为200 g/L,反应时间为2 h;pH对银浸出率的影响如图5所示。
从图5可见:在pH<7时,银浸出率很低,这个是由于亚硫酸钠为强碱弱酸盐,在此 pH下,亚硫酸根会和氢离子发生加质子反应,主要以亚硫酸氢根和亚硫酸的形式存在于水溶液中。因此,此时溶液中的游离亚硫酸根质量浓度较低,浸出效果不是很理想;当pH在8~10之间时,此时溶液中的亚硫酸根质量浓度较高,银的浸出率最好;随着 pH继续升高,的稳定性下降易形成银的氧化物而沉淀,导致银的浸出率有所下降。综上分析得出反应pH在8左右为佳。
3.4 浸出温度的影响
实验条件:分银渣为10 g,固液比为1:8,pH为8,亚硫酸钠质量浓度为200 g/L,反应时间为2 h;反应温度对银浸出率的影响如图6所示。
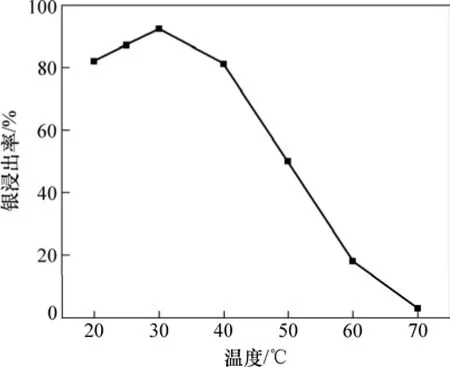
图6 浸出温度对银浸出率影响Fig. 6 Effect of temperature on leaching rate of silver
从图6可见:温度对银浸出率影响很大;当温度小于30 ℃时,银的浸出率随着温度的升高而升高,并在30 ℃时达到最大值91.7%;当随着温度的进一步升高,银的浸出率反而降低。分析其原因可能如下:温度较低时,升温有利于加大反应的驱动力;当温度进一步升高时,由于配合离子高温不太稳定,更易被氧化而沉淀[17]。因此,显现出银的浸出率随着温度的进一步升高而降低的实验结果。
综合银的浸出效果以及能耗考虑,选定浸出温度为30 ℃为宜。
3.5 浸出固液比的影响
实验条件:分银渣为10 g,亚硫酸钠质量浓度为200 g/L,pH为8,反应时间为2 h,温度为30 ℃。固液比对银浸出率的影响如图7所示。
由图7可见:随着固液比的减小,银的浸出率也逐渐增大,固液比达到1:6以上后浸出率增长渐趋平缓。若固液比太大,则不利于银的浸出,达不到有效回收的目的;若固液比太小,在工业生产中浸出液体积太大,银的浓度会比较低,不仅不利于回收银工序的操作,亦会造成废水量的大增,所以,选择固液比为1:8较合适。
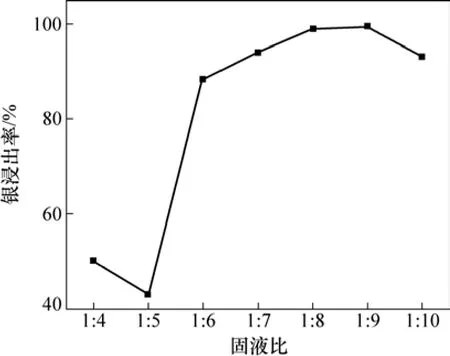
图7 浸出固液比对银浸出率影响Fig. 7 Effect of solid-liquid ratio on leaching rate of silver
4 结论
(1) 实验证明采用稀硝酸预处理亚硫酸钠浸出体系浸取分银渣中的银是可行的,且该工艺简单、有效。
(2) 稀硝酸预处理亚硫酸钠浸出体系浸取分银渣中的银的最佳条件为:2%硝酸预处理,亚硫酸钠质量浓度200 g/L,固液比为1:8,反应时间2 h,温度30 ℃,pH应控制在8,银的浸出率可达95%以上。
[1]张钦发, 龚竹青, 陈白珍, 等. 用硫代硫酸钠从分银渣中提取银[J]. 贵金属, 2003, 24(1): 5−9.ZHANG Qinfa, GONG Zhuqing, CHEN Baizhen, et al.Extracting Ag from residue containing silver with sodium thiosulfate[J]. Precious Metals, 2003, 24(1): 5−9.
[2]孙文达. 分银渣中贵金属的回收[J]. 铜业工程, 2008, 15(1):35−36.SUN Wenda. Recovery of precious metals in silver separating residue[J]. Copper Engineering, 2008, 15(1): 35−36.
[3]周康民, 王璇, 时其衡, 等. 铜阳极泥中提取金银的工艺研究[J]. 江苏地质, 1998, 22(3): 169.ZHOU Kangmin, WANG Xuan, SHI Qiheng, et al. The study of recovering gold and silver from copper anode slime[J]. Jiangsu Geology, 1998, 22(3): 169.
[4]张华. 从富银渣中回收银的方法的研究[J]. 四川有色金属,2000, 17(1): 32−35.ZHANG Hua. Research on the method for recovering silver from sludge with high silver[J]. Sichuan Nonferrous Metals, 2000,17(1): 32−35.
[5]邓昭玉. 几种银盐的提纯与还原方法[J]. 广西冶金, 1992, 4(l):33−36.DENG Zhaoyu. Several silver salt purification and reduction methods[J]. Guangxi Metallurgy, 1992, 4(1): 33−36.
[6]黎鼎鑫, 王永录. 贵金属提取与精炼[M]. 长沙: 中南大学出版社, 2000: 375−385.LI Dingxin, WANG Yonglu. Precious Metal extraction and refining[M]. Changsha: Central South University Press, 2000:375−385.
[7]卢宜源, 宾万达. 贵金属冶金学[M]. 长沙: 中南工业大学出版社, 1994: 452−460.LU Yiyuan, BIN Wanda. Precious metals metallurgy[M].Changsha: Central South University of Technology Press, 1994:452−460.
[8]林成福. 从铜阳极泥中提取金银的湿法工艺[J]. 黄金, 1991,12(1): 43−45.Lin Chengfu. The wet treatment process to extract gold and silver ftom anode copper mud[J]. Gold, 1991, 12(1): 43−45.
[9]张钦发, 龚竹青, 陈白珍. 含银废料中银的综合回收和利用工艺方法[J]. 有色金属, 2004, 56(1): 60−62.ZHANG Qinfa, GONG Zhuqing, CHEN Baizhen. Technologies for recycling of silver scrap[J]. Nonferrous Metals, 2004, 56(1):60−62.
[10]杨茂才, 周杨霎, 孙粤庭. 从铜阳极泥提取金和银[J].贵金属,1997, 18(4): 24−27.YANG Maocai, ZHOU Yangji, SUN Eting. Extraction of gold and silver from copper anode slime[J]. Precious Metals, 1997,18(4): 24−27.
[11]蔡旭麒. 从杂铜阳极泥中提取银金的研究[J]. 有色金属, 1999,20(1): 25−26.CAI Xuqi. Extracting silver and gold from miscellaneous copper anode slime[J]. Nonferrous Metals, 1999, 20(1): 25−26.
[12]付绸林. 铅阳极泥全湿法提取金银的研究[J]. 湿法冶金, 1996,15(3): 27−30.FU Choulin. Study on extracting gold and silver from lead anode slime by hydrometallurgical process[J]. Hydrometallurgy of China, 1996, 15(3): 27−30.
[13]李义兵, 陈白珍, 龚竹青, 等. 用亚硫酸钠从分银渣中浸出银[J]. 湿法冶金, 2003, 22(1): 34−38.LI Yibing, CHEN Baizhen, GONG Zhuqing, et al. Leaching of Ag from residue containing silver with sodium sulfite[J].Hydrometallurgy of China, 2003, 22(1): 34−38.
[14]陈庆邦, 聂晓军, 李明建. 铜阳极泥湿法回收贵金属的工艺研究[J]. 黄金, 1999, 20(5): 38−40.CHEN Qingbang, NIE Xiaojun, LI Mingjian. The study of recovering precious metal from copper anode slime by hydrometallurgical process[J]. Gold, 1999, 20(5): 38−40.
[15]WANG Xuewen, HU Jianhui. Behavior of Cl−ions in Ag(SO3)23−solution[J]. Rare Metals, 1997, 16(4): 269−272.
[16]卢宜源, 宾万达. 贵金属冶金学[M]. 长沙: 中南工业大学出版社, 2004: 223−224.LU Yiyuan, BIN Wanda. Precious metals metallrugy[M].Changsha: Central South University of Technology Press, 2004:223−224.
[17]程德平, 夏式均. Ag(SO3)23−-H2O 系热力学分析[J].杭州大学学报, 1991, 18(4): 449−454.CHENG Deping, XIA Shijun. Thermodynamic analysis of Ag-SO32−-H2O system[J]. Journal of Hangzhou University, 1991,18(4): 449−454.

