Pak1在小鼠卵母细胞纺锤体形成中的相关性
李秀红,张献彩,周德山*,马 伟*
(1.首都医科大学 基础医学院 组织学与胚胎学教研室,北京 100069;2.邢台医学高等专科学校解剖学教研室,河北 邢台 054000)
Pak1在小鼠卵母细胞纺锤体形成中的相关性
李秀红1,张献彩2,周德山1*,马 伟1*
(1.首都医科大学 基础医学院 组织学与胚胎学教研室,北京 100069;2.邢台医学高等专科学校解剖学教研室,河北 邢台 054000)
目的研究自动磷酸化Pak1在小鼠卵母细胞减数分裂过程中的亚细胞定位模式及其在纺锤体形成中的相关性。方法用Western blot检测Ser144位点自动磷酸化的Pak1(pPak1S144)的蛋白表达量的动态变化;免疫荧光染色追踪pPak1S144的亚细胞定位模式及其与纺锤体和微管组织中心蛋白之间的时空关系。结果在小鼠卵母细胞内pPak1S144持续稳定地表达于减数分裂各期,pPak1S144与中心粒周围蛋白(pericentrin)和γ微管蛋白(γ-tubulin)在时空上呈现紧密的共定位关系并特异地定位于纺锤体两极。结论pPak1S144是小鼠卵母细胞MTOC相关蛋白,提示其与减数分裂纺锤体形成相关。
pPak1S144;卵母细胞;减数分裂;微管组织中心;纺锤体
卵母细胞减数分裂过程中染色体分离错误会导致产生非整倍体(aneuploidy) 胚胎,是流产和出生缺陷的最常见原因[1]。哺乳动物卵母细胞没有中心粒,其纺锤体的形成依赖于微管组织中心(microtubule organizing centers, MTOC)[2]。研究证实卵母细胞内γ-tubulin和Pericentrin是MTOC核心成分,前者催化微管的形成和释放[3],后者参与形成MTOC结构平台。
P21-activated kinase (Pak1)是一种Ser/Thr蛋白激酶,参与细胞骨架的组织、细胞形态维持和细胞生存等过程[4]。Pak1在Ser144位点发生自动磷酸化,对于Pak1活性的维持有重要的作用[5]。有研究证实Pak1与小鼠卵母细胞减数分裂纺锤体的稳定性相关,但其自动磷酸化活性在卵母细胞减数分裂过程中的形态和作用仍需进一步探讨[6]。
1 材料与方法
1.1 材料
清洁级雌性21~23日龄C57BL/6与BALB/C杂交后的F1代(CB6F1)小鼠,体质量10~15 g[由北京维通利华实验动物技术有限公司提供,许可证编号SCXK(京)2012-0001]。兔抗Ser144位点磷酸化的PAK1(pPak1S144)单克隆抗体(Abcam公司),鼠抗Ace-tubulin单克隆抗体、鼠抗γ-tubulin单克隆抗体(Sigma公司),鼠抗Pericentrin单克隆抗体(BD公司),胎牛血清(Gibco公司),孕马血清促性腺激素、人绒毛膜促性腺激素(宁波第二激素厂),40% Acrylamide/Bis Solution 29∶1(3.3%C)(Bio-Rad公司),Pre-stained Marker(Thermo公司),PVDF膜(Amersham HybondTM公司)
1.2 方法
1.2.1 小鼠卵母细胞收集和培养:给CB6F1代雌性小鼠腹腔注射10 IU孕马血清促性腺激素,44~48 h后以CO2窒息处死小鼠,收集卵丘-卵母细胞复合体(cumulus cell-oocyte complexes,COC),体外培养至不同时期[7]。
1.2.2 蛋白免疫印迹 (Western blot):卵母细胞脱去卵丘后收集在含有蛋白酶抑制剂(protease inhibitor cocktail)的缓冲液(Laemmli Sample Buffer)中,在100 ℃沸水中处理5 min;样品利用10%丙烯酰胺0.1%十二烷基磺酸钠的凝胶分离,之后转移到聚偏氟乙烯膜上,聚偏氟乙烯膜在封闭后转入适当稀释的一抗溶液中4 ℃过夜;聚偏氟乙烯膜漂洗后,二抗孵育液中孵育,然后暗室曝光。
1.2.3 免疫荧光染色(Immunofluorecent staining):卵母细胞在2%多聚甲醛0.5%曲拉通X-100的PEM缓冲液(100 mmol/L Pipes,1 mmol/L MgCl2,1 mmol/L乙二醇二乙醚二胺四乙酸,pH 6.9)中固定45 min, 1%牛血清蛋白中漂洗和封闭后,一抗4 ℃过夜。兔抗pPak1S144抗体(1∶3 000)、鼠抗Acetylated-tubulin抗体(1∶12 000)、鼠抗γ微管蛋白的抗体(1∶3 000)和鼠抗中心粒周围蛋白的抗体(1∶3 000)。漂洗后利用Alexa Flour 488或555标记的二抗避光孵育1 h,DNA用DAPI标记封片。使用Olympus(D7)结合软件ImageJ进行拍照和分析。
1.3 统计学分析
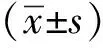
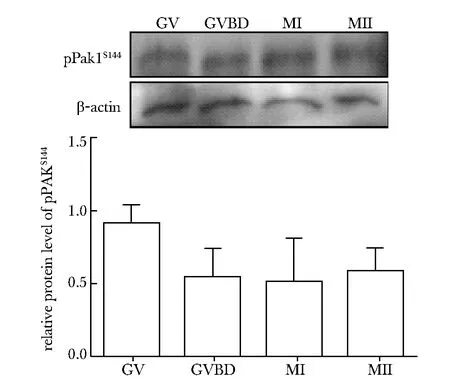
With Western blot analysis, high level of pPak1S144 was detected at GV stage and remained stable up to MII stage图1 pPak1S144在小鼠卵母细胞减数分裂过程中的蛋白表达Fig 1 Protein expression of pPak1S144 in mouse oocytes
2 结果
2.1pPak1S144在小鼠卵母细胞减数分裂过程中蛋白表达量
pPak1S144蛋白在小鼠卵母细胞内有特异表达,在GV期高水平表达,并持续保持至MII期,各个时期蛋白表达量无明显差异(图1)。
2.2pPak1S144亚细胞定位模式及其与MTOC蛋白的相关关系
在GV期,pPak1S144呈现出单个高度致密的点状聚集,定位于胞质中,并表现出与中心粒周围蛋白共定位的特性 (图2A:b,c,d)。在GVBD期,染色质开始凝集形成单个染色体,pPak1S144呈点片状聚集在凝集中的染色体周围,仍旧保持与中心粒周围蛋白的共定位性质(图2A:f,g,h)。随着染色体逐渐向赤道板聚集,pPak1S144和中心粒周围蛋白同时向赤道板两侧纺锤体两极的部位聚集(图2A:j,k,i),当卵母细胞成熟至MI期时,所有的染色体整齐排列于赤道板中央(图2A:m),pPak1S144呈“O”或“C”形聚集在推测的纺锤体两极的位置,在纺锤体以外的胞质中也有点状的聚集,并在所有这些区域,均表现出与中心粒周围蛋白共定位特性(图2A:n,o,p)。pPak1S144在MII期表现出与MI期相似的分布模式(图2A:v,w,x)。如图2B所示,在MI和MII期,pPak1S144与MTOC的另一核心蛋白,γ微管蛋白,共同定位于纺锤体两极(图2B:b,c,d,f,g,h),同时在胞质中呈点状分布(图2B:b,c,f,g)。在第一次减数分裂后期(Ana-Ⅰ期)以及末期(Tel-Ⅰ期)进程中,染色体向纺锤体两极分离, pPak1S144离开MTOC的位置,弥散地分布在细胞质收缩环周围(图2A:r,s,t)。pPak1S144与MTOC关键蛋白在时空上的共定位关系表明其间存在高度关联性,提示pPak1S144是卵母细胞MTOC相关蛋白。

A.immunofluorescent staining reveals tight co-localization of pPak1S144with MTOC structural component, pericentrin in oocytes during the whole meiosis; B.pPak1S144is co-localized with MTOC key component, microtubule nucleating protein, γ-tubulin on the poles of meiotic spindles; pPak1S144is labeled in red, while Percientin/γ-tubulin in green and chromosome in blue
图2小鼠卵母细胞减数分裂过程中pPak1S144与MTOC核心蛋白的共定位特性
Fig2Co-localizationofpPak1S144andMTOCkeyproteinsinmouseoocytesduringmeiosis
2.3pPak1S144聚集在减数分裂纺锤体两极
在MI期卵母细胞内染色体整齐排列于赤道板中央(图3a),微管装配成典型的双极对称圆桶状的纺锤体结构(图3b),此时pPak1S144呈“O”或“C”形聚集在纺锤体两极(图3c,d),同时在胞质中呈点状分布(图3c),这一分布特性同样出现在MII期卵母细胞内(图3f,g,h),再次提示了pPak1S144与卵母细胞减数分裂纺锤体形成的相关性。
3 讨论
胚胎的非整倍体是临床上流产和出生缺陷的最常见原因,这与母亲卵母细胞在减数分裂成熟过程中染色体的分离错误密切相关[1]。染色体的分离依赖于纺锤体的有序牵引,揭示其形成和维持机制是认识和预防人类非整倍体胚胎形成的重要研究内容。哺乳动物卵母细胞中缺少中心粒,不形成中心体,减数分裂进程中微管组装形成纺锤体依赖于特异的MTOC[8]。
迄今,MTOC结构的组装、成熟和功能维持的分子调控机制仍然不甚清楚。最新证据表明蛋白激酶AUKA,PKC、MAPK kinase1 (MEK1)和Breast cancer 1 (BRCA1) 等在卵母细胞MTOC的形成和结构维持中发挥一定作用[7,9-11]。本研究证实了在小鼠卵母细胞减数分裂过程中pPak1S144始终与γ-tubulin和Pericentrin呈现出紧密的亚细胞共定位特性,共同聚集在纺锤体两极,遵循与AUKA、磷酸化PKC和MEK1相似的分布模式,提示pPak1S144是MTOC相关蛋白。
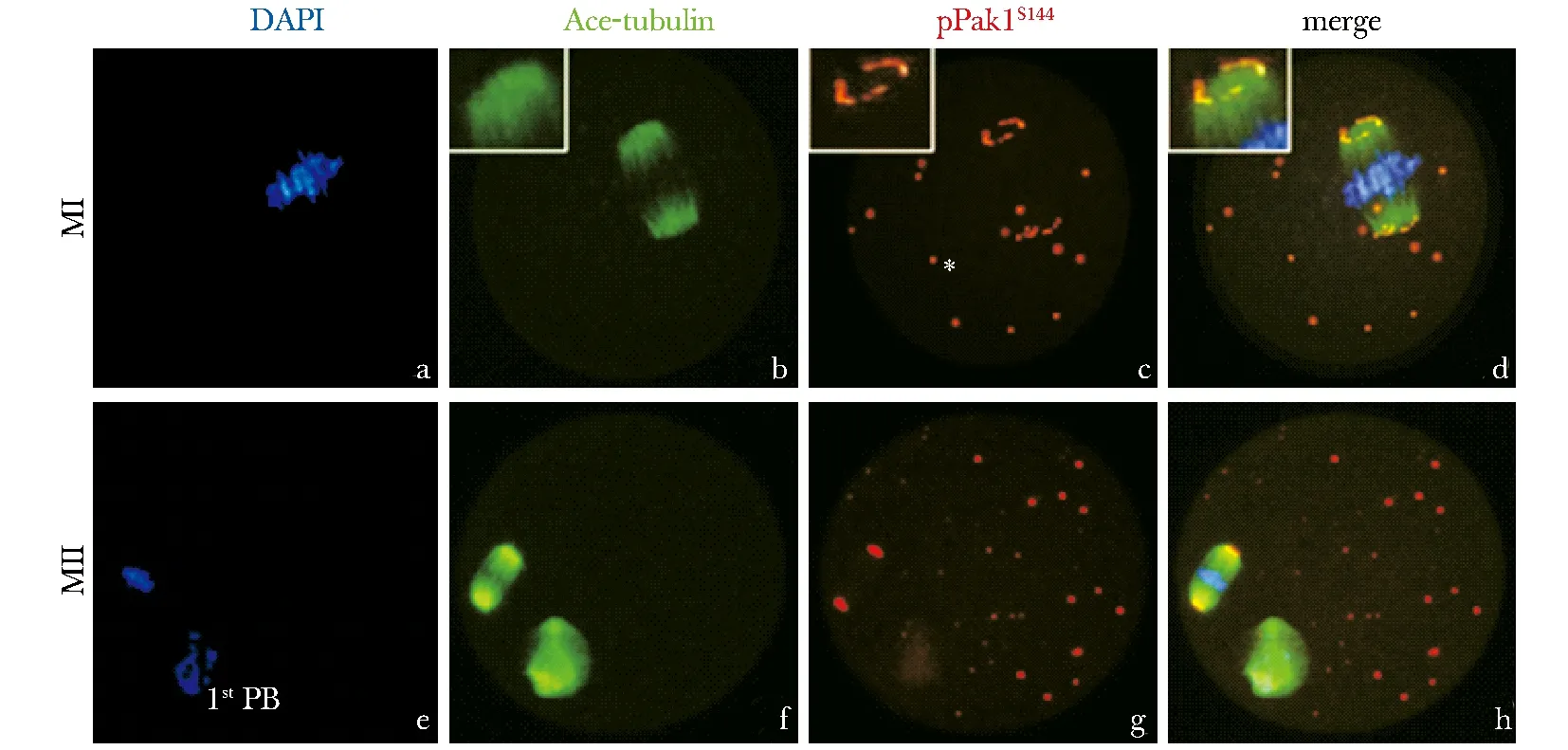
Immunofluorescent staining determined specific localization of pPak1S144on spindle poles in oocytes at MI and MII stages; pPak1S144was labeled in red, while ace-tubulin in green and chromosome in blue
图3pPak1S144定位于小鼠卵母细胞纺锤体两极
Fig3LocalizationofpPak1S144onmeioticspindlepolesinmouseoocytesduringmeiosis
Pak1的功能的活化需要在多个位点发生一系列的自动磷酸化过程,其中在Ser144位点的磷酸化(pPak1S144)可以抑制Pak1形成非活性的同源二聚体,维持其活化状态[12]。在体细胞有丝分裂过程中活化的Pak1能够特异地激活AUKA催化中心体成熟的活性[13],可以介导和调节PKC和MEK1等激酶的活性[14~15]。卵母细胞减数分裂过程中,pPak1S144是否与AUKA、PKC和MEK1等在调节MTOC功能方面存在协同作用尚待研究。
[1] Hunt P, Hassold T. Female meiosis: coming unglued with age [J]. Curr Biol, 2010, 20:699-702.
[2] Miao YL, Kikuchi K, Sun QY,etal. Oocyte aging:cellular and molecular changes, developmental potential and reversal possibility[J]. Hum Reprod Update, 2009, 15:573-585.
[3] Gueth-Hallonet C, Antony C, Aghion J,etal. γ-tubulin is present in acentriolar MTOCs during early mouse development [J]. J Cell Sci, 1993, 105:157-166.
[4] Molli PR, Li DQ, Murray BW,etal. PAK signaling in oncogenesis [J]. Oncogene, 2009, 28: 2545-2555.
[5] Dummler B, Ohshiro K, Kumar R,etal. Pak protein kinases and their role in cancer[J]. Cancer Metastasis Rev, 2009, 28:51-63.
[6] Lin SL, Qi ST, Sun SC,etal.PAK1 regulates spindle microtubule organization during oocyte meiotic maturation[J]. Front Biosci (Elite Ed), 2010, 2:1254-1264.
[7] Ma W, Koch JA, Viveiros MM. Protein kinase C delta (PKCδ) interacts with microtubule organizing center (MTOC)-associated proteins and participates in meiotic spindle organization[J].Dev Biol,2008,320:414-425.
[8] Zimmerman WC, Sillibourne J, Rosa J,etal. Mitosis-specific anchoring of γ-tubulin complexes by pericentrin controls spindle organization and mitotic entry[J]. Mol Biol Cell, 2004, 15:3642-3657.
[9] Suja JA, Barbero JL.Cohesin complexes and sister chromatid cohesion in mammalian meiosis[J]. Genome Dyn, 2009, 5:94-116.
[10] Xiong B, Sun SC, Lin SL,etal. Involvement of Polo-like kinase 1 in MEK1/2 regulated spindle formation during mouse oocyte meiosis[J].Cell Cycle, 2008,7:1804-1809.
[11] Xiong B, Li S, Ai JS,etal. BRCA1 is required for meiotic spindle assembly and spindle assembly checkpoint activation in mouse oocytes[J]. Biol Reprod, 2008, 79:718-726.
[12]Ke Y, Lei M, Solaro RJ. Regulation of cardiac excitation and contraction by p21 activated kinase-1[J]. Prog Biophys Mol Biol, 2008, 98:238-250.
[13] Zhao ZS, Lim JP, Ng YW,etal. The GIT-associated kinase PAK targets to the centrosome and regulates Aurora-A[J]. Mol Cell,2005, 20:237-249.
[14] Wang Z, Fu M, Wang L,etal. P21-activated kinase 1 (PAK1) can promote ERK activation in a kinase-independent manner[J]. J Biol Chem,2013, 288:20093-20099.
[15] Wada-Kiyama Y, Suzuki C, Hamada T,etal. Estrogen-induced cell signaling in the sexually dimorphic nucleus of the rat preoptic area: potential involvement of cofilin in actin dynamics for cell migration[J]. Biochem Biophys Res Commun,2013, 434:287-292.
The role of Pak1 in spindle formation of mouse oocytes
LI Xiu-hong1, ZHANG Xian-cai2, ZHOU De-shan1*, MA Wei1*
(1.Dept. of Histology and Embryology, Basic Medical College Capital Medical University, Beijing 100069;2.Dept. of Anatomy, Xingtai Medical College, Xingtai 054000, China)
ObjectiveTo investigate the subcellular localization of autophosphorylated Pak1 in mouse oocytes during meiosis and its correlation with spindle formation.MethodsWestern blot procedure was employed to assay the dynamic changes in protein expression of autophosphated Pak1 at Ser144(pPak1S144); immunofluorescence staining was carried out to label pPak1S144subcellular distribution and its temporal-spatial relationship with spindle and microtubule organizing centers(MTOCs) proteins, Pericentrin and γ-tubulin.ResultspPak1S144was stably expressed during meiotic progression in mouse oocytes; it was specifically co-localized with Pericentrin and γ-tubulin and concentrated on spindle poles.ConclusionspPak1S144is MTOC-associated protein, implying a role in meiotic spindle formation.
pPak1S144;oocytes;meiosis;microtubule organizing centers(MTOCs);spindle
2013-12-07
2014-01-17
国家自然科学基金(31271253);教育部博士点基金 (20121107120019)
*通信作者(correspondingauthor): zhouds08@ccmu.edu.cn;mawei1026@ccmu.edu.cn
1001-6325(2014)04-0449-05
研究论文
R 321.1
A
——水芹主要害虫识别与为害症状

