粉煤灰合成沸石对Cr3+的吸附性能研究*
程 婷,刘海霞,陈 晨,王志良
(1.江苏城市职业学院城市科学系,江苏南京210017;2.江苏科技大学生物与化学工程学院,江苏镇江212018;3.江苏省环境科学研究院环境工程重点实验室,江苏南京210036)
近年来大量重金属污染物排向环境当中,对生态环境和人体健康造成极其不利的影响。因此,水体中重金属的有效去除成为研究热点[1、2]。铬污染主要来自于冶金工业、金属加工、电镀、制革、油漆、印染以及化工等多个行业。粉煤灰是燃煤电厂排放的固体废弃物。粉煤灰来源广泛,价格低廉,具有较大的比表面积和固体吸附剂性能[3、4]。近年来,利用粉煤灰作吸附剂去除水中重金属离子的研究备受关注。已有研究表明,粉煤灰及其合成材料对水中重金属离子具有较好的去除能力[5-7]。本文利用粉煤灰合成的Linde type F(K)(以下简称沸石)为基本吸附材料处理重金属Cr3+,研究吸附剂投加量、初始pH值、反应温度以及反应时间对Cr3+吸附效果的影响;同时对吸附数据进行拟合,探讨合成的沸石材料吸附Cr3+的吸附等温线与吸附动力学方程。
1 试验材料和方法
1.1 试验器材
粉煤灰样品取自江苏太仓协鑫发电厂,主要化学成分为:SiO2质量分数为51.06%,Al2O3质量分数为32.36%,Fe2O3质量分数为4.68%,CaO质量分数为2.91%,TiO2质量分数为1.17%,MgO质量分数为0.9%。
THZ-82型恒温振荡器(金坛市顺华仪器有限公司),PHS-3C型 PH计酸度计(上海雷磁仪器厂),AA240DUO原子吸收光谱仪(美国安捷伦科技有限公司)。
1.2 试验方法
1.2.1 Linde type F(K)沸石的制备 根据文献,Linde type F(K)沸石的制备过程为:将2g粉煤灰加入到50mL的浓度为8mol/L的KOH溶液中,在反应温度为95℃下反应48h。完成后将得到的材料用去离子水水洗至中性后在105℃的烘箱中干燥至恒重。合成完成后[8],所有样品均经过X射线衍射分析鉴定,确定为 Linde type F(K)沸石[9]。
1.2.2 试验步骤 在10ml具塞聚丙烯管中投加一定量合成的粉煤灰Linde type F(K)沸石,并移取一定体积的Cr3+溶液。用0.01mol/L的盐酸和氢氧化钠溶液调节其pH值后,置于一定温度下的水浴恒温振荡器中进行震荡吸附反应(120rpm)。吸附试验完成后利用0.45μm的水系滤膜对混合液进行过滤并分析样品中Cr3+浓度。
1.2.3 分析方法采用AA240DUO原子吸收光谱仪测定吸附后水样中Cr3+的浓度。吸附容量的计算公(1)式为
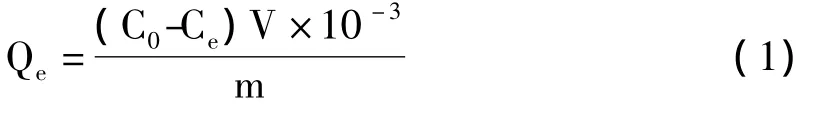
式中:Qe为吸附容量(mg/g),C0为金属离子初始浓度(mg/L),Ce为金属离子吸附平衡浓度(mg/L),V为溶液体积(mL),m为吸附剂用量(g)。去除率计算公式(2)为

2 结果与讨论
2.1 吸附剂投加量的影响
沸石的投加量对Cr3+去除率的影响如图1。沸石的投加量分别为:0.5、1、2、3、4、5、6、7 与 8 g/L,Cr3+的初始浓度分别为50 mg/L和100 mg/L,初始pH为6,反应时间为20h。由图1可知,当Cr3+初始浓度为100 mg/L,沸石投加量为0.5~5g/L时,Cr3+去除率随着吸附剂投加量的增大迅速增加,去除率由36.80%增加到92.87%;而之后继续提高吸附剂的量,Cr3+去除率提高不大,吸附趋于平衡。当Cr3+初始浓度为50 mg/L,沸石投加量为0.5~3g/L时,Cr3+去除率从42.58%增加到98.97%;此后继续增加吸附剂的量Cr3+吸附已经趋于饱和。
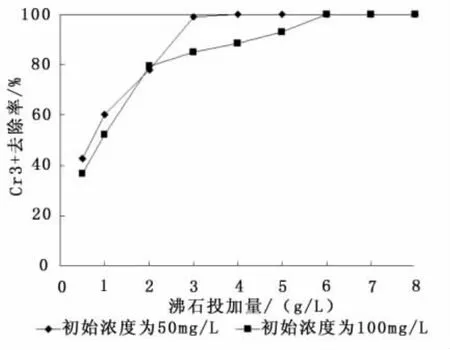
图1 吸附剂量对Cr3+去除率的影响

图2 吸附剂量对Cr3+饱和吸附量的影响
图2为沸石投加量对Cr3+饱和吸附量的影响。由图2可知,随着沸石投加量的增加,单位质量的沸石吸附剂对Cr3+的吸附容量不断下降。当Cr3+初始浓度为100 mg/L,吸附剂量从0.5 g/L增加到8 g/L时,吸附容量由73.61 mg/g下降到12.5 mg/g;当Cr3+初始浓度为50 mg/L,吸附剂量从0.5 g/L增加到8 g/L时,吸附容量由42.58 mg/g下降到6.25 mg/g。吸附剂投加量增加以后,其与水中Cr3+的接触面积也随之增加,从而使吸附剂利用率降低。
2.2 初始pH值的影响
为考察pH值对沸石吸附Cr3+的效果影响,试验调节吸附体系初始 pH 值分别为 2、3、4、5、6、7、8、9、10,污染物Cr3+的初始浓度为50 mg/L,吸附剂投加量为3g/L,反应时间为20h。初始 pH值对沸石吸附Cr3+的去除效果影响如图3。由图3可知,当初始pH值为2~4时,随着初始pH值的升高,沸石对Cr3+的去除率迅速提高,从64%提高到100%。之后继续提高pH值Cr3+的去除率不变。pH值不仅影响吸附剂的表面电荷,还会影响吸附剂和金属离子的存在状态,从而影响其相互作用。Hui等[10]在采用粉煤灰合成的沸石4A去除混合重金属离子的实验中指出,当混合重金属离子初始浓度为50mg/L时,Cr3+的沉淀pH值为5.07。推测本试验中低 pH值条件下,溶液中H+浓度较大,占据了吸附剂的位置,与其形成竞争吸附。而随着pH值的升高,离子交换作用增强,金属离子逐步取代沸石表面的H+离子,Cr3+去除率增大。pH值大于5时,水溶液中氢氧根离子增多,与Cr3+发生沉淀作用去除率较高。
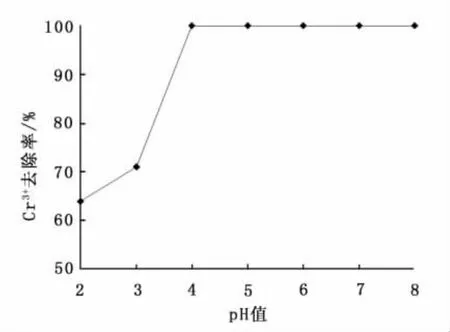
图3 初始pH对Cr3+去除率的影响
2.3 反应温度的影响
初始浓度为50mg/L与100mg/L时反应温度对Cr3+吸附效果的影响如图4与图5。反应温度分别为25℃、35℃、45℃,吸附剂投加量为3g/L,体系初始 pH值为4,反应时间为0~15h。由图4与图5可知,反应温度对沸石吸附Cr3+的去除效果影响显著。随着反应温度的上升,沸石对Cr3+的吸附效果逐渐下降,即反应温度的上升不利于Cr3+的去除。
反应温度为25℃时,随着反应时间的延长,沸石对Cr3+的吸附效果不断增强,其去除率不断提高。当初始浓度为50mg/L时,Cr3+去除率从反应时间为0.5h时的57.59%提高到5h时的99.11%;反应时间为6h时吸附趋于饱和。而当反应温度提高到35℃时,沸石对Cr3+的去除效果较反应温度为25℃时有所降低。反应时间为5h时Cr3+去除率为80.63%,13h吸附反应趋于饱和。当反应温度进一步提升至45℃,沸石对Cr3+的吸附效果进一步下降。反应时间为5h时Cr3+去除率为72.02%,15h时吸附反应趋于平衡。当初始浓度为100mg/L时,反应温度对Cr3+去除规律与初始浓度为50 mg/L时类似,即随着反应时间的延长,沸石对Cr3+的吸附效果逐渐增强;而随着反应温度的上升,沸石对Cr3+的去除率逐渐下降。
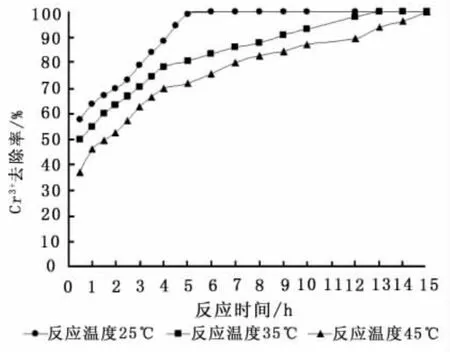
图4 初始浓度为50 mg/L时反应温度对Cr3+去除率的影响
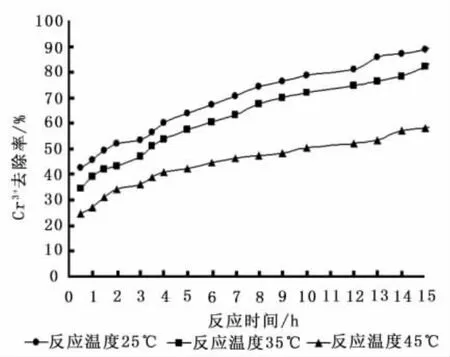
图5 初始浓度为100mg/L时反应温度对Cr3+去除率的影响
2.4 吸附等温线
对于单一组分的溶质,水处理中常见的吸附等温线有2种,一种是Langmuir等温吸附模型,其标准形式和线性形式分别为式(3)、(4)。
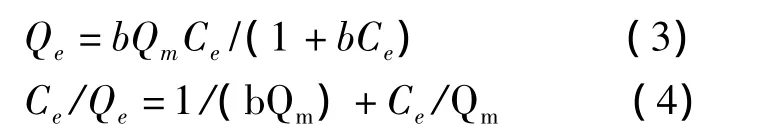
式3和4中,Qm为最大吸附量(或称极限吸附量);b为吸附常数,其大小与吸附剂、吸附质的本性及温度有关。b值越大,则表示吸附能力越强。
另一种是Freundlich等温吸附模型,这是一个经验公式,其标准形式和线性形式分别为式(5)、(6)。

式(5)、(6)中,K、n均为常数,通常 n>1。利用Langmuir吸附等温式和Freundlich吸附等温式对沸石吸附Cr3+的数据进行线性拟合,拟合结果如表1。
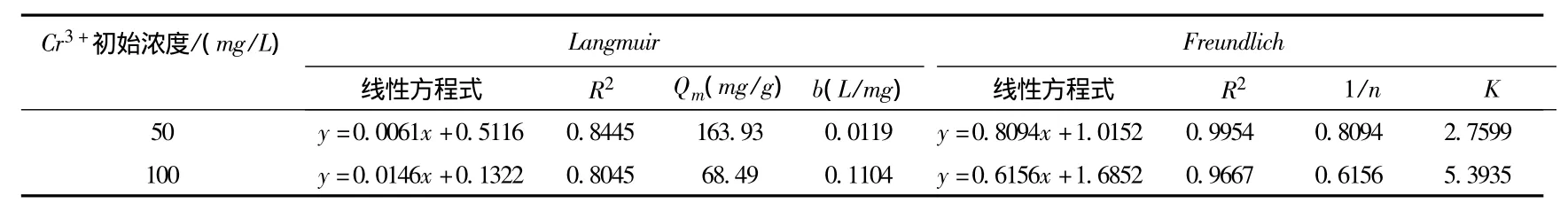
表1 沸石对Cr3+的吸附等温线拟合结果
表1为沸石对Cr3+吸附的吸附等温线拟合结果。由表1的拟合结果可知,沸石吸附Cr3+的过程更符合Freundlich吸附等温式,与Langmuir吸附等温式的符合较差。
2.5 吸附动力学
对于一般的固液吸附过程而言,通常采用准一级和准二级动力学方程来进行动力学拟合。准一级动力学方程为式(7):

Qt表示t时刻的吸附量(mg/g),Qe表示准一级动力学模型的平衡吸附量(mg/g),K1为准一级动力学模型的吸附平衡速率常数(1/min)。
考虑边界条件:t=0 时,Qt=0;t=t时,Qt=Qt,积分可得式(8)。
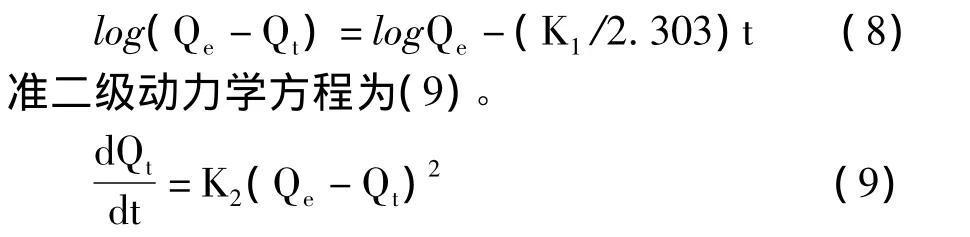
K2为准二级动力学模型的吸附平衡速率常数g/(mg·min),积分可得式(10)。
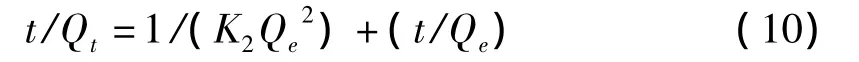
初始浓度为50mg/L与100mg/L时沸石对Cr3+的吸附动力学拟合结果分别如表2与表3所示。比较表2与表3中各个方程拟合的相关系数(R2)可知,准二级动力学方程对沸石吸附Cr3+的方程有较好的描述(初始浓度为 50mg/L时,R2>0.98;初始浓度为100mg/L时,R2>0.97),能够反映沸石对Cr3+的吸附行为。而准一级动力学方程的拟合程度较差。

表2 初始浓度为50mg/L时吸附动力学方程拟合结果

表3 初始浓度为100mg/L时吸附动力学方程拟合结果
3 结论
吸附剂投加量对沸石吸附Cr3+去除效果影响显著。Cr3+去除率随着吸附剂投加量的增大不断提高,而单位质量沸石吸附剂对Cr3+的吸附容量不断下降。初始pH值为2~4时,随着初始pH值的上升,沸石对Cr3+的去除率迅速提高,pH值为4时Cr3+去除率可达100%。反应温度的上升不利于沸石对Cr3+吸附。随着反应温度的升高,沸石对Cr3+的吸附效果逐渐降低。初始浓度为50 mg/L和100 mg/L时,沸石吸附Cr3+的过程更符合Freundlich吸附等温式;此外,沸石吸附Cr3+的动力学符合准二级反应动力学方程。
[1] 张蕊,葛滢.稻壳基活性炭制备及其对重金属吸附研究[J].环境污染与防治,2011,33(2):41-45,51.
[2] 饶品华,张文启,李永峰,等.氧化铝对水体中重金属离子吸附去除研究[J].水处理技术,2009,35(12):71-74.
[3] 蔡昌凤,徐建平.矿区电厂粉煤灰物化特性与吸附特性关联研究[J].安徽工程科技学院学报,2005,20(4):1-4.
[4] 王金梅,王庆生,刘长占,等.粉煤灰的改性及吸附作用的研究[J].工业用水与废水,2005,36(1):44-47.
[5] 潘国营,周卫,王素娜.粉煤灰处理含铅废水的试验研究[J].煤炭工程,2008,(9):77-79.
[6] 崔杏雨,陈树伟,闫晓亮,等.粉煤灰合成Na-X沸石去除废水中镍离子的研究[J].燃料化学学报,2009,37(6):752-756.
[7]Wei Q,Ying Z.Removal of lead,copper,nickel,cobalt,and zinc from water by a cancrinite-type zeolite synthesized from fly ash[J].Chemical Engineering Journal,2009,145:483-488.
[8]MIYAJI F,MuRAKAMI T,SUYAMA Y.Formation of linde F zeolite by KOH treatment of coal fly ash[J].Journal of the Ceramic Society of Japan,2009,117(5):619-622.
[9]Chen C,Cheng T.Application of Avrami Equation to Kinetics Analysis of Fly Ash Based Linde F(K)Zeolite[J].Asian journal of Chemistry,2013,25(4):1811-1813.
[10]Hui K S,Chao C Y H,Kot S C.Removal of mixed heavy mental irons in wastewater by zeolite4A and residual products from recycled coal fly ash[J].Journal of Hazardous Materials,2005,B127:89-101.

