火焰原子吸收对K元素激光诱导击穿光谱测量的影响
张志昊,宋 蔷,姚 强
(清华大学 热科学与动力工程教育部重点实验室,北京100084)
引言
在煤和生物质的热转化过程中,其灰分中碱金属元素的气态排放一直是人们极为关心的问题。在热转化过程中气态释放的K、Na元素会随烟气降温过程冷凝,造成受热面积灰、结渣、腐蚀等问题[1],影响了热力设备的安全运行。关于煤和生物质热利用终态碱金属的迁移分布研究较多[2-4],但限于测量条件,对开发碱金属迁移机理和调控方法有重要意义的碱金属释放过程的在线观测研究却很少。
随着测量技术的进步,在线的激光诱导击穿光谱技术(LIBS)正在被逐步用于相关领域的研究。LIBS技术具有分析简便、无需样品预处理、能够多元素同时在线检测等优点[5-6]。该测量技术的原理是利用光学透镜聚焦一束高能量的激光,使得激光聚焦点内的温度骤升,极高的温度会导致聚焦点内的物质呈现出等离子体的状态,并发射出带有样品内元素特征波长的等离子体光谱,谱线的波长和强度分别反应了样品中的元素组成与含量[7]。因此,该技术适合于在工业复杂环境中开展在线测量[8]。
Blevins等人[9]利用LIBS技术在线测量了燃煤锅炉过热器附近、燃烧天然气玻璃熔炉尾气出口和燃烧黑液的工业锅炉折焰角处包括碱金属元素在内的多种元素;Molina等人[10]利用LIBS技术定性测量了玻璃炉尾气中的碱金属元素。Hsu等人[11]以及 He等人[12]均采用LIBS分别测量了松木颗粒、褐煤颗粒燃烧过程中K、Na元素的释放过程,对揭示K、Na的迁移机理作出了重要的贡献。
不过,在高温火焰场内进行LIBS测量时,等离子体内的K、Na元素所发出的LIBS信号会受到等离子体外火焰中基态K、Na原子的吸收,造成信号衰减。Hsu等人[11]研究发现,当K、Na在火焰场内均匀分布时,在K、Na元素的体积分数高于4×10-6后,随着K、Na元素体积分数的升高,其LIBS信号强度几乎停止了增加,并分析认为这主要是由火焰场内K、Na原子对信号的吸收所导致,严重影响了测量精度。
生物质中碱金属以K为主,本文以K元素为例,建立了火焰场内K元素LIBS信号的原子吸收模型,对影响火焰原子吸收效率的多个因素进行分析,提出了降低火焰原子吸收效率的方法,为提高火焰场内K元素的LIBS测量精度提供指导。
1 火焰场内K元素的LIBS测量系统和方法
火焰场内K元素的LIBS测量系统简图如图1所示。
一般而言,火焰场内K元素的LIBS测量系统由3部分组成,分别为LIBS测量系统、燃烧器系统和K元素释放源。LIBS测量系统一般由激光、反射镜、聚焦镜及光谱议组成。燃烧器系统可以提供高温火焰环境。K元素释放源为燃料,燃料可以经燃烧器入口由空气或燃气携带进入火焰场,也可以作为颗粒悬挂在燃烧器的上方。
燃料接触到高温烟气后,开始热解或燃烧,并伴随着向气相释放K元素。释放到气相的K元素化合形式在火焰中迅速达到热力学平衡。随后,处于热力学平衡的含K气态物质伴随火焰场气流向下游流动。在流动过程中,气态含K物质将通过分子扩散作用而在火焰空间中呈现一定的浓度分布。该浓度分布与燃料的给入方式相关。如通过多股射流通入,则在火焰中产生均匀分布;如仅通过中心毛细管给入,则产生中心浓度高四周浓度低的射流分布。分布在火焰中的K元素会因热力学平衡而部分以K原子形式存在。
通过调整光谱仪的测量波长范围,并设置合理的等离子体激发后的相机延迟时间,就可以利用该系统对火焰中等离子体内的K元素进行观测。不过,分布在火焰中的K原子会对火焰中心等离子体内K元素发出的LIBS信号产生一定的吸收作用。
2 LIBS信号的火焰原子吸收模型和计算方法
图2给出了火焰场内K原子吸收LIBS信号的示意图。

图2 火焰场内K原子对K元素LIBS信号的吸收过程Fig.2 Absorption of K LIBS signal by K atoms in flame
利用Beer-Lambert公式计算火焰环境中K原子对K元素LIBS信号的吸收效应,得
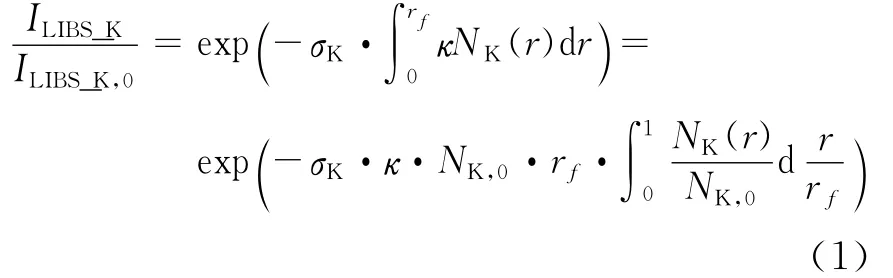
式中:ILIBS_K代表了经K原子吸收后的LIBS信号强度;ILIBS_K,0代表了原始 LIBS信号强度;σK为 K 原子的吸收截面积,取值[13]为(1.15×10-16)m2;NK为测量平面内气态含K分子的总数浓度(1/m3);κ为当地K原子数占总K分子数的比例;rf为圆形火焰面半径;NK,0代表了测量平面中心点,亦即等离子体内气态含K分子的总数浓度(1/m3)。
令积分参数
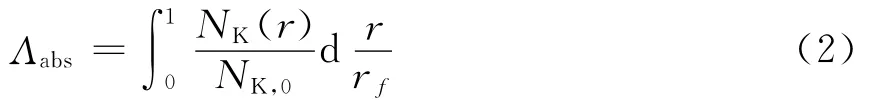
则(1)式可简化为

那么,(3)式可以确定火焰中K原子对K元素LIBS信号的吸收效率为

3 火焰原子吸收对K元素LIBS信号的影响分析
影响火焰内K原子对K元素LIBS信号吸收的可调节参数有2个,分别为当地K原子数占总K分子数的比例κ以及与K元素浓度分布相关的积分参数Λabs。
假设火焰由CH4在空气中燃烧形成,火焰温度为1 650K,燃料颗粒中的K元素以KCl形式气态释放进入火焰中。通过Chemkin软件的热力学平衡计算模块,可以计算不同初始气态KCl分子数浓度及火焰气氛条件下,各气态含K物质热力学平衡条件下的分布比例。
图3给出了不同初始气态KCl分子数浓度和热力学平衡条件下主要气态含K物质摩尔比例随火焰气氛变化的计算结果。在实际生物质颗粒燃烧过程中,K元素在火焰中的最高体积分数一般在2.5×10-5左右[11],因此本文选择的 KCl初始体积分数分别为1×10-5和2×10-5,转化为分子数浓度则分别为 NK1=4.446 5×1019和NK2=8.893×10191/m3。
从图3中可以发现,随火焰中O2/CH4摩尔比值的增加,火焰中K原子数占总K分子数的摩尔比例,κ,会从约25%逐步下降。KCl初始数浓度的变化会对火焰中KCl和KOH的比例产生显著影响,但是对K原子的比例影响较小。
考虑火焰中2种不同的K元素气态分布形式,分别为:
1)均匀分布,即火焰中K元素浓度为均一值,此时Λabs取值为1。

图3 热力学平衡状态下主要气态含K物质摩尔比例随O2/CH4摩尔比值变化的计算结果Fig.3 Predicted molar fraction of major K-containing species in equilibrium condition at different O2/CH4m ratios
2)中心射流,即火焰中心K元素浓度最高,周围K元素浓度逐步降低,此时Λabs取值小于1,本文按中心射流计算为0.3。
图4给出了依据(4)式计算得到的对应1和2两种浓度分布,不同初始气态KCl分子数浓度(NK1=4.446 5×10191/m3、NK2=8.893×10191/m3)条件下,K原子吸收效率随火焰气氛变化的计算结果。

图4 火焰原子吸收效率随O2/CH4摩尔比值变化的计算结果Fig.4 Predicted flame atomic absorption efficiency at different O2/CH4ratios
从图4中可以看到,在O2/CH4摩尔比值为1.48、高K浓度且K均匀分布的情况下,火焰中K原子对K元素LIBS信号的吸收效率可达86.8%,且吸收效率随O2/CH4摩尔比值、K浓度和分布等参数而变。总体上,随着O2/CH4摩尔比值的增加,K原子对K元素LIBS信号的吸收效率逐步降低;当O2/CH4摩尔比值超过2时,火焰尾气中会存在未参与燃烧的过量O2,此时火焰内K原子的吸收效率均低于13%;在相同O2/CH4摩尔比值下(以1.48为例),K均匀分布时,随着初始KCl浓度的降低,K原子对LIBS信号的吸收效率从86.8%降至69.5%;K非均匀分布时,随着初始KCl浓度的降低,K原子对LIBS信号的吸收效率从45.6%降至29.9%。以上计算结果表明,保持高温燃烧环境的氧化性气氛对减小火焰中的K原子吸收效率而言是非常重要的。同时,改变K元素分布也是减小K原子吸收的有效方法。
基于以上结论,本文建议在利用LIBS测量生物质燃烧火焰场内K元素时,应调整燃烧气氛使火焰中存在一定的过量O2,并使用中心给入燃料或单颗粒悬挂的方式形成中心高、四周低的非均匀K元素浓度分布,以降低火焰内K原子对K元素LIBS信号的吸收效率,提高测量精度。
4 结论
本文基于Beer-Lambert定律和火焰场内气态含K物质的热力学平衡原理,建立了火焰场内K元素LIBS信号的原子吸收模型,并分析了火焰气氛、K元素浓度分布以及总K浓度对火焰原子吸收效率的影响。计算结果表明,随着O2/CH4的摩尔比值的增加,火焰中热力学平衡状态下K原子占总K的比例从约25%逐步降低,火焰原子吸收效率也逐步从86.8%逐步降低。当O2/CH4的摩尔比值大于2时,火焰尾气中会存在未参与燃烧的过量O2,此时火焰内K原子的吸收效率均低于13%。在火焰气氛相同的情况下,随着测点周围K元素浓度的降低,火焰内K原子的吸收效率也会逐步降低。在此基础上,提出通过创造氧化性火焰气氛和合理组织K元素分布的方法来减少火焰原子吸收对LIBS测量精度的影响。
[1] Baxter L,Miles R,Miles R J,et al.The behavior of inorganic material in biomass-fired power boilers:field and laboratory experiences[J].Fuel Process.Technol,1998,54(1-3):47-78.
[2] Knudsen J N,Jensen P A,Dam-johansen K.Transformation and release to the gas phase of Cl,K and S during combustion of annual biomass[J].Energy Fu-els,2004,18(5):1385-1399.
[3] Li Chunzhu.Some recent advances in the understanding of the pyrolysis and gasification behaviour of victorian brown coal[J].Fuel,2007,86(12-13):1664-1683.
[4] Zhang Zhihao,Song Qiang,Yao Qiang,et al.Influence of the atmosphere on the transformation of alkali and alkaline earth metallic species during rice straw thermal conversion[J].Energy Fuels,2012,26(3):1892-1899.
[5] Hahn D W,Omenetto N.Laser-induced breakdown spectroscopy(LIBS),part I:Review of basic diagnostics and plasma-particle interactions:still-challenging issues within the analytical plasma community[J].Appl.Spectrosc.,2010,64(12):335A-366A.
[6] Hahn D W,Omenetto N.Laser-induced breakdown spectroscopy(LIBS),part II:Review of instrumental and methodological approaches to material analysis and applications to different fields[J].Appl.Spectrosc.,2012,66(4):347-419.
[7] Cremers D A,Radziemski L J.Laser-induced breakdown spectroscopy (LIBS):fundamentals and applications[M]. Cambridge:Cambridge University Press,2006:1-36.
[8] Shao Yan,Zhang Yanbo,Gao Xun,et al.Latest research on and applications progress in laser-induced breakdown spectroscopy[J].Spectroscopy and Spec-tral Analysis,2013,33(10):2593-2598.邵妍,张艳波,高勋,等.激光诱导击穿光谱技术的研究与应用新进展[J].光谱学与光谱分析,2013,33(10):2593-2598.
[9] Blevins L,Shaddix C,Sickafoose S,et al.Laser-induced breakdown spectroscopy at high temperatures in industrial boilers and furnaces[J].Applied Optics,2003,42(30):6107-6118.
[10] Molina A,Walsh P,Shaddix C,et al.Laser-induced breakdown spectroscopy of alkali metals in hightemperature gas[J].Applied Optics,2006,45(18):4411-4423.
[11] Hsu L J,Alwahabi Z T,Nathan G J,et al.Sodium and potassium released from burning particles of brown coal and pine wood in a laminar premixed methane flame using quantitative laser-induced breakdown spectroscopy[J].Appl.Spectrosc.,2011,65(6):684-691.
[12] He Y,Zhu J,Li B,et al.In-situ measurement of sodium and potassium release during oxy-fuel combustion of lignite using laser-Induced breakdown spectroscopy:effects of O2and CO2concentration[J].Energy Fuels,2013,27(2):1123-1130.
[13] Sorajarvi T,Toivonen J.Principles and calibration of collinear photofragmentation and atomic absorption spectroscopy[J].Appl.Phys.B,2014(115):533-539.

