补骨脂有效成分在大鼠血清、肝、肾中的测定
张 昀,张 瑜
(河南大学药学院,河南开封 475001)
补骨脂是常用中药之一,具有温补脾肾、壮阳止泻之功效,目前已从中分离鉴定出三十余种化合物。现代药理研究表明,补骨脂具有抑制分离破骨细胞、抑制人胃癌细胞的生长、抗氧化、抗菌抗病毒、增强免疫力等作用[1-12]。补骨脂药材中主要活性成分为补骨脂素和异补骨脂素[13-15],其定量测定已收载于《中国药典》2010年版[16]。因此,本实验旨在建立一种同时测定大鼠血清、肝脏、肾脏中补骨脂素和异补骨脂素的量的方法,为两者在体内的分布规律及药代动力学研究奠定基础。
1 仪器及试剂
AE200S电子分析天平 (上海梅特勒-托利多仪器有限公司);Agilent 1260型高效液相色谱仪;氯霉素 (中国药品生物制品检定所,产品批号130303-200614);补骨脂素对照品 (批号110739-201115,供含量测定用,中国食品药品检定院);异补骨脂素对照品 (批号110738-201012,供含量测定用,中国食品药品检定研究院);甲醇、乙腈为色谱纯 (均为天津四友精细化学品有限公司);水为超纯水;其他试剂均为分析纯。
2 方法与结果
2.1 色谱条件 Agilent TC-C18(2)高效液相色谱柱 (4.6 mm×250 mm,5 μm);流动相为水(A)-乙腈 (B)(65∶35),梯度洗脱 (0~10 min,35%B→45%B;10~25 min,45%B→50%B),体积流量1 mL/min,柱温30℃,检测波长295 nm(0~10 min,氯霉素),246 nm(10~25 min,补骨脂素、异补骨脂素),进样量20 μL。图谱见图1。
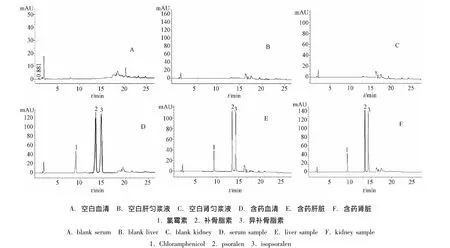
图1 对照品溶液和样品溶液的高效液相色谱图Fig.1 HPLC chromatograms of reference substances and samples
2.2 对照品贮备液的配制 精密称取补骨脂素、异补骨脂素对照品分别至10 mL量瓶中,加甲醇溶解,定容,摇匀,储存于4℃冰箱待用。
2.3 内标标准溶液的配制 精密称取氯霉素对照品至25 mL量瓶中,加甲醇溶解,定容,摇匀,储存于4℃冰箱待用。
2.4 供试品溶液的制备
2.4.1 血清供试品溶液 精密吸取内标溶液20 μL置具塞离心管中,于缓和氮气流下吹干溶剂,加入血清样品 200 μL,乙酸乙酯-正己烷 (8 ∶1)800 μL,涡旋 2 min,低温离心 10 min(12000 r/min),分取上层有机相置另一试管中,于缓和氮气流下吹干溶剂,残渣用100 μL甲醇溶解,即得。
2.4.2 肝脏供试品溶液 称取肝脏相同部位0.3 g,加生理盐水0.5 mL,10000 r/min匀浆,离心10 min(5000 r/min),取上清液200 μL置于氮气吹干的含有20 μL内标标准液的具塞离心管中,加入乙酸乙酯-正己烷 (8∶1)800 μL,涡旋2 min,低温离心10 min(12000 r/min),取上层有机相置另一试管中,缓和氮气流下吹干溶剂,残渣用100 μL甲醇溶解,即得。
2.4.3 肾脏供试品溶液的制备 称取肾脏相同部位0.5 g,加生理盐水0.5 mL,10000 r/min匀浆,离心10 min(5000 r/min),取上清液200 μL置于氮气吹干的含有20 μL内标标准液的具塞离心管中,加入乙酸乙酯-正己烷 (8∶1)800 μL,涡旋2 min,低温离心10 min(12000 r/min),取上层有机相置另一试管中,氮气流下吹干溶剂,残渣用100 μL甲醇溶解,即得。
2.5 线性关系考察 精密吸取内标溶液20 μL及一定体积的标准溶液于离心管中,于氮气流吹干溶剂,加入空白血清200 μL,配制补骨脂素、异补骨脂素质量浓度均为10、6、3、1、0.5、0.1 mg/L的系列血清样品溶液,按“2.4.1”项下操作,建立血清标准曲线。精密吸取内标溶液20 μL及一定体积的标准溶液于离心管中,于缓和氮气流吹干溶剂,加入空白肝匀浆200 μL,配制补骨脂素、异补骨脂素质量浓度均为10、6、3、1、0.5、0.1 mg/L的系列肝脏样品溶液,按“2.4.2”项下操作,建立肝脏标准曲线。精密吸取内标溶液20 μL及一定体积的标准溶液于离心管中,于氮气流吹干溶剂,加入空白肾匀浆200 μL,配制补骨脂素、异补骨脂素质量浓度均为10、6、3、1、0.5、0.1 mg/L的系列肾脏样品溶液,按“2.4.3”项下操作,建立肾脏标准曲线。分别以各样品中补骨脂素、异补骨脂素的质量浓度为横坐标,补骨脂素、异补骨脂素与内标峰面积之比为纵坐标,求得补骨脂素在血清、肝脏、肾脏中的线性回归方程分别为 Y=1.2467X+0.2028,r=0.9813;Y=1.6294X-0.0372,r=0.9901;Y=1.3354X+0.1379,r=0.9928。异补骨脂素在血清、肝脏、肾脏中的线性回归方程分别为Y=1.0984X+0.3472,r=0.9916;Y=1.5961X+0.0104,r=0.9924;Y=1.1278X-0.1495,r=0.9926。结果表明,补骨脂素、异补骨脂素在0.1~10.0 mg/L范围内线性关系良好。
2.6 日内日间精密度试验 大鼠空白血清中加入已知量的补骨脂素、异补骨脂素对照品,分别制成高、中、低质量浓度的样品,按“2.4.1”项下操作,结果补骨脂素日内精密度RSD(n=6)依次为3.62%、3.81%、10.54%,异补骨脂素为3.59%、3.67%、11.04%;补骨脂素日间精密度RSD(n=3)值依次为7.56%、7.07%、11.32%,异补骨脂素为7.34%、7.49%、9.67%。大鼠空白肝匀浆液中加入已知量的补骨脂素、异补骨脂素对照品,分别制成高、中、低质量浓度的样品,按“2.4.2”项下操作,结果补骨脂素日内精密度RSD(n=6)依次为3.96%、3.72%、10.63%,异补骨脂素为3.79%、4.02%、10.83%;补骨脂素日间精密度 RSD(n=3)依次为6.37%、6.89%、11.24%,异补骨脂素为6.74%、6.97%、10.86%。大鼠空白肾匀浆液中加入已知量的补骨脂素和异补骨脂素对照品,分别制成高、中、低质量浓度的样品,按“2.4.3”项下操作,结果补骨脂素日内精密度RSD(n=6)依次为4.53%、4.62%、11.65%,异补骨脂素为4.38%、4.69%、10.86%;补骨脂素日间精密度RSD(n=3)依次为7.24%、7.58%、12.31%,异补骨脂素为7.85%、8.04%、12.08%。
2.7 稳定性试验 取同一血清样品,分别于0、2、6、12、24 h进样,测得补骨脂素 RSD为4.59%,异补骨脂素RSD为4.96%,说明该样品在24 h内稳定。
2.8 加样回收率试验 大鼠空白血清中加入已知量的补骨脂素、异补骨脂素对照品,分别制成高、中、低质量浓度的样品,按“2.4.1”项下操作,结果平均回收率(n=6)依次为补骨脂素97.84%(3.54%),93.08%(4.36%),90.69%(5.21%);异补骨脂素97.12% (3.76%),93.22%(3.82%),89.68%(5.47%)。大鼠空白肝匀浆液中加入已知量的补骨脂素、异补骨脂素对照品,分别制成高、中、低质量浓度的样品,按“2.4.2”项下操作,结果平均回收率 (n=6)值依次为补骨脂素 98.79% (2.97%),97.60%(3.52%),91.25% (4.03%);异补骨脂素97.97%(4.40%),96.55%(5.86%),90.71%(5.28%)。大鼠空白肾匀浆液中加入已知量的补骨脂素、异补骨脂素对照品,分别制成高、中、低质量浓度的样品,按“2.4.3”项下操作,结果平均回收率(n=6)值依次为补骨脂素96.80%(4.92%),96.56%(5.09%),92.30%(5.76%);异补骨脂素98.79%(4.94%),96.22%(5.29%),91.34%(5.67%)。结果表明,该方法切实可行。
2.9 样品测定 精密称取补骨脂药材粉末 (过四号筛),按3.0 g/kg大鼠灌胃给药,1 h后眼眶取血,按“2.4”项下方法操作,制备血清、肝、肾供试品,内标法计算各供试品中补骨脂素、异补骨脂素的量。结果,血清中补骨脂素为6.96 mg/L、异补骨脂素为1.67 mg/L;肝脏中补骨脂素为4.98 mg/L、异补骨脂素为0.76 mg/L;肾脏中补骨脂素为2.04 mg/L、异补骨脂素为0.29 mg/L。
3 讨论
本实验建立了大鼠体内补骨脂中主要成分补骨脂素、异补骨脂素的同时检测方法。采用常用的紫外检测器,操作简单可行。对不同色谱柱进行了对比,补骨脂素与异补骨脂素均达到了基线分离,分离度良好。实验中对血清、肝、肾不同预处理方法做了初步考察,筛选了不同的萃取溶剂,丙酮、三氯甲烷等回收率低或有干扰,对不同配比的乙酸乙酯-正己烷进行考察,其中乙酸乙酯-正己烷(8∶1)提取效果最好,回收率高。故确定最佳萃取溶剂为乙酸乙酯-正己烷 (8∶1)。
通过预试验发现,空白血清、肝匀浆液、肾匀浆液在补骨脂素、异补骨脂素相同的保留时间内没有干扰。但是,如果大鼠有脂肪肝或高脂血症,则在补骨脂素和异补骨脂素相同的保留时间有干扰。因此,在选择大鼠时应注意检测血脂水平。对不同年龄的大鼠也进行了考察,发现24月龄大鼠,在补骨脂素、异补骨脂素相同的保留时间内有干扰,2月龄大鼠没有干扰。估计是老龄动物的基础代谢物质与青年动物不同造成的。对于雌鼠与雄鼠,预试验发现对补骨脂素和异补骨脂素的代谢速度不一样,具体差异尚需药代动力学进一步研究。综上所述,在测定补骨脂在体内分布及代谢时,应选用4月龄左右的大鼠,雌雄各半,同时给予低脂饲料。
本实验建立了一种快速分析大鼠体内血清、肝、肾中补骨脂药材有效成分补骨脂素和异补骨脂素含量的方法。该方法具有高灵敏度、操作简单等特点,为补骨脂药代动力学研究以及在体内各组织的分布,提供了必要的参考。
[1]Yin Sheng,Fan Chengqi,Dong Lei,et al.Psoracorylifols A-E,five novel compounds with activity against helicobacterpylon from seeds of Psoralea corylifolia[J].Tetrahedron,2006,62(11):2569-2575.
[2]Ruan B,Kong L Y,Takaya Y,et al.Studies on the chemical constituents of Psoralea corylifolia[J].J Asian Nat Prod Res ,2007,9(1):41-44.
[3]蔡 宇.补骨脂素逆转白血病HL60/HT耐药细胞研究[J].中成药,2004,26(9):772-773.
[4]郑里翔,崔志远,郭慧君,等.补骨脂汤对痴呆大鼠海马NR2B,BDNF/TrkB表达的影响[J].时珍国医国药,2009,20(12):1230-1233.
[5]冯 怡,邓远辉,袁小红.补骨脂注射剂致局部刺激反应的原因分析[J].中成药,2003,25(11):929-931.
[6]王天晓,伊震花,张 伟,等.补骨脂抗氧化、抑制α-葡萄糖苷酶和抗菌活性成分研究[J].中国中药杂志,2013,38(14):2329-2333.
[7]唐昌娟,施 贝,修彦凤.四神丸水煎液中补骨脂素和异补骨脂素的大鼠体内药动学研究[J].中成药,2012,34(2):248-251.
[8]陈红莉,冯慧瑾,李援朝.补骨脂酚的体外抗肿瘤活性及其关键中间体的合成研究[J].药学学报,2010,45(4):467-470.
[9]宋 潇,戚爱棣,王跃飞,等.不同炮制方法对补骨脂中4类化学成分的影响[J].中国中药杂志,2011,36(15):2071-2075.
[10]邱蓉丽,李 璘,乐 巍.补骨脂的化学成分与药理作用研究进展[J].中药材,2010,33(10):1656-1659.
[11]李晶晶,鹿秀梅,李发美,等.补骨脂的化学及代谢成分的超高效液相色谱串联质谱法鉴定[J].时珍国医国药,2010,21(9):2235-2238.
[12]丁黎艳,郭晏华,黄 婷,等.基于补骨脂抗骨质疏松成分的炮制评价方法研究[J].中成药,2013,35(2):346-349.
[13]李俊娟,李 军.HPLC法测定补骨脂药材中补骨脂素和异补骨脂素[J].中成药,2012,34(8):1545-1548.
[14]胡 馨,王 平,张英华,等.补骨脂炮制工艺与质量标准研究[J].中成药,2007,29(7):1026-1031.
[15]田永华,钱 叶,俞 圆.HPLC测定腰痛片中补骨脂素和异补骨脂素的含量[J].中成药,2007,29(8):附12-13.
[16]国家药典委员会.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010:174.

