山东产区黄芩HPLC定量指纹图谱研究△
赵恒强,王晓*,周洁,周思多,2,东莎莎,耿岩玲,刘建华,杨丙田,杨鹏
(1.山东省科学院 中药过程控制研究中心/山东省大型精密分析仪器应用技术重点实验室/ 山东省分析测试中心,山东 济南 250014; 2.山东农业大学 食品科学与工程学院,山东 泰安 271018; 3.济南三峰生物工程技术有限公司,山东 济南 251400)
山东产区黄芩HPLC定量指纹图谱研究△
赵恒强1,王晓1*,周洁1,周思多1,2,东莎莎1,耿岩玲1,刘建华1,杨丙田3,杨鹏3
(1.山东省科学院 中药过程控制研究中心/山东省大型精密分析仪器应用技术重点实验室/ 山东省分析测试中心,山东 济南 250014; 2.山东农业大学 食品科学与工程学院,山东 泰安 271018; 3.济南三峰生物工程技术有限公司,山东 济南 251400)
目的建立山东产区黄芩药材定量指纹图谱,为黄芩药材的真伪鉴别及质量控制提供方法支持。方法采用Agilent ZORBAX SB-C18色谱柱,乙腈-水(含1%甲酸、20 mmol·L-1甲酸铵)为流动相进行梯度洗脱,流速为0.8 mL·min-1,柱温为25 ℃,检测波长为274 nm,进样量5 μL,进行了10批次黄芩药材的分析。结果该分析方法具有良好的精密度、重现性,10批黄芩指纹图谱有17个共有峰,4个特征峰,采用ESI-TOF/MS 对4 个特征峰进行了指认,10个批次山东产黄芩样品中6种黄酮类化合物含量分布规律相似,其相似度系数均大于0.955 7。结论黄芩HPLC定量指纹图谱有望成为黄芩样品真伪鉴别及质量控制的有力工具。
黄芩;HPLC;定量指纹图谱
黄芩为唇形科植物黄芩ScutellariabaicalensisGeorgi的干燥根,最早收载于《神农本草经》,为传统常用中药,具有清热燥湿,泻火解毒,止血,安胎功能[1-2]。黄芩是我国中医临床常用大宗药材品种之一,山东省黄芩药材种植面积较大,全省种植面积在6 667 hm2以上[3]。
目前,黄芩的质量控制方法主要是采用单指标成分对其进行质量控制,2010版《中国药典》中采用黄芩苷含量作为质量控制指标[1],但是单一的指标成分难以反映中药多成分、多靶点的特点。中药指纹图谱是一种综合的、可量化的鉴别手段,是当前符合中药特色的评价中药真实性、稳定性和一致性的质量控制模式,具有整体性、模糊性等特点,体现系统性、特征性和稳定性的基本原则[4-6]。指纹图谱目前已广泛应用于中药质量控制中,在黄芩质量控制和真伪鉴别中也有大量应用[7-9]。但是,已有的指纹图谱方法主要是对共有峰的指认及结合模式识别等方法对其进行质量评价和产地鉴别,缺少特征峰的含量信息。指纹图谱技术与多指标成分定量相结合可以更加全面地反应中药质量特点,是一种值得继续探索的中药质量控制模式,果德安等对其进行了大量研究工作[10-11]。而有关多指标定量指纹图谱技术在黄芩质量控制中的研究应用未见报道。
本研究采用HPLC建立山东产区黄芩样品的多指标定量指纹图谱,为有效控制黄芩药材质量,保证建立符合规模化生产的黄芩基地及生产过程控制提供方法和技术支持。
1 仪器与材料
1.1 仪器
1200型高效液相色谱仪(美国Agilent公司),配有二极管阵列(DAD)检测器,四元泵,柱温箱,自动进样器等;G6520型四级杆串联飞行时间质谱仪,配有电喷雾离子源(美国Agilent公司);KQ-400KDE型超声波仪(昆山市超声仪器有限公司);Milli-Q(18.2 MΩ)超纯水处理系统(美国Millipore公司);THZ-8 恒温水浴锅(中国浙江嘉兴电热仪器厂)。
Agilent ZORBAX SB-C18色谱柱(250 mm×4.6 mm,5 μm,美国Agilent公司),Agilent Eclipse XDB-C18色谱柱(250 mm×4.6 mm,5 μm,美国Agilent公司),Waters XBridgeTMC18(150 mm×2.1 mm,3.5 μm,美国Waters公司),依利特Hypersil ODS2(250 mm×4.6 mm,5 μm,大连依利特)。
1.2 材料
黄芩苷(批号:110715-200514)、黄芩素(批号:111595-200905)、汉黄芩素(批号:111514-200403)对照品均购自中国食品药品检定研究院;汉黄芩苷(批号:20090319)、黄芩新素(批号:20090617)、千层纸素A(批号:20091124)对照品均购自上海顺勃生物工程技术有限公司,纯度均大于98.5%。甲醇、乙腈(色谱纯,美国Fisher Scientific),甲醇(分析纯,天津市广成化学试剂有限公司),甲酸(色谱纯,天津市科密欧化学试剂有限公司),甲酸铵(色谱纯,天津市科密欧化学试剂有限公司),其余试剂均为分析纯,水为自制Milli-Q超纯水,其余试剂均为分析纯。
本研究采集的10个不同批次的黄芩样品分别于2011~2012年购自济南市各大药店及山东各GAP种植基地,经山东省分析测试中心王晓研究员鉴定为黄芩ScutellariabaicalensisGeorgi的干燥根,样品详细信息见表1。
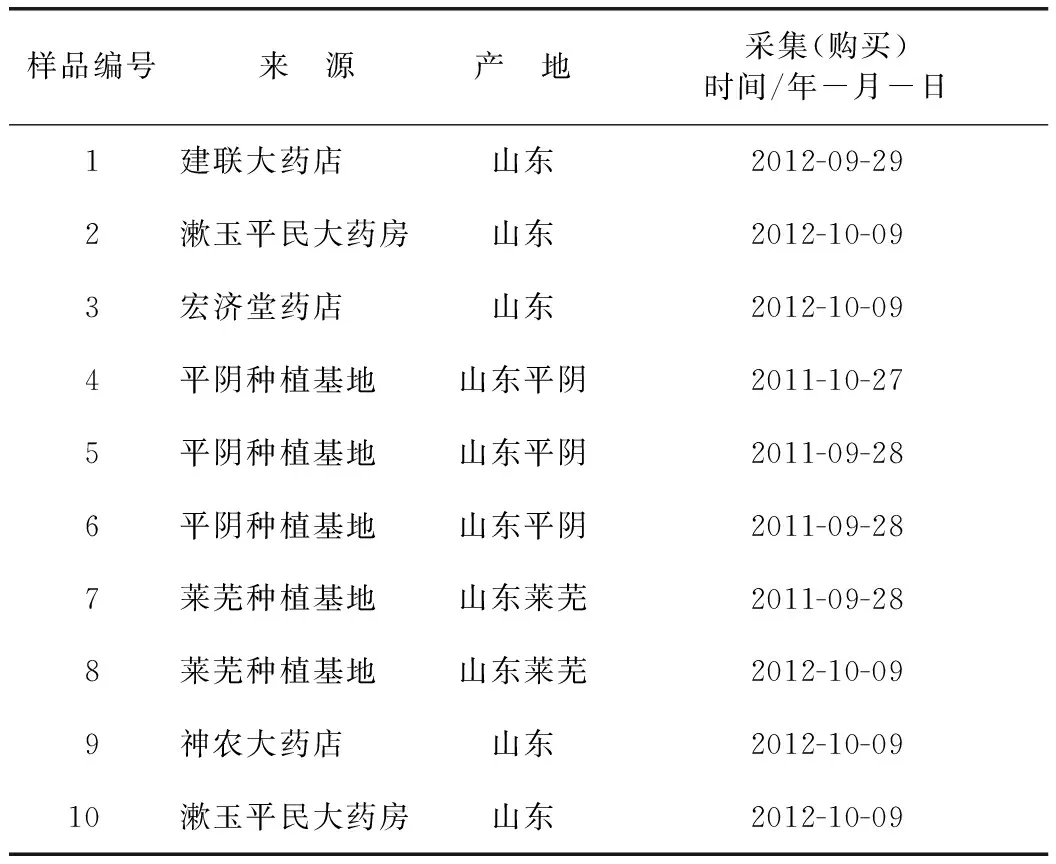
表1 黄芩样品信息
黄芩样品置于烘箱中55 ℃鼓风干燥4 h,然后置于真空干燥箱中55 ℃干燥4 h至干。干燥后粉碎,过40目筛,混合均匀,制备成黄芩干粉样品,密闭、避光、干燥、常温贮藏。
2 方法与结果
2.1 供试品溶液的制备
准确称取0.5 g黄芩干粉样品,置于100 mL 具塞锥形瓶中,加入25 mL甲醇,超声提取10 min(提取功率320 W,频率40 Hz),在52~55 ℃条件下将提取液旋转蒸发浓缩至干,用甲醇重新溶解,并定容至5 mL,过0.22 μm微孔滤膜后作为供试品溶液。
2.2 对照品溶液的制备
分别精密称取5.0 mg黄芩苷、黄芩素、汉黄芩苷、汉黄芩素、黄芩新素、千层纸素 A对照品置50 mL量瓶中,用甲醇溶解,定容至刻度作为对照品溶液。
2.3 色谱条件
Agilent ZORBAX SB-C18色谱柱(250 mm×4.6 mm,5 μm),流动相A:1%甲酸、20 mmol·L-1甲酸铵的水溶液,流动相B:乙腈,流速为0.8 mL·min-1,柱温25 ℃,检测波长为274 nm,进样量为5 μL,按表2进行梯度洗脱,黄芩样品HPLC分析图见图1。
2.4 质谱条件
ESI-MS工作条件如下:色谱柱后分流进入质谱的流动相流速为0.4 mL·min-1,正离子电离模式,雾化气压力45 psi,干燥气(N2)流速10.0 L·min-1,干燥气体温度350 ℃,毛细管电压4 500 V,裂解电压:100 V;锥孔电压:60 V,全扫描(Scan)质荷比(m/z)范围为50~1 000。
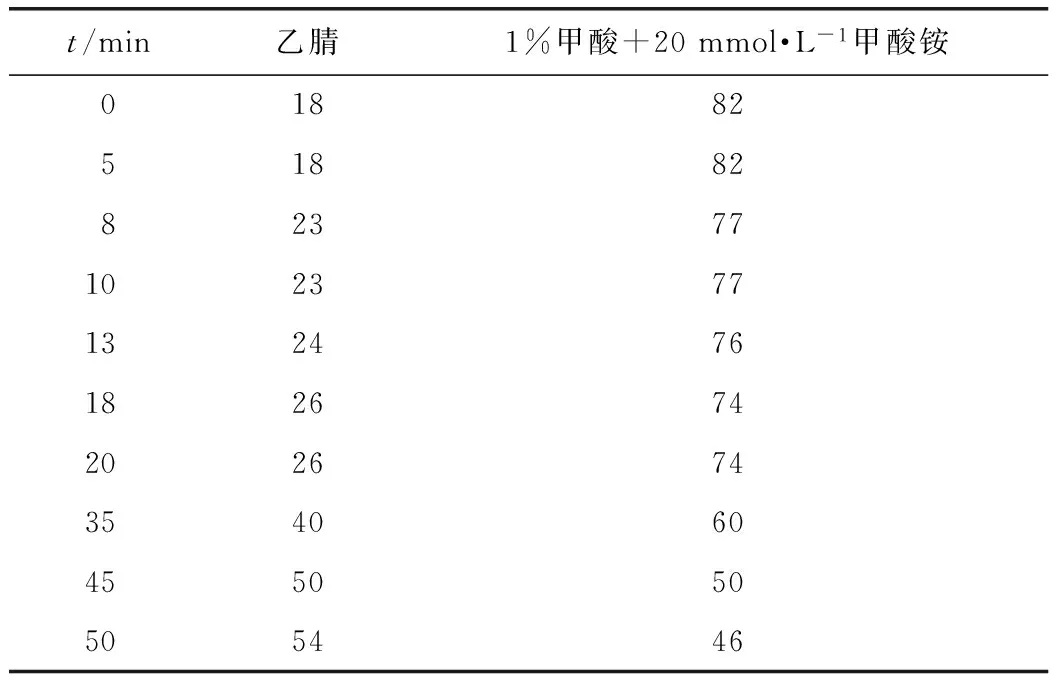
表2 流动相梯度条件 /%
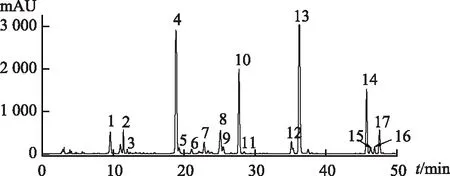
图1 黄芩HPLC-DAD图谱(274 nm)
2.5 方法学考察
2.5.1 标准曲线及检测限 按2.3色谱条件进样分析,测定各不同质量浓度(0.10,0.20,0.50,1.00,10.00,50.00 μg·mL-1)混合对照品溶液中各化合物的峰面积,以各化合物质量浓度(μg·mL-1)为横坐标,以峰面积为纵坐标,绘制标准曲线,并求得回归方程(见表3)。将标准溶液稀释至低浓度进样,以3倍信噪比计算各成分的检测限,以10倍信噪比计算定量限,结果见表3。
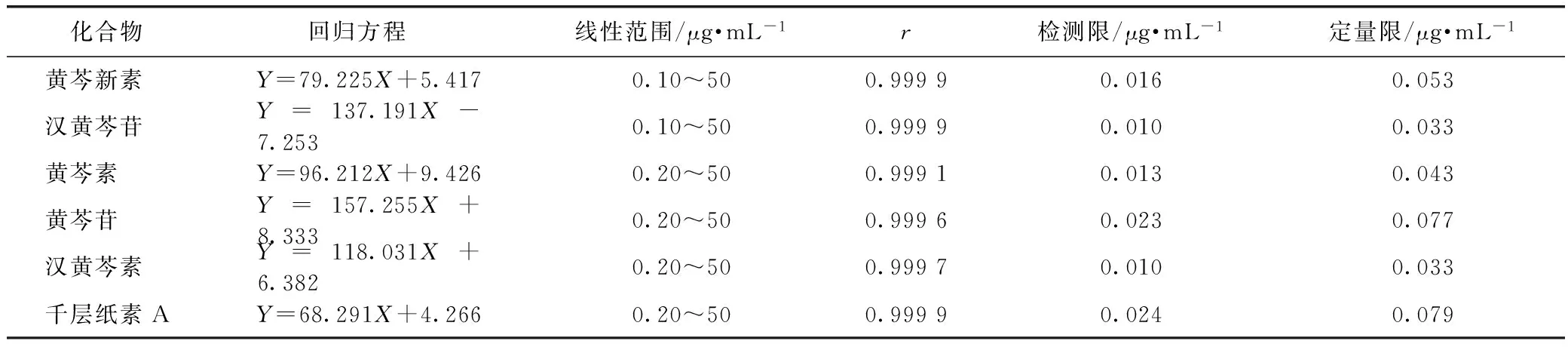
表3 6种黄酮HPLC分析回归方程、线性范围及检测限、定量限测定结果
2.5.2 精密度试验 按照2.1供试样品的制备方法制备供试溶液,按照2.3色谱条件,重复进样6次测定,分别测得其中4个主要峰(分别为峰4,10,13,14)的峰面积和保留时间,分别计算其RSD。4个主峰峰面积和保留时间的RSD值在0.12%~0.78% 和0.09%~0.25%,表明仪器精密度良好。
2.5.3 重复性试验 精密称取同一黄芩样品6份,按照2.1供试样品的制备方法分别制成供试品溶液,按照2.3的色谱条件,进行色谱分析,测得4个特征峰的峰面积和保留时间,并计算其RSD,4个主要峰(分别为峰4,10,13,14)峰面积和保留时间的RSD值分别在1.42%~3.58%和0.11%~0.21%,表明该方法重复性良好。
2.5.4 稳定性试验 按照2.1供试样品的制备方法制备供试溶液,按照2.3的色谱条件,分别在0,1,3,6,12,24,48,72 h进样测定,结果显示黄芩提取物溶液的峰面积和保留时间无明显变化,4个主要峰(分别为峰4,10,13,14)峰面积和保留时间的RSD 值分别在1.67%~3.90%和0.59%~2.09%,说明供试品溶液在72 h内化学性质稳定。
2.5.5 加样回收率试验 精密称取已知含各对照品含量的黄芩样品0.50 g,按高、中、低3种浓度分别准确加入黄芩苷、黄芩素、汉黄芩苷、汉黄芩素、黄芩新素、千层纸素 A对照品适量,按照供试品溶液制备方法处理6 份,按上述色谱条件进样分析,测定各对照品峰面积,计算平均加样回收率,结果见表4。
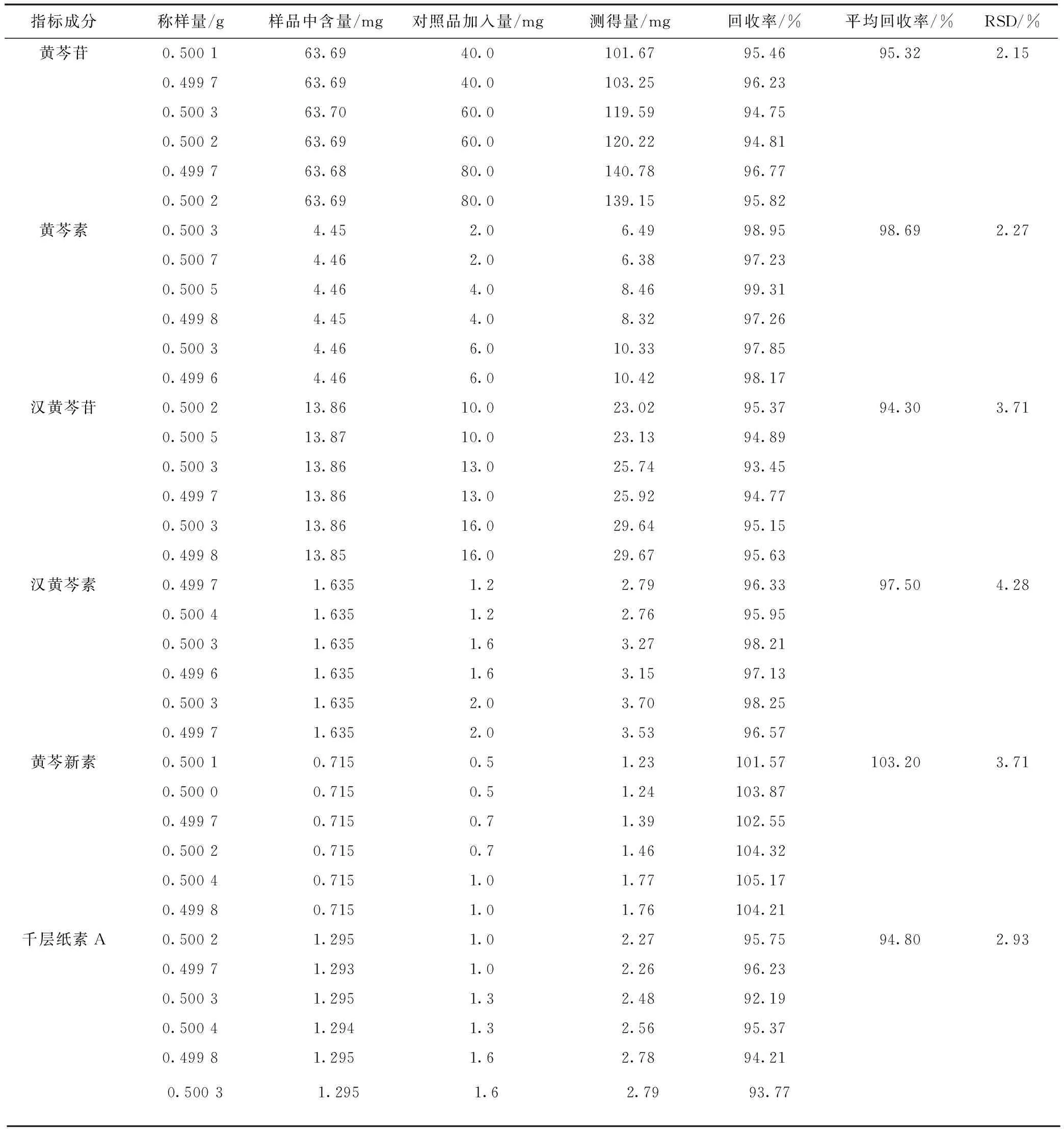
表4 黄芩中各成分加样回收率试验
2.6 指纹图谱的建立与分析
2.6.1指纹图谱的建立 取10批黄芩样品,按2.1供试品溶液制备方法将其制备成供试品溶液,按2.3HPLC色谱条件进样分析,记录色谱图,建立黄芩样品的HPLC指纹图谱,10批黄芩样品的色谱图见图2。从图2可以看出10批黄芩样品的指纹图谱差异不大,因此,10批黄芩样品均可用于共有峰的确定。10批黄芩样品HPLC指纹图谱的共有峰有17个(较大的峰,已扣除溶剂峰)。
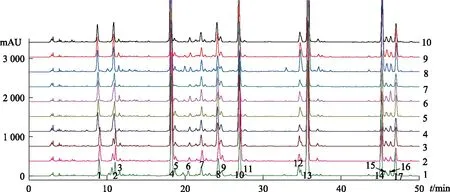
图2 山东产区10批黄芩HPLC指纹图谱
在本研究所建立的分析系统下,黄芩甲醇提取物各成分出峰时间主要在50 min之前,特征性明显的主要有4个色谱峰,这4个色谱峰即构成黄芩HPLC指纹图谱的特征峰(分别为峰4,10,13,14),其中以峰高最高的10号峰为指标峰,该峰化学性质稳定,保留时间以及峰面积重复性良好,与其他相邻峰分离良好,采用化学工作站计算该峰的纯度表明该峰为一纯化合物。因此选择10号峰为指标峰(保留时间和峰面积均设为1),用于计算各共有峰相对保留时间和相对峰面积。结果表明,山东产区10批黄芩样品各共有峰保留时间的RSD均在5%以内,各共有峰相对峰面积的RSD相差较大,但其谱图轮廓一致。
2.6.2 特征峰的指认 采用对照品和高效液相色谱-电喷雾飞行时间质谱联用技术(HPLC-ESI-TOF/MS)对黄芩指纹图谱中的特征峰进行分析,HPLC工作条件同2.3色谱条件,在选定的实验条件下对黄芩甲醇提取物进行分析,获得其总离子流色谱图,黄芩指纹图谱中的4个特征峰的精确质量测量结果见表5。

表5 黄芩甲醇提取物中4个化合物的HPLC-ESI-TOF/MS精确质量测量结果
2.6.3 相似度评价 通过《中药色谱指纹图谱相似度评价系统》(《中国药典》2004 A版)对10批黄芩样品进行相似度分析。首先将色谱工作站数据导入中药指纹图谱相似度计算软件,选定上述17个共有峰进行谱峰匹配,采用共有模式作为对照指纹图谱,用于10批黄芩样品相似度评价,见表6。
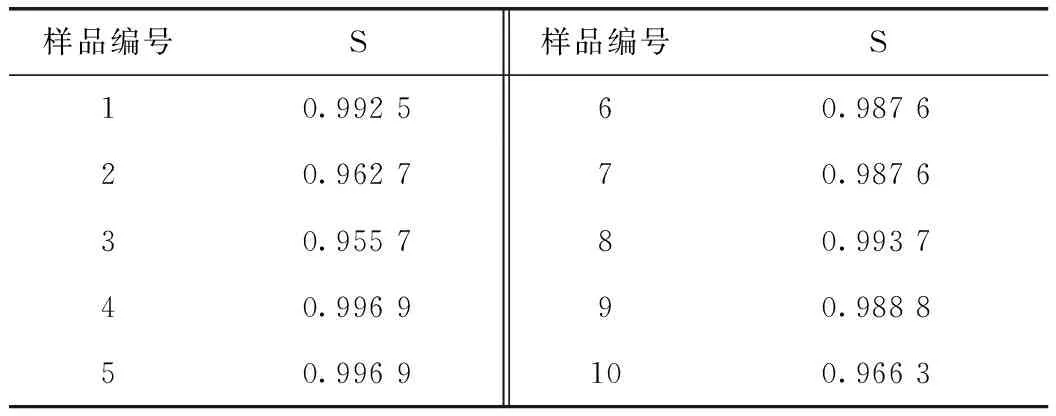
表6 山东产区10批黄芩药材相似度评价结果
从表6可以看出,10批山东产区的黄芩样品指纹图谱相似度较高,均在0.955 7以上。研究结果为山东产区黄芩药材的质量控制研究提供了依据。
2.7 黄芩样品测定
按2.1供试品溶液制备方法制备样品溶液,按2.3色谱条件分别进样分析,获得山东产区10批黄芩样品中6个共有峰所对应化合物的色谱峰面积,将测得结果代入表3线性回归方程,计算黄芩样品中各化合物的质量分数(见表7)。从表7可以看出,山东产区10个批次的黄芩样品中6种黄酮类化合物质量分数分布规律相似。

表7 山东产区10批黄芩中6种黄酮类化合物的测定(n=3) /%
3 讨论
3.1 提取条件优化
本研究采用2.3色谱条件,采用超声提取技术,首先对黄芩不同提取溶剂(水、25%甲醇、50%甲醇、75%甲醇、100%甲醇)提取物溶液进行分析,结果显示,当水或25%甲醇作为提取溶剂时,中间段色谱峰峰高较低,提取较差;后三者相比,100%甲醇作为提取溶剂时,所得色谱图色谱峰信号较强,且各峰分离度好、基线平稳,指纹特征明显,因此选择100%甲醇作为黄芩指纹图谱样品提取溶剂。
在优化的提取溶剂条件下,考察了不同料液比(1∶20、1∶50、1∶80)对提取率的影响,结果表明,当料液比为1∶50时,黄芩各成分提取率较高。进一步考察了不同提取时间(5,10,15 min)对黄芩成分提取率的影响,结果表明当提取时间为10 min时,黄芩各成分已基本提取完全。
3.2 色谱条件优化
黄芩甲醇提取物化学成分复杂,采用等度洗脱的方法很难将黄芩醇提物中的多种化合物分离开,因此采用线性梯度洗脱方式进行分离。本研究对仪器与试药中所列的4根不同生产厂家的色谱柱进行了比较,结果表明,使用Agilent ZORBAX SB-C18色谱柱获得的黄芩醇提物指纹图谱各峰分离度高,色谱峰分布均匀,峰型较好,具有较好的代表性,因此选择Agilent ZORBAX SB-C18柱用于黄芩药材的指纹图谱研究。在此基础上,比较了甲醇-水、乙腈-水作为流动相时的色谱图效果,发现乙腈-水效果明显优于甲醇-水。黄芩含有多种化学成分,其中黄酮类化合物为主要有效成分,其大多呈弱酸性,因此实验中加入甲酸、甲酸铵调节流动相pH以改善分离度和色谱峰形,结果发现以1%甲酸、20 mmol·L-1甲酸铵水溶液-乙腈为流动相时,色谱指纹图谱效果最好。通过二极管阵列检测器全波段扫描(190~400 nm),考察了不同检测波长对指纹图谱的影响,结果表明,在UV 274 nm条件下检测获得的色谱指纹图谱信息量大,指纹峰特征性强,具有较好的代表性,因此选择274 nm作为黄芩HPLC指纹图谱研究的检测波长(见图1)。
3.3 指纹图谱评价
本研究在多批次样品分析的基础上,建立了山东产区黄芩样品的HPLC指纹图谱,选取了17个稳定性好,特征性明显的峰作为共有峰,并采用对照品和ESI-TOF/MS技术对4个特征峰进行了指认,分别为:峰4(汉黄芩苷)、峰10(黄芩素)、峰13(黄芩苷)、峰14(汉黄芩素)。采用相似度分析对山东产区的10批黄芩样品进行了对比,结果表明,相似度系数均大于0.955 7。定量分析结果表明,山东产区的10批黄芩样品中6种黄酮类化合物含量分布规律相似。黄芩为大宗常用中药材,本研究建立的山东产区黄芩HPLC多指标定量指纹图谱,为山东产区黄芩药材的质量控制研究提供了方法和技术支持。
[1] 国家药典委员会.中国药典 [S].一部.北京:中国医药科技出版社,2010:282.
[2] 周永妍,程秀民,于海英,等.黄芩药材中主要黄酮类成分含量测定及指纹图谱研究[J].中华中医药杂志,2009,24(7):882-885.
[3] 赵渤年,高燕,丁晓彦.山东栽培黄芩的指纹图谱研究[J].时珍国医国药,2009,20(5):1243-1245.
[4] 李强,李超.中药指纹图谱研究综述[J].齐鲁药事,2010,29(3):158-161.
[5] 孙磊,乔善义,赵毅民.中药指纹图谱应用研究进展[J].国际药学研究杂志,2009,36(3):194-198.
[6] 王小如,黎先春,李磊.中药及中药材质量控制关键技术[M].北京:化学工业出版社,2006:146.
[7] 肖蓉,张志斐,袁志芳,等.河北道地药材黄芩指纹图谱的研究[J].药物分析杂志,2007,27(7):1018-1023.
[8] 王健,张晓军,郑淑艳.黄芩药材RP-HPLC指纹图谱研究[J].现代中西医结合杂志,2008,17(16):2456-2457.
[9] 肖丽和,王红燕,李发美,等.不同来源黄芩药材HPLC指纹图谱比较[J].沈阳药科大学学报,2004,21(1):28-31.
[10] 果德安.中药质量控制研究的思路与方法[J].中国天然药物,2009,7(1):1.
[11] 刘荣霞,叶敏,果德安.中药质量控制研究的思路与方法[J].中国天然药物,2006,4(5):332-337.
StudyOnQuantitativeHPLCFingerprintofScutellariabaicalensisGeorgi
ZHAOHengqiang1,WANGXiao1,ZHOUJie1,ZHOUSiduo1,2,DONGShasha1,GENGYanling1,LIUJianhua1,YANGBingtian3,YANGPeng3
(1.ProcessControlResearchCenterofTraditionalChineseMedicineofShandongAcademyofSciences,ShandongAnalysisandTestCenter,KeyLaboratoryforAppliedTechnologyofSophisticatedAnalyticalInstrumentsofShandongProvince,Jinan250014,China2.CollegeofFoodScienceandEngineering,ShandongAgriculturalUniversity,Taian271018,China3.JinanSanfengBioengineeringTechnologyCompany,Jinan251400,China)
Objective:A quantitative high performance liquid chromatography(HPLC)fingerprinting method had been used for the quality evaluation and discrimination ofScutellariabaicalensisGeorgi.MethodsThe chromatographic fingerprints were determined by injecting 5 μL of the sample solution each time on C18column(Agilent ZORBAX SB-C18column)with the gradient elution solvent system composed of 20 mmol·L-1HCOONH4+1% HCOOH and acetonitrile.The flow rate was 0.8 mL·min-1,the column temperature was maintained at 25 ℃ and the signals were acquired at 274 nm.ResultsIt was indicated that the developed HPLC method was simple,accurate and reliable for the development ofS.baicalensisfingerprint.The HPLC fingerprinting for ten batches samples tested contained the same seventeen peaks,and it could be used to discriminate different origins ofS.baicalensissamples combined with similarity analysis.ConclusionThe HPLC fingerprinting technique is an important tool in identification and quality evaluation ofS.baicalensis.
ScutellariabaicalensisGeorgi;HPLC;Quantitative fingerprint
国家重大新药创制——中药大品种脑心通胶囊技术改造研究(2011ZX09201-201-26);山东省自然基金(ZR2013HL029);山东省科学院科技发展基金项目[科基合字(2012)第15号];山东省科技攻关计划(2011GSF11908)
*
王晓,博士,研究员,研究方向:中药质量控制及资源;Tel:(0531)82605319,E-mail:wangx@sdas.org
10.13313/j.issn.1673-4890.2014.07.003
2013-10-17)

