右美托咪定对全麻腹腔镜手术术后CO2蓄积患者复苏阶段的影响
邓方方,吴 昱
(武汉市第一医院 麻醉科,湖北 武汉 430030)
腹腔镜手术时,二氧化碳的吸收会导致高碳酸血症。患者在苏醒期往往出现意识不清、烦躁、心率增快、血压增高等症状,造成伤口裂开、渗血、留置针脱落、坠床骨折、心脑血管意外等不良后果。传统的如咪达唑仑、丙泊酚等药物的使用或是镇静深度不够,或是在镇静的同时也抑制了患者的呼吸,导致二氧化碳不能及时有效地排出,甚至迫使麻醉师再次对患者行气管插管。而右美托咪定的应用可有效地改善这一状况。本研究旨在观察右美托咪定对全麻腹腔镜手术术后二氧化碳蓄积患者复苏阶段的影响。
1 资料与方法
1.1 一般资料
2013年6月至2013年12月在武汉市第一医院择期全麻行腹腔镜手术的患者,年龄20~59岁,无心血管病史,无特殊药物应用史,无精神或神经系统疾病,体重无明显差异。ASAⅠ~Ⅱ级。术毕前约40min测动脉血气,选取其中PaCO270~90mmHg,pH<7.30的患者40例,其中男性26例,女性14例。随机分为对照组(N组)和右美托咪定组(D组)各20例。两组患者在性别、年龄、身高、体重及ASA分级上均无显著性差异,具有可比性。
1.2 麻醉方法
所有患者均在诱导前5 min静脉注射长托宁0.01mg/kg、托烷司琼2 mg;咪达唑仑2 mg、舒芬太尼 0.5 μg/kg、顺式阿曲库铵 0.2 mg/kg、丙泊酚1~2 mg/kg静脉注射快速诱导后行气管插管;术中以瑞芬太尼0.5 μg/kg/min、丙泊酚3mg/(kg·h)维持麻醉,每30 min追加顺式阿曲库铵0.1mg/kg;术毕前约15 min均静脉注射帕瑞昔布钠40 mg行术后镇痛。取得动脉血气结果后,在手术结束前约30 min,N组患者给予0.9%氯化钠10 mL静脉缓注,D组患者用右美托咪定配成4 μg/mL浓度以0.8μg/kg剂量缓慢静注,输注时间超过15min。手术结束时给予新斯的明和阿托品拮抗肌松药残留作用,待患者呼吸恢复满意后拔管并面罩给氧。
1.3 观察指标
记录两组患者在拔管时(T0)、拔管后5min(T1)、拔管后30min(T2)的心率、血压及Riker评分(SAS)标准:1分,嗜睡,对触碰或大声刺激有轻微反应;2分,嗜睡,对触碰或大声刺激反应迟钝;3分,嗜睡,对触碰或大声刺激只能做简单反应;4分,病人安静合作;5分,病人焦虑躁动,可听劝阻;6分,病人躁动不安,需要束缚;7分,病人攻击性躁动、不安,在床上辗转挣扎。并同时记录患者从拔管开始到恢复满意(Aldrete评分≥9)可以送回病房所需时间(T3)。
1.4 统计学方法
检验指标资料的数据采用SPSS13.0统计软件分析,计量数据以均数±标准差()表示,组间进行t检验,以P<0.05为差异有统计学意义。
2 结果
2.1 两组患者血压、心率比较
两组患者在拔管时、拔管后5min、拔管后30min的心率、血压的比较:D组患者在拔管时、拔管后5min、拔管后30min的心率、收缩压、舒张压与N组患者比较差异均有统计学意义(P<0.05),见表1。
2.2 两组患者SAS评分及T3的比较
两组患者在SAS评分及从拔管开始到完全清醒可以送回病房所需时间的比较:D组患者在拔管时、拔管后5min、拔管后30min的SAS评分明显低于N组患者(P<0.05)。在患者至拔管开始到完全清醒可以送回病房所需时间上两组数据的比较差异无统计学意义(P>0.05),见表2。
表1 两组患者血压、心率比较()Tab.1 Comparison of blood pressure and heart rate of two groups()
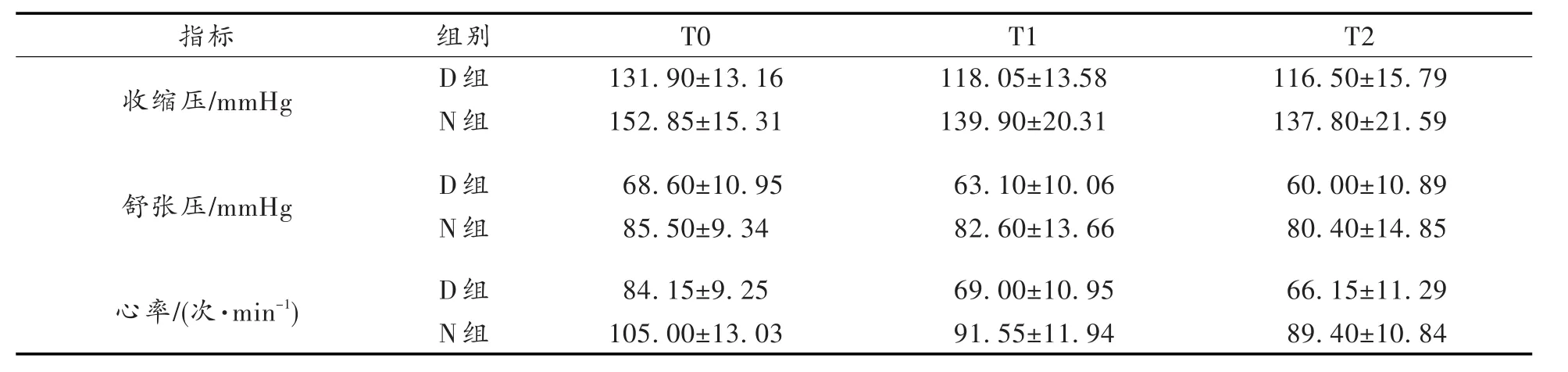
表1 两组患者血压、心率比较()Tab.1 Comparison of blood pressure and heart rate of two groups()
指标收缩压/mmHg舒张压/mmHg心率/(次·min-1)组别D组N组D组N组D组N组T0131.90±13.16152.85±15.3168.60±10.9585.50±9.3484.15±9.25105.00±13.03 T1118.05±13.58139.90±20.3163.10±10.0682.60±13.6669.00±10.9591.55±11.94 T2116.50±15.79137.80±21.5960.00±10.8980.40±14.8566.15±11.2989.40±10.84
表2 两组患者SAS评分及T3的比较()Tab.2 Comparison of SAS score and T3 of two groups()

表2 两组患者SAS评分及T3的比较()Tab.2 Comparison of SAS score and T3 of two groups()
D组N组T0 SAS评分2.75±0.715.85±0.74 T1 SAS评分2.80±0.835.90±0.76 T2 SAS评分3.95±0.755.05±0.68 T3/min 66.25±17.7667.50±15.85
3 讨论
目前,随着腹腔镜手术的迅猛发展,其临床上并发症的发生率也越来越高。最常见的就是CO2蓄积导致的高碳酸血症引起一系列的不良后果。如本研究中的N组患者,术毕拔管后常见意识不清、躁动不安、循环不稳。更有不在少数的患者极度烦躁,无法约束,完全无法配合麻醉师的后续工作。极可能发生坠床、伤口裂开及心脑血管意外等,增加了手术护理及麻醉处理的难度。而D组患者在术毕前预注右美托咪定后情况明显改观。
理想的镇静剂应具有以下几种特征:镇静同时可以唤醒;兼有镇痛、抗焦虑等作用;没有呼吸抑制作用;血流动力学稳定;不会引起恶心、呕吐、便秘的不良反应[1]。根据文献[2]报道,右美托咪定是目前最为理想的、符合上述特征的镇静药物。该药的主要药效学作用较广[3],具有镇静、镇痛、交感阻断等作用,而且不会产生呼吸抑制,可以维持患者在围术期的血流动力学稳定,有效减少心脑血管意外的发生。
研究表明,右美托咪定通过脑干蓝斑区的α2受体及血管运动中枢来发挥抗交感作用。α2肾上腺素能受体激动剂抑制中枢交感神经发放冲动,使交感神经张力降低及迷走神经活动性增强,并激动交感神经末梢的突触前α2受体,抑制去甲肾上腺素的释放及降低血浆中儿茶酚胺浓度[4]。因此,右美托咪定能有效地拮抗高碳酸血症所引起的儿茶酚胺释放,在药效学上主要表现出血压和心率下降。由表1可见,D组患者在拔管时、拔管后5min、拔管后30min的心率、血压表现持续平稳,其数值明显低于N组患者(P<0.05)。平稳的血流动力学表现在麻醉复苏期对患者是非常有益的。
右美托咪定属咪唑类衍生物,其激动蓝斑的α2-肾上腺受体,引发并维持自然非动眼状态,产生镇静、催眠作用,且无呼吸抑制,易于唤醒[5]。EBERT 等[6]发现,在自主呼吸志愿者中注入盐酸右美托咪定,最高血药浓度时PaCO2增加20%,而随血药浓度增加呼吸频率也相应增加。而在瑞芬太尼和盐酸右美托咪定对呼吸影响的比较研究中,应用盐酸右美托咪定对高碳酸血症的通气反应性始终存在,此外盐酸右美托咪定能阻止组胺诱发的支气管痉挛[7]。因此,右美托咪定产生明显镇静时,患者对高碳酸血症的兴奋性可使分钟通气量得到维持。
CO2蓄积所致高碳酸血症的处理关键在于维持足够的通气使CO2能顺利排出。表2可见,D组患者SAS评分明显低于N组患者(P<0.05)。且在镇静的同时未见麻醉医师所担心的明显呼吸抑制。D组患者良好的镇静状态和足够的通气保证了其可以平稳安全地度过这一复苏阶段。而N组患者常见躁动不安甚至难以束缚,迫使在30min后使用如咪达唑仑、丙泊酚等药物,若产生明显的呼吸抑制还需面罩加压辅助通气,甚至再次行气管插管(1例),使麻醉处理复杂化,增加了患者的医疗费用及医疗风险。
在此研究中,笔者还发现,右美托咪定的使用并不延长此类患者在手术室的停留时间。因其在维持镇静期间保持一定的可唤醒能力的特点[8],所以不延迟唤醒时间。如表2所示,两组患者的离室时间比较差异无统计学意义(P>0.05),因此不必过多担心右美托咪定的使用造成时间更久的苏醒延迟。
综上所述,在CO2蓄积致高碳酸血症患者的麻醉复苏阶段,右美托咪定完全满足高碳酸血症患者的镇静需要,血流动力学平稳,无呼吸抑制,使用上既对症又安全。
(References)
[1]YAPICI N,CORUH T,KEHLIBAR T,et al.Dexme⁃detomidine in cardiac surgery patients who fail extuba⁃tion and present with a delirium state[J].Heart Surg Forum,2011,14(2):E93.
[2]PATELl A,DAVIDSON M,TRAN M C,et al.Dexme⁃detomidine infusion for analgesia and prevention of emergence agitation in children with obstructive sleep apnea syndrome undergoing tonsillectomy and adenoid⁃ectomy[J].Anesth Analg,2010,111(4):1004-1013.
[3]BLIESENER B,KLEINSCHMIDT S.Incidence and du⁃ration of postoperative delirium after cardiac surgery:Comparison between dexmedetomidine and morphine for postoperative sedat ion and analgesia[J].Anaesthe⁃sist,2010,59(3):256-257.
[4]PEKKA T.Pharmacodynam ice of alpha 2-adrenocep⁃tor agonists[J].Bailliere′s Clinical Anaesthesiology,2000,14:271-283.
[5]易利丹,彭六保,谭重庆,等.新型镇痛镇静药右美托咪定[J].中国新药与临床杂志,2011,30(1):5-10.
[6]EBERT T J,HALL J E,BARNEY J A,et a l.The ef⁃fects of increasing plasma concentrations of dexmedeto⁃midine in humans[J].Anesthesiology,2000,93(3):382-394.
[7]LOU Y P,FRANCO-CERECEDA A,LUNDBERG J M.Variable alpha 2-adrenoceptor-mediated inhibition of bronchconstriction and peptide release upon activa⁃tion of pulmonary afferents [J].Eur J Pharmacol,1992,210(2):173-181.
[8]ARPINO P A,KALAFATAS K,THOMPSON B T.Fea⁃sibility of dexmedetomidine infacilitating extubation in the intensive care unit[J].J Clin Pharm Ther,2008,33(1):25-30.

