海带浸泡液中碘离子的新型氧化工艺的研究*
闫绍鹏 ,苗钧魁 ,蒋 鹏 ,冷凯良 ,孙伟红 ,邢丽红 ,于跃芹
(1.青岛科技大学化学与分子工程学院,山东青岛 266042;2.中国水产科学研究院黄海水产研究所)
碘是人体所需要的微量元素之一,也是一种贵重的资源,广泛用于工农业,特别是医药卫生领域[1-3]。将I-氧化为I2是当前大多数提碘工艺中的重要程序之一。以海藻为原料的提碘行业中,最常用的氧化剂有氯气、次氯酸钠、亚硝酸钠和双氧水等[4-8]。氯气和次氯酸钠是工业上常用的氧化剂,但稍过量容易将I2氧化成。亚硝酸钠在pH<2.0的酸性介质中有较好的氧化效果,操作简单,过量也不会将I-过氧化,但是反应过程中会有NO气体生成,污染空气。双氧水的还原产物为水,不会向水体中引入杂质离子,具有环境友好性。双氧水在酸性条件下具有强氧化性容易将I-氧化成为。已知反应5I-++6H+=3I2+3H2O,但采用HIO3作为氧化剂成本较高,而H2O2可以将I-过氧化生成。所以笔者利用海带浸泡液中已有的I-,首先采用NaNO2与H2O2作为混合氧化剂制备新型氧化剂HIO3,然后再在酸性条件下与浸泡液中的I-反应生成I2,为海带提碘工业提供了一种新型的碘离子氧化方法。
1 实验部分
1.1 主要原料及实验设备
干海带(市售);浓盐酸、30%(质量分数)过氧化氢、氢氧化钠、环己烷、硫代硫酸钠、重铬酸钾、可溶性淀粉、碘化钾、液溴、甲酸钠,均为分析纯。
BSA224S-CW电子天平(精确度0.0001 g);JJ-1精密增力电动搅拌器;电子调温专用炉;78-1磁力加热搅拌器;PB-10型酸度计。
1.2 实验方法
1.2.1 海带浸泡液的制备
采用浸提法提取海带中的碘[9]。取100 g干海带,加入1.5 L的蒸馏水浸泡2 h。加碱凝聚沉淀后,过滤除杂,制得海带浸泡水。
1.2.2 氧化剂HIO3的制备
取一定体积的海带浸泡液,加入盐酸,调节pH。在磁力搅拌下,加入微量亚硝酸钠,然后加入几滴淀粉指示剂,溶液变蓝,按一定的H2O2与I-物质的量比加入双氧水。秒表计时,当蓝色消退时,记录时间。此时溶液中的I-被氧化成为。
1.2.3 海带浸泡液中的碘的提取
在磁力搅拌下,向海带浸泡液中缓慢滴加盐酸,调节pH。将已酸化的浸泡液与氧化剂按一定的体积比(即I-与物质的量比)混合,反应一定时间。用环己烷按 V(有机相)︰V(水相)=1∶5 萃取 3 min,萃取 3 次[10]。 根据水产行业标准 SC/T 3010—2001《海带碘含量的测定》中溴化氧化法测定溶液中剩余的碘含量。海带浸泡液中碘的氧化率X按下式计算。
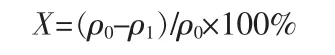
式中:ρ0为海带浸泡液中的碘含量,mg/L;ρ1为海带浸泡液中经过环己烷萃取后剩余的碘含量,mg/L。
2 结果与讨论
2.1 氧化剂HIO3的制备
双氧水具有较强的氧化能力,可以达到过氧化效果,而且环保无污染。但单一使用H2O2作I-的氧化剂不能取得好的氧化效果[11-14]。实验中发现,在加入微量NaNO2的情况下,H2O2能够在短时间内将I-氧化成可以达到生产要求。
2.1.1 NaNO2的用量对氧化反应的影响
取100 mL含碘量为498 mg/kg的海带浸泡液置于碘量瓶中,用盐酸调节pH为2。磁力搅拌下,加入50 μL不同浓度的NaNO2溶液,搅拌2 min,滴加淀粉指示剂,按H2O2与I-物质的量比为3.5∶1加入双氧水。塞上塞子,微量水液封。秒表计时,观察并记录蓝色消失的时间。采用硫代硫酸钠法测定含量(氧化的I-占总I-的质量分数)。结果如表1所示。由表1可以看出,加入微量的NaNO2对氧化反应有很大影响,极大地缩短了反应时间。随着NaNO2浓度的升高,双氧水将I-过氧化为的时间越来越短,而含量变化不大。
在实验反应体系中主要发生以下发应:
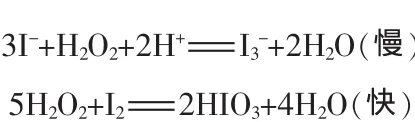
加入NaNO2后有反应+2I-+4H+=2NO↑+I2+2H2O 发生,生成了 I2。 H2O2氧化 I-生成是含氧酸根对反应具有催化作用,故氧化反应速度加快,缩短了反应时间。

表1 NaNO2用量对氧化反应的影响
2.1.2 H2O2与I-物质的量比对氧化反应的影响
取100 mL含碘量为498 mg/kg的海带浸泡液置于锥形瓶中,用盐酸调节pH为2。磁力搅拌下,加入50 μL 8%NaNO2溶液,滴加淀粉指示剂,按不同的H2O2与I-物质的量比加入30%H2O2。秒表计时,观察并记录蓝色消失的时间,然后测定含量,结果如表2所示。由表2可以看出,随着双氧水用量的增加,将I-过氧化为所需要的时间越来越少。说明增加双氧水的用量,增大了反应物浓度,反应速度加快,反应时间减少。
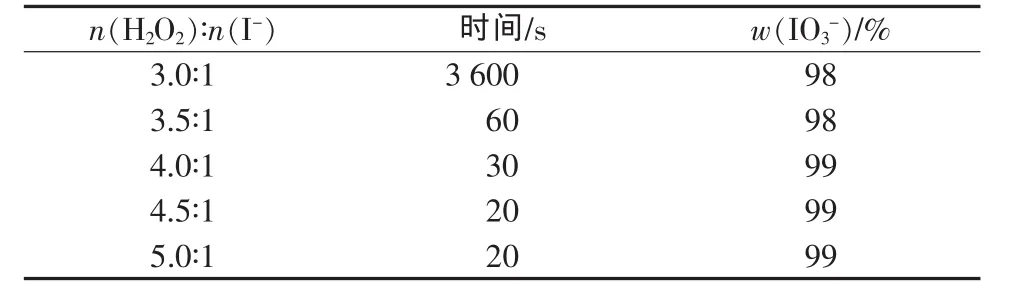
表2 H2O2与I-物质的量比对氧化反应的影响
2.2 海带浸泡液中碘的氧化工艺研究
海带浸泡液含碘量为498 mg/kg,在pH为2.0、反应时间为30 min的条件下,研究I-与物质的量比对I-氧化率的影响,结果见图1。由图1可以看出,I-的氧化率随着I-与物质的量比的增大先升高后降低。当I-与物质的量比为5∶1时,氧化率达到最大,为94.96%。氧化剂过少或者过多,都会使I-氧化率偏低。氧化剂过少时,I-没有被氧化完全;氧化剂过多时,I-被过氧化生成其他价态的碘化物,浪费资源。
海带浸泡液含碘量为498 mg/kg,在反应时间为30 min、I-与物质的量比为 5∶1 的条件下,考察体系的pH对I-氧化率的影响,结果见图2。由图2可以看出,随着溶液pH从3.3逐渐减小到1.5,I-的氧化率逐渐增大,在pH为1.5时,氧化率达到最高。因为在H+大量存在的情况下氧化性能得到相应提高。在弱酸条件下,I-只是部分被氧化,而在强酸性条件下,溶液中存在大量的H+使反应平衡向正反应方向移动,I-的氧化率升高。由图2可以看出,在pH为1.5或2.0时,I-的氧化率相差不大,从经济与环保角度考虑,确定氧化反应最佳pH为2.0。
海带浸泡液含碘量为498 mg/kg,在pH为2.0、I-与物质的量比为5∶1的条件下,研究反应时间对I-氧化率的影响,结果见图3。由图3可以看出,I-氧化率随反应时间的增加逐渐升高。反应时间为10~30 min时,I-氧化率升高较快;反应时间为30~50 min时,I-氧化率升高较为平缓。随着反应的进行,产物浓度逐渐增大,底物浓度逐渐减小,反应趋于平衡,最佳反应时间为30min。
综上所述,海带浸泡液中碘的氧化工艺条件为pH为 2.0、I-与物质的量比为5∶1、 反应时间为30 min时,碘的氧化率最大。

图1 I-与IO3-物质的量比对I-氧化率的影响

图2 pH对I-氧化率的影响
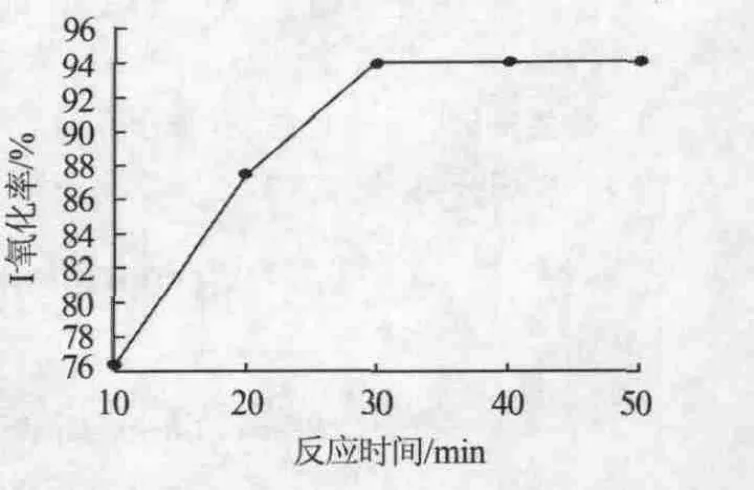
图3 反应时间对I-氧化率的影响
3 结论
首先采用NaNO2-H2O2混合氧化剂将海带浸泡液中的I-氧化为,并以其为氧化剂进一步氧化海带浸泡液中的I-生成单质碘,达到回收碘的目的。将海带浸泡液中的I-氧化为最佳工艺条件为:100 mL的含碘量为498 mg/kg的海带浸泡液需要加入混合氧化剂的量分别为50 μL 8%NaNO2溶液、150 μL 30%H2O2(H2O2与 I-物质的量比为 3.5∶1)。 氧化海带浸泡液中I-的最佳工艺条件为:pH为2、I-与物质的量比为5∶1、反应时间为30 min,此时碘的氧化率为94.96%。该工艺改变了传统工艺中依靠精确调节氧化剂用量才能达到理想氧化率的情况。采用混合氧化剂进行反应,I-氧化率高,绿色环保。
[1]王景刚,冯丽娟,相湛昌,等.碘提取方法的研究进展[J].无机盐工业,2008,40(11):11-14.
[2]高书宝,张雨山,张慧峰,等.提碘技术研究进展[J].化学工业与工程,2010,27(2):122-127.
[3]Shen Bo,Makley D M,Johnston J N.Umpolung reactivity in amide and peptide synthesis[J].Nature,2010,465(7301):1027-1032.
[4]盖利刚,段秀全,姜海辉,等.电位滴定-双氧水氧化法从海带中提取碘[J].无机盐工业,2011,43(1):52-55.
[5]盖利刚,姜海辉,马万勇.从海带中提取碘的实验教学设计与改革[J].大学化学,2011(5):71-73.
[6]朱兆友,高秀,牛志芳,等.过氧化氢氧化-活性炭吸附法回收碘的研究[J].化学与生物工程,2011,28(10):60-62.
[7]苗钧魁,冷凯良,许洋,等.活性炭吸附法回收海带化工提碘废水中的碘[J].无机盐工业,2010,42(10):54-55.
[8]孙克萍,刘福源,先桁,等.黄磷生产废水中碘的提取实验研究与机理探讨[J].贵州工业大学学报:自然科学版,2007(6):94-97,102.
[9]严爱兰.海带活性碘提取的研究[J].杭州农业与科技,2009(2):26-28.
[10]代允,周婷婷,毕琴,等.溶剂萃取法回收4-溴-2-氟碘苯萃余废水中的碘[J].环境科学与技术,2012(4):165-169.
[11]陈肖虎,薛安,杨善志,等.过氧化氢-硫酸氧化碘离子反应动力学研究[J].过程工程学报,2009(S1):181-184.
[12]Karunakaran C,Muthukumaran B.Zirconium catalysis in perborate oxidation of iodide[J].React.Kinet.Catal.Lett.,1997,60(2):387-394.
[13]Ogata Y,Tanaka K.Kinetics of the oxidation of diphenyl sulfide with hydrogen peroxide catalyzed by sodium metavanadate[J].Can.J.Chem.,1982,60(7):848-852.
[14]Lawrance G A,Ward C B.Kinetics of oxidation of manganese(Ⅱ)by peroxomonosulfuric acid in aqueous acidic solution[J].Transition Met.Chem.,1985,10(7):258-261.

