超声波降解溴系阻燃剂六溴环十二烷
叶 威,何 祥,柳 龙,王 浩,韩 军
(武汉科技大学化学工程与技术学院,湖北 武汉430081)
六溴环十二烷(HBCD)是一种添加型溴系阻燃剂,商用HBCD主要由3种同分异构体(图1),即α-、β-和γ-HBCD组成,含量分别为10%~13%、1%~12%和75%~89%,广泛应用于各种纺织品、建筑材料以及电子产品中。据统计,HBCD的全球生产量超过20 000t·a-1[1],在生产、加工、使用和后处理过程中,HBCD会被释放,残存于环境和生物体中[2],有可能导致人体基因重组,并进一步引起一系列疾病[3-5]。2008年,欧盟委员会将HBCD划为具有持久性、生物蓄积性及毒性的一类化合物[6]。2013年5月,《关于持久性有机污染物的斯德哥尔摩公约》将HBCD添加到了附件A(Annex A)中:在全球范围内禁止使用HBCD[7]。因此,研究并发展有效的降解方式来降低HBCD在环境中的浓度从而减小甚至消除其潜在威胁是很有必要的。目前,国内外有关HBCD降解的研究报道很少,而且主要集中在微生物降解[8-9],但降解效果不够理想。

图1 HBCD 3种主要同分异构体的结构Fig.1 Structure of three major HBCD isomers
超声波技术作为一种高效、清洁的新型水处理技术,近20年来引起了国内外学者的广泛关注,有效应用于各种有机污染物的降解,包括杀虫剂[10]、染料[11]、氯代烃类[12]等。超声波处理有机污染废水的原理源于声空化,当超声波照射到水溶液中时,溶液中会产生大量的微小气泡,这些气泡在超声波周期性的压缩/稀疏作用下经历生长、振动、收缩,最后崩溃,产生大量的热量和氧化性极强的自由基(·OH和H·)[13],而有机污染物则主要通过直接热解或者与自由基反应两种途径得到降解。溶液中的溶解气体能影响空化效应程度或自由基的反应历程,从而对降解产生重要影响[14]。研究[15-17]表明,由于氩气的比热容最大,在空化泡崩溃时产生的温度最高,超声波反应最激烈,所以向溶液中通入氩气,对有机物的降解效果最好。事实上,在氩气气氛、不添加其它氧化剂的条件下,超声波就能够有效地降解污染物,使有机污染物矿物质化而不产生污泥或其它新污染物。
作者采用超声波降解HBCD,研究了氩气气氛下超声波对 HBCD 3种主要同分异构体α-、β-和γ-HBCD的降解情况,并进行了动力学分析,对降解过程中溶液pH值及H2O2浓度的变化进行了研究。
1 实验
1.1 试剂与仪器
HBCD粉末,分析纯,Japan Urase Corp.;α-、β-和γ-HBCD标准溶液,纯度均为99.9%,USA Wellington Laboratories;其它试剂均为分析纯;实验用水为超纯水。
1100Series型高效液相色谱,美国Agilent Technologies Corp.;Mightysil RP18GP Aqua(4.6mm×250 mm)分离柱,日本 Kanto Chemical Co.,Inc.;BF-4型流动注射分析仪,日本Oji Scientific Iustruments Co.,Inc.;便携式pH计,日本 Horiba Co.,Inc.。
1.2 方法
实验装置主要由超声波供给系统、反应系统和冷凝系统构成,如图2所示。

图2 实验装置示意图Fig.2 Schematic diagram of experimental apparatus
实验过程:温度为25℃,HBCD初始浓度为0.05 mg·L-1,反应液体积为250mL。超声波照射前,向反应液中通入氩气(200mL·min-1)40min,在超声波(404kHz,60W)照射过程中,始终连续通入氩气(100mL·min-1),并以400r·min-1的速度搅拌。降解结束后,用二氯甲烷萃取,然后用氮气洗吹至绝干,最后将溶质溶解于2.5mL体积分数为85%的甲醇溶液中,并用0.45μm的滤膜过滤,用作HPLC检测分析。
在相同的实验条件下,分别测定超声波照射HBCD水溶液和超纯水过程中的溶液pH值和H2O2浓度。
1.3 分析测试
采用高效液相色谱分析检测HBCD,色谱条件为:Mightysil RP18GP Aqua分离柱;柱温40 ℃;流速1mL·min-1;流动相为15%70mmol·L-1醋酸铵溶液-85%甲醇;波长220nm。
采用流动注射分析仪测定H2O2的浓度。实验条件为:以0.1mol·L-1磷酸二氢钠+0.05mol·L-1氯化钾+0.001mol·L-1叠氮化钠为缓冲溶液;流速1.2mL·min-1;温度37℃。
采用便携式pH计测定溶液的pH值。
2 结果与讨论
本研究所得的结果,均为2次平行实验的平均值,且标准方差均小于2%。
2.1 HPLC分析
α-、β-和γ-HBCD在色谱条件下洗脱出峰的时间分别为12.9min、15.5min和17.0min。α-、β-和γ-HBCD的浓度采用标准曲线的方法来测定。实验发现,α-、β-和γ-HBCD 的标准曲线的相关系数均大于0.9999。
2.2 降解过程中,溶液pH值和H2O2浓度的变化
超声波照射HBCD水溶液和超纯水过程中,pH值和H2O2浓度的变化情况如图3所示。

图3 降解过程中,pH值(a)和H2O2浓度(b)的变化Fig.3 Change of pH value(a)and H2O2concentration(b)during degradation process
由图3可看出:随着降解的进行,溶液的pH值逐渐减小,说明在降解过程中不断有H+生成;同时溶液中H2O2浓度逐渐增大,正好证明了这一点;超声波降解HBCD水溶液时,溶液中H2O2浓度较超声波照射超纯水时要低,这是因为HBCD的降解消耗了一些自由基·OH,而H2O2主要来源于·OH自由基的相互反应(·OH+·→ OH H2O2)。
2.3 氩气气氛下,α-、β-和γ-HBCD的降解

图4 氩气气氛下,α-、β-和γ-HBCD的降解Fig.4 Degradation ofα-,β-andγ-HBCD in the presence of argon atmosphere
由图4可看出:在氩气气氛下,α-、β-和γ-HBCD均得到了有效降解。其中,α-和β-HBCD比γ-HBCD降解更快,降解效率更高,尤其是α-HBCD在超声波照射1h后,已经完全降解;而超声波照射6h后,β-和γ-HBCD的降解率才分别达到98.0%和60.0%。这可能与它们在水中的溶解度不同有关,α-、β-和γ-HBCD在水中的溶解度分别为48.8μg·L-1、14.7μg·L-1和2.1μg·L-1,溶解度越大,与超声波反应生成的强氧化性自由基(如·OH)碰撞并发生反应的几率越大,被氧化降解的可能性就越大,降解率相应越高。
由图4还可看出,α-、β-和γ-HBCD均在开始阶段降解很快,随着降解过程的进行,降解速率越来越慢,尤其是γ-HBCD,在超声波照射2h、4h、6h时,降解率分别为55.5%、57.9%和60.0%。这可能是因为,在HBCD降解的过程中,会产生大量的中间产物,随着降解时间的延长,中间产物的浓度会越来越大,而超声波反应过程中产生的氧化性自由基和热量等,不仅会降解 HBCD,同时也会降解中间产物,从而导致HBCD的降解速率越来越慢。
2.4 降解速率常数
根据HBCD超声波降解情况,假设HBCD降解的初始速率常数服从假一级反应动力学规律。首先,对于HBCD的降解,可以表示为HBCD与·OH反应而得到降解,如下式所示:

相应地,HBCD降解过程的反应速率为:
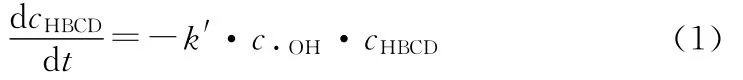
由于·OH作为活泼的中间产物,反应能力极强,且其浓度很低,因此在超声波降解过程中,可近似认为其处于稳态,浓度不发生变化,即:

因此,可以得到

进一步可以表示为
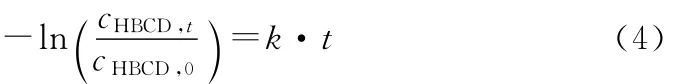

图5 )与t之间的关系Fig.5 Relationship betweenand t
由图5还可看出,α-HBCD的降解速率常数最大(Kα-HBCD=0.0877±0.0011min-1,R2=0.980),分别为β-HBCD 的 3.1 倍 (Kβ-HBCD=0.0282±0.0006 min-1,R2=0.990)、γ-HBCD 的 7.9 倍 (Kγ-HBCD=0.0111±0.0008min-1,R2=0.986)。这也可以解释为:α-HBCD在水中的溶解度最大,更容易与·OH发生反应而被降解,因此降解速率常数也最大。
2.5 HBCD降解机理
超声波降解有机污染物主要通过两条途径[18]:一是有机污染物以气态的形式进入到空化泡内部,在高温高压条件下直接热解;二是在溶液中与水热解产生的强氧化性自由基(主要为·OH)发生反应而得以降解。HBCD的挥发性极低(21℃时HBCD的饱和蒸汽压为6.27×10-5Pa),因此,认为 HBCD进入空化泡内被直接热解的可能性很小。此外,HBCD在降解过程中,明显消耗了·OH,所以,初步推测,HBCD降解的主要途径是在溶液中与·OH发生反应。
3 结论
超声波能够有效降解HBCD。在氩气气氛下,超声波照射1h后,α-HBCD 被完全降解;β-和γ-HBCD在超声波照射6h后降解率分别达98.0%和60.0%;α-、β-和γ-HBCD的降解在最初0.5h内服从假一级反应动力学规律,降解速率常数大小依次为α-HBCD>β-HBCD>γ-HBCD。初步推测,HBCD降解的主要途径是在溶液中与·OH发生反应。
[1]Bromine Science and Environmental Forum (BSEF),Estimated Market Demand for Brominated Flame Retardants in 2003.http://www.bsef.com/bromine/ourindustry/(last accessed June,2006).
[2]COVACI A,GERECKE A C,LAW R J,et al.Hexabromocyclododecanes(HBCDs)in the environment and humans:A review[J].Environmental Science and Technology,2006,40(12):3679-3688.
[3]张晓岭,杨方星.三对六溴环十二烷手性异构体对人体肝细胞(HepG2)的毒性评价[C]//第四届全国环境化学学术大会论文集.北京,2007:299.
[4]SAEGUSA Y,FUJIMOTO H,WOO G H,et al.Developmental toxicity of brominated flame retardants,tetrabromobisphenol A and 1,2,5,6,9,10-hexabromocyclododecane in rat offspring after matermal exposure from mid-gestation through lactation[J].Reproductive Toxicology,2009,28(4):456-467.
[5]王晓蓉,苏燕,罗义.HBCD诱导鲫鱼ROS和HSP70的产生及分子致毒机制[C]//第二届持久性有机污染物全国学术研讨会论集.北京,2007:111.
[6]European Commission,in E.C.Agency(Ed.)ED/67/2008,2008.
[7]Conference of the Parties to the Stockholm Convention,on Persistent Organic Pollutants Sixth meeting,Geneva.UNEP/POPS/COP.6/33,2013.
[8]YAMADA T,TAKAHAMA Y,YAMADA Y.Isolation of Pseudomonas sp.strain HB01which degrades the persistent brominated flame retardant gamma-hexabromocyclododecane[J].Bioscience,Biotechnology,and Biochemistry,2009,73(7):1674-1678.
[9]DAVIS J W,GONSIOR S,MARTY G,et al.The transformation of hexabromocyclododecane in aerobic and anaerobic soils and aquatic sediments[J].Water Research,2005,39(6):1075-1084.
[10]傅敏,丁培道,蒋永生,等.超声波降解有机磷农药乐果的实验研究[J].三峡环境与生态,2003,25(12):27-29.
[11]周烈,刘邵刚,周泽广.超声波降解染料废水的实验研究[J].广西民族大学学报(自然科学版),2006,12(4):96-99,121.
[12]LIANG J,KOMAROV S,HAYASHI N,et al.Improvement in sonochemical degradation of 4-chlorophenol by combined use of Fenton-like reagents[J].Ultrasonics Sonochemistry,2007,14(2):201-207.
[13]吕小佳,林逢凯,胥峥.超声波降解水溶液中对二氯苯[J].环境污染与防治,2010,32(6):55-59.
[14]马军,赵雷.超声波降解水中有机物的影响因素[J].黑龙江大学自然科学学报,2005,22(2):141-149,153.
[15]张光明,张锡辉,吴敏生.超声波降解溴苯:操作参数与环境因素的影响[J].应用声学,2005,24(1):44-47.
[16]孙红杰,赵明举,张志群.超声降解十二烷基苯磺酸钠的实验研究[J].环境科学学报,2003,23(3):386-390.
[17]王宏青,聂长明,徐伟昌,等.灭多威的超声降解研究[J].应用声学,2001,20(2):35-37.
[18]KOJIMA Y,FUJITA T,ONA E P.Effects of dissolved gas species on ultrasonic degradation of (4-chloro-2-methylphenoxy)acetic acid (MCPA)in aqueous solution[J].Ultrasonics Sonochemistry,2005,12(5):359-365.

