甲烷水合物在冰浆中生成特性的研究
范兴龙,谢应明,谢振兴,杨 迟
(上海理工大学 制冷技术研究所,上海 200093)
甲烷水合物在冰浆中生成特性的研究
范兴龙,谢应明,谢振兴,杨 迟
(上海理工大学 制冷技术研究所,上海 200093)
在定容条件下进行甲烷水合物在冰浆中和纯水中的生成实验。在3~5 MPa,273.15~277.15 K,500~1 000 r/min的条件下考察初始压力、水浴温度和搅拌转速对甲烷水合物生成过程的影响。实验结果表明,甲烷水合物在冰浆中的生成速率比在纯水中的快;初始压力为3 MPa、搅拌转速为1 000 r/min时,甲烷水合物在冰浆中的生成时间为42 min,生成速率为47.7 mL/min;甲烷水合物在纯水中的生成时间为90 min,生成速率为22.3 mL/min;甲烷水合物在冰浆中具有更好的生成特性,具有工业化应用的潜力。
甲烷水合物; 冰浆;定容实验
气体水合物是水与甲烷、乙烷、二氧化碳、氮气或硫化氢等小分子气体形成的非化学计量性的笼形晶体物质。据统计全球以水合物形式存在的天然气量约为2.1×1016m3[1-2],是已探明常规天然气储量的几十倍。天然气水合物的含气率高,储能密度大,1体积天然气水合物分解可得到180体积的天然气。所以水合物储运天然气技术被作为一种新型储运天然气技术得到了广泛的研究。Gudmundsson等[3]证实,天然气水合物的储运成本比液化天然气的低24%。但到目前为止,天然气水合物并没有实现产业化,原因在于天然气水合物的生成速率慢、储气密度低且生成过程的诱导时间较长。
近年来,人们为促进天然气水合物的快速生成做了大量研究,Park等[4-7]研究了碳纳米管对甲烷水合物生成的影响; Ganji等[8-12]研究了多种阴阳离子表面活性剂对甲烷水合物生成特性的影响。目前,针对促进天然气水合物生成方面的研究大都集中在气-液或气-固两相的反应,针对气-液-固三相反应的研究较少。
黄犊子等[13]研究了水的形态对甲烷水合物生成的影响,发现冰粉比水更容易与甲烷反应生成甲烷水合物;刘芙蓉等[14]曾研究过冰-水-气三相状态下甲烷水合物的生成过程,但只简单描述了各相关参数的依赖关系,并没有具体的数据。冰粉为固体,且反应前需要研磨,不具备较好的流动性,用于工业生产天然气水合物的可能性不大。冰浆作为一种“可泵冰”,流动性好,已经作为蓄冷介质得到广泛的研究和应用,适合用于流程工业,具有用于天然气水合物工业生产的潜力。
本工作在实验装置中进行甲烷水合物在冰浆中生成特性的研究,考察初始压力、水浴温度和搅拌转速对甲烷水合物生成过程的影响, 并与甲烷在纯水中的生成过程进行了对比。
1 实验部分
1.1 实验装置
水合物储能实验装置见图1。实验系统主要包括高压反应釜、供气、供水、温度控制、压力控制、数据采集等系统。高压反应釜体为316 L不锈钢材质,设计压力为10 MPa,有效容积为500 mL;釜体前后装有观察实验现象的钢化玻璃视窗;釜体上端盖装有磁力搅拌器,电机调速范围为0~1 050 r/min;真空泵为旋片式,极限真空度为6×10-2Pa;恒温水浴的控温精度为±0.1 K,水浴槽内的工作介质为乙二醇水溶液,可控制的温度范围为-15~50 ℃;数据采集系统主要采集反应釜内气体压力和气液相温度,压力传感器的量程为20 MPa,精度为±0.25%,温度传感器为Pt100铂电阻,测量精度为±0.05 ℃。

图1 水合物储能实验装置Fig.1 Schematic diagram of gas hydrate energy storage apparatus.
甲烷:99.99%(φ),上海伟创标准气体有限公司;水:去离子水,实验室采用Hitech-Sciencetool系列超纯水系统制得。
1.2 实验方法
实验目的是为了研究甲烷水合物在冰浆中的生成特性,考察不同的搅拌转速、初始压力和水浴温度条件下水合物的生成速率。
分别采用冰浆和纯水与甲烷反应,进行生成甲烷水合物的实验。实验步骤如下:1)用去离子水将反应釜反复冲洗3遍,向反应釜中注入一定体积的去离子水,开启真空泵30 min,将反应釜内抽真空;2)开启恒温水浴(温度设置为270.65 K),待反应釜内温度恒定之后开启磁力搅拌器,并将转速调到最大,这时反应釜内会生成冰浆,且液相温度随之升高,待液相温度升到273.15 K时,停止搅拌,并将恒温水浴调至所要设定的温度;3)向反应釜内充入甲烷气体,待恒温水浴温度达到所设定的温度且反应釜压力稳定之后,开启搅拌器,并开始采集实验数据;4)当反应釜压力停止下降时,表明水合物的生成过程结束,关闭实验台,保存数据。
对于纯水与甲烷反应,只是步骤2)中无需生成冰浆,直接将液相温度调至所需温度即可,其他步骤同上。
1.3 数据处理
t时刻甲烷气体消耗量(Δn)由式(1)计算。

式中,VSV为反应釜内甲烷气体所占的体积,L;p为反应釜内的压力,MPa;T为反应釜内的温度,K;R为气体常数,J/(mol·K);z为甲烷的压缩因子,由式(2)计算。


水合物的储气密度(ρ)由式(4)计算。

式中,V为反应前水的体积,L。
5 min内的平均甲烷气体消耗速率(V5min)可由式(5)计算。

式中,Δn5为反应开始后5 min内的甲烷气体消耗量,mol。
2 结果与讨论
2.1 甲烷水合物生成实验结果
甲烷水合物生成实验结果见表1。
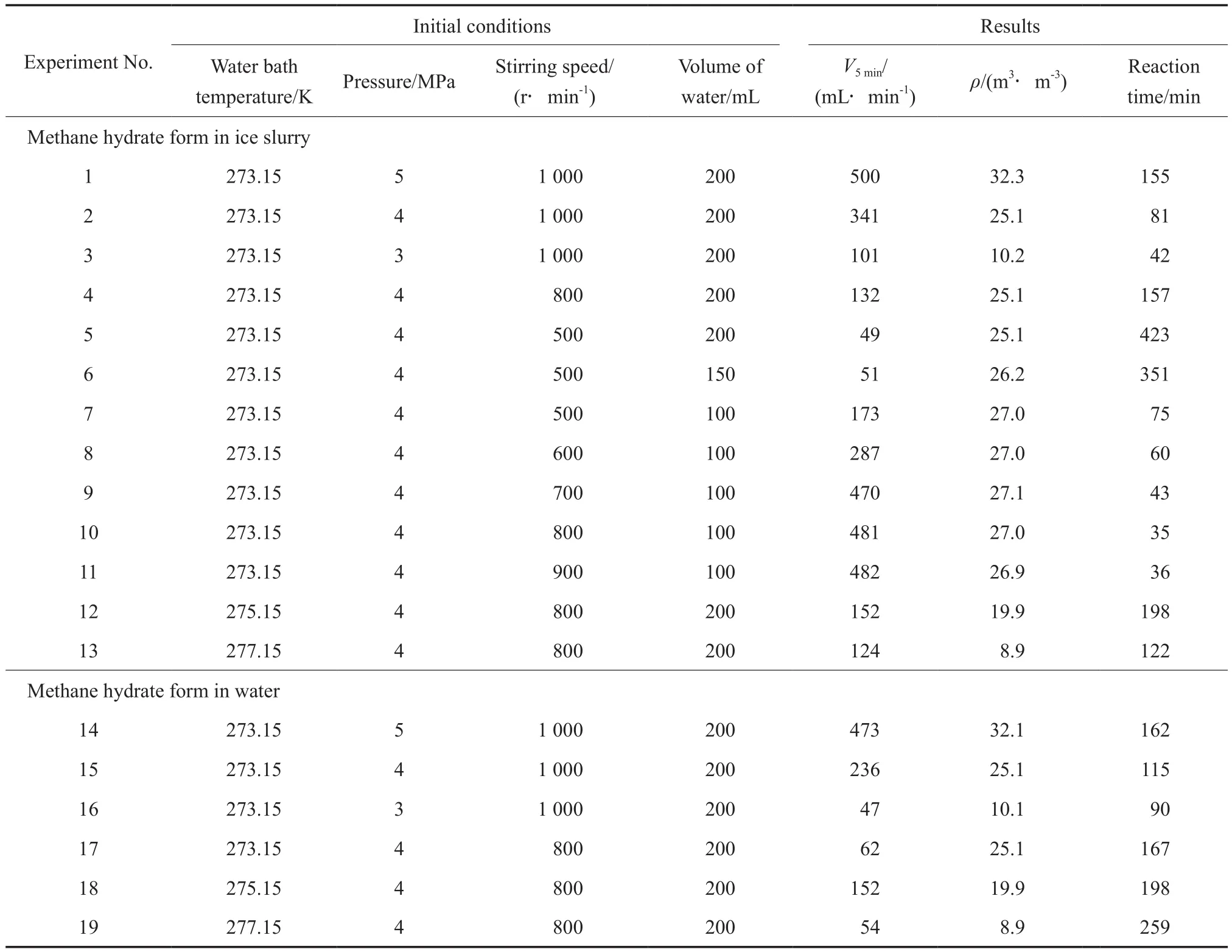
表1 甲烷水合物生成实验结果Table 1 The experimental results of methane hydrate formation
2.2 甲烷水合物在冰浆中的生成特性
通过反应釜的玻璃视窗观察到,甲烷水合物在冰浆中和在纯水中的生成现象有所不同。在冰浆中,开启搅拌器后,反应釜内部的透光率迅速下降,快速变为黑色之后透光率又逐渐增大,最终反应釜内呈现乳白色(见图2);而在纯水中,开启搅拌器后,反应釜内部的透光率变化速度较慢,随反应的进行反应釜内部逐渐变浑浊,最终呈现乳白色(见图3)。
反应釜内液相温度的变化曲线见图4。由图4可见,甲烷水合物在冰浆中生成时,最大温升为0.9 K,而在水中的最大温度波动为3.2 K,甲烷水合物在冰浆中生成时的温度波动比在水中要小很多。这是因为水合物生成为放热反应,在冰浆中甲烷生成水合物时其生成过程中伴随着冰的融解,一部分甲烷水合物生成所释放的热量被融冰所吸收,所以在冰浆中甲烷水合物生成反应时的温升要小于在水中的温升。

图2 在冰浆中甲烷水合物生成过程的照片Fig.2 Images of the methane hydrate formation process in ice slurry.

图3 在纯水中甲烷水合物生成过程的照片Fig.3 Images of the methane hydrate formation process in water.

图4 反应釜内液相温度的变化曲线Fig.4 Curves of liquid phase temperature in the reactor.
2.3 初始压力的影响
初始压力对反应釜内压力的影响见图5。由图5可见,随反应的进行,釜内压力逐渐降低,最后趋于恒定;在冰浆中压力降低得比水中快,表明甲烷水合物在冰浆中的生成速率比在水中的快。这可能是因为:1)冰以及冰融化的水中存在与水合物空笼相近的水分子结构[15-16],与纯水相比,更易与甲烷生成水合物;2)温度是影响甲烷水合物生成速率的因素,水合物生成时放出的反应热正好被用作冰融化时的融解热,使甲烷水合物在冰浆中生成时温升较小,所以生成速率较快。
由图5还可见,初始压力为3 MPa时,甲烷水合物在冰浆中的生成速率明显快于在水中的生成速率;当初始压力为5 MPa时,甲烷水合物在冰浆中的生成速率优势几乎消失。当初始压力为3 MPa、搅拌转速为1 000 r/min时,甲烷水合物在冰浆中和在水中生成所需的时间分别为42,90 min(见表1),甲烷水合物平均生成速率分别为47.7,22.3 mL/min,但甲烷水合物生成速率在冰浆中和在水中的差异随初始压力的升高越来越不明显。这可能是因为水合物的生成速率受压力的影响,随初始压力的升高,冰浆对水合物生成的影响逐渐减弱。因此,水中存在冰可以促进甲烷水合物的生成,但促进效果受初始压力的制约,初始压力越低,促进效果越明显;实验还发现水中冰的存在与否对最终储气密度并没有影响。
从表1还可看出,初始压力对甲烷水合物在冰浆中生成的影响与在纯水中类似,初始压力越大,甲烷水合物的生成速率越快,且最终储气密度越大。
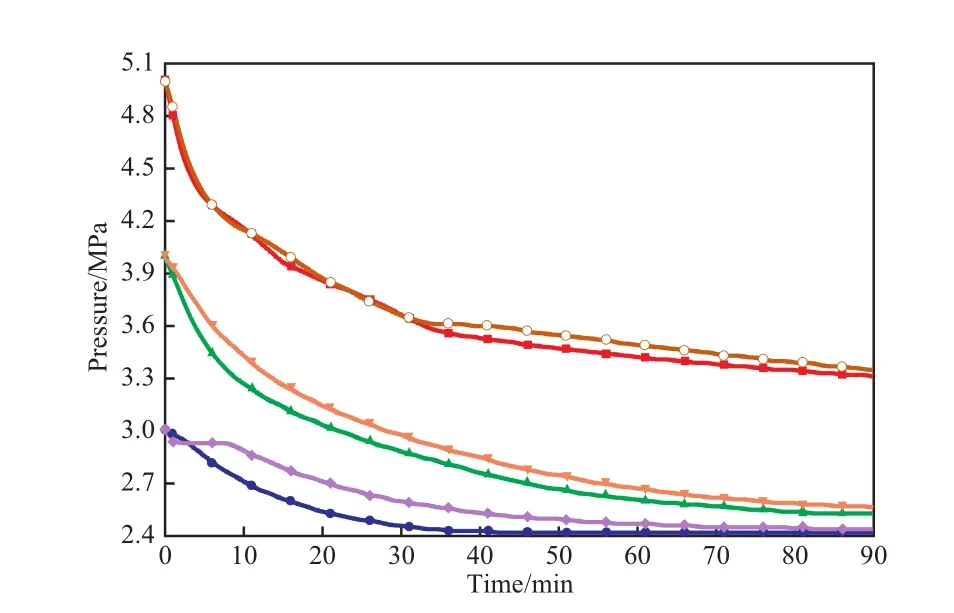
图5 初始压力对反应釜内压力的影响Fig.5 Effects of initial pressure on pressure in the reactor.
2.4 水浴温度的影响
水浴温度对反应釜内压力的影响见图6。由图6可见,在水中,当水浴温度为275.15,277.15 K时,甲烷水合物的生成过程存在明显的诱导时间,水浴温度为275.15 K所对应的诱导时间为12 min,水浴温度为277.15 K时所对应的诱导时间为48 min;在冰浆中,甲烷水合物的生成过程不存在明显的诱导时间,在任何水浴温度下甲烷水合物在冰浆中的生成速率均比在水中的生成速率快。这可能是因为冰以及冰融化的水中存在与水合物空笼相近的水分子结构,与纯水相比更易与甲烷生成水合物,从而缩短诱导时间。
水浴温度对甲烷水合物的储气密度有明显的影响。在冰浆中,水浴温度为273.15,275.15,277.15 K所对应的储气密度分别为25.1,19.9,8.9 m3/m3。这是因为温度是影响甲烷水合物相平衡的因素之一,温度越高,越不利于甲烷水合物的生成。在冰浆或水中,相同的水浴温度下甲烷水合物最终的储气密度并没有明显差异(见表1)。

图6 水浴温度对反应釜内压力的影响Fig.6 Effects of water bath temperature on pressure in the reactor.
2.5 扰动的影响
搅拌转速对反应釜内压力的影响见图7。由图7可见,搅拌转速越大,压力降低得越快,即甲烷水合物的生成速率越快。搅拌转速对初始反应速率的影响尤其明显,搅拌转速分别为1 000,800,500 r/min时,对应的V5min分别为0.341,0.132,0.049 L/min。这是因为甲烷在冰浆中的传质速率是影响甲烷水合物生成的因素,搅拌可以加快传质速率。因此,搅拌转速越大,传质速率越快,甲烷水合物的生成速率越快。

图7 搅拌转速对反应釜内压力的影响Fig.7 Effects of stirring speed on pressure in the reactor.
当搅拌转速为500 r/min时,甲烷水合物的生成速率先加快后减小,即水合物生成速率的最大值是随着反应的进行而出现的;而搅拌转速为1 000,800 r/min时此现象并不明显。这是因为搅拌转速越大,在气液界面形成的扰动越剧烈,甲烷在冰浆中的传质速率越大,搅拌转速为800,1 000 r/min时,甲烷在冰浆内可以瞬间达到最大过饱和度,而搅拌转速为500 r/min时达到最大过饱和度需要一定的时间。实验还发现,搅拌转速仅影响甲烷水合物的生成速率,对甲烷水合物储气密度没有影响。
水合物的生长为界面生长,气液界面扰动的剧烈程度决定水合物生成速率的快慢,而搅拌转速并不是决定气液界面扰动程度的唯一因素。在同一搅拌转速下,搅拌器叶片距离气液界面越近,扰动程度越剧烈。
水的体积对反应釜内压力的影响见图8。由图8可见,水的体积越小,压力降低得越快。当水的体积为100 mL时V5min为173 mL/min,而在初始压力为4 MPa、搅拌转速为800 r/min条件下,当水的体积为200 mL时V5min仅为132 mL/min(见表1)。其原因是搅拌器叶片位于反应器底部,水的体积越小,液面与搅拌器叶片的距离越小,叶片产生的扰动更容易传递到气液界面,这样加快了水合物的生成速率。
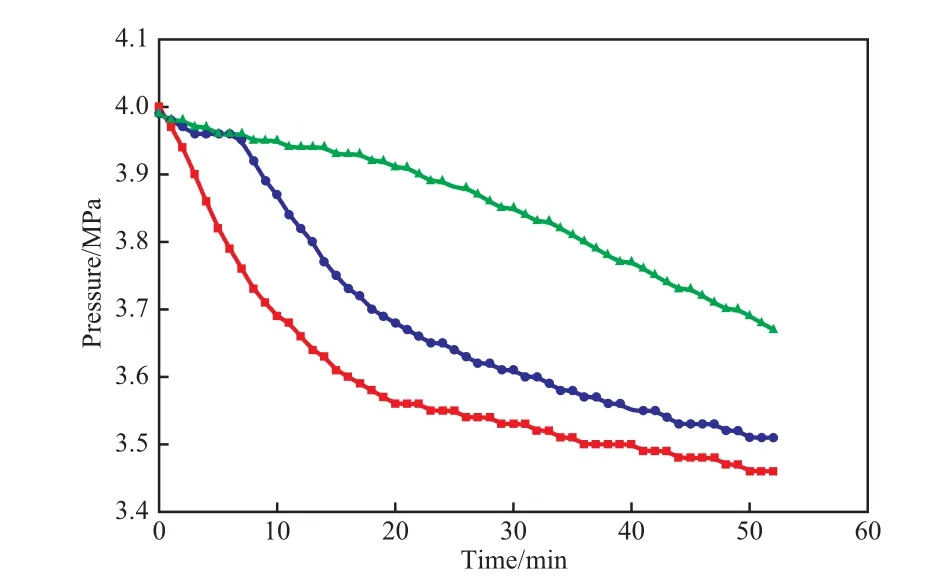
图8 水的体积对反应釜内压力的影响Fig.8 Effects of water volume on pressure in the reactor.
由表1中的第7~11组数据可看出,当水的体积为100 mL时,V5min随搅拌转速的增大而增大,但当搅拌转速达到800 r/min时,再进一步增大搅拌转速,V5min及反应时间并没有明显变化。
综合以上分析可知,与在水中相比,甲烷水合物在冰浆中具有更好的生成特性,具有工业化应用的潜力。
3 结论
1)甲烷水合物在冰浆中的生成速率比在水中的快,初始压力越低越明显。
2)当温度高于273.15 K时,甲烷水合物在纯水中生成时存在明显的诱导时间,而在冰浆中生成时不存在诱导时间。
3)初始压力越高,甲烷水合物在冰浆中的生成速率越快,最终储气密度越大。
4)搅拌转速能影响甲烷水合物的生成速率,影响程度受搅拌器与液面距离的限制,相同搅拌转速下,搅拌器与液面的距离越小,影响程度越大。
5)当搅拌器与液面的距离一定时,存在最佳搅拌转速。当搅拌转速超过最佳值后,再增大搅拌转速,甲烷水合物的生成速率不再加快。
[1] Seol Jiwoong,Lee Huen. Natural Gas Hydrate as a Potential Energy Resource:From Occurrence to Production[J].Korean J Chem Eng,2013,30(4):771 - 786.
[2] Collett T S. Energy Resource Potential of Natural Gas Hydrates[J].AAPG Bulletin,2002,86(11):1971 - 1992.
[3] Gudmundsson J S,Mork M. Stranded Gas to Hydrate for Storage and Transport Stockage ET Transport DU Gas Natural Marginal Souls Formed Hydrate[C]//2001 International Gas Research Conference. Amsterdam,2001:5 - 8.
[4] Park Sung-Seek,An Eoung-Jin,Lee Sang-Baek. Characteristics of Methane Hydrate Formation in Carbon Nano fl uids[J].J Ind Eng Chem,2012,18(1):443 - 448.
[5] Kim Nam-Jin,Park Sung-Seek,Kim Hyung-Taek,et al. A Comparative Study on the Enhanced Formation of Methane Hydrate Using CM-95 and CM-100 MWCNTs[J].Int Commun Heat Mass Transfer,2011,38(1):31 - 36.
[6] Park Sung-Seek,Lee Sang-Baek,Kim Nam-Jin. Effect of Multi-Walled Carbon Nanotubes on Methane Hydrate Formation[J].J Ind Eng Chem,2010,16(4):551 - 555.
[7] 臧小亚,梁德清,吴能友. 碳纳米管-水合物法储甲烷性能研究[J]. 工程热物理学报,2010,31(5):725 - 728.
[8] Ganji H,Manteghian M,Sadaghiani Zadeh K,et al. Effect of Different Surfactants on Methane Hydrate Formation Rate,Stability and Storage Capacity[J].Fuel,2007,86(3):434 - 441.
[9] Okutani Kazunori,Kuwabara Yui,Mori Yasuhiko H. Surfactant Effects on Hydrate Formation in an Unstirred Gas/Liquid System:An Experimental Study Using Methane and Sodium Alkyl Sulfates[J].Chem Eng Sci,2008,63(1):183 - 194.
[10] Kwon Young-Ah,Park Jong-Mok,Jeong Kwang-Eun. Synthesis of Anionic Multichain Type Surfactant and Its Effect on Methane Gas Hydrate Formation[J].J Ind Eng Chem,2011,17(1):120 - 124.
[11] Verrett J,Posteraro D,Servio P. Surfactant Effects on Methane Solubility and Mole Fraction During Hydrate Growth[J].Chem Eng Sci,2012,84:80 - 84.
[12] Jeffry Y,Ling P,Englezos P. Enhanced Growth of Methane-Propane Clathrate Hydrate Crystals with Sodium Dodecyl Sulfate,Sodium Tetradecyl Sulfate,and Sodium Hexadecyl Sulfate Surfactants[J].J Cryst Growth,2010,313(1):68 - 80.
[13] 黄犊子,樊栓狮. 水的形态与甲烷水合物的生成[J]. 天然气工业,2004,24(7):29 - 31.
[14] 刘芙蓉,王胜杰,张文玲,等. 冰-水-气生成天然气水合物的实验研究[J]. 西安交通大学学报,2000,34(12):66 - 69.
[15] Xie Yingming,Guo Kaihua,Liang Deqing,et al. Gas Hydrate Growth Morphology Outside of Horizontal Heat Transfer Tube[J].J Cryst Growth,2005,276(1/2):253 - 264.
[16] 谢应明,郭开华,梁德青,等. 气体水合物垂直换热管外融冰快速成核与静态渗透生长[J]. 中国科学:B,2004,34(5):375 - 381.
(编辑 李治泉)
Study on Formation of Methane Hydrate in Ice Slurry
Fan Xinglong,Xie Yingming,Xie Zhenxing,Yang Chi
(Refrigeration Technology Institute,University of Shanghai for Science and Technology,Shanghai 200093,China)
The formation of methane hydrate in ice slurry and in pure water was studied. The influences of initial pressure,water bath temperature and stirring speed on the formation were investigated in the ranges of 3-5 MPa,273.15-277.15 K and 500-1 000 r/min,respectively. The results showed that the growth rate of the methane hydrate in the ice slurry was faster than that in pure water. Under the conditions of the initial pressure of 3 MPa and the stirring speed of 1 000 r/min,the methane hydrate formation time in the ice slurry was 42 min with the average formation rate of 47.7 mL/min,while the formation time in pure water was 90 min with the average formation rate of 22.3 mL/min.
methane hydrate;ice slurry;constant volume experiment
1000 - 8144(2014)04 - 0372 - 07
TQ 026
A
2013 - 10 - 30;[修改稿日期]2014 - 12 - 30。
范兴龙(1987—),男,山东省临沂市人,硕士生,电话 18817582846,电邮 15020966869@163.com。
国家自然科学基金项目(50806050);上海市教委科研创新项目(14YZ097)。

