纳米微反应器介导化学发光法测定盐酸布比卡因
谭建红, 万邦江, 石文兵, 庞向东*
(1.长江师范学院无机特种功能材料重庆市重点实验室,重庆涪陵408100; 2.长江师范学院化学化工学院,重庆涪陵408100)
盐酸布比卡因是比盐酸利多卡因安全性更高且局部麻醉效能强约4倍的芳酞胺类局部麻醉药,临床应用使用过量时会导致心搏骤停、抽搐、惊厥等严重副作用,因此,对其含量的精确定量测定在临床引用上具有重要的指导意义.中国药典(2010年版)用高氯酸滴定法测定盐酸布比卡因注射液[1],其手续较为繁琐.此外,测定其含量的常用方法有高效液相色谱法(HPLC)法[2-3],但其仪器及试剂价格昂贵,操作复杂.
化学发光具有线性范围宽、灵敏度高、仪器设备简单等特点,近年来已经收到广泛关注[4].反胶束纳米微反应器不但能够增稳、增溶、改善环境的pH值还能提高选择性度和灵敏,故其在化学发光分析中日益受到关注[5].本文利用CH2CI2(二氯甲烷)将在盐酸溶液中质子化的盐酸布比卡因与AuCl4-形成的离子缔合物带入反胶束纳米微反应器中,由于环境的pH改变使得AuCl4-被离解出来,从而氧化微反应器中的鲁米诺并产生化学发光,在一定浓度范围内,盐酸布比卡因的浓度与发光强度成正比,用此法可测定盐酸布比卡因的含量.该方法与常规的高效液相色谱法相比,具有灵敏度更高,线性范围更宽和仪器设备操作简单廉价的优点.
1 实验部分
1.1 仪器与试剂IFFL-DD型流动注射化学发光分析仪(西安瑞迈科技有限公司);八通阀;内径为0.8 mm的聚四氟乙烯管;30 r/min的ND型交流可逆电动蠕动泵.
1.0×10-3mol/L鲁米诺储备液:称取0.177 7 g鲁米诺(Merck公司,德国,分析纯)溶于0.1 mol/L NaOH溶液中,摇匀,避光保存.用pH值为11.5的Na2CO3-NaHCO3(用等体积为0.3 mol/L Na2CO3和25 mmol/L NaHCO3混合即可)将其稀释100倍即可得到1.0×10-3mol/L的鲁米诺储备液.
1.0×10-2μg/mL氯金酸储备液:准确称取1.000 0 g氯金酸(Sigma公司,美国,分析纯)用二次蒸馏水溶解于小烧杯中,转移到100 mL的容量瓶中,定容至刻度即可;CH2CI2-C6H12体积比1∶1混合液:取等体积的2物质进行混合即可.
储备液500 μg/mL盐酸布比卡因制备:准确称取盐酸布比卡因(中国药品生物制品检定所,标准品)0.500 0 g溶于100 mL棕色容量瓶中,用二次蒸馏水定容至刻度即得的储备液;
反胶束纳米微反应器的制备:于25 mL比色管中取1 mL鲁米诺储备液,然后用上述CH2CI2-C6H12混合溶液(含有0.2 mol/L的CTAC)定容,振荡1 min,静置5 min得内含浓度为0.4×10-5mol/L的鲁米诺反胶束纳米微反应器[6-8].其它试剂均为分析纯;水为二次蒸馏水.

1.2 试验方法用IFFM-D型流动注射分析仪设定实验参数,按图1所示流路,CH2CI2将样品带到e点与鲁米诺反胶束纳米微反应器溶液汇合,在反应盘管F处反应产生化学发光.
在10 mL具塞比色管中,分别移取不同体积的盐酸布比卡因标准储备液,在分别加0.5 mL的1.0 mol/L盐酸储备液和0.2 mL 1.0×10-3μg/mL的氯金酸,稀释至刻度得盐酸的最终浓度为50.0 mmol/L,氯金酸的最终质量浓度为20.0 μg/mL,摇匀.然后再各加5 mL的CH2CI2.萃取分液后取下层有机相待测.按图1装好流路,开启蠕动(单管泵速3.6 mL/min),待基线稳定后用光电倍增管记录化学发光信号,以峰高定量.
2 结果与讨论
2.1 R([H2O]/[CTAC])值对发光强度的影响微反应器中水与表面活性剂的摩尔比(R)值是微反应器的一个非常重要的物理化学特性参数,R=[H2O]/[CTAC],即微反应器中水与表面活性剂的物质的量的浓度之比,R值的变化直接影响到微反应器“水池”体积的大小和其它理化性能[6],通过改变[H2O]与[CTAC]比值,可获得最佳的R值.实验结果表明,如固定表面活性剂的浓度,改变水的含量,当R值为11时,发光强度达最大,随后下降;固定水的含量不变,结果发现发光强度与R值的变化关系与前者的变化情况一致.起初,增大R值,发光强度有明显提高,这因为是加大了微反应器的体积,从而增加了溶液中微反应器的表面积,也就是增加了发光试剂相接触的空间(因为化学反应是在微反应器的表面进行的),然而随着R的增加,微反应器的体积不断增大,最终将导致微反应器不稳定.考虑到微反应器的稳定性,本试验选择2.2 mol/L的水和0.2 mol/L的CTAC作为最佳浓度,此时R值为11;实验还表明,保持R值为11时,发光强度还随着表面活性剂和含水量的增加而增强,这可能是因为虽然单个微反应器的体积不变,但其数量增加的缘故.
2.2 AuCl4-质量浓度对发光强度的影响实验结果表明,无AuCl4-时,鲁米诺与盐酸布比卡因反应无发光信号,然而无盐酸布比卡因时,AuCl4-与鲁米诺反应能产生化学发光,这是因为在酸性条件下H+·AuCl4-·nH2O被微量萃取,加入酸化的盐酸布比卡因后信号得到大大增强,且两者发光强度的最高点一致,表明盐酸布比卡因只是起到携带AuCl4-的作用,盐酸布比卡因被质子化后立即与AuCl4-形成离子缔合物,当其进入微反应器中的“水池”时就立即离解,AuCl4-马上氧化“水池”中的鲁米诺产生发光信号,盐酸布比卡因的浓度越大,进入水池中的AuCl4-量越多,发光强度就越大.若盐酸布比卡因和其它实验条件不变,当AuCl4-为20 μg/mL时发光信号最强,故选择该质量浓度为最佳AuCl4-质量浓度.
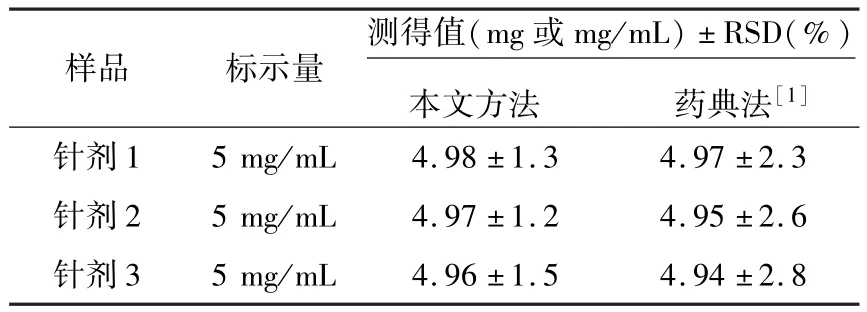
表1 针剂中盐酸布比卡因的测定结果(n=5)Table 1 The determination results on Bupivacaine Hydrochlorid in injections(n=5)
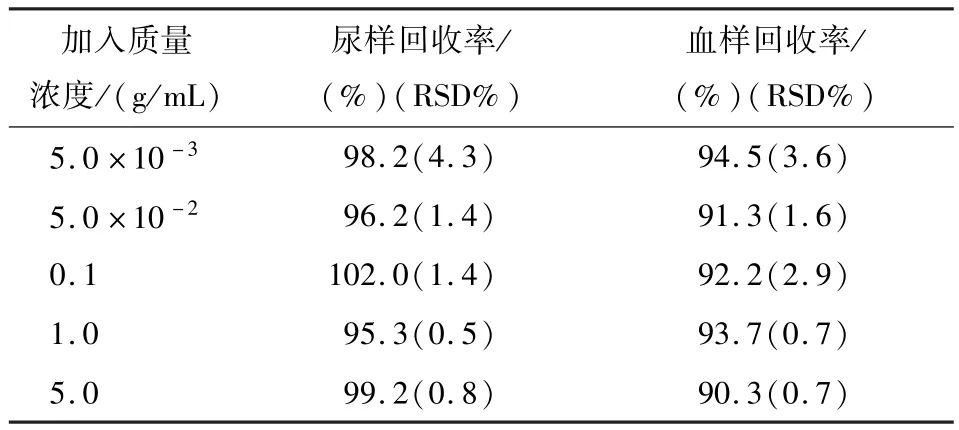
表2 尿样和血样中盐酸布比卡因的回收结果(n=5)Table 2 The recycling results on Bupivacaine Hydrochlorid in urine and blood samples
2.3 盐酸浓度对发光强度的影响无盐酸时,因为不能产生离子缔合物DH·H+·AuCl4-·nH2O,故只有试剂的空白信号,随着盐酸浓度的增加,发光强度也随着增加,当其浓度达到0.05 mol/L时发光强度达最大值,然而超过该浓度信号反而下降,这是因为有少量气态HCl被带进了水池,从而破坏了微反应器中鲁米诺pH值环境的缘故.故本实验选择0.05 mol/L的盐酸为最佳酸性条件.
2.4 其它试验条件对发光强度的影响另外,当CH2CI2为萃取剂,进样体积为120 L,反应盘管长度为120 mm,2个蠕动泵的速度均为3.6 mL/min(单管),e点至流通池的距离为6 cm,直径为2 mm;负高压为-600 V;增益为2时;鲁米诺浓度为0.4×10-4mol/L;Na2CO3浓度为0.3 mol/L(pH=11.5)时,发光达最大值.
2.5 校准曲线、精密度和检出限在最佳试验条件下,在1.0×10-3~10.0 μg/mL质量浓度范围内盐酸布比卡因浓度与发光强度呈线性关系,ICL=632.5c+678.9,R2=0.999 4(n=9)(ICL为相对发光强度,c为盐酸布比卡因质量浓度,单位为μg/mL,R2为相关系数).根据IUPAC建议算出的检出限(3σ)为6.0×10-2ng/mL,对质量浓度为1.0 μg/mL的盐酸布比卡因平行测定11次,得RSD为2.3%.
2.6 方法的选择性对1.0 μg/mL盐酸布比卡因进行干扰试验,以相对误差小于5%计,以下常见阴离子、阳离子和有机物不干扰测定:1 000倍的Ca2+、Cr3+、K+、Mn2+、Hg2、Mg2+、Pb2+、Zn2+、NH4+、、HSO3-、HCO3-、尿素、麦芽糖、尿酸、100倍Na+、650倍淀粉葡萄糖、500倍糊精;400倍.另外,对与盐酸布比卡因有类似结构的物质进行试验,结果发现200倍马来酸氯苯那敏、硫酸奎宁和硫酸阿托品;100倍盐酸氯丙嗪、盐酸异丙嗪均没有干扰.该方法具有良好的选择性.
2.7 样品分析
2.7.1 针剂的测定 取10支针剂(标示量为5.0 mg/mL)混合,移取相当于1支针剂体积(1.0 mL)溶于1 000 mL容量瓶中,定容后按标准曲线方法处理,测定结果见表1.可以看出,本法得到的结果与药典法相当吻合.
2.7.2 尿样和血样的回收率试验 加一定量盐酸布比卡因标准溶液于尿样中得含盐酸布比卡因100 μg/mL溶液,过滤(用45 m的滤膜抽滤)后,用二次蒸馏水稀释至线性范围内再按标准曲线方法处理.以不加盐酸布比卡因的溶液做空白试验,结果见表2.
加一定量的盐酸布比卡因标准溶液到5.0 mL的血样中,然后加5.0 mL质量分数10%的三氯乙酸,以3 000 r/min的转速离心10 min以除去血浆中的蛋白质.然后按标准曲线方法处理.以不加盐酸布比卡因的溶液做空白试验,结果见表2.
结果表明,盐酸布比卡因在尿样和血样中的回收率均在91%以上,由此可以看出该法可用于生物样品中盐酸布比卡因的测定.
[1]中华人民共和国药典委员会.中华人民共和国药典:2部[M].北京:化学工业出版社,2010:656.
[2]陈效兰,杨娟,徐淑静,等.基于纳米银对鲁米诺-铁氰化钾化学发光体系的增敏作用测定硫酸特布他林[J].分析化学,2009,37(11):1662-1666.
[3]张肖宁,田秀丽,杨利红.HPLC法测定盐酸布比卡因注射液含量的不确定度分析[J].黑龙江医药,2011,24(3):344.
[4]赵颖,贾珊珊,石红梅,等.流动注射-化学发光法测定盐酸罂粟碱注射液中的盐酸罂粟碱[J].光谱实验室,2012,29(1):21-24.
[5]方卢秋,李晓燕.代森铵在紫色土中吸附和解吸行为的流动注射化学发光法研究[J].四川师范大学学报:自然科学版,2011,34(2):226-230.
[6]王玮,段梦茹,翟一静,等.流动注射-化学发光法用于药物分析研究进展[J].光谱实验室,2013,30(3):1488-1491.
[7]陈波,石文兵,黄玉明.纳米微反应器化学发光法测定盐氢溴酸加兰他敏[J].西南大学学报:自然科学版,2009,31(3):58-61.
[8]罗道斌,王娟.流动注射化学发光分析测定奋乃静[J].分析试验室,2010,29(6):53-56.
[9]邓翔,王亚宁,袁暾,等.流动注射微乳液化学发光法测定片剂和注射中磷酸可待因的含量[J].药物分析杂志,2012,32(10):1818-1821.
[10]朱乾华.流动注射纳米微反应器化学发光法测定盐酸阿米替林[J].分析试验室,2011,30(6):39-41.
[11]胡筱,陈莉,凌伟坚.流动注射化学发光法测定片剂中阿昔洛韦含量[J].分析试验室,2011,30(10):81-84.
[12]樊雪梅,王书民,苏智魁,等.流动注射-化学发光法测定扑热息痛[J].理化检验:化学分册,2011,47(10):1149-1151.
[13]邓庆文,朱春燕,郭洁,等.流动注射-化学发光法测定非洛地平[J].分析试验室,2011,30(5):66-68.
[14]刘丽娟,王辉,梅林,等.流动注射-化学发光检测利福平[J].药物分析杂志,2011,31(11):2131-2134.
[15]苑洁,王玮,康维钧,等.流动注射-鲁米诺-Ag(III)化学发光法测定文拉法辛[J].分析测试学报,2011,30(12):1436-1439.
[16]陈小利,马红燕,杜乙磊.流动注射化学发光法测定曲克芦丁[J].分析科学学报,2011,27(1):119-121.
[17]吴雄志,吕晓惠,王立红.鲁米诺-高锰酸钾体系化学发光法测定5-磺基水杨酸[J].分析试验室,2010,29(12):94-97.
[18]陈效兰,徐淑静,肖柳婧,等.鲁米诺-铁氰化钾流动注射化学发光法测定头孢拉定[J].分析试验室,2010,29(1):80-82.
[19]李世君,杨冉,屈凌波,等.鲁米诺-高碘酸钾化学发光法测定盐酸阿朴吗啡[J].药物分析杂志,2011,7(7):1376-1378.
[20]周娟,陈荟芸,杨华松,等.化学发光法测定痕量绿原酸[J].分析试验室,2012,31(2):13-16.
[21]周艳梅,张成丽,雷建都,等.分子印迹流动注射化学发光法测定盐酸强力霉素[J].光谱学与光谱分析,2009,29(7):1745-1749.

