推进剂安定剂与硝酸酯(NG-NC)相互作用研究①
丁 黎,郑朝民,翟高红,王琼林
(1.西安近代化学研究所,西安 710065;2.西北大学 化学系,西安 710068)
推进剂安定剂与硝酸酯(NG-NC)相互作用研究①
丁 黎1,郑朝民1,翟高红2,王琼林1
(1.西安近代化学研究所,西安 710065;2.西北大学 化学系,西安 710068)
采用高压差示扫描量热(PDSC)和绝热加速量热(ARC)2种方法,研究了DPA、C2、AKII与NC-NG的相互作用;采用密度泛函理论B3LYP方法和6-31g(d)基组,优化得到了安定剂C2、AKII及其与H+作用后各中间体的稳定构型,计算了安定剂结合H+的反应能变,以解释该3种安定剂安定化作用的强弱。结果表明,3种安定剂与硝酸酯存在明显的相互作用,且安定剂对硝酸酯化学稳定性的影响由强到弱依次为DPA>C2>AKⅡ,与安定剂亲核性顺序一致。
物理化学;相互作用;安定剂;硝酸酯;化学稳定性
0 引言
固体推进剂在贮存期内保持其化学性能不发生超过允许变化范围的能力称之为化学安定性。常用的硝化纤维素、硝化甘油等含硝酸酯基化合物是双基和改性双基推进剂中的主要能量组分,其硝酸酯键易于断裂(键能 150.5~167.2 kJ/mol),产生热分解,放出大量的气体和热量,分解释放出氮氧化物,又加速硝酸酯分解,形成自催化反应,导致推进剂力学性能、燃烧性能下降,甚至发生燃烧、爆炸等恶性事故。硝酸酯的热分解动力学服从Arrhenius关系式[1],理论上任何温度下都能发生热分解。因此,含有硝酸酯基组分的推进剂在贮存条件下也会发生分解,致使推进剂安定性下降。为了延缓推进剂热分解,提高安定性,含硝酸酯类推进剂加入苯胺衍生物、酰胺类和苯酚类衍生物等安定剂,用于吸收硝酸酯分解产生的酸、氮氧化物及其自由基,从而抑制或延缓硝酸酯的自催化分解反应。
DPA和C2是国内常用的2种安定剂,AKⅡ国外已有应用报道[2],国内至今尚未应用。目前,国外对安定作用的研究多关注安定反应及其动力学[3-4],国内安定剂在推进剂的应用多以经验为主,安定剂与推进剂组分间相互作用的机理研究还不多见。由于硝酸酯在碱性条件下会发生水解皂化,降低推进剂的安定性。因此,配方中安定剂的选择,不仅要了解安定剂对硝酸酯分解释放的氮氧化物的吸收能力,还要掌握安定剂对硝酸酯类材料化学稳定性的影响,指导安定剂在推进剂中的应用及新型安定剂的结构设计。
本文采用高压差示扫描量热(PDSC)和绝热加速量热(ARC)2种方法,研究了DPA、C2、AKⅡ与NC-NG的相互作用;采用密度泛函理论的B3LYP方法和6-31g(d)基组,优化安定剂C2、AKⅡ及其与H+作用后各中间体的稳定构型,通过计算安定剂结合H+的反应能变,比较了亲核能力的强弱,对实验结果进行了理论分析,为安定剂在推进剂中的应用提供了理论依据。
1 实验
1.1 试样
安定剂与硝酸酯的混合试样组成见表1。所用NC为1#棉,安定剂与硝酸酯摩尔比为1∶1。DPA、C2、AKⅡ化学结构如图1所示。

表1NC、NG、NC-NG与安定剂混合体系试样Table 1 Sample of NC,NG,NC-NG mixed with stabilities
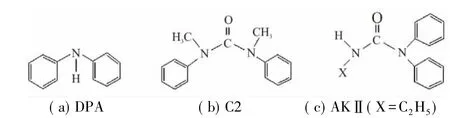
图1 安定剂的化学结构式Fig.1 Chemical structural formula of stability
1.2 仪器及条件
高压热分解采用德国Ntzsch STA 409型PDSC仪。试样量 0.5~l.0 mg,升温速率 β=2.5 ℃ /min,试验在高压(1 MPa)动态N2气氛下进行,气体流速40 ml/min。
绝热加速法采用德国Ntzsch 264型APTAC仪,ARC模式下,10 ml钛合金反应器;试样量0.1 g。起始温度100℃;加热-等待-搜寻模式;升温速率为5℃/min。
2 结果与讨论
2.1 热减量法评价安定剂的作用效果
将5 g不同安定剂的双基推进剂试样放入带有毛细孔塞的玻璃瓶中,置于95℃烘箱中,间隔24 h称重,得到质量损失曲线(图2)。从图2可知,该热减量实验结果可评价安定剂作用的效果,未加安定级的双基药在约10 d就已开始加速分解,而加有C2和DPA的双基体系都在30 d后才始加速分解,加有AKⅡ者则直到本实验结束(40 d)仍未见加速分解。尽管C2和DPA均在30 d后开始加速分解,但加有DPA的双基药在95℃贮存的第2天就有棕烟出现。可见,AKⅡ与分解产物的发生反应的能力优于C2和DPA,C2优于DPA,即3种安定剂对双基药的安定化作用强弱为 AKⅡ>C2>DPA。
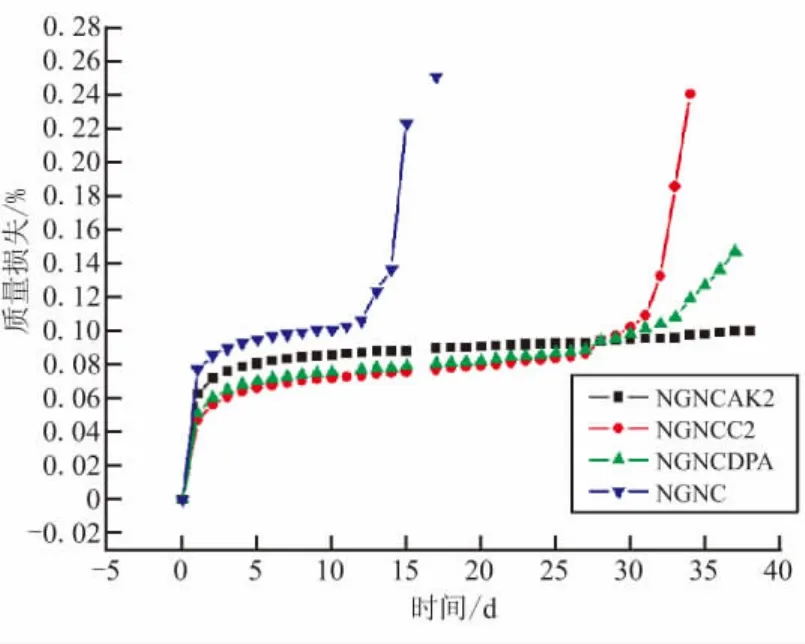
图2 不同安定剂的双基体系质量损失曲线Fig.2 Mass lost-t curves of double base propellant with different stability
2.2 安定剂对硝酸酯化学稳定性的PDSC研究
热分析技术是描述安定剂与硝酸酯化学稳定性的重要手段之一,能够通过等温或程序升温状态下安定剂与硝酸酯混合体系的热分解特性[5],了解安定剂对硝酸酯化学稳定性的影响。
NG具有挥发性,在常压DSC上不能获得完全的分解放热峰,只有在压力下,才可看到其真正放热分解过程[6]。因此,选择高压(1 MPa)条件下对NC、NG和NC-NG与安定剂混合体系进行差示扫描量热试验,得到PDSC曲线如图3所示。
NC、NG和NC-NG与安定剂混合体系的PDSC特征参数见表2。表2中,ΔTp1为安定剂/NG混合体系与NG分解峰温差值,℃;ΔTp2为安定剂/NC混合体系与NC分解峰温差值,℃;ΔTp3为安定剂/NC-NG混合体系与NC-NG分解峰温差值,℃。
由图3可看出,1 MPa时,3种安定剂均使 NG、NC、NC-NG的PDSC分解峰温降低。表2数据显示,DPA使NG和NC-NG分解峰温降低最显著,AKⅡ使3种试样的PDSC分解峰温降低最小,而C2的降低分解峰温作用则处于DPA和AKⅡ之间。可见,这3种安定剂与 NC、NC-NG作用的强弱程度是 DPA>C2>AKⅡ,与上述减量法评价这3种安定剂安定化作用效果的顺序相反。

图3NG、NC、NC-NG与安定剂混合体系PDSC曲线(1 MPa,β=2.5 ℃/min)Fig.3 PDSC curves of mixed system of NG,NC and NC-NG with stabilities(1 MPa,β=2.5 ℃/min)
2.3 绝热加速(ARC)试验研究安定剂对硝酸酯化学稳定性的影响
ARC实验能够发现待测体系微弱的热量变化,精确测得硝酸酯火药分解反应的初始温度、绝热分解过程中温度变化。通过ARC试验获得了NC/DPA、NC/C2、NC/AKⅡ、NC的自加热速率-温度曲线(见图4)试验数据见表3。表3中,Tc为自加热临界温度,℃;ΔTc为混合体系自加热临界温度与NC自加热临界温度差,℃。
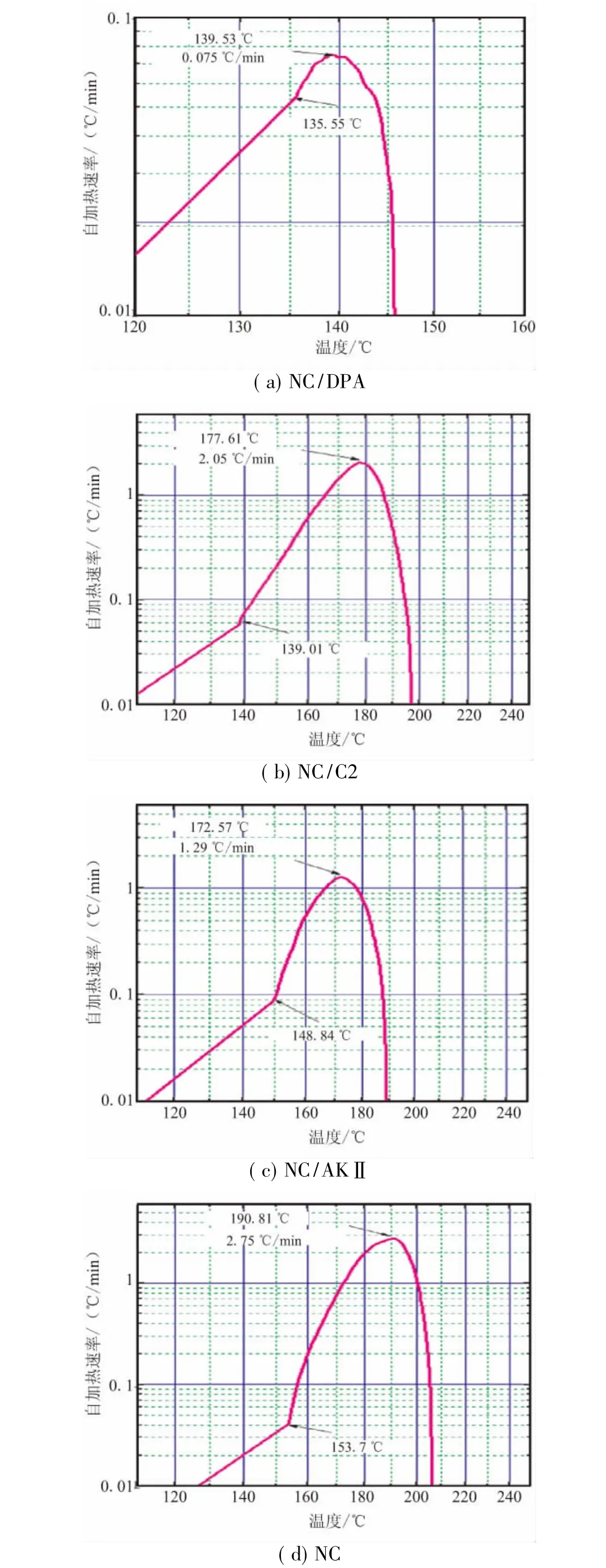
图4 NC和安定剂/NC混合体系的自加热速率-温度曲线Fig.4 Self heat rate-T curves of mixed system of NC with stabilities

表2 NC、NG和NC-NG与安定剂混合体系的PDSC特征参数(1 MPa)Table 2 PDSC characteristic for mixed systems of NC,NG and NC-NG with stabilities at 1 MPa
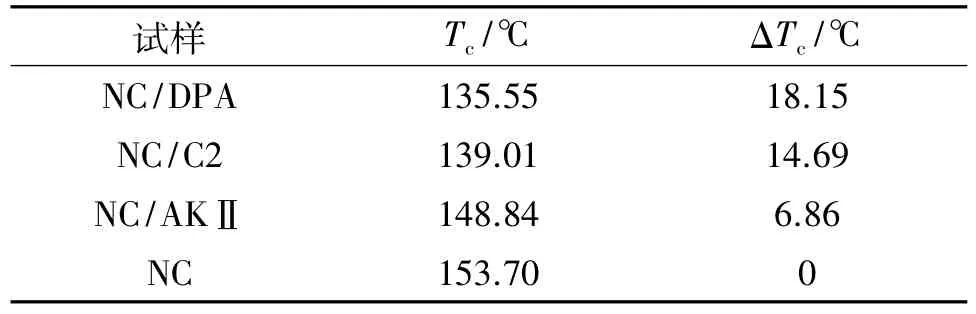
表3 ARC试验自加热临界温度数据Table 3 Self heat critical temperature by ARC test
图4表明,NC及其与3种安定混合体系都有一个较慢的匀速升温到加速升温的拐点,该拐点即为自加热临界温度Tc(或自加热起始温度)。从表3数据看出,自加热起始温度由低到高依次为 NC+DPA 135.55 ℃,NC+C2 139.01 ℃,NC+AKⅡ 148.84 ℃,NC 153.70℃,即安定剂与NC的相互作用由强到弱的顺序为DPA>C2>AKII。这一结果与上述PDSC的结果是一致的。
值得指出的是,上述减量法主要考察双基体系初期分解时安定剂对硝酸酯的安定化作用,硝酸酯处于分解延滞期的缓慢过程,安定剂的作用是吸收消耗硝酸酯分解的酸性产物,以阻止其自催化分解或加速分解。但DSC和ARC是考察这些试样较高温度下的全分解过程,这时安定剂吸收产物达到安定化作用的效果已消失,而反映出的是安定剂本身与硝酸酯的相互作用。PDSC与ARC的结果与安定剂相互作用强弱的顺序一致,说明安定剂安定化作用,除了吸收分解产物外,也与本身和硝酸酯的作用有关。
2.4 安定剂与硝酸酯作用的结构分析
为讨论安定剂对硝酸酯类的相互作用,通过分析计算安定剂亲核能力的强弱,比较了安定剂的碱性。DPA为芳香族胺类化合物,N上孤对电子的存在能与质子结合,具有碱性 DPA pKb=13.1[7];C2、AKII为酰胺类物质,羰基的吸电子作用使其N原子结合质子的能力变差,呈中性,但通过理论计算,比较了 C2和AKII上羰基结合质子的能力。计算采用Gaussian 03程序[8],采用密度泛函理论(DFT)中的B3LYP方法,在6-31g(d)基组水平上计算了C2和AKII上羰基的与H+作用后各中间体构型(见图5),各构型的能量参数见表4,安定剂结合H+的反应能变见表5。从表5可看出,C2结合质子的反应能变低于AKII。

图5 B3LYP/6-31g(d)水平下安定剂与H+形成的中间体结构(Å)Fig.5 Complex structures of stability combined with H+(Å)at B3LYP/6-31g(d)
上述结果表明,DPA的碱性强于C2和AKII,而C2结合质子的能力又比AKII强,则3种物质的亲核能力的强弱依次为DPA>C2>AKII。安定剂亲核能力强,即碱性强,则易使硝酸酯皂化,发生相互作用的能力就强,导致其化学稳定性下降。
PDSC和ARC试验均表明,安定剂与NC间存在明显的相互作用,且这种相互作用的强弱与安定剂亲核能力相关:安定剂亲核能力的强弱直接影响硝酸酯的分解,亲核能力强的安定剂更易引起硝酸酯结构单元中的酯基(—O—NO2)的破坏。因此,贮存过程中安定剂分子亲核能力愈弱,愈有利于酯基(—O—NO2)的稳定。因此,鉴于不同的安定剂对硝酸酯化学稳定性的影响不同,配方中安定剂的选择既要满足安定剂对硝酸酯分解释放的氮氧化物的有效吸收,还要考虑安定剂对硝酸酯类材料化学稳定性的影响。

表4 B3LYP/6-31g(d)计算的安定剂及安定剂与H+作用后各中间体构型的能量Table 4 Energies of equilibrium geometeies for stability reacted with H+calculated at B3LYP/6-31g(d)
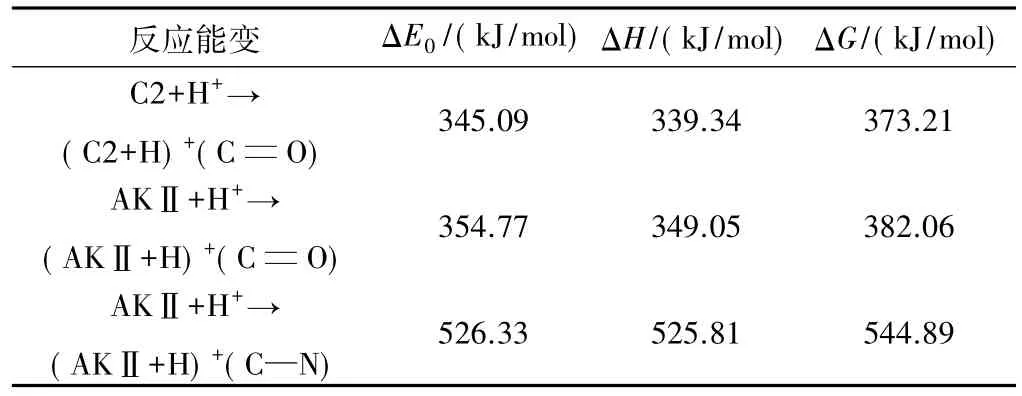
表5 B3LYP/6-31g(d)计算的安定剂结合H+的反应能变Table 5 Energies of stability reacted with H+calculated at B3LYP/6-31g(d)
3 结论
(1)95℃热减量实验表明,AKⅡ与分解产物的发生反应的能力优于C2和DPA,C2优于DPA,即3种安定剂对双基药的安定化作用强弱为AKⅡ>C2>DPA。
(2)采用高压差示扫描量热(PDSC)和绝热加速量热(ARC)两种方法研究,证明 DPA、C2、AKII与NC/NG存在相互作用,且安定剂对硝酸酯稳定性的影响由强到弱依次为DPA>C2>AKⅡ,与安定剂亲核性顺序一致,理论分析与计算支持了这一实验结果。
(3)理论分析与计算表明,安定剂和硝酸酯间的相互作用与安定剂的亲核能力密切相关,亲核能力弱有利于硝酸酯基的稳定;同时,据此可解释PDSC和ARC的试验结果。
(4)配方中安定剂的选择既要满足安定剂对硝酸酯分解释放的氮氧化物的有效吸收,还要考虑安定剂对硝酸酯类材料化学稳定性的影响。
(5)推进剂中安定剂的选择应根据硝酸酯的结构,结构稳定的硝酸酯适合选择亲核性强的安定剂,活泼的硝酸酯则应在亲核性较弱的安定剂中选择。这样,在贮存过程中不至发生因为安定剂碱性强引起硝酸酯皂化,而硝酸酯一旦发生分解,安定剂能够有效地吸收分解产物,起到安定作用。
[1]刘继华.火药物理化学性能[M].北京:北京理工大学,1997:215.
[2]Eric R Bixon,Lucas Lopez.Reaction kinetic modelings of AkarditeⅡdepletion in single base propellant formulation[J].Propellants,Explosives,Pyrotechnics,2006,31(4):673-679.
[3]Anton Chin,Daniel S Ellison.Mechanistic approach to study the moisture and acidity effect on the stability of single and double based propellants[C]//28th International Pyrotechnics seminar,2001:173-186.
[4]Lussier Louis Simon,Eric Bergeron,Hélène Gagnon.A mothed to characterize gun power stabilizers[C]//37th International Annual Conference of ICT,2006.
[5]刘子如.含能材料热分析[M].北京:国防工业出版社,2008:66.
[6]丁黎,赵凤起,刘子如,等.含CL-20的NEPE推进剂各组分热分解的相互影响[J].火炸药学报,2008,31(2):38-42.
[7]姚允斌,解涛,高英敏.物理化学手册[M].上海:上海科学技术出版社,1983:796-803.
[8]Frisch M J,et al.Gaussian 03,Revision D.01[M].Gaussian Inc.,Pittsburgh,PA,2003.
(编辑:刘红利)
Interaction of stability and nitric acid ester(NG-NC)of propellant
DING Li1,ZHENG Chao-min1,ZHAI Gao-hong2,WANG Qiong-lin1
(1.Xi′an Modern Chemistry Research Institute,Xi’an 710065,China;2.Chemical School of North West Univercity,Xi’an 710068,China)
The interaction of stability and nitric acid ester were studied by PDSC and ARC.The result show that decomposition temperature of nitric acid ester decreases because of adding stability.The structures of C2,AKII and its complexes with the H+,namely(C2+H)+(C = O),(AKⅡ+H)+(C = O),(AKⅡ+H)+(C—N),were optimized using the density function theory(DFT)at the B3LYP/6-31g(d)level.The energy of stability reacted with H+calculated at B3LYP/6-31g(d)was used to explain ability of stability.It was obvious interaction between stability and nitric acid ester,and the influence on chemical stability of nitric acid ester from strong to weak were DPA>C2>AKⅡ,which is in accord with nucleophilic ability.
physical chemistry;interaction;stability;nitric acid ester;chemical stability
V512
A
1006-2793(2014)04-0525-05
10.7673/j.issn.1006-2793.2014.04.018
2013-08-29;
2013-10-15。
丁黎(1970—),女,硕士,主要从事含能材料热化学与热安全特性研究。E-mail:dingli166@163.com
郑朝民,男,高级工程师。E-mail:zheng.chaomin@xtc.slbcn.com

