钢铁基体上EDTA弱酸性预镀铜工艺
刘存海, 罗 媛
(陕西科技大学 化学与化工学院,陕西 西安 710021)
钢铁基体上EDTA弱酸性预镀铜工艺
刘存海, 罗 媛
(陕西科技大学 化学与化工学院,陕西 西安 710021)
以CuSO4·5H2O为主盐,以EDTA为配体,在铸铁基体表面电镀铜。确定了镀铜液的基本组成为:CuSO4·5H2O 15g/L,EDTA 25g/L,Na2B4O7·10H2O 37g/L,硫脲0.2mg/L,丙三醇2mL/L,O-20(脂肪醇聚氧乙烯醚)0.05g/L。选择了无氰镀铜的最佳工艺条件为:pH值5.5,电压3V,时间5~7min,温度35℃。结果表明:在该工艺条件下制得的镀铜层光亮、均一,纯度高(99.89%),与基体结合紧密,无氢脆现象,具有与氰化物镀铜相当的质量。
EDTA;电镀铜;铸铁
0 前言
传统的氰化物镀铜因具有稳定性好、镀层与基体的结合力强等优点,在电镀领域中具有绝对的优势,曾得到广泛的应用。然而,氰化物镀铜对环境造成的极大污染及给操作者带来的危害,也是不容忽视的。禁止氰化物镀铜已是大势所趋。因此,越来越多的研究人员致力于发展新型环保的无氰镀铜工艺[1-4]。
近年来,研究者们提出了不少无氰镀铜工艺,如焦磷酸盐镀铜、柠檬酸镀铜、双配位剂镀铜、氟硼酸镀铜、氨基磺酸镀铜等[5-6]。但是始终没能很好地解决镀层与基体的结合力问题,镀层质量也不能和氰化物镀铜的相媲美[7-11]。因此,进一步改变镀液的组成、寻求良好的工艺条件、加强镀层与基体的结合力、保证镀液的性能及提高镀铜层的质量,是研究的目的之所在。本文以CuSO4·5H2O,EDTA为主要的镀铜原料,在弱酸性条件下研究了镀铜液的组成和工艺条件,有利于钢铁基体的活化,保证了镀铜层与基体结合良好且镀液稳定,提高了镀铜的质量,并且消除了氢脆现象。
1 实验
1.1 基材及主要试剂
铸铁(圆柱体,表面直径1.3cm,高2.4cm),由陕西科技大学机电学院的机械加工实验室提供。CuSO4·5H2O,EDTA,Na2B4O7·10H2O,丙三醇,硫脲,O-20(脂肪醇聚氧乙烯醚),以上试剂均为分析纯。
1.2 电镀铜
1.2.1 前处理
除锈(用0.5mol/L的HCl浸泡5min)—→二次水清洗—→砂纸打磨—→抛光—→二次水清洗—→备用
1.2.2 镀液配方及工艺条件
CuSO4·5H2O 5~30g/L,EDTA 10~40 g/L,Na2B4O7·10H2O 23~47g/L,硫 脲 0.2 mg/L,丙三醇2mL/L,表面活性剂0.05g/L,pH值3.5~7.0,1.5~5.5V,20~45℃,1~9min。
将处理好的镀件快速准确称重后,放入蒸馏水中浸泡片刻,取出后立即连接上负极导线;放入配制好的镀液中,再将正极导线连上包着纱布的碳棒,插入镀液中,在合适的条件下电镀一段时间后,铸铁镀件表面就镀上一层光亮的红色铜层;取出镀件,用蒸馏水冲洗干净后烘干,即为铸铁电镀铜件。
1.2.3 镀液性能测试
(1)电导率
镀液的电导率采用上海雷磁仪器厂生产的DDS-11A型数字电导率仪测量。
(2)稳定性
按最佳组成配制1L镀铜液。将其分成两份,一份加热到70~80℃,观察溶液是否分解,是否能正常进行电镀,镀层质量与新配镀液的进行比较;另一份盖上盖子,在室温下放置两周,随后进行电镀,镀层质量与新配镀液的进行比较。
(3)分散能力
用远近阴极法测定镀液的分散能力,计算公式如下:

式中:T为分散能力,%;K为远阴极离阳极的距离与近阴极离阳极的距离之比;m近为近阴极上镀层的质量,g;m远为远阴极上镀层的质量,g。本实验中K值取5。
1.2.4 镀层性能测试
(1)厚度
镀层厚度采用称量法测定,计算公式如下:

式中:δ为镀层厚度,μm;Δm为镀铜质量,g;ρ为铜的密度,g/cm3;A 为铸铁的表面积,cm2。
(2)纯度
采用日本Hitachi公司生产的170-30型原子吸收光谱仪测定铜的纯度。
(3)表面形貌
采用日本电子公司生产的SM-6390型扫描电镜分析镀层的粗糙度、平整性和均一性。
(4)结合力
采用打磨法及加热骤冷法测试镀层的结合力。
2 结果与讨论
2.1 镀铜液组成的确定
在温度40℃,时间4min,pH值6.0,电压3.5 V的初选工艺条件下,分别调节镀铜液中CuSO4·5H2O,EDTA和Na2B4O7·10H2O的质量浓度,进行电镀。以镀层厚度分别对CuSO4·5H2O,EDTA和Na2B4O7·10H2O的质量浓度作图,如图1所示。从图1中可以看出:当CuSO4·5H2O 15 g/L,EDTA 25g/L,Na2B4O7·10H2O 37g/L时,其镀层厚度均最大且镀层平整、光亮。故镀铜液的最佳组成为:CuSO4·5H2O 15g/L,EDTA 25 g/L,Na2B4O7·10H2O 37g/L。

图1 各物质的质量浓度对镀层厚度的影响
2.2 工艺条件对镀层厚度的影响
按镀铜液的最佳组成(CuSO4·5H2O 15g/L,EDTA 25g/L,Na2B4O7·10H2O 37g/L)进行电镀,确定最佳的工艺条件。
2.2.1 pH值的影响
控制电压3.5V,温度30℃,在不同的pH值下电镀4min,测镀层厚度,结果如图2所示。由图2可知:当pH值约为5.5时,镀层厚度达到最大值,同时外观也较好;而当pH值大于6时,镀速变慢,镀层稍显粗糙,镀液中开始产生沉淀。故最佳的pH值为5.5。
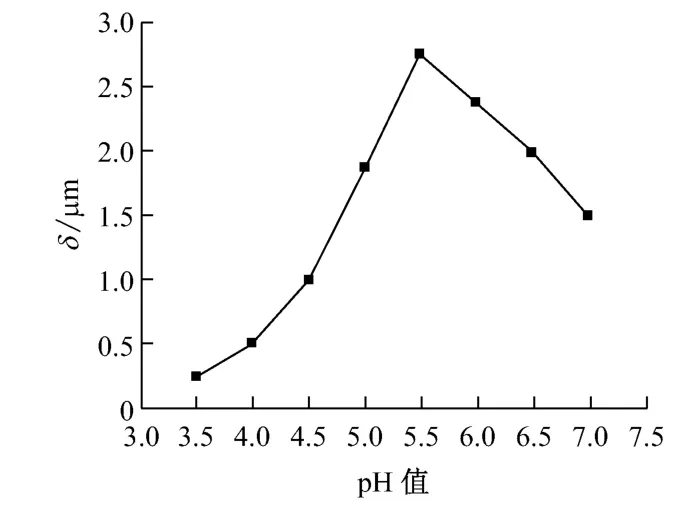
图2 pH值对镀层厚度的影响
2.2.2 温度的影响
控制pH值5.5,电压3.5V,在不同的温度下电镀4min,测镀层厚度,结果如图3所示。由图3可知:随着温度的升高,镀层厚度呈上升趋势;当温度升至35℃时,镀层厚度最大;继续升高温度,表面开始有微量镀层脱落。故最佳的温度为35℃。
2.2.3 时间的影响
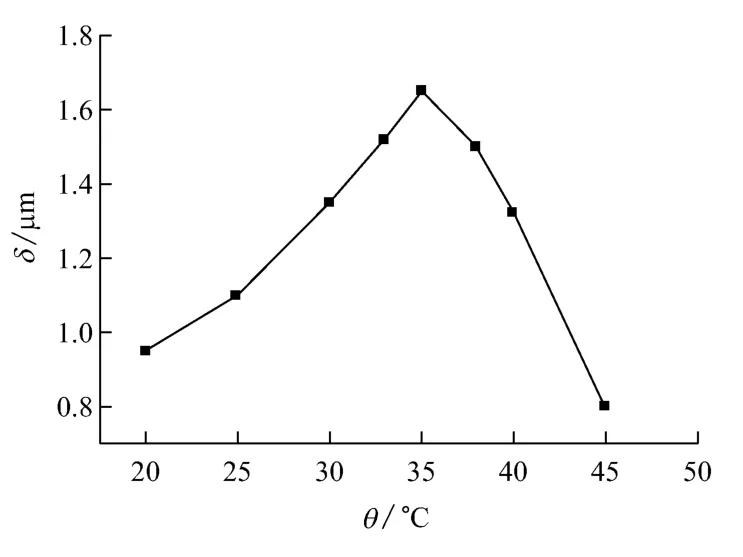
图3 温度对镀层厚度的影响
控制pH值5.5,温度35℃,电压3.5V,在不同时间下测镀层厚度,结果如图4所示。由图4可知:随着时间的延长,镀层厚度呈上升趋势,尤其是3min之后,镀层厚度增加明显;当时间达到5min时,镀层厚度的增加趋于平缓;7min之后,镀层厚度的增加更加缓慢;若再延长时间,镀层开始发黑。故最佳的时间为5~7min。
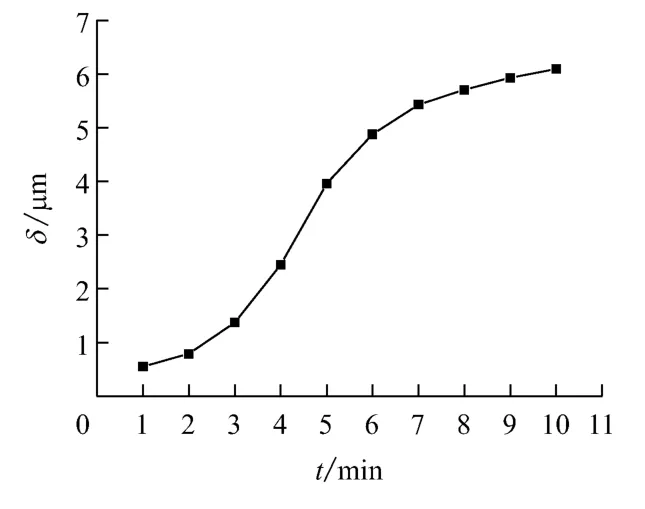
图4 时间对镀层厚度的影响
2.2.4 电压的影响
控制pH值5.5,温度35℃,在不同的电压下电镀6min,测镀层厚度,结果如图5所示。由图5可知:随着电压的上升,镀层厚度呈现先增后减的趋势;当电压为3V时,镀层厚度达到最大值;若进一步升高电压,电场力过大,使铜离子的沉积速率远远大于其整齐排列的速率,故表面出现了不平整的现象,铜镀层的质量明显下降。故最佳的电压为3V。

图5 电压对镀层厚度的影响
2.3 镀层厚度
从以上分析中可以看出:镀层厚度达到了镀铜的要求,且镀层表面平整、光洁,不仅可以作预镀层,也可以作中间层或表面镀层。
2.4 镀液的稳定性
将一份溶液加热到80℃,冷却后进行电镀。结果发现:镀层质量与新配镀液的一样。
将另一份溶液加盖后,在室温下放置1个月,然后进行电镀。结果发现:镀层质量与新配镀液的一样。可见,镀液的稳定性好。
2.5 镀液的电导率
测得镀液的电导率为0.479S/m,电导率较小。
2.6 镀液的分散能力
用远近阴极法测得镀液的分散能力为58.3%,说明镀液的分散能力良好。
2.7 镀层的纯度
将铸铁镀层表面的铜层剥离,用原子吸收法测得其纯度为99.89%。
2.8 SEM分析
镀铜工件的SEM分析结果,如图6所示。

图6 镀铜工件的SEM分析图
从图6中可以看出:镀铜层表面均一、光洁、无凹凸现象,且表面活性剂O-20的加入有效地减轻了氢脆现象,镀层效果良好。
2.9 镀层的结合力
将镀好的铸铁用2 400r/min的砂轮打磨其边沿,磨口处镀层与铸铁基体无脱离现象。
将镀好的铸铁放入300℃的烘箱中加热20 min,拿出后迅速放入冷水中冷却。结果未发现镀层脱落或起泡。以上均说明镀层与基体结合较好。
3 结论
(1)以CuSO4·5H2O为主盐,以EDTA为配体的无氰镀铜工艺,顺应了镀铜工艺的发展趋势,也有利于保护环境。
(2)镀铜液的最佳配方为:CuSO4·5H2O 15 g/L,EDTA 25g/L,Na2B4O7·10H2O 37g/L,硫脲0.2mg/L,丙三醇2mL/L,O-20(脂肪醇聚氧乙烯醚)0.05g/L。无氰镀铜的最佳工艺条件为:pH值5.5,电压3V,时间5~7min,温度35℃。
(3)通过对镀件的SEM分析得出:镀铜层光亮、均一、平整、几乎无氢脆现象。通过原子吸收法测得镀层的纯度为99.89%,且镀层厚度达到了镀铜的要求。通过结合力测试说明镀层与铸铁结合较好。通过对镀液性能的测试得出:镀液的稳定性好,电导率较低,且镀液的分散能力良好。
:
[1]霍栓成.镀铜[M].北京:化学工业出版社,2007:57-59.
[2]安茂忠.电镀理论与技术[M].哈尔滨:哈尔滨工业大学出版社,2004:102-119.
[3]陈春成.碱性无氰镀铜新工艺[J].电镀与环保,2003,23(4):10-11.
[4]徐金来,邓正平,赵国鹏,等.无氰碱性镀铜工艺实践[J].电镀与涂饰,2008,27(3):7-8.
[5]陈高,杨志强,刘烈炜,等.新型柠檬酸盐镀铜工艺[J].材料保护,2005,38(6):24-26.
[6]何建平.无氰电镀工艺的研究现状及解决问题的途径[J].电镀与涂饰,2005,24(7):42-45.
[7]张景双,石金声,石磊,等.电镀溶液与镀层性能测试[M].北京:化学工业出版社,2003:58-60.
[8]袁诗璞.再谈光亮酸性镀铜的使用和维护[J].电镀与环保,2001,21(1):16-21.
[9]王瑞祥.钢铁基体上碱性无氰镀铜[J].电镀与涂饰,2005,24(7):13-15.
[10]蔡爱清,王建华,曹相锋.碱性无氰镀铜工艺研究[J].电镀与精饰,2007,29(3):45-47.
[11]高泉涌,赵国鹏,胡耀红.酸性镀铜添加剂研究进展[J].电镀与涂饰,2010,29(1):26-29.
EDTA Weak Acid Strike Copper Plating on Steel Substrate
LⅠU Cun-hai, LUO Yuan
(College of Chemistry &Chemical Engineering,Shaanxi University of Science and Technology,Xi’an 710021,China)
Copper was plated on the surface of cast iron substrate using CuSO4·5H2O as main salt and EDTA as ligand.The basic composition of the plating solution were determined as:CuSO4·5H2O 15g/L,EDTA 25g/L,Na2B4O7·10H2O 37g/L,thiourea 0.2mg/L,glycerine 2mL/L and O-20(fatty alcoholpolyoxyethylene ether)0.05g/L.The optimal technological conditions of cyanide-free copper plating were selected as:pH value 5.5,voltage 3V,plating time 5~7minutes,temperature 35℃.The results show that the copper coating plated under these process conditions is bright,uniform,highly pure(99.89%),closely combined with the substrate,without hydrogen embrittlement phenomenon,with a quality comparable to that of cyanide copper plating.
EDTA;copper plating;cast iron
国家自然科学基金项目(No.51103081)
TQ 153
A
1000-4742(2014)03-0010-04
2013-12-03

