印染废水厌氧水解过程挥发性脂肪酸的产生及影响因素
操家顺,唐思远,李 超1,,周彬宇
(1.河海大学浅水湖泊综合治理与资源开发教育部重点实验室,江苏南京 210098;2.河海大学环境学院,江苏南京210098;3.水文水资源高效利用与工程安全国家研究中心,江苏南京 210098)
印染废水成分复杂,难降解有机物含量高,同时印染过程中大量含氮染料及助剂的使用,使得废水中有机氮含量偏高[1,2]。由于印染废水属于难降解废水,可以用作反硝化碳源的小分子物质非常少。同时《纺织染整工业水污染物排放标准》(GB 4287—2012)的实施对出水总氮值提出了更加严格的要求。为此污水厂往往采取外加碳源方式(如甲醇、乙醇、乙酸钠和葡萄糖等[3])来提高总氮的去除率。虽然,外加碳源的投入有助于反硝化的进行,但会增加运营成本[4]。
厌氧法是一种低成本的废水处理技术,包括水解、发酵、产乙酸及产甲烷四个阶段。目前,对于难降解废水的厌氧处理研究主要集中在如何提高甲烷化效率,进而在厌氧段充分降解有机物,对于水解酸化产挥发性脂肪酸(VFAs)的研究较少[5]。VFAs是厌氧生物处理法发酵末端产物。在发酵阶段,水解阶段所产生的小分子化合物在发酵菌的细胞内转化为更为简单的以挥发性脂肪酸为主的末端产物,并分泌到细胞外。VFAs是一种有机酸,主链上为一系列碳源,通常包括甲酸、乙酸、丙酸、丁酸、戊酸和己酸以及它们的异构体。
VFAs作为碳源可以很好地促进污水的脱氮除磷效果,吴一平[6]研究表明,以初沉污泥水解酸化产生的VFAs作为碳源脱氮率较未加碳源的脱氮率增大了1倍,同时脱氮速率也是常规外加碳源(甲醇)脱氮速率的 1.33倍,而且碳源分子越小,在缺氧条件下越容易被聚磷菌直接利用[7]。Hong S K等[8]利用连续搅拌槽反应器(CSTR)对棕榈油废水进行研究,在进水CODCr为88 000 mg/L、HRT为4 d、温度为30℃的条件下,厌氧出水VFAs最高可达15 300 mg/L,其中乙酸、丙酸和丁酸含量分别占VFAs总量的51.5%、27.0%和 21.5%。同时对牛奶废水[9,10]、造纸废水[11]的研究也表明生化性较高的废水经过水解酸化可以获得高浓度的VFAs,但是对于B/C低、水质成分复杂的工业废水却鲜有报道。
本文主要研究废水厌氧段水解酸化产VFAs,探明厌氧水解影响因素对VFAs产生量及组成成分的影响,以期为解决印染废水处理过程中脱氮碳源不足、总氮难以削减等问题提供理论依据及实际工程指导。
1 材料与方法
1.1 中试装置图
中试装置和流程如图1所示。6个UASB外形尺寸为:Φ1 232 mm×4 000 mm,有效容积为4 m3。2个A/O外形尺寸为B×L×H=4 000 mm×1 100 mm×2 700 mm,其中缺氧池有效容积为2.3 m3,好氧池有效容积为6.7 m3。UASB接种污泥采用柠檬酸厂颗粒污泥,接种污泥中挥发性悬浮固体与悬浮固体的质量浓度之比为 ρ(VSS)/ρ(SS)=0.60 ~0.80。接种污泥为黑色,粒径以1~3 mm为主。
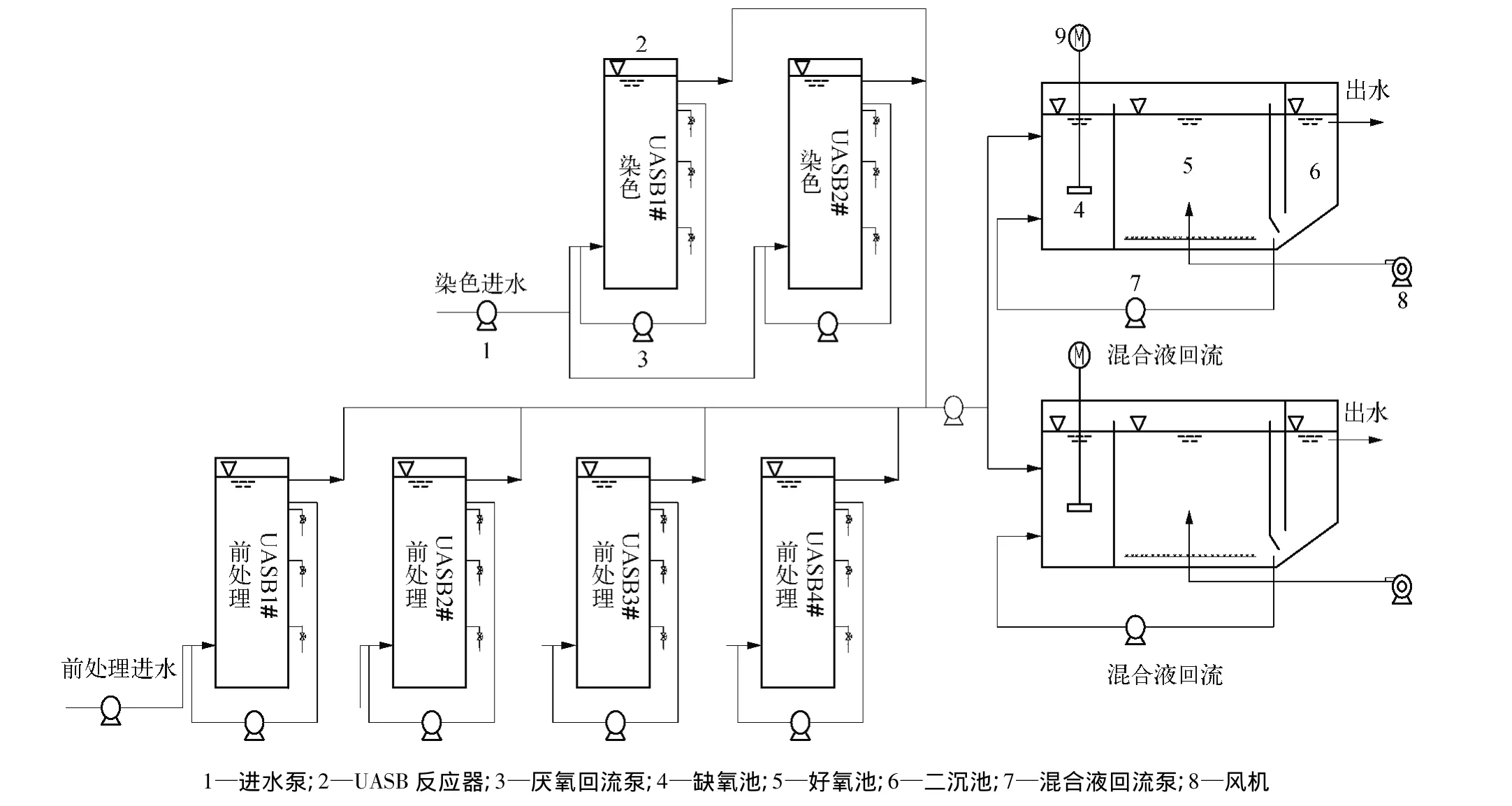
图1 中试装置示意图Fig.1 Schematic of Pilot-Plant
1.2 试验水质
中试试验的原水取自某印染企业的废水调节池,分为前处理废水和染色废水,前处理废水主要由退浆、煮练、漂洗产生的废水组成。染色废水主要由染料、印花和牛仔布废水组成。中试进水水质如表1所示。
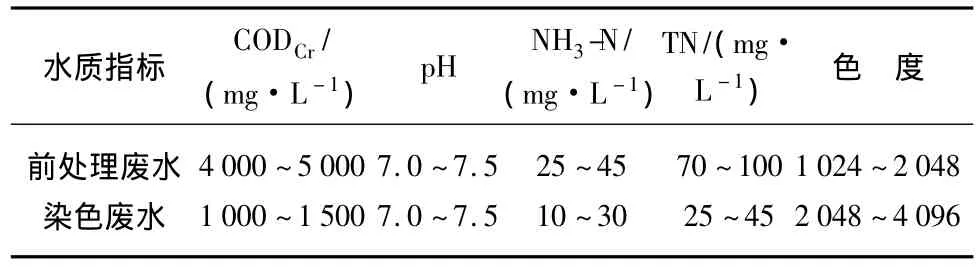
表1 进水水质Tab.1 Quality of Influent
1.3 检测指标与分析方法
VFAs检测采用气相色谱法。测定前,样品的处理方法为:样品先在5 000 r/min转速下离心10 min,再用0.45 μm的微孔滤膜进行抽滤式过滤,取1 mL滤液收集在1.5 mL的气相色谱专用棕色小瓶中,然后往每一小管中加入0.2 mL的50%的甲酸,以确保每一样品的 pH小于3.0[12]。气相色谱型号为安捷伦(GC7890A)。进样口参数:温度200℃,载气高纯氮气,不分流;柱温箱初始温度为80℃,采用程序升温,以10℃/min升温至180℃,保持1 min,最终升温至220℃,保持5 min;检测器参数:FID温度为250℃,空气流量为400 mL/min,H2流量为30 mL/min,尾吹流量为30 mL/min。
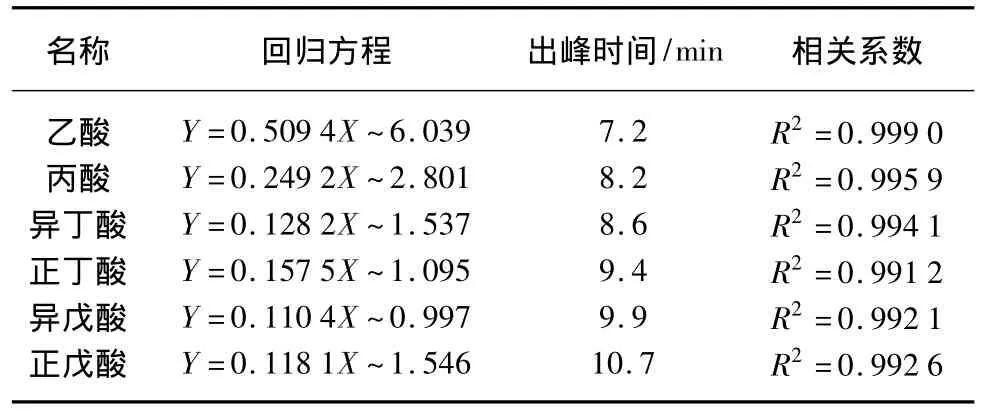
表2 VFAs的标准曲线回归方程Tab.2 Standard Curve Equation of VFAs
2 结果与讨论
2.1 厌氧HRT对VFAs的影响
印染废水CODCr较高,废水含大量难降解有机物质。同时印染过程中含氮染料与印花工艺含氮助剂等的应用,使印染废水中有机氮的含量上升。对宜兴市某印染厂出水水质进行监测,结果表明出水的TN含量高达30~40 mg/L。针对印染废水C/N较低,脱氮碳源不足、脱氮效率不高的特点,本研究采用高效UASB反应器将废水进行水解酸化,控制UASB反应器内温度在35~40℃,上升流速为1 m/h。根据染色废水和前处理废水进水水质的不同,结合印染厂现场UASB运行结果,调节染色废水HRT分别为5、10、15和20 h,前处理废水 HRT分别为20、40、60和80 h。每个周期运行15 d后,取样检测VFAs的浓度及成分。
2.1.1 HRT对染色废水厌氧产VFAs量的影响
图2为HRT对染色废水厌氧产VFAs量的影响。由图2可知,染色废水在厌氧条件下较容易发生水解酸化。据调查,该印染厂染色废水主要由染料、印花和牛仔布废水组成,其中染料废水约占总染色废水的70%,使用的染料也多为亲水性的直接染料。厌氧过程中,控制 HRT为5、10、15、20 h时,染色 UASB1#中 VFAs浓度分别为 97.3、229.2、472.1、457.1 mg/L,当 HRT=15 h 时,VFAs浓度达到最大值。根据 Qiu 等[13]及 Hui等[14]的调查研究,现在很多的污水厂都存在着反硝化碳源不足的问题,这一现象在冬天尤为明显。而印染废水中总氮含量较高,印花等过程中使用的偶氮染料,更是增加了脱氮的压力。而通过调节UASB的HRT控制厌氧段出水的VFAs可以保证小分子碳源在厌氧段不被过度削减,从而为后续反硝化脱氮服务。
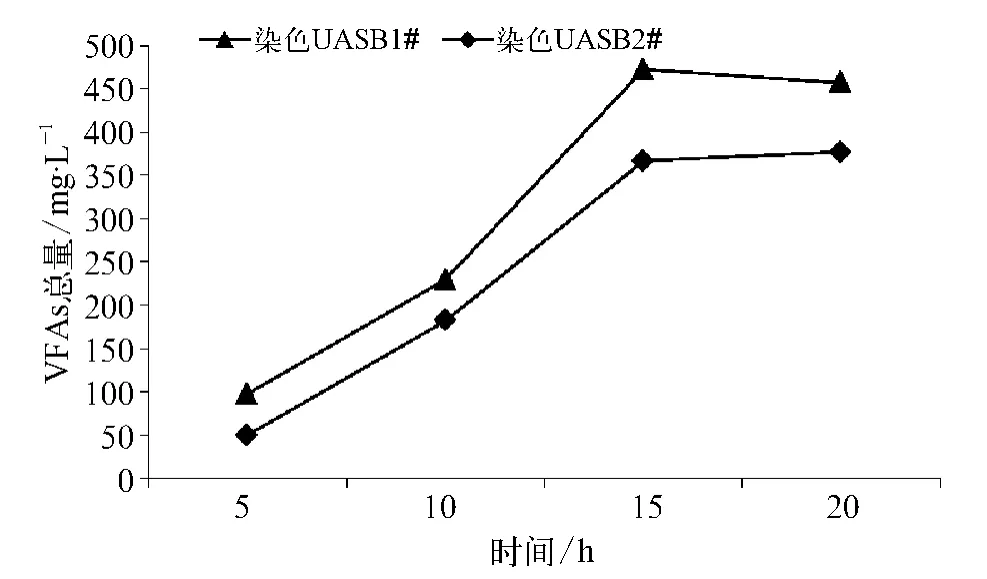
图2 HRT对染色废水厌氧产VFAs量的影响Fig.2 Effect of HRT on Generation of VFAs in Dyeing Wastewater Anaerobic Process
HRT对VFAs的组成成分也有较大的影响。表3为UASB1#中VFAs各组分浓度,由表3可知,当HRT为0~15 h时,乙酸、丙酸和异戊酸浓度增加比较迅速,但正戊酸、异丁酸浓度未发生很大改变。当HRT为15~20 h时,乙酸和丙酸浓度有所下降,可能是产甲烷菌利用这部分VFAs产生气体。当HRT为15 h时,乙酸浓度占VFAs浓度的86.5%,较高的乙酸浓度可以保证较快的反硝化速率。Pavan等[15]认为在反硝化过程中,乙酸在形成乙酰辅酶A后可直接被利用,故有较高的反硝化速率。而丙酸先形成丙酰辅酶A,通过一系列的酶促羧化反应和异构反应,被转化成琥珀酰辅酶A并进入TCA循环继续被氧化,因此它用作碳源时反硝化速率较低。Elefsiniotis等[16]的研究也表明乙酸的反硝化速率是丙酸的两倍。丙酸虽然反硝化脱氮速率较低,但Chen等[17]研究表明VFAs中丙酸存在,可以提高总磷的去除效率。印染废水中总磷的含量较低,在实际运行过程中往往会往废水中添加磷酸二氢钾。当HRT=15 h时,丙酸浓度占VFAs总量的9.4%,少量的丙酸存在可以促进总磷的去除,又不至于因为大量丙酸的堆积造成反应器酸化。

表3 不同HRT下染色废水VFAs各组分浓度Tab.3 Components of VFAs in Dyeing Wastewater Anaerobic Effluent at Different HRTs
2.1.2 HRT对前处理废水厌氧产 VFAs浓度的影响
相对于染色废水,前处理废水成分较为复杂。胚布退浆煮练的过程中使用了大量的精炼剂、渗透剂、退浆酶等试剂,经检测该印染厂使用的精炼剂中的CODCr高达40 g/L,渗透剂中的CODCr也有15 g/L。同时退浆废水中还会含有聚乙烯醇(简称PVA),PVA是一种生物难降解物质,生化性极差,BOD5/COD仅为0.064[18]。本次试验中,前处理废水在厌氧过程中保持较长的HRT。图3为HRT对前处理废水厌氧产VFAs的影响。由图3可知,当 HRT达到60 h时,VFAs浓度最高可以达到692.4 mg/L。
表4为前处理UASB1#中VFAs各组分浓度。由表4可知VFAs中乙酸、丙酸依旧占到很大的比重。与染色废水不同的是,前处理废水厌氧出水VFAs中乙酸的比重有所下降。HRT为20、40、60和 80 h时,乙酸/VFAs分别为 59.6%、66.4%、67.0%和67.2%。丁酸及戊酸含量较染色厌氧出水也有升高的趋势,根据 Elefsiniotis等[19]的研究发现厌氧出水VFAs中丁酸的量会随着原水中多糖类物质含量的增加而增加;同时在厌氧水解的过程中,异丁酸可能会转化为正丁酸。本试验中,当HRT达到60 h时,正丁酸含量增加到23.6 mg/L,而异丁酸含量在此过程中几乎未发生变化,这可能是因为一部分异丁酸在水解过程中变成了正丁酸。出水戊酸的生成主要依靠stlckland反应进行,即单氨基酸分子氧化脱氨或是多个氨基酸分子的氧化还原。对于碳原子数超过4个的脂肪酸会通过β氧化继续降解,其中含偶数个碳原子的脂肪酸最终产物为乙酸,含奇数个碳原子的脂肪酸最终产物为丙酸。
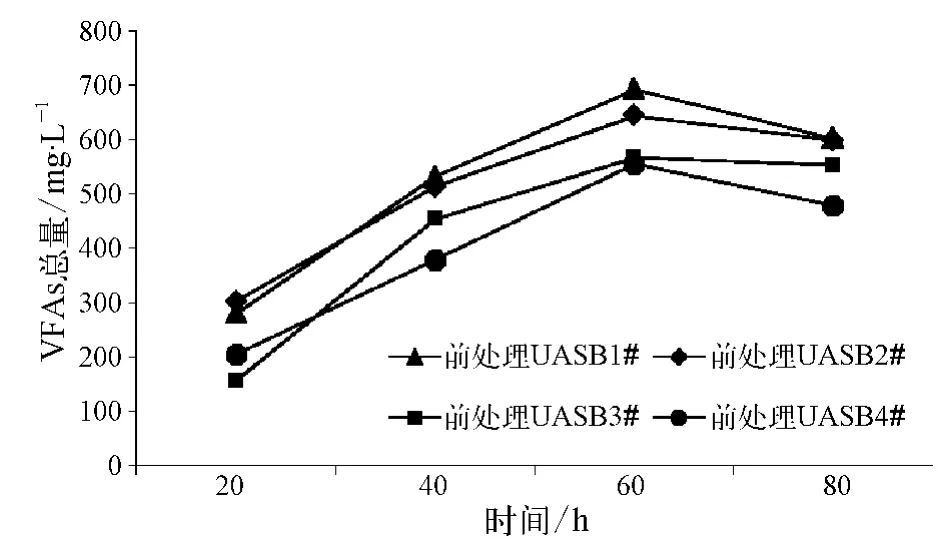
图3 HRT对前处理废水厌氧产VFAs的影响Fig.3 Effect of HRT on Generation of VFAs in Pretreatment Wastewater Anaerobic Process
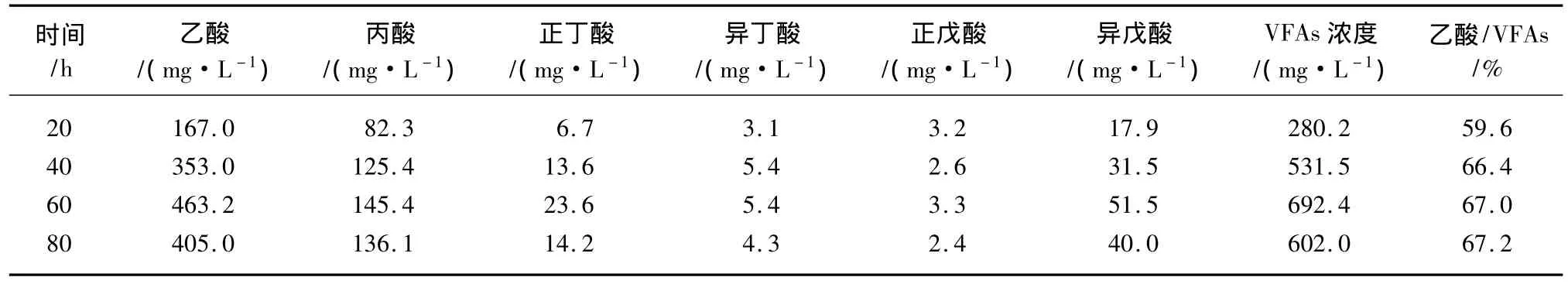
表4 不同HRT下前处理废水VFAs各组分浓度Tab.4 Components of VFAs in Pretreatment Wastewater Anaerobic Effluent at Different HRTs
2.2 温度对VFAs的影响
温度对微生物的种类及代谢活性有较大的影响。本试验考察了夏季(罐内温度为35~37℃)和秋季(罐内温度为20~23℃)的温度变化对厌氧水解的影响及对VFAs浓度及组分的影响。其中染色废水HRT控制为15 h,前处理废水HRT控制为60 h,每3天取样检测 VFAs含量,运行40 d后对VFAs的组分进行检测。
2.2.1 温度对染色废水厌氧产VFAs的影响
污水处理厂在秋冬季节,温度下降,厌氧段也很难保证在中温阶段。本试验对染色废水在夏季(罐内温度为35~37℃)和秋季(罐内温度为20~23℃)的厌氧效果进行了比较。考察温度对VFAs的影响,可以利用阿仑尼乌斯方程。

其中r——速率常数;
A ——频率分子;
Ea——活化能;
R——摩尔气体常数;
T ——温度。
其中r可以通过VFAs和气体产生量表示,即
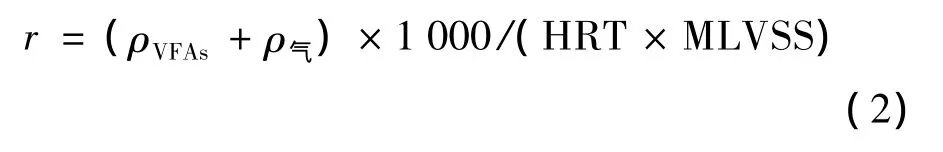
图4为温度对染色废水厌氧产VFAs的影响。由图4可知,UASB反应器内温度控制在35~37℃时更易于VFAs的产生,产生量为20~23℃时的两倍,速率常速r较大。由图4亦可知,UASB在秋季运行时,出水的VFAs的波动较大,其中第4 d VFAs浓度为110.1 mg/L,第22 d时VFAs的浓度却高达401.2 mg/L。
表5为不同温度下染色废水VFAs各组分浓度,由表5可知,温度对VFAs组分变化影响较小。以乙酸和丙酸为例,在35~37℃时,UASB反应器出水乙酸和丙酸浓度分别占VFAs的86.5%和9.3%。当反应器温度降为20~23℃时,出水乙酸、丙酸所占比例分别为83.2%和11.2%。由此可见当温度变化时,虽然VFAs浓度会有所改变,但是组分所占比重并没有因此发生很大的改变,这与 Yu[20]和Sparling[21]的结论相似,可能的解释是温度的改变对厌氧颗粒污泥中的菌种组分并没有太大的影响。
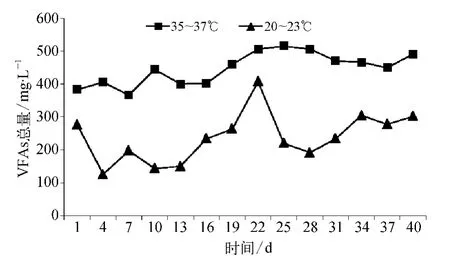
图4 温度对染色废水厌氧产VFAs的影响Fig.4 Effect of Temperature on Generation of VFAs in Dyeing Wastewater Anaerobic Process
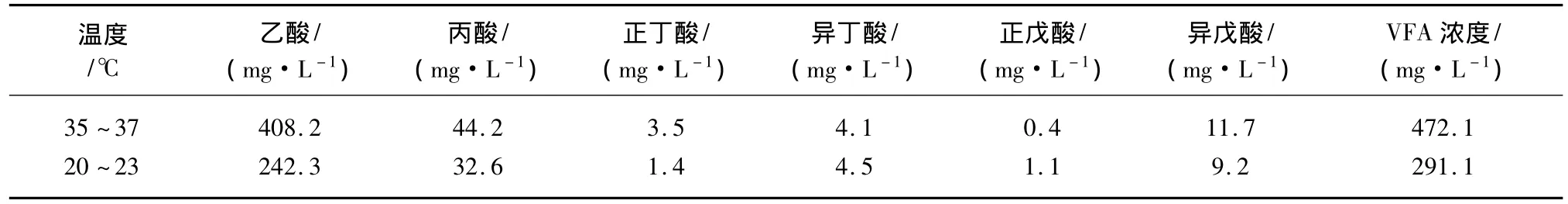
表5 不同温度下染色废水VFAs各组分浓度Tab.5 Components of VFAs in Dyeing Wastewater Anaerobic Effluent at Different Temperature
2.2.2 温度对前处理废水厌氧产VFAs的影响
图5为温度对前处理废水厌氧产VFAs的影响,表6为不同温度下前处理废水VFAs各组分浓度。由图5可知,前处理废水在秋季运行过程中出现了VFAs浓度大幅升高的现象,观察VFAs的组分:出现了丙酸大量的堆积。由图5和表6可知,在UASB反应器运行到31~40 d时,出水VFAs的浓度超过了1 000 mg/L,其中第40 d时,VFAs浓度达到1 223.0 mg/L,丙酸的浓度占VFAs总浓度的比重由之前的23.9%上升到41.2%,出水的pH也降至5.6,并出现了带泥现象。
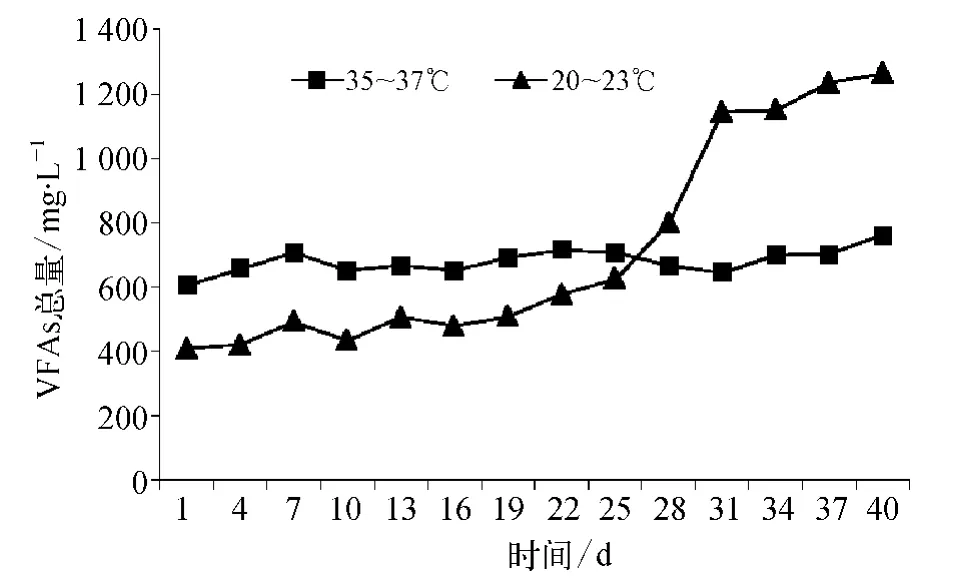
图5 温度对前处理废水厌氧产VFAs的影响Fig.5 Effect of Temperature on Generation of VFAs in Pretreatment Wastewater Anaerobic Process
对VFAs的浓度和组分的检测可适时反映厌氧反应器运行的好坏及稳定性,因为VFAs的变化要比环境因子pH、ORP等因子的变化提前出现1~2 d。Hill等[22]指出通常利用乙酸和丙酸的量来衡量厌氧反应器的稳定性,其中乙酸的量不应该大于800 mg/L,或是丙酸与乙酸浓度的比值不应该大于1.4。Malina 等[23]则认为厌氧反应器中 VFAs的含量小于1 500 mg/L。对于含有复杂有机物的化工废水,当温度出现波动、水质变化时,反应器出现酸化的概率更大。所以在工业废水厌氧水解酸化产VFAs的过程中,要密切注意反应器中VFAs浓度及组分的变化,出现反应器酸化的迹象要及时进行调整。
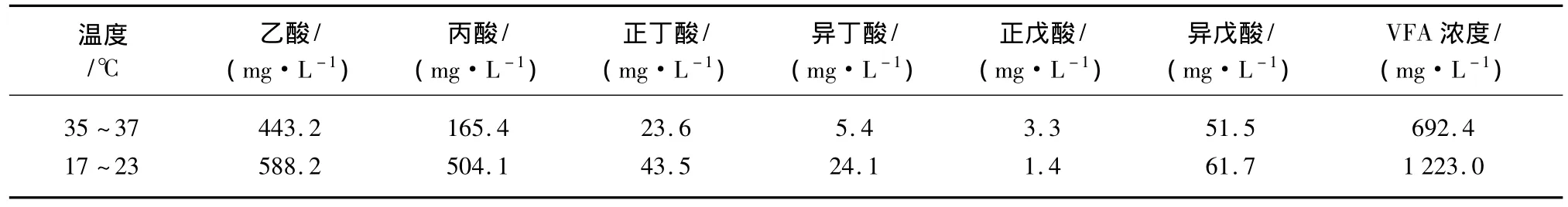
表6 不同温度下前处理废水VFAs各组分浓度Tab.6 Components of VFAs in Pretreatment Wastewater Anaerobic Effluent at Different Temperature
2.3 VFAs对总氮去除率的影响
在中温厌氧的条件下,两股废水经厌氧预处理后混合进入A/O系统,考察进水VFAs浓度对总氮去除率的影响。其中A/O系统运行参数如表7所示。系统稳定运行1个月后,每隔3 d对A/O系统进水VFAs浓度、总氮值及出水的总氮值进行检测。
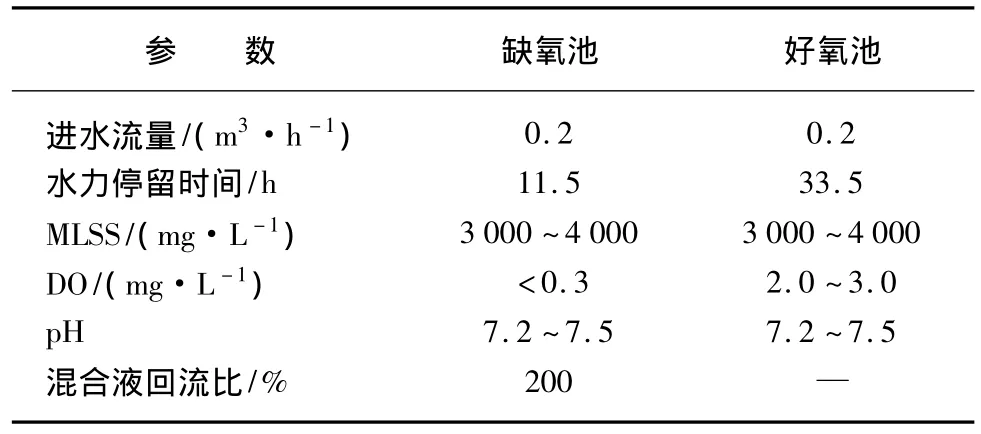
表7 A/O系统运行参数Tab.7 Operating Parameters of A/O Process
在反硝化系统中,VFAs可作为硝酸盐还原的氢供体。当VFAs作为碳源反硝化脱氮时,方程式表示为(由于厌氧出水VFAs中乙酸含量较高,特以乙酸为例)如下:
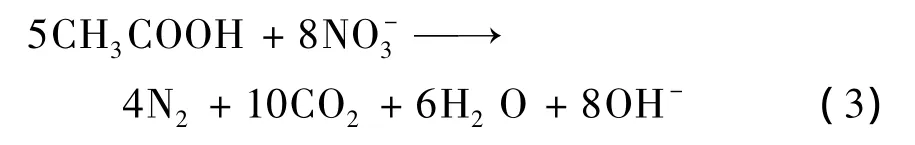
由式(3)可知,需要1.07 mg CH3COO--C才能还原1 mg NO-3-N。考虑到细胞同化及脱氧作用,则乙酸总消耗为:
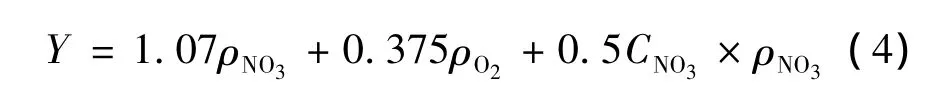
其中ρNO3——进水中硝酸盐含量;

ρO2——溶氧量;

CNO3——污泥产率。
通过对UASB参数的调整,控制前处理和染色废水HRT分别为60和15 h,两股废水混合后进入A/O系统,VFAs浓度约为550 mg/L,VFAs/TN保持在7左右。在缺氧段停留 11.5 h,好氧段停留33.5 h后,出水的总氮值在 11.0 ~15.2 mg/L,平均脱氮率为78.2%,满足《纺织染整工业水污染物排放标准》(GB 4287—2012)中要求的TN小于30 mg/L的水污染排放限值。
3 结论
(1)可以通过对UASB的运行参数调整来调控印染废水厌氧出水的VFAs,为后续反硝化单元提供优质的碳源,最终实现低品质碳源高效水解及反硝化耦合的高效脱氮技术。
(2)HRT对印染废水厌氧水解过程中VFAs的产生量及组成成分有较大影响。染色废水和前处理废水最佳的HRT分别为15和60 h,厌氧出水VFAs浓度可达到472.1及692.4 mg/L,组成成分中乙酸/VFAs分别为86.5%和67.0%。
(3)温度的改变会引起厌氧水解产VFAs浓度的变化。对于染色废水,UASB反应器内温度控制在35~37℃时更易于VFAs的产生,产生量约为20~23℃时的两倍;前处理UASB在20~23℃条件下运行时,厌氧出水VFAs浓度达到1 223.0 mg/L,丙酸的浓度占到了VFAs浓度的41.2%,出现了酸化迹象。
(4)对于印染废水,A/O系统进水的VFAs/TN值保持在6.5左右时较为合理,反映出水总氮值小于15 mg/L,去除率超过75%,满足《纺织染整工业水污染物排放标准》(GB 4287—2012)规定的对总氮排放限值。
[1]高春梅,冀世锋,储鸣,等.生物促生剂强化膜生物反应器处理印染废水的研究[J].净水技术,2010,29(2):32-35,61.
[2]周维民,王拯,刘丽芝,等.印染废水处理污泥内源消解技术工程实例[J].供水技术,2012,6(5):58-60.
[3]杨敏,孙永利,郑兴灿,等.不同外加碳源的反硝化效能与技术经济性分析[J].给水排水,2010,35(11):125-128.
[4]邵留,徐祖信,尹海龙.污染水体脱氮工艺中外加碳源的研究进展[J].工业水处理,2007,27(12):10-14.
[5]Nizami A S,Thamsiriroj T,Singh A,et al.Role of leaching and hydrolysis in a two-phase grass digestion system[J].Energy&Fuels,2010,24(8):4549-4559.
[6]吴一平.初沉污泥水解产酸及利用研究[D].西安:西安建筑科技大学,2004.
[7 ]Fernández F J,Castro M C,Villasenor J,et al.Agro-food wastewaters asexternalcarbon sourcetoenhancebiological phosphorus removal[J].Chemical Engineering Journal,2011,166(2):559-567.
[8]Hong S K,Shirai Y,Nor Aini A R,et al.Semi-continuous and continuous anaerobic treatment of palm oil mill effluent for the production of organic acids and polyhydroxyalkanoates [J].Research Journal of Environmental Sciences,2009,3(5):552-559.
[9]DemirelB, Yenigun O. Anaerobic acidogenesis ofdairy wastewater:the effects of variations in hydraulic retention time with no pH control[J]. JournalofChemicalTechnology and Biotechnology,2004,79(7):755-760.
[10]Yu H Q,Fang H P.Acidification of mid-and high-strength dairy wastewaters[J].Water research,2001,35(15):3697-3705.
[11]Jiang Y,Marang L,Tamis J,et al.Waste to resource:Converting paper mill wastewater to bioplastic[J].Water Research,2012.
[12]Chen Y,Chen Y S,Xu Q,et al.Comparison between acclimated and unacclimated biomass affecting anaerobic-aerobic transformations in the biological removal of phosphorus[J].Process Biochemistry,2005,40(2):723-732.
[13]Qiu Z F,Zhou Q,Yang D H,et al.Short-cut nitrification and denitrification of low C/N ratio municipal wastewater in a pilotscale research [J].Industrial Water Treatment,2006,11(26),35-38.
[14]Hui Y Z,Li L,Shang G Y.On Guangzhou municipal wastewater quality and treatment[J].Journal of Yunyang Teachers College,2010,3(30),23-25.
[15]Pavan P,Battistioni P,Traverso P.Effect of addition of anaerobic fermented OFMSW on BNR process:preliminary results[J].Water Science and Technology,1998,38(1):327-334.
[16]Elefsiniotis P,Wareham D G.Utilization patterns of volatile fatty acids in the denitrification reaction[J].Enzyme and microbial technology,2007,41(1):92-97.
[17]Chen Y,Randall A A,McCue T.The efficiency of enhanced biological phosphorus removal from real wastewater affected by different ratios of acetic to propionic acid[J].Water Research,2004,38(1):27-36.
[18]Chou W.Removal and adsorption characteristics of polyvinyl alcohol from aqueous solutions using electrocoagulation [J].Journal of hazardous materials,2010,177(1):842-850.
[19]Elefsiniotis P,Wareham D G,Smith M O.Effect of a starch-rich industrial wastewater on the acid-phase anaerobic digestion process[J].Water Environmental Ressearch.2005,77(4):366-371.
[20]Yu H Q,Fang H H P.Acidogenesis of dairy wastewater at various pH levels[J].Water Science and Technology,2002,45(10):201-206.
[21]Sparling R,Oleszkiewicz J A.VFA generation from waste activated sludge:Effect of temperature and mixing [J].Chemosphere,2011,82(4):603-607.
[22]Hill D T,Cobb S A,Bolte J P.Using volatile fatty acid relationships to predict anaerobic digester failure[J].Trans ASAE,1987,30:496-501.
[23]Malina J F,Pohland G F.Design of anaerobic processes for the treatment of industrial and municipal wastes[M].Technomic publication,1992.

