埃克替尼治疗NSCLC的有效性:基于病理学类型与ECOG评分的M eta分析
廖础欣,刘锐锋,李运景,卢荣枝,赵伟国
(中山市人民医院药学部,广东中山528403)
埃克替尼治疗NSCLC的有效性:基于病理学类型与ECOG评分的M eta分析
廖础欣,刘锐锋,李运景,卢荣枝,赵伟国
(中山市人民医院药学部,广东中山528403)
目的系统评价埃克替尼治疗非小细胞肺癌(non-small cell lung cancer,NSCLC)的不同组织病理学类型与ECOG评分差异的临床有效性。方法收集国内外埃克替尼治疗NSCLC的临床治疗性试验研究数据,用Revman5.2进行meta分析。结果腺癌vs鳞癌纳入了8篇研究,固定效应M-H分析合并效应优势比OR=2.46,P=0.0005;ECOG评分:0~1 vs 2~4和0~2 vs 3~4 2个亚组分别纳入研究6篇和3篇,均存在异质性,随机效应M-H分析合并效应分别是RR=1.20,P=0.15和RR=1.77,P=0.09。结论埃克替尼治疗NSCLC的有效性腺癌比鳞癌更敏感;ECOG评分高低不影响治疗的有效性,但仍可扩大研究样本进行分析。
埃克替尼;NSCLC;组织病理学类型;ECOG评分;临床有效性;Meta分析
埃克替尼(Icotinib)是具有中国自主知识产权的小分子靶向高效特异性的EGFR-TKI抗癌新药,其理化特性、作用机理及其治疗NSCLC的临床有效性等方面均可与国外同类药物吉非替尼(Gefitinib)和厄洛替尼(Erlotinib)媲美,其安全性等方面甚至优于上述2种药物[1-2]。
较多的基于自身前后对照的临床试验研究表明,埃克替尼治疗NSCLC的客观有效性(ORR)和疾病控制率(DCR)均达到了较高的水准[3-10]。除了埃克替尼本身的有效性外,影响其临床有效性的因素应当包括个体差异,如年龄、性别、遗传特征和生活行为(如吸烟)等[3,5,10];NSCLC的性质,如肿瘤的组织病理学类型、临床分期、ECOG评分(美国东部肿瘤协作组评分,Eastern Cooperative Oncology Group,ECOG);埃克替尼与其他肿瘤药物的相互作用或其他辅助治疗药物的相互作用,也可能会影响其临床治疗的有效性,以上因素均值得研究。基于上述原因及其当前临床研究进展,本文从组织病理学类型与ECOG评分的角度探讨埃克替尼的临床治疗的有效性。
1 资料与方法
1.1 文献检索与纳入 通过因特网检索世界主要文献数据库,重点是中文数据库,因为埃克替尼具有中国自主知识产权,中文文献较多。主要文献数据库包括中国知网(CNKI)、万方数据(Wangfan Data)、维普网(VIP)、Pubmed及其链接的医学文献数据库、CBM和Cochrane图书馆随机对照试验资料库等数据库。
搜索关键词或主题词主要包括Icotinib、埃克替尼、NSCLC和非小细胞肺癌等。参照预先设定的纳入标准与排除标准,最后获得相关文献 8篇纳入腺癌 vs鳞癌分析[3,6,7,10,12-15],6篇[3,6,10,13-15]与3篇[4,12,17]研究分别纳入ECOG评分的2个亚组分析。
1.2 研究的纳入与排除标准 所有纳入研究的肿瘤病例均为原发性,有完整的病理分类和治疗前有完整的ECOG评分数据,所有研究必须有完整的临床对照实验数据,但不限于随机临床对照实验(Randomized Clinical Trials,RCTs),考虑到埃克替尼在国内应用于临床的时间并不太长,因此,纳入的研究未考虑年龄、性别、肿瘤分级和前期用药等临床干预情况。不符合上述要求的研究,在对数据进行分析时均一一排除或排除后进行亚组分析。
1.3 文献质量评价方法 研究的质量评价主要从7个方面进行,分别包括随机、隐藏、双盲、结局评价、非终点结局、挑选性报告和其他偏倚。将每一个研究的评价输入Revman5.2进行评价。
1.4 数据提取与统计学方法 根据研究的需要与目的要求,设计数据提取表,整合全部纳入研究中的数据及文本叙述中提及到的相应的数据,由2人相互核对后确定,这些数据包括每一个研究中涉及的病理类型即腺癌和鳞癌的总人数和治疗后的有效与无效人数,各研究的ECOG评分分级人数,根据研究需要,将ECOG评分数据划分为不同等级。将所得到的数据分别输入Meta分析软件Revman5.2,异质性检验以I2=50为临界值,当P≤0.1且I2≥50%时,采用固定效应模型分析,反之,采用随机效应模型分析。计数资料计算相对危险度(RR)和95%可信区间(CI)表示,发表偏倚绘制倒漏斗图进行判断。
2 结果
2.1 文献质量综合评价 作为治疗性研究,伦理等问题是首先需要考虑的,因此,纳入的研究偏倚主要存在的问题是选择偏倚和实施偏倚,主要包括随机、分配隐藏与双盲等(见图1)。
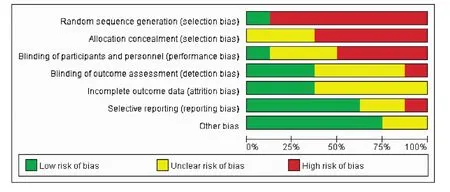
图1 纳入研究的偏倚来源及综合风险构成比Fig.1 Constituent ratio of bias sources and comprehensive risk on the included study
2.2 病理组织学类型与疗效 8个研究无异质性(P=0.29,I2=17%<40%,见图2),研究偏倚漏斗图对称(见图3),故采用固定效应的M-H分析方法,合并效应优势比OR为 2.46,95%CI为1.49~4.08,P=0.0005,表明埃克替尼治疗NSCLC腺癌的临床效果优于鳞癌。
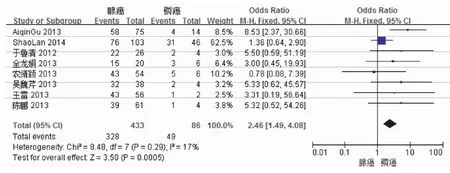
图2 晚期NSCLC腺癌vs鳞癌的森林图Fig.2 The forestmap of late stage NSCLC adenocarcinoma vs squamous cell carcinoma
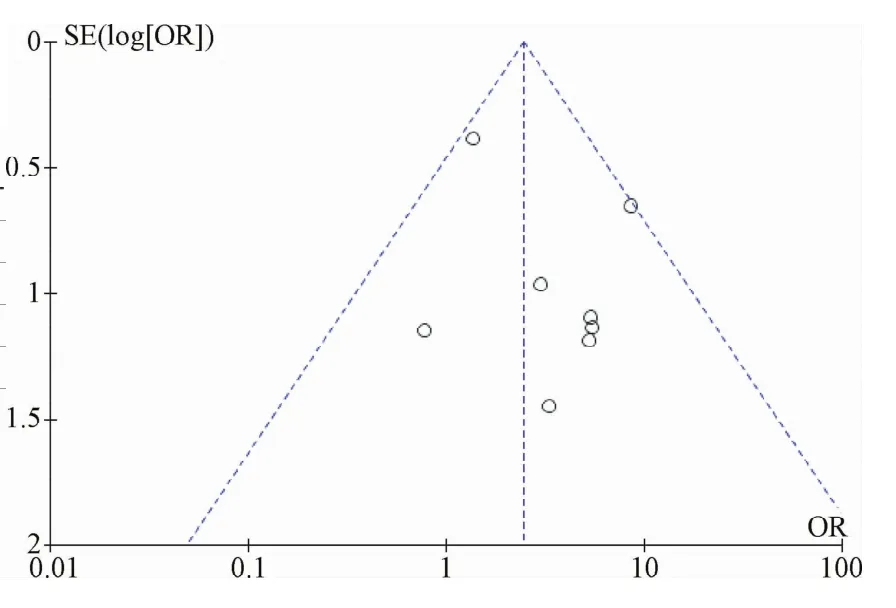
图3 晚期NSCLC腺癌vs鳞癌的研究偏倚Fig.3 The study bias of late stage NSCLC adenocarcinoma vs squamous cell carcinoma
2.3 ECOG评分与临床效果 ECOG评分多用于判定患者的活动能力,包括工作能力和生活能力等,同时ECOG也部分地反映了患者的健康状况,因此,将ECOG评分划分为二分类变量评判埃克替尼对NSCLC的疗效。
2.3.1 ECOG评分0~1 vs评分2~4:ECOG评分0~1,表明患者活动能力很好,但由于评分方法或多或少地带有主观性,图2显示ECOG评分0~1 vs评分2~4存在一定的异质性,I2=47%>40%,P=0.15>0.05,故采用随机效应的M-H分析方法,尽管合并效应危险比RR为1.20,但无统计学差异,合并效应菱形穿过RR=1(见图4);研究存在偏倚(见图5)。
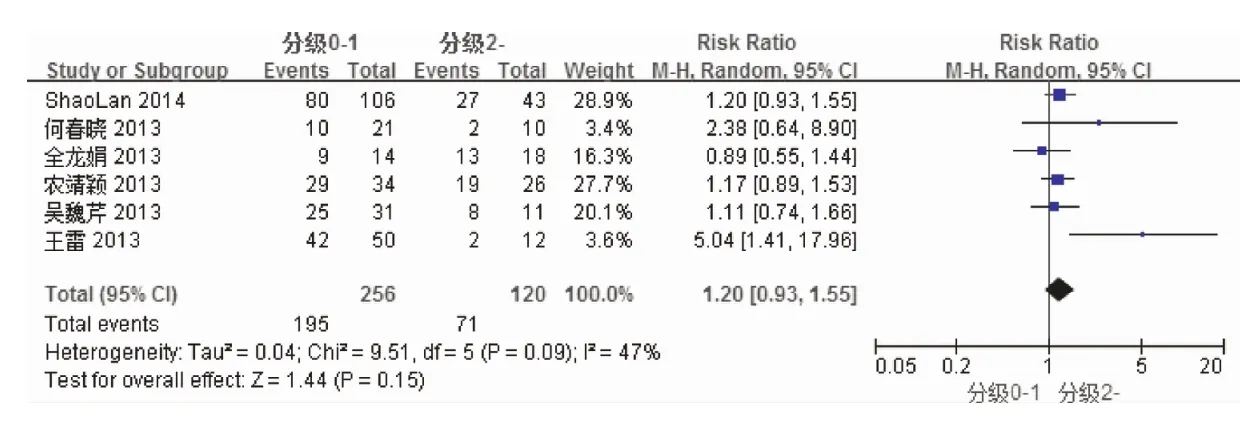
图4 ECOG评分0-1 vs ECOG评分2-4的森林图Fig.4 The forestmap of ECOG score 0-1 vs 2-4

图5 ECOG评分0-1 vs ECOG评分2-4的研究偏倚Fig.5 The study bias of ECOG score 0-1 vs 2-4
2.3.2 ECOG评分0~2 vs评分3~4:鉴于上述研究分组存在一定的偏倚,因此再进行评分0~2 vs评分3~4亚组分析,尽管RR=1.77,较上一亚组更高,同样表明研究存在一定的异质性和偏倚,但差异无统计学意义(见图6和图7)。因此,埃克替尼对晚期NSCLC的临床治疗效果,就当前的数据而言,ECOG评分的高低并无影响。
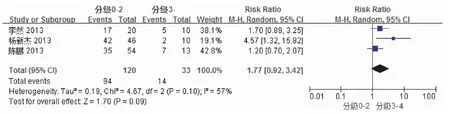
图6 ECOG评分0-2 vs ECOG评分3-4的森林图Fig.6 The forestmap of ECOG score 0-2 vs 3-4

图7 ECOG评分0-2 vs ECOG评分3-4的研究偏倚Fig.7 The study bias of ECOG score 0-2 vs 3-4
3 讨论
埃克替尼投入临床应用于治疗NSCLC仅十余年[11],鉴于临床治疗道德风险的存在,临床研究多为自身前后对照试验(before and after study in the same patient),因此,尽管纳入的研究没有随机对照试验(random control trial,RCT)方法的应用,通过隐藏、双盲、结局评价、非终点结局、挑选性报告和其他偏倚等的控制,纳入研究仍具有良好的可靠性[16]。
通过Revman的Meta分析,基于组织病理学类型,埃克替尼治疗NSCLC腺癌的临床效果优于鳞癌,合并效应优势比OR= 2.46,95%CI=1.49~4.08,P=0.0005(见图2和图3)。
ECOG评分包括2个亚组,分别是ECOG 0~1 vs ECOG 2~4(ECOG-1)和ECOG 0~2 vs ECOG 2~4(ECOG-2)。2个亚组都具有一定的异质性,合并效应分析均采用了随机条件下的M-H分析,结果分别是ECOG-1的RR=1.20,P=0.15;ECOG-2的RR=1.77,P=0.09;2个亚组的差异均无统计学意义(见图4、图5、图6和图7)。
纳入的单个研究或多或少地存在病例数较少的问题,因此,得出结论的正确性与可靠性因样本量偏低而存在一些问题[18],图2中的8个研究除第1个外,95%CI值均穿过中线1,表明单个的研究均不能从统计学角度说明埃克替尼治疗NSCLC腺癌比鳞癌具有优势,但合并效应的菱形偏离中线1较远(见图2),统计学角度可以认为埃克替尼治疗NSCLC腺癌比鳞癌具有一定优势,可能的原因是,这2种不同组织学类型的肿瘤起源于支气管粘膜上皮的不同细胞,对埃克替尼的敏感性存在一定的差异,因此,临床有效性也不相同;ECOG评分的依据仅仅是肿瘤患者的活动能力,存在一定的主观性,各研究之间存在一定差异,评分的高低也不一定能表达肿瘤的进展,也非肿瘤的临床分级,因此,无论是ECOG-1还是ECOG-2,Meta分析的结果均表明埃克替尼治疗NSCLC的临床有效性与ECOG评分无关(见图4和图6)。
埃克替尼从研发到投入临床应用仅十余年,能检索到的研究十分有限,鉴于临床研究中医疗道德风险的存在,研究设计均非随机,难免存在某些偏倚如选择性偏倚,这对Meta分析结果或多或少会有一定的影响。但是,事实上以组织病理学方法进行分类,选择性偏倚应当会相对较小,而选择性偏倚对ECOG评分的影响可能会更大一些。
与其他的表皮生长因子受体激酶为靶标的分子靶向药物相比,如吉非替尼和厄洛替尼等,埃克替尼对NSCLC的临床有效性毋庸置疑。但哪些因素会影响其有效性及其影响程度仍然值得今后进一步研究,这些因素包括患者个体生物学特征、肿瘤类型及其临床进展等诸多方面。
[1]Shi Y,Zhang L,Liu X,et al.Icotinib versus gefitinib in previously treated advanced non-small-cell lung cancer(ICOGEN):a randomised,double-blind phase 3 non-inferiority trial[J].Lancet Oncol,2013,14(10):953-961.
[2]Gu A,Shi C,Xiong L,et al.Efficacy and safety evaluation of icotinib in patients with advanced non-small cell lung cancer[J].Chin J Cancer Res,2013,25(1):90-94.
[3]Ren GJ,Zhao YY,Zhu YJ,et al.Tumor genemutations and messenger RNA expression:correlation with clinical response to icotinib hydrochloride in non-small cell lung cancer[J].Chin Med J(Engl),2011,124(1):19-25.
[4]农靖颖,秦娜,王敬慧,等.盐酸埃克替尼治疗晚期复发非小细胞肺癌的临床疗效[J].中国肺癌杂志,2013,16(5):240-245.
[5]李然,彭宗玉,任韶韶,等.盐酸埃克替尼治疗晚期非小细胞肺癌疗效观察[J].现代医药卫生,2013,29(15):2255-2259.
[6]Song Z,Yu X,Cai J,et al.Efficacy of icotinib for advanced non-small cell lung cancer patientswith EGFR status identified[J].Zhongguo Fei Ai Za Zhi,2013,16(3):138-143.
[7]Shao L,Zhang B,He C,et al.Efficacy and safety of icotinib in Chinese patients with advanced non-small cell lung cancer after failure of chemotherapy[J].Chin Med J(Engl),2014,127(2):266-271.
[8]Aiqin Gu,Chunlei Shi,Liwen Xiong,et al Efficacy and safety evaluation of icotinib in patients with advanced non-small cell lung cancer[J].Chin JCancer Res,2013,25(1):90-94.
[9]Yang G,Yao Y,Zhou J,et al.Effects of icotinib,a novel epidermal growth factor receptor tyrosine kinase inhibitor,in EGFR-mutated nonsmall cell lung cancer[J].Oncol Rep,2012,27(6):2066-2072.
[10]Li X,Yang XJ,Sun YF,et al.Clinical observation of icotinib hydrochloride for patients with advanced non-small cell lung cancer[J].Zhonghua Zhong Liu Za Zhi,2012,34(8):627-631.
[11]何春晓,张贝贝,郑蕾,等.盐酸埃克替尼治疗31例晚期鳞状细胞肺癌临床疗效分析[J].中国新药杂志,2013,22(12):1430-1433.
[12]石远凯.盐酸埃克替尼(凯美纳)中国临床使用经验专家共识[J].中国新药杂志,2012,21(6):578.
[13]陈鹏,李凯,王长利,等.埃克替尼治疗晚期非小细胞肺癌近期疗效及不良反应评价[J].肿瘤学杂志,2012,18(12):947-951.
[14]王雷,刘基巍,于佩瑶,等.盐酸埃克替尼治疗66例晚期非小细胞肺癌的临床研究[J].中国新药杂志,2013,22(16):1930-1941.
[15]吴魏芹,卢凯华,张梅玲,等.盐酸埃克替尼治疗晚期非小细胞肺癌的临床观察[J].中国肿瘤,2013,22(6):497-501.
[16]全龙娟,毛伟敏,徐长青,等.埃克替尼治疗胸腔积液为首发症状的34例晚期非小细胞肺癌观察[J].全科医学临床与教育,2013,11(4):422-423.
[17]杨新杰,张卉,秦娜,等.盐酸埃克替尼一线治疗晚期肺腺癌的临床疗效观察[J].中国肺癌杂志,2013,16(7):364-368.
[18]李幼平.循证医学[M].第2版.北京:高等教育出版社,2009,133-135.
(编校:吴茜,刘路路)
Effectiveness of icotinib in treatment of NSCLC:M eta analysis based on pathological type and ECOG score
LIAO Chu-xin,LIU Rui-feng,LIYun-jing,LU Rong-zhi,ZHAOWei-guo
(Department of Pharmaceutical,Zhongshan People's Hospital,Zhongshan 528403,China)
ObjectiveTo evaluate effectiveness of icotinib in treatment of differenthistopathological types of non small cell lung cancer(NSCLC)and ECOG.MethodsClinical trials research data about icotinib treatment of NSCLC of Chinese and English were collected and
.Meta-analyze with Revman5.2.ResultsAdenocarcinoma vs squamous cell carcinoma involved 8 studies.M-H analysiswith fixed effectwas OR=2.46,P=0.0005;ECOG score:0~1 vs 2~4 and 0~2 vs 3~4,the two subgroups included respectively 6 and 3 studies.There was heterogeneity,and combined effects of random effects M-H analysis were RR=1.20,P=0.15 and RR=1.77,P=0.09 respectively.Conclusion Icotinib of adenocarcinoma ismore effective than that in squamous cell carcinoma in the treatmentof NSCLC;ECOG score does notaffect the effectiveness of the treatment,butwe can still expand the sample for analysis.
icotinib;NSCLC;pathological type;ECOG score;clinical efficacy;Meta analysis
R319
A
1005-1678(2014)08-0110-04
中山市科技计划项目(20132A128)
廖础欣,女,本科,副主任药师,研究方向:临床药学的研究,E-mail:liaochuxinzs@163.com。

