不同化疗方案用于晚期结直肠癌治疗中的疗效比较
汪金云 邓文霞 王跃华
结直肠癌是临床常见的消化道恶性肿瘤,起病隐匿、早期诊断率低,远期预后差[1-2]。对于晚期转移性大肠癌,化疗是其标准的治疗手段。本实验对比应用替吉奥和卡培他滨联合奥沙利铂对晚期结直肠癌患者的临床治疗情况,并观察和比较2种方案的近期疗效和不良反应。
1 资料与方法
1.1 一般资料
连续选择从2008 年 2月至 2013 年 10 月来我院诊治的晚期结直肠癌患者41例,男性25例,女性16例,年龄 38~84岁,平均年龄(57±12)岁。所有患者均经病理学诊断为腺癌,经胸、腹部增强 CT 检查证实为肺、肝合并淋巴结转移,临床分期均为Ⅳ期。结肠癌23例,直肠癌18例;初治者27例,复治者14例;患者主要表现为肝、肺、腹腔多发性转移,其中肝转移26例,肺转移4例,腹腔淋巴结转移13例(其中合并肝、腹腔淋巴结转移2例)。治疗前无化疗禁忌证,ECOG PS 评分为0~2 分,具有可测量的病灶,预计生存时间≥3个月。所有患者均签署化疗知情同意书。将所有患者随机分为实验组(替吉奥联合奥沙利铂方案,n=21)和对照组(奥沙利铂联合卡培他滨,n=20)。
1.2 治疗方法
实验组:奥沙利铂100 mg/m2,静脉滴注,第1天。根据体表面积确定替吉奥,初始剂量:体表面积<1.25 m2,替吉奥胶囊40 mg/次,2次/天;体表面积1.25~1.5 m2,替吉奥胶囊50 mg/次,2次/天;体表面积 >1.5 m2,替吉奥胶囊60 mg/次,2次/天。对照组:奥沙利铂给药方法与实验组相同;卡培他滨2 500 mg/m2。2组药物均早、晚饭后口服,第1~14天,服用14天后停药7天;2组均为21天1个周期;每2个周期评价疗效,有效患者继续化疗,进展者更换其他方案。化疗期间监测血常规、肝肾功能、电解质。针对出现的血液学毒性,必要时给予升白细胞、升血小板及促红细胞生成治疗,出现Ⅳ度血液毒性时暂时停用化疗药物,待缓解后继续用药,但不补充停用药量;每位患者至少化疗2个周期。
1.3 评价标准
化疗 2 个周期后复查胸部、腹部 CT 增强扫描,以≥10 mm的肿瘤最大径之和对比基线片评价疗效。疗效评价采用 RECIST标准,疗效分完全缓解(CR)、部分缓解(PR)、稳定(SD)、进展(PD),客观有效率(ORR)为CR+PR,疾病控制率(DCR)为CR+PR+SD。肿瘤进展时间(TTP) 指化疗开始到肿瘤出现进展的时间。不良反应按 WHO 抗癌药物急性与亚急性不良反应表现及分级标准,分为0~Ⅳ级。
1.4 统计学处理
计数资料采用例数或百分比表示,采用卡方检验;所有数据均采用SPSS 17.0统计软件进行分析。
2 结果
2.1 基线资料比较
2组患者的年龄分别为(56±11)岁、(58±13)岁,差异无统计学意义(χ2=0.261,P=0.827);在性别、年龄、结肠癌比例、初治者比例及转移部位等方面,2组差异均无统计学意义(P>0.05)。见表1。
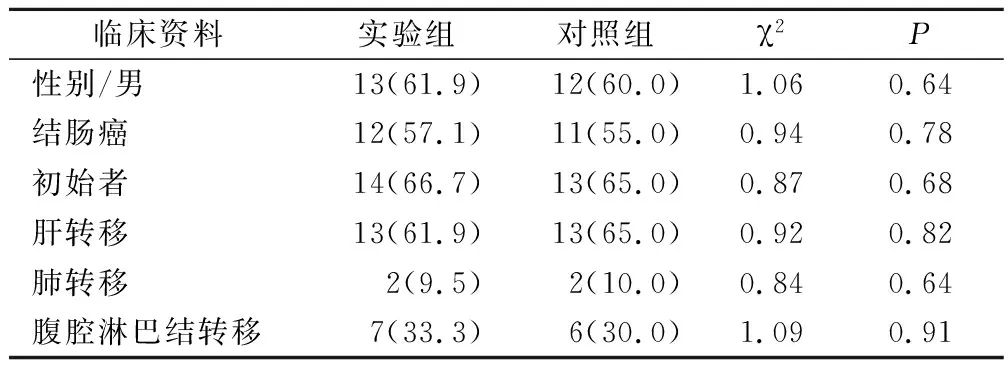
表1 2组患者的基线资料比较(例,%)
2.2 2组患者的近期疗效比较
2组患者治疗过程基本顺利,无1例患者因特殊情况(如严重感染、出血,白细胞严重下降药物无法纠正等)中断化疗,全部患者均可做疗效评价。2组均至少化疗5个周期,实验组患者中CR 2例,PR 10例,SD 5例,PD 4例,对照组分别为0,10,5,5例,2组患者的客观有效率(ORR)、疾病控制率(DCR)和中位进展期(mTTP)比较,差异均无统计学差异(ORR:57.50% vs 50.00%,χ2=0.282,P=0.595;DCR:82.50%vs77.78,χ2=0.180,P=0.671;mTTP:8.7 vs 7.9月,χ2=1.324,P=0.247)。
2.3 2组患者的不良反应比较
多数患者的不良反应发生在第3周期化疗后,以Ⅰ、Ⅱ级为主。不良反应有骨髓抑制、胃肠道反应(恶心呕吐、腹泻等)、肝肾功能受损、手足综合征及神经系统毒性等。实验组血小板减少发生率与手足综合征发生率均低于对照组,差异有统计学意义(P<0.05),见表2。
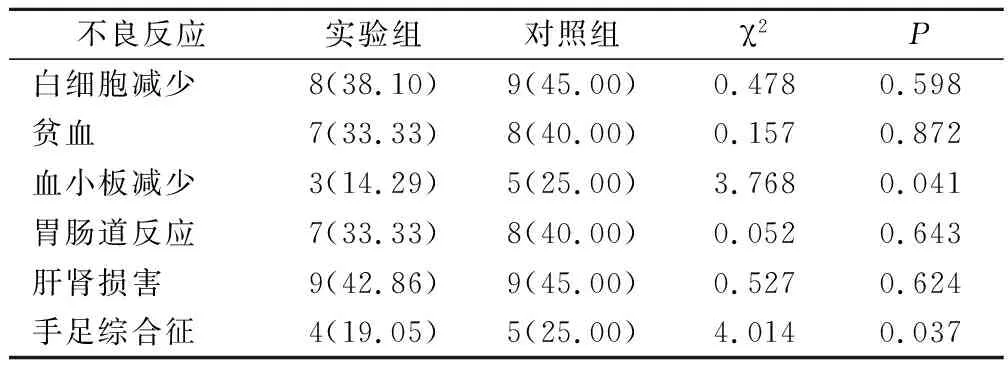
表2 2组患者的不良反应比较(例,%)
3 讨论
临床上确诊为结直肠癌的患者有 55%~63%已经发生转移,以肝、肺及腹腔淋巴结转移为最多,尽管肝、肺转移病灶可行手术切除,但远期预后比非手术治疗无较大提高,且患者多不愿意接受手术治疗,因此化疗仍是晚期结直肠癌患者的首选[3-4]。NCCN指南和我国大肠癌诊疗规范均推荐 FOLFOX、FOLFIRI、CapeOx联合妥昔单抗或CapeOx联合依贝伐珠单抗治疗方案作为一线治疗方案,其中CapeOx方案中包含口服的氟尿嘧啶类药物卡培他滨。卡培他滨是口服氟尿嘧啶甲氨酸酯剂,可经胸苷磷酸化酶降解为5-FU;替吉奥同为氟尿嘧啶类药物,其毒性约是氟尿嘧啶1/5,而化疗指数为氟尿嘧啶的2~3倍;吉美嘧啶是1种有效的5-FU降解酶抑制剂,可延长5-FU的作用时间;奥替拉西钾能够特异性抑制肠道黏膜细胞内乳清酸核糖转移酶,阻断5-FU的磷酸化,从而保护肠道黏膜[5-6]。
Hong等[7]对340例结直肠癌患者的Ⅲ期随机对照临床试验得出:应用替吉奥联合奥沙利铂(168 例)客观有效率为48%、中位进展时间为8.9个月(95%CI 7.8~9.4个月);应用卡培他滨联合奥沙利铂(172例)客观有效率为 35%、中位进展时间为6.4个月(95%CI 6.0 ~7.4个月);本实验通过2种方案的对照研究,发现替吉奥联合奥沙利铂组的客观有效率及疾病控制率均有增加的趋势,且中位进展时间有延长的趋势,血小板减少发生率与手足综合征发生率均显著低于奥沙利铂联合卡培他滨方案,与既往研究基本吻合[8]。该研究观察病例较少,观察时间不长,可能造成实验结果(如不良反应)有一定的偏差,但是仍可认定替吉奥联合奥沙利铂是晚期结直肠癌化疗的一种较好的选择,但其临床效果尚需大规模前瞻性临床试验进一步探索证实。
[1] Toda Y,Machida N,Boku N.The role of oral furopyrimidines in colorectal cancer treatment-a review〔J〕.Gan To Kagaku Ryoho,2010,37(7):1198-1202.
[2] 曹桂侠,程朝辉,周冬梅,等.替吉奥联合奥沙利铂治疗晚期胃癌的临床观察〔J〕.肿瘤基础与临床,2011,24(1):27-29.
[3] 谢 猛,马 福,李洪渊,等.替吉奥联合奥沙利铂治疗晚期大肠癌的临床观察〔J〕.中国癌症防治杂志,2013,5(2):159-161.
[4] 支波波,林雨冬,高 远,等.替吉奥联合奥沙利铂治疗胃癌伴肝转移1例报告〔J〕.实用癌症杂志,2012,27(1):82.
[5] 陈永昌,安 欣,张 乐,等.奥沙利铂辅助化疗失败后一线再引入治疗晚期结直肠癌的研究〔J〕.中国肿瘤临床,2012,39(13):927-931.
[6] 陆红梅,周鲁莲,刘金菊,等.替吉奥及卡培他滨联合奥沙利铂一线治疗晚期大肠癌的近期疗效比较 [J].肿瘤研究与临床,2012,24(9):613-615.
[7] Hong YS,Park YS,Lim HY,et al.S-1 plus oxaliplatin versus capecitabine plus oxaliplatin for first-line treatment of patients with metastatic colorectal cancer:a randomized,noninferiority phase 3 trial〔J〕.Lancet Oncol,2012,13(11):1125-1132.
[8] 李智强,王小龙.替吉奥胶囊联合奥沙利铂治疗晚期及复发性大肠癌的疗效观察〔J〕.实用癌症杂志,2012,27(2):208.

