天然气净化装置胶状堵塞物形成原因与机理研究①
颜晓琴 何培东 何金龙 郑 斌 李富元 唐 浠 涂陈媛
(1.中国石油西南油气田公司天然气研究院)
(2.中国石油西南油气田公司重庆天然气净化总厂)
(3.中国石油西南油气田公司开发部 4.中国石油西南油气田公司川中油气矿)
在天然气净化过程中,净化装置的原料气过滤器、吸收塔盘表面、胺液过滤器等部位经常会出现胶状堵塞物。这些胶状物可能堵塞吸收塔,影响气液正常流动,导致净化装置运行参数出现不同程度的波动,从而影响装置能耗及产品气质量。堵塞物较少时,工艺参数波动不大,产品气中H2S质量浓度虽有所增加,但通过调整装置操作参数仍可将其控制在20 mg/m3以下;当堵塞物较多时,吸收塔压差将大幅度增加,大量液体积聚在吸收塔内,无法实现正常的溶液循环,导致装置操作困难,处理量下降,产品气中H2S质量浓度超标,严重时频繁发生吸收塔拦液及冲塔,装置被迫停产清洗[1-3]。为此,针对胶状堵塞物的形成原因开展研究非常必要。
1 胶状堵塞物性状与组成
在运行出现问题的天然气净化装置中采集到的堵塞物样品为半固体状胶质,与果冻相似,颜色为黑色,但在空气中暴露一段时间后外层会变成灰白色,如图1所示。堵塞物在水中仍保持半固体状,在酸溶液中转变为液体,见图2和图3。
对胶状堵塞物组成的分析结果表明,吸收塔、胺液过滤器等部位的胶状堵塞物主要由水、甲基二乙醇胺、长链羧酸混合物、长链烃混合物、三甘醇、炭、硫化亚铁和钠盐等8种组分构成。表1是龙岗天然气净化厂净化装置中胶状堵塞物的样品分析结果,虽然来自万州、忠县、磨溪、垫江等净化厂的胶状堵塞物样品还分别含有酰胺、长链醚、磷酸酯等其他组分,但这些胶状堵塞物样品共有的组分是以上8种。取自原料气过滤器的黑色胶状堵塞物样品中不含甲基二乙醇胺,炭含量很低甚至没有,但同样含有长链羧酸、长链烃、三甘醇、硫化亚铁和钠盐。



分离去除胶状堵塞物样品中的硫化亚铁和炭粉后,所有样品的颜色变为浅黄色或无色,可见堵塞物呈黑色主要是因为胶状物中分散着硫化亚铁或炭等黑色微粒。硫化亚铁在空气中可能发生氧化并生成硫。因此,黑色堵塞物暴露在空气中会逐渐变成灰白色。
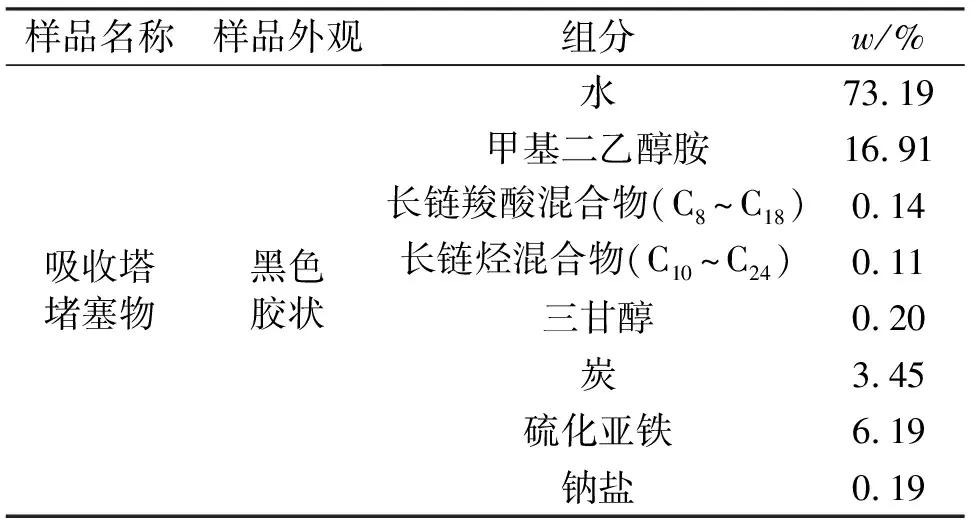
表1 龙岗天然气净化厂净化装置中堵塞物样品组成分析结果
2 胶状物形成原因研究
2.1 实验部分
2.1.1实验材料
甲基二乙醇胺(优等品)、十八烷酸(分析纯)、十六烷酸(分析纯)、十二烷酸(分析纯)、异辛酸(分析纯)、柴油、三甘醇(优等品)、硫化亚铁(粉状)、氯化钠(分析纯)、氢氧化钠(分析纯)、盐酸溶液(3 mol/L)。
长链羧酸混合物由十八烷酸、十六烷酸、十二烷酸、异辛酸等比例(w)混合制成。
2.1.2实验方法
在室温下,按表1分析结果配制16.91%(w)的甲基二乙醇胺水溶液,在此水溶液中分别添加长链羧酸混合物、柴油(长链烃)、三甘醇、硫化亚铁、氯化钠及其混合物,各种物质的添加量与表1分析结果中相应组分的质量分数相同,将溶液混合均匀并使其静置一定时间后观察是否有胶状物形成。
通过以上实验明确导致胶状堵塞物形成的关键组分后,改变关键组分的浓度、溶液温度和酸度,重复上述实验,研究组分浓度、温度与酸度对胶状物形成的影响。
2.2 实验结果及讨论
2.2.1形成胶状物的关键组分
单组分实验结果:在甲基二乙醇胺水溶液中单独添加长链羧酸混合物、柴油、三甘醇、硫化亚铁和氯化钠5种化学物质中的任意一种,溶液静置12 h后均无胶状物形成。加大各化学物质的添加量后重复实验,仍无胶状物形成。
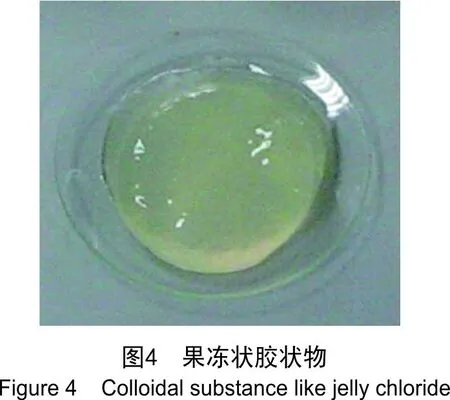
双组分实验结果:添加了长链羧酸混合物与氯化钠的甲基二乙醇胺水溶液,静置约2 min后,溶液全部胶凝并失去流动性,形成像果冻一样的胶状物,见图4。其余物质两两混合后添加在胺液中未形成胶状物。将氯化钠换成氢氧化钠重复实验,得到相同的实验结果。在甲基二乙醇胺水溶液中添加硫化亚铁粉末后再加入长链羧酸与氯化钠,会形成黑色胶状物,见图5。

多组分实验结果:在甲基二乙醇胺水溶液中添加长链羧酸混合物、柴油、三甘醇、硫化亚铁和氯化钠,溶液混合均匀后静置约2 min就全部发生胶凝并失去流动性,形成黑色胶状物。在甲基二乙醇胺水溶液中添加除长链羧酸混合物以外的其余4种物质,或添加除氯化钠以外的其余4种物质,溶液静置12 h后无胶状物形成。
加料顺序实验结果:在水中先加入长链羧酸混合物、氯化钠,再加入甲基二乙醇胺,在加入甲基二乙醇胺前长链羧酸不溶解,溶液也不胶凝。加入甲基二乙醇胺后长链羧酸逐渐溶解,同时,溶液也逐渐发生胶凝。将氯化钠改为氢氧化钠后重复实验,溶液未加入甲基二乙醇胺长链羧酸时就已溶解并发生胶凝。
以上实验结果表明,长链羧酸混合物与钠盐同时存在于醇胺溶液中时,溶液会发生胶凝并形成胶状物。将氯化钠改为氢氧化钠后,溶液仍能形成胶状物,说明钠盐中的阴离子不是决定胶状物是否形成的关键因素,决定胶状物形成的关键因素是钠离子。在水中加入甲基二乙醇胺和长链羧酸混合物无胶状物形成,但在水中加入氢氧化钠和长链羧酸混合物则有胶状物形成,说明形成胶状堵塞物的关键组分是长链羧酸钠。长链羧酸不溶于水,在水中不能电离出长链羧酸根与氯化钠生成长链羧酸钠,故在水中加入长链羧酸和氯化钠无胶状物形成。加入甲基二乙醇胺与长链羧酸先生成长链羧酸胺,长链羧酸胺电离出长链羧酸根再与钠离子生成长链羧酸钠,才使溶液发生胶凝生成胶状物。
前述5个天然气净化厂的原料气过滤器中也出现了黑色胶状物,这些黑色胶状物样品中有更高浓度的长链羧酸混合物与钠盐,所以不难推测出长链羧酸混合物是原料天然气带入净化装置的污染物。
2.2.2长链羧酸种类及其浓度的影响
将长链羧酸混合物依次改为单一的异辛酸、十二烷酸、十六烷酸、十八烷酸后重复双组分实验,各种长链羧酸的添加量从0.005%(w)至1%(w)逐渐增大,钠离子的摩尔分数与长链羧酸的摩尔分数相等,实验结果见表2。
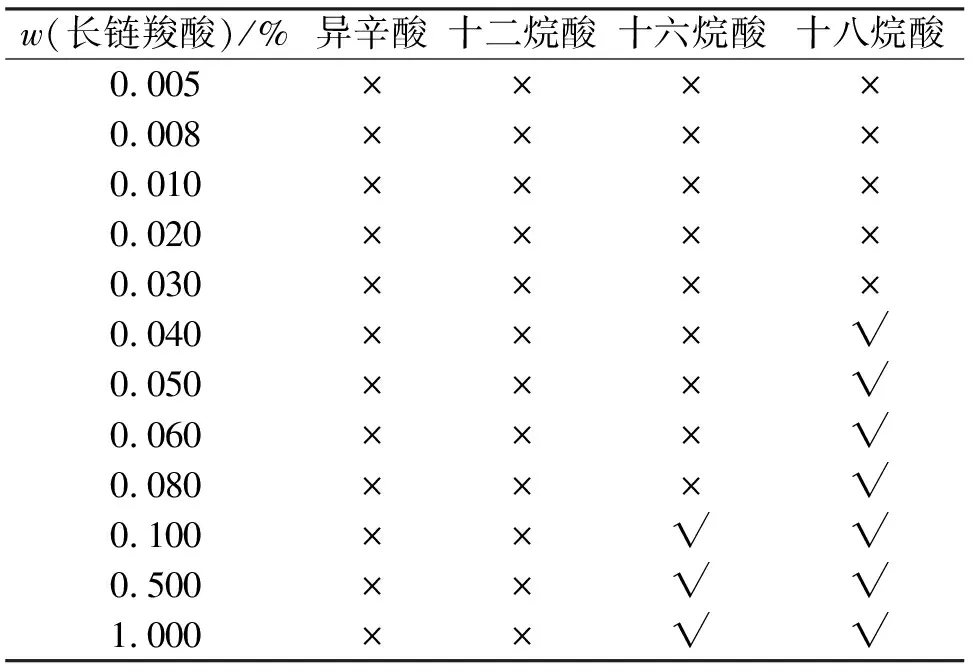
表2 长链羧酸种类及其浓度影响实验结果
表2所示实验结果表明,长链羧酸使溶液全部发生胶凝的最低浓度与长链羧酸分子的烷基碳原子数相关。长链羧酸分子的烷基碳原子数越多,使溶液全部发生胶凝所需的浓度越低。溶液中钠离子的摩尔分数与长链羧酸摩尔分数相等时,C16羧酸根、C18羧酸根质量分数分别达到0.100%、0.040%就能使醇胺溶液全部发生胶凝,C8羧酸、C12羧酸不能形成胶状物。钠离子过量时,长链羧酸使醇胺溶液全部发生胶凝所需的浓度会降低。例如:当醇胺溶液中钠离子质量分数增大至1%时,加入0.050%(w)的C16羧酸或0.020%(w)的C18羧酸就能使溶液全部发生胶凝。C12羧酸只有在钠离子浓度过量时才能形成胶状物:在含2.3%(w)钠离子的醇胺溶液中加入0.100%(w)的C12羧酸后,溶液会全部发生胶凝。但是,即使醇胺溶液中钠离子质量分数达到5%,C8羧酸也不能使溶液形成胶状物。
溶液中的长链羧酸钠分子有相互逐渐靠近的趋势,这种趋势能使低浓度的长链羧酸钠水溶液局部达到形成胶状物的条件。例如,在含80×10-6(w)C16羧酸的甲基二乙醇胺水溶液中添加200×10-6(w)的氯化钠并混合均匀,静置较长的时间(约8 h)后,在溶液中间出现一小团悬浮着的胶状物,见图6,继续静置溶液,胶状物的体积没有进一步增大。

2.2.3温度与酸度的影响
实验结果表明,当温度升至70~80 ℃时,胶状物会转变成水溶液;当温度降至60 ℃时,溶液中开始出现胶状物,降至40 ℃时溶液全部发生胶凝。pH值低于6时,胶状物也会“融化”为水溶液,说明升温和增大酸度都能破坏长链羧酸根与钠离子形成的胶状物。
综上所述,长链羧酸钠是形成胶状堵塞物的关键组分,溶液中长链羧酸钠的浓度越高,溶液温度越低,就越容易形成胶状堵塞物。吸收塔与富胺液过滤器中的胺液温度约40 ℃,原料天然气中携带的长链羧酸、钠盐首先进入吸收塔。因此,吸收塔胺液中长链羧酸根、钠离子浓度往往很高。再生塔内胺液温度在100 ℃以上,且胺液中的胶状物经过吸收塔塔盘和富胺液过滤器两级拦截后,能进入再生塔的胶状物量较少,故再生塔中基本未出现胶状堵塞物。
3 胶状物形成机理研究
3.1 实验部分
3.1.1实验材料
甲基二乙醇胺(优等品)、十六烷酸(分析纯)、氯化钠(分析纯)、氯化钙(分析纯)、氯化镁(分析纯)、氯化钡(分析纯)。
3.1.2实验方法
离浆实验:用含0.1%(w)C16羧酸的甲基二乙醇胺水溶液与氯化钠制成胶状物后,静置1周,观察胶状物的外观变化。
丁达尔效应实验:在含80×10-6(w)C16羧酸的甲基二乙醇胺水溶液中添加200 ×10-6(w)氯化钠并混匀,在暗处将一束强光射入溶液,观察是否出现一条明亮的光带。
Ca2+、Mg2+、Ba2+实验:在含0.1%(w)C16羧酸的甲基二乙醇胺水溶液中分别添加氯化钙、氯化镁、氯化钡水溶液,将溶液混合均匀并静置后,观察是否有胶状物形成。
3.2 胶状物形成机理分析
在离浆实验中观察到的现象是:随着时间的延长,长链羧酸钠盐形成的胶状物逐渐分离出一部分液体,但其形状未变,只是体积变小,即出现离浆现象。可见长链羧酸钠形成的胶状物具有凝胶的特点:含有大量液体,呈半固体状,放置一段时间后出现离浆现象。溶液形成凝胶需要满足以下条件:①质点在溶液中的溶解度低,能以胶体分散状态析出;②析出的质点相互作用形成空间网状结构,质点间的吸引力与排斥力的大小必须处于一个适当的平衡点,吸引力过大,质点会聚集形成沉淀或不溶悬浮物,排斥力过大则会分散。
长链羧酸钠的以下性质使其具备了形成凝胶的条件:
(1) 长链羧酸钠在水中的溶解度低,能以胶体分散状态析出。在丁达尔效应实验中,强光射入长链羧酸钠溶液时,溶液中出现一道明亮的光带,如图7所示,说明C16羧酸钠盐析出,形成了既不溶于水又不发生沉降的胶体微粒。

(2) 长链羧酸钠分子能形成胶束。分子间的范德华力与分子量成正比,单个长链羧酸钠分子分子量小,分子间的范德华力较弱,不足以束缚住各质点形成稳定的网状结构。长链羧酸钠分子形成胶束后,由于胶束“分子量”大,胶束间产生较强的作用力从而相互吸引连接成网。C16羧酸钠和C18羧酸钠的临界胶束浓度分别为550×10-6(w)和126×10-6(w)[3],低于使溶液全部发生胶凝所需的最低浓度,说明溶液中的长链羧酸钠分子先形成胶束,然后以胶束为质点构成网状结构。较大的胶束更容易形成网状结构,胶束大小的量度是胶束聚集数。长链羧酸钠的胶束聚集数与其分子上烷基的碳原子数成正比,例如C10羧酸钠、C12羧酸钠、C16羧酸钠在0.013 mol/L NaBr水溶液中的胶束聚集数依次为38、56和170,胶束“相对分子质量”依次为7 400、12 400和47 300[4]。C16羧酸钠胶束比C12羧酸钠胶束大得多,所以C16羧酸钠更容易形成胶状物。C8羧酸钠浓度很高,也不能形成胶状物,正是因为其形成的胶束“相对分子质量”不够大,胶束间的范德华力不足以束缚住各质点。胶束的形状有球状、棒状、蠕虫状、碟形等等[5-8],棒状或蠕虫状的胶束更易搭成网架。无机盐的阳离子能显著降低长链羧酸盐的临界胶束浓度,增加胶束的不对称性并使其变为棒形[4],故钠离子过量后,会降低长链羧酸形成胶状物所需的浓度。
(3) 长链羧酸钠可部分电离,使胶束表面带电。长链羧酸钠胶束间如果只有吸引力,那么各质点会逐渐聚集,并以沉淀的形式析出。由于长链羧酸钠盐能部分电离使胶束表面带一定量的负电荷,各胶束因带相同电荷而互相排斥,阻止了质点进一步聚集形成沉淀。Ca2+、Mg2+、Ba2+实验结果表明,Ca2+、Mg2+、Ba2+与长链羧酸会形成沉淀,不能形成胶状物。长链羧酸与Ca2+、Mg2+、Ba2+形成的盐难以发生电离,其胶束表面的电荷量小,胶束间的排斥力弱,无法阻止质点进一步聚集形成沉淀。曹绪龙等人计算了Na+、Ca2+、Mg2+与C12羧酸的结合能依次为95 kJ/mol、193 kJ/mol、198 kJ/mol[9],Na+与C12羧酸的结合能明显低于Ca2+、Mg2+与C12羧酸的结合能,意味着C12羧酸的钠盐比其钙、镁盐更易电离,故C12羧酸钠形成的胶束带有更高的电荷。但胶束带的电荷量也不能太大,长链羧酸与甲基二乙醇胺形成的盐几乎完全电离,胶束表面的电荷量大使胶束间的排斥力大于吸引力而分散,表现出溶解的状态。
综上所述,净化装置中胶状堵塞物的形成过程应为:醇胺脱硫溶液中的C12及C12以上的长链羧酸钠形成胶束后,胶束“相对分子质量”达到10 000以上[4],胶束间的范德华力足够大,不断拉近各胶束使其相互连接;另一方面,长链羧酸钠部分电离,使胶束表面带负电,各胶束因带相同电荷而相互排斥,阻止胶束进一步聚集。当胶束间的排斥力与吸引力达到平衡时,胶束不再自由运动,被束缚在相对固定的位置,形成立体三维网状结构,将水溶液包住并使其失去流动性,呈半固体状。
长链羧酸钠的碳链越长,其临界胶束浓度越低,形成的胶束“相对分子质量”也越大,所以碳链越长的羧酸钠越易形成胶状物,其形成胶状物所需浓度也越低。溶液温度升高时,分子的热运动加剧,长链羧酸钠在水中的溶解度增大,网状结构上的质点因为剧烈热运动或溶解而离开原有的固定位置,使网状结构瓦解。因此,出现胶状物被破坏的现象。盐酸与长链羧酸钠反应生成难电离的长链羧酸,各质点间的排斥力减小而聚集析出,网状结构因此被破坏,表现为胶状物“融化”为水溶液。
4 结论与建议
(1) 取自不同天然气净化装置、净化装置不同部位的胶状堵塞物样品均含有长链羧酸混合物、长链烃、三甘醇、硫化亚铁和钠盐。
(2) 在甲基二乙醇胺水溶液中加入长链羧酸和氯化钠,或在水中加入长链羧酸和氢氧化钠,均观察到溶液胶凝形成胶状物。温度升至70 ℃以上或加入酸使pH值降至6以下时,胶状物被破坏并转变为水溶液。
(3) 长链羧酸钠的碳链足够长,且其在溶液中的浓度大于其临界胶束浓度时才能形成胶状物。长链羧酸的钙、镁、钡盐均不能形成胶状物。
(4) 除去胺液中的长链羧酸根或钠离子可以防止胶状堵塞物的形成。长链羧酸不仅会与钠离子形成胶状堵塞物,它与醇胺形成的胺盐还会导致脱硫溶液发泡。因此,有必要开发一种能在线脱除胺液中长链羧酸盐的技术,以保障净化装置的平稳、高效运行。
参考文献
[1] 王隆,汪忖理. 甲基二乙醇胺选择性脱硫技术在川东天然气净化总厂的应用[J]. 石油与天然气化工,1994,23(4):201-204.
[2] 王宪堂,常宏岗. 川东天然气净化总厂引进分厂脱硫溶液污染原因的探讨[R]. 泸州:四川石油管理局天然气研究所,1995.
[3] 赵国玺. 表面活性剂物理化学[M]. 北京:北京大学出版社,1991.
[4] 沈钟,王果庭. 胶体与表面化学[M]. 北京:化学工业出版社,1997.
[5] Wang Wei, Shlomo Efrima, Oren Regev. Directing silver nanoparticles into colloid-surfactant lyotropic lamellar systems[J]. J Phys Chem B, 1999, 103(27) : 5613-5615.
[6] Zhang Zhiqiang, Ramesh C Patel, et al. Stable silver clusters and nanoparticles prepared in polyacrylate and inverse micellar solutions[J]. J Phys Chem B, 2000, 104(6): 1176-1178.
[7] Antonietti M. Surfactants for novel templating applications[J]. Curr Opin Colloid Interf Sci, 2001(6): 244-247.
[8] Zhang Mingfu, Markus Drechsler, Axel H E Müller. Template-controlled synthesis of wire-like cadmium sulfide nanoparticle assemblies within core-shell cylindrical polymer brushes[J]. Chem Mater, 2004(16): 537-581.
[9] 曹绪龙,吕凯,等. 阴离子表面活性剂与阳离子的相互作用[J]. 物理化学学报,2010,26(7):1959-1964.

