正骨洗剂的质量标准研究
桂林医学院附属医院药学部,广西 桂林 541001
正骨洗剂的质量标准研究
蔡小玲秦贻强陈越
桂林医学院附属医院药学部,广西 桂林 541001
目的建立正骨洗剂的质量标准。方法用薄层色谱法定性鉴别制剂中的牡丹皮、防风、当归、续断,用高效液相色谱法测定制剂中丹皮酚的含量。结果TLC法可鉴别制剂中的牡丹皮、防风、当归、续断;HPLC法定量测定丹皮酚在0.043~0.428μg范围内线性关系良好,相关系数为r=0.9999,平均回收率为99.22%,RSD=0.70%。结论本法简便,准确,可作为本品重要的质量控制指标。
正骨洗剂;TLC;HPLC;丹皮酚
正骨洗剂是我院骨外科的中药验方,由牡丹皮、防风、当归、续断等11味中药提取精制而成。多年的临床应用研究证实,该洗剂具有舒筋活络,消肿止痛,活血祛瘀的功效,用于跌打扭伤、各种骨折、关节肿痛、脱臼、软组织损伤、瘀血等具良好效果;并对风湿骨痛具有较好的防治效果。本课题组对本洗剂进行深入研究,开发成医疗机构中药民族药正骨洗剂,不仅能使住院病患及时方便地用药,也为门诊患者提供优良的便于携带、使用的中成药制剂,发挥中医药在风湿骨伤方面的优势作用。为了控制本品质量、确保其临床疗效,本文对其质量标准进行了系统研究,采用薄层色谱法[1]建立了牡丹皮、防风、当归、续断的薄层色谱鉴别,并对制剂中牡丹皮的主要活性成分丹皮酚进行含量测定[2-4],本法操作简便、快速、结果准确,可用于该制剂的质量控制。
1 仪器与试药
日本岛津AEL2-200型电子天平;日本岛津LC-20AT型HPLC仪;威玛龙色谱工作站。丹皮酚对照品(批号:0708-9704,中国药品生物制品检定所);牡丹皮对照药材、防风对照药材、当归对照药材、续断对照药材均有中国药品生物制品检定所提供;正骨洗剂及各阴性样品均由桂林医学院附属医院提供。甲醇为色谱纯;水为超纯水;其余试剂均为分析纯。
2 方法与结果
2.1 定性鉴别
2.1.1 牡丹皮的鉴别 牡丹皮主要成分有酚类及酚苷类、单萜及单萜苷类、三萜、甾醇及其苷类、黄酮、有机酸、香豆素等[5],其中丹皮酚等主要有效成分易溶于低极性的有机溶剂,故采用乙醚作为提取溶剂。取本品20ml,加入乙醚充分振摇,提取2次,每次20ml,合并乙醚提取溶液,挥干,残渣加入丙酮1ml使其溶解,作为供试品溶液。另取牡丹皮对照药材1g,加乙醚10ml,超声处理10min,滤过,滤液挥干,残渣加入丙酮1ml使其溶解,制成对照药材溶液。再取丹皮酚对照品适量,加丙酮制成每1ml含1mg的对照品溶液。吸取上述三种溶液各10μl,分别点于同一以羧甲基纤维素钠为黏合剂的硅胶G薄层板上,以环己烷-乙酸乙酯-冰乙酸(4∶1∶0.1)为展开剂,展开,取出晾干,喷以2%香草醛硫酸乙醇溶液,加热至斑点显色清晰。供试品色谱中,在与对照品及对照药材色谱相应的位置上,显相同颜色的斑点,阴性无干扰。见图1。
2.1.2 防风的鉴别 防风主要含挥发油、色原酮类、香豆素类、多糖类等成分[6]。其中其主要成分多能溶于丙酮,故采用丙酮为溶剂。将供试品蒸干用丙酮溶解作为供试品溶液,对照药材用丙酮超声提取,经试验以硅胶G薄层板,三氯甲烷-甲醇 (4∶1)为展开剂,展开,置紫外光灯(365mn)下检视。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的荧光斑点,阴性无干扰。见图2A。
2.1.3 当归的鉴别 当归的主要有效成分挥发油及有机酸均易溶于极性低的有机溶剂。经试用乙醚,乙酸乙酯及三氯甲烷等提取,结果以乙醚提取效果最好。取本品20ml,加入乙醚充分振摇,提取2次,每次20ml,合并乙醚提取溶液,挥干,残渣加甲醇1ml使其溶解,作为供试品溶液。另取当归对照药材1g,加入乙醚10ml,超声处理10min,滤过,滤液挥干,残渣加甲醇1ml使溶解,作为对照药材溶液。吸取上述二种溶液各10ml,分别点于同一以羧甲基纤维素钠为黏合剂的硅胶G薄层板上,以正己烷-乙酸乙酯(8.5 ∶1.5)为展开剂,展开,取出,晾干,置紫外光灯(365mn)下检视。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的荧光斑点,阴性无干扰。见图2B。
2.1.4 续断的鉴别 续断主要含环烯醚萜糖苷及挥发油。糖苷类易溶于正丁醇,故供试品溶液采用水饱和正丁醇溶液振摇提取。取本品20ml,加入水饱和正丁醇溶液充分振摇,提取2次,每次20ml,合并正丁醇溶液提取溶液,水浴蒸干,残渣加甲醇1ml使其溶解,作为供试品溶液。另取续断对照药材1g,加甲醇10ml,超声处理20min,滤过,滤液蒸干,残渣加甲醇1ml使其溶解,作为对照药材溶液。吸取上述三种溶液各10ml,分别点于同一以羧甲基纤维素钠为黏合剂的硅胶G薄层板上,以正丁醇-乙酸-水(4∶1∶5)上层溶液为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液,加热至斑点显色清晰。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的斑点,阴性无干扰。见图2C。
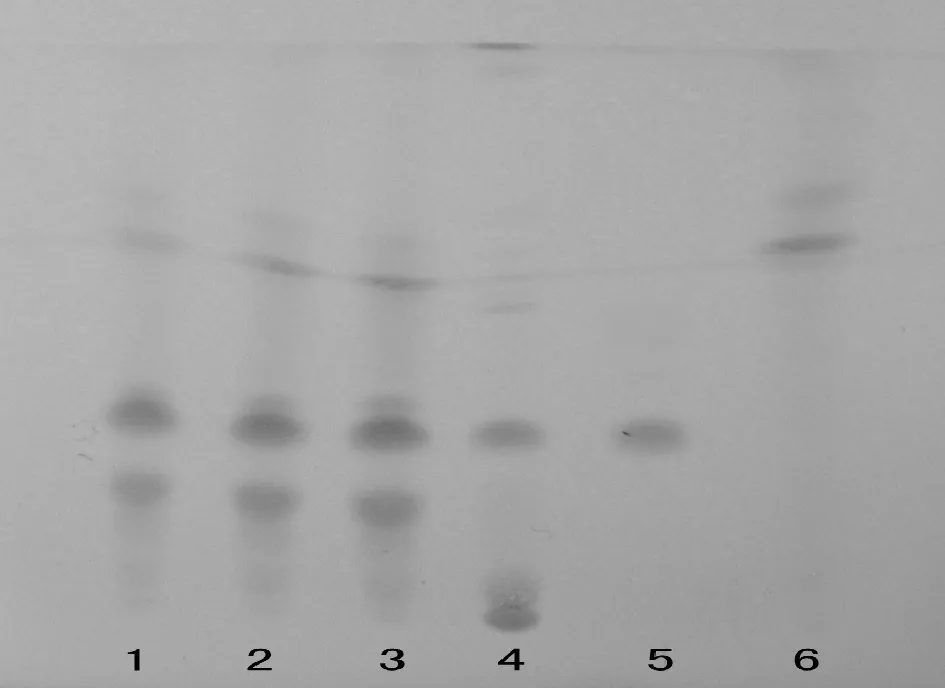
1,2,3样品(sample) 4对照药材(reference crude herb) 5对照品(reference) 6阴性样品(negative sample)

防风 当归 续断1,2,3样品(sample) 4 对照药材(reference crude herb) 5 阴性样品(negative sample)
2.2 丹皮酚的含量测定
2.2.1 色谱条件 Shim-pack VP-ODS色谱柱(4.6 mm×150 mm,5μm),流动相:甲醇-水(60 ∶40);检测波长:274 nm;柱温:室温,进样量为10μl。理论板数按丹皮酚峰计算,不低于2000。
2.2.2 对照品溶液的制备 精密称取丹皮酚对照品适量,加80%甲醇溶液制成每1ml含20μg的溶液,即得。
2.2.3 供试品溶液的制备 精密量取本品10ml,置50ml量瓶中,加甲醇适量,超声处理(功率250W,频率33kHz)15min,放冷,加甲醇至刻度,摇匀,取上清液,滤过,取续滤液,即得。
2.2.4 阴性样品溶液的制备 取缺牡丹皮的阴性样品,照“2.2.3”项下方法制备,即得。
2.2.5 系统适应性试验 精密吸取丹皮酚对照品溶液、供试品溶液及阴性样品溶液各10μl,注入HPLC仪,记录色谱图,结果在阴性样品色谱图中,在丹皮酚出峰位置没有吸收峰,表明阴性样品对测定无干扰,在供试品色谱图中,丹皮酚与相临峰分离度>1.5,理论塔板数符合要求。对照品、样品和阴性样品溶液的色谱见图3。
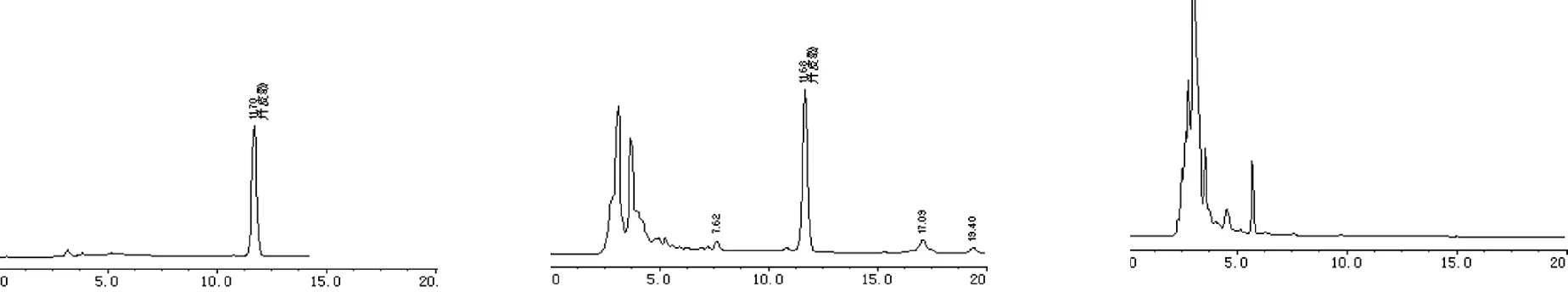
A 对照品 B 样品 C 阴性样品
2.2.6 线性关系考察 分别精密量取浓度为42.8μg·ml-1的丹皮酚80%甲醇的对照品溶液1、2、3、5、10 ml,分别置10 ml量瓶中,加80%甲醇溶液稀释至刻度,摇匀,分别作为对照品溶液(浓度分别为4.28、8.56、12.84、21.40、42.80μg·mL-1)。按上述的色谱条件分别进样10μl,测定。以进样量(μg)为横坐标,峰面积为纵坐标绘制标准曲线,线性回归方程为: Y=4.149×106X - 6.013×103(r=0.999 9),结果表明:丹皮酚在 0.043~0.428μg范围内线性关系良好。
2.2.7 精密度试验 对同一对照品溶液,连续测定6次,6次测定峰面积的RSD=0.67%,试验表明,仪器精密度良好。
2.2.8 重复性试验 对同一供试品(20130201)平行测定6份,6份测定结果的平均值为104.6μg·mL-1,RSD =0.61%(n=6)。结果表明,本法的重复性良好。
2.2.9 稳定性试验 制备同一供试品溶液后,以0、1、2、4、6、8、12 h分别精密吸取10μl测定一次,峰面积积分值RSD=0.92%。试验表明,在12h内供试品溶液稳定。
2.2.10 加样回收率试验 精密量取已知丹皮酚含量为104.6μg·ml-1的供试品5 ml,置50 ml量瓶中,平行取6份样,分别精密加入5 ml水和10 ml浓度为53.6μg·ml-1的丹皮酚对照品甲醇溶液,加甲醇适量,超声处理(功率250 W,频率33 kHz)15min,放冷,加甲醇至刻度,摇匀,取上清液,滤过,取续滤液测定,计算回收率,结果平均回收率为99.22%,RSD =0.70%(n=6),符合定量分析的要求。
2.2.11 样品测定 按上述的含量测定方法,测定了本品5批样品中的丹皮酚含量,结果5批样品平均含量91.2μg·ml-1,含量最高为110.5μg·ml[-1],最低74.2μg·ml-1。
3 讨论
3.1 通过对正骨洗剂质量标准进行系统研究,建立牡丹皮、防风、当归、续断等4个专属性强的薄层色谱鉴别。对处方中红花、桂枝等进行了鉴别研究,色谱斑点清晰,结果因重现性较差,未收入标准。另外对川芎、没药等进行了鉴别研究,结果色谱斑点清晰,但阴性有干扰,未收入标准。
3.2 本品为洗剂,水为溶剂,在含量测定供试液制备过程中,曾试验用乙醚对供试品进行萃取,乙醚挥干用甲醇溶解作为供试品溶液,相对于本法采用的供试品溶液制备方法具有去除杂质效果更好的优点,但本法采用的方法更简便、避免了萃取的繁杂操作和多次萃取及转移可能带来的误差,并且色谱图中丹皮酚和相临杂峰分离良好,无干扰,符合定量分析的要求。
3.3 复方中药制剂的质量控制是一个系统的评价过程,建立全面的TLC鉴别和适当的含量测定方法,能够较全面地控制复方中药制剂的质量[7]。
[1] 高冠喜,董宙.中药质量标准化与中药现代化发展的探讨[J].中国医药导报,2010,30(2):76-77.
[2] 孙瑛蔚,徐芝育.高效液相色谱法测定蒲黄止血口服液中丹皮酚的含量[J].吉林中医药,2010,30(2):172.
[3] 刘智生,李嘉,黄建猷. 乳康酊的薄层鉴别及丹皮酚的含量测定[J].中国实验方剂学杂志,2011,17(2):50-52.
[4] 吴振宇,王书婷,蒋英,等.HPLC法对舒新片中丹皮酚的含量测定[J].现代生物医学进展,2012,12(30):5930-5932.
[5] 王祝举,唐力英,赫炎.牡丹皮的化学成分和药理作用[J].国外医药:植物药分册,2006,21(4):155-159.
[6] 窦红霞,高玉兰.防风的化学成分和药理作用研究进展[J].中医药信息,2009,26(2):15-17.
[7] 王峥涛.中药质量标准研究进展与展望[J].中国天然药物,2006,4(6):404-409.
ResearchonthemethodofcontrolingqualityinBonesettingLotion
CAI Xiao-ling QIN Yi-qiang CHEN Yue
Department of Pharmacology, The Affiliated Hospital of Guilin Medical College, Guilin 541004,China
ObjectiveTo establish the standard of quality for Bone setting Lotion.MethodsTLC was adopted to identify Cortex moutan Radicis,Radix sileris,Angelica and Radix Dipsaci, and HPLC was adopted to determine the content of paeonol in Bone setting Lotion.ResultsCortex moutan Radicis,Radix sileris,Angelica and Radix Dipsaci could be identified by TLC. The linear range of Paeonol was 0.043~0.428 mg(r=0.999 9),the average recovery was 99.22%,RSD=0.70%.ConclusionThe method is simple,accurate, It is suitable for quality control of Bone setting Lotion.
Bone setting Lotion; TLC;HPLC; paeonol
广西壮族自治区卫生厅中医药科技专项(GZYZ1226)。
蔡小玲,副主任药师,主要从事中药制剂研究。E-mail:516442235@qq.com
R284.1
A
1007-8517(2014)14-0013-03
2014.05.27)

