HPLC法测定盐酸雷诺嗪在不同种属血浆中的蛋白结合率
王艳梅 李秀轻 王俊学
·药物研究·
HPLC法测定盐酸雷诺嗪在不同种属血浆中的蛋白结合率
王艳梅 李秀轻 王俊学
目的研究盐酸雷诺嗪与不同种属血浆的蛋白结合情况。方法采用高效液相色谱法(HPLC法)和平衡透析法测定管状半透膜内的血浆药物浓度及管状半透膜外的缓冲液中药物浓度,并计算蛋白结合率。结果盐酸雷诺嗪在不同种属血浆(大鼠血浆、人血浆和牛血清白蛋白)中的蛋白结合率均大于50%,分别为:大鼠血浆:(63.43±1.9)%;人血浆:(61.58±4.1)%;牛血清白蛋白:(62.16±2.9)%。且盐酸雷诺嗪在各种属血浆中最低定量下限均为0.05 mg/L。结论盐酸雷诺嗪在不同种属血浆(大鼠血浆、人血浆和牛血清白蛋白)中的蛋白结合率及蛋白结合药物的表观最大能力均较高。随着药物血浆浓度升高,盐酸雷诺嗪结合率升高,有较强的浓度依赖性。
盐酸雷诺嗪;蛋白结合率;半透膜;平衡透析法;高效液相色谱法
盐酸雷诺嗪为吡嗪类抗心绞痛药,具有全新的抗心绞痛机制,是一种晚钠离子电流选择性阻滞剂,通过改善缺血心肌细胞代谢和氧的利用,达到抗心肌缺血、抗心律失常和抗心力衰竭作用[1],该药于2006 年1月获得FDA批准在美国正式上市[2],主要用于治疗慢性心绞痛。目前,国内文献中关于盐酸雷诺嗪在不同种属不同浓度血浆中蛋白结合的研究笔者未见报道,本研究通过探索盐酸雷诺嗪在不同种属血浆中蛋白结合情况,进一步为该药在药效、药动学等方面的行为差异提供理论和实验依据[3]。
1 仪器与试药
Waters公司1525-2487型高效液相色谱仪(美国):1525泵,2487紫外检测器;XW-80型旋涡混合器(上海);管状半透膜(北京华美,型号:DM-6(MD-10)USA)。
盐酸雷诺嗪对照品(购自上海凯峰化工有限公司,批号:060811);内标:苯海拉明(批号:1006631-20089705)由中国药品生物制品检定所提供。大鼠(河北省实验动物中心提供);人血浆(河北省血液中心提供,批号:0050107040084);BSA(Sino-American Biofee公司)。甲醇为色谱纯,水为二次重蒸水,其他所用试剂均为分析纯试剂。
2 方法
2.1 溶液的配制 对照品溶液:取盐酸雷诺嗪和苯海拉明对照品各适量,精密称定,分别加甲醇、水溶解配制成浓度为50 mg/L的盐酸雷诺嗪对照品溶液和50 mg/L的苯海拉明对照品溶液。BSA溶液:称取BSA适量,用重蒸水稀释成浓度为45 g/L的溶液,4℃保存备用。
2.2 色谱条件和系统适用性试验 色谱柱:RESTEKCR C18色谱柱(4.6 mm×250 mm;5 μm);流动相为甲醇-水(醋酸-醋酸铵缓冲溶液, pH值4.5)(55∶45),流速为1 ml/min,检测波长为272 nm,柱温为35℃,进样量为20 μl。见图1。
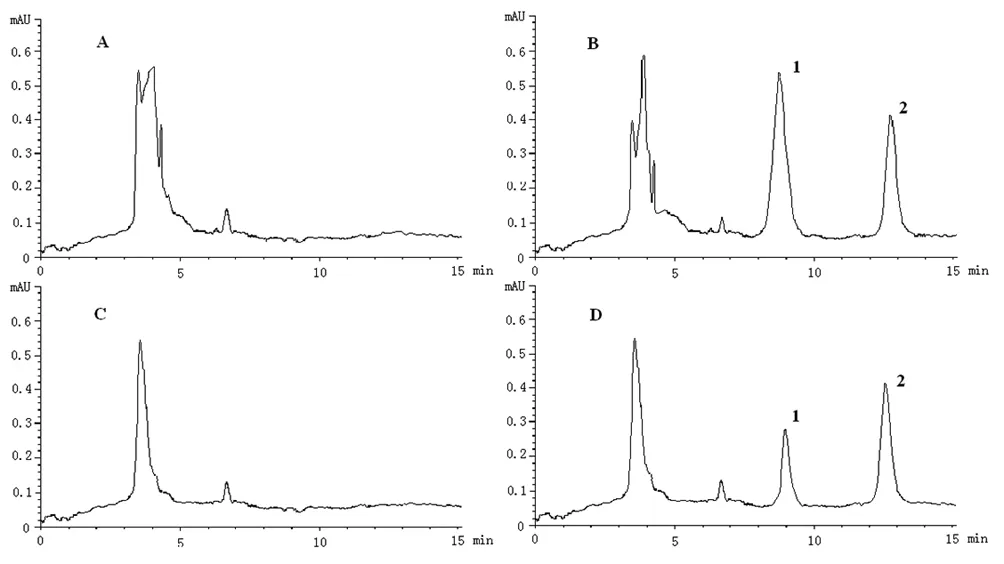
图1 盐酸雷诺嗪在空白人血浆和磷酸盐缓冲液中的色谱图
A.空白血浆;B.盐酸雷诺嗪与内标的血浆样品;C.空白缓冲盐;D.盐酸雷诺嗪与内标的透析袋外样品;1-内标苯海拉明;2-盐酸雷诺嗪
2.3 样品处理 透析袋内血浆和透析袋外缓冲液分别取0.3 ml,分置5 ml离心管中,以5 mol/L的NaOH溶液50 μl碱化样品后,涡旋10 s混匀,精密加入50 mg/L的苯海拉明溶液50 μl,涡旋10 s, 用3 ml乙醚溶液萃取,涡旋15 s,离心(2 000×g)5 min。 取上清液2.5 ml,N2吹干,40 μl流动相溶解,进样,记录盐酸雷诺嗪及苯海拉明的色谱峰面积。
2.4 方法学考察
2.4.1 盐酸雷诺嗪在不同种属血浆及pH值7.4磷酸盐缓冲液中的标准曲线:精密称取“2.1” 项下盐酸雷诺嗪溶液适量,加至各血浆和磷酸盐缓冲液中,分别配制成0.05、0.1、0.25、0.5、1.0、2.5、5.0 mg/L和0.005,0.01、0.02、0.04、0.08、0.2、0.5 mg/L浓度的溶液,混合均匀。上述溶液各精密量取0.3 ml,分置5 ml离心管中,按“2.3”项下方法处理后进样测定,记录色谱图。用盐酸雷诺嗪与内标的峰面积比(Y)对上述相应浓度(X)进行线性回归。盐酸雷诺嗪在各种属血浆中最低定量下限均为0.05 mg/L,在磷酸盐中最低定量下限为0.005 mg/L。见表1。
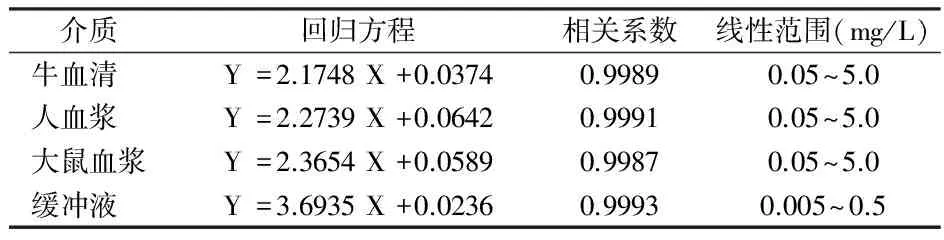
表1 盐酸雷诺嗪在不同介质中的回归方程、相关系数与线性范围
2.4.2 回收率与精密度试验:按“2.3样品处理”项下方法,在各血浆和磷酸盐缓冲液中加入“2.1” 项下盐酸雷诺嗪溶液,配制成浓度为0.1、1.0、4.0 mg/L的血浆样品和浓度为0.01、0.1、0.4 mg/L的磷酸盐缓冲液样品,按上述色谱条件测定,计算得盐酸雷诺嗪在3种浓度不同介质中,回收率、日内及日间RSD均小于15%,符合生物样品分析要求。
2.4.3 提取回收率和基质效应:在4种不同介质中,分别配制盐酸雷诺嗪上述低、中、高3种浓度的样品,以提取后的药物峰面积与直接进样的盐酸雷诺嗪峰面积之比计算提取回收率。同上用流动相代替上述4种介质,按“2.3”项下方法(无内标)测定,记录峰面积为Y1。另取4种不同介质按“2.3”项下方法处理后,加入低、中、高3种浓度的标准品溶液,按上述色谱条件测定,记录盐酸雷诺嗪的峰面积为Y2。计算基质效应ME=Y2/Y1×100%。结果3种浓度不同介质中盐酸雷诺嗪的提取回收率RSD均小于15%,符合生物样品分析要求。且基质效应对样品测定没有影响。
2.4.4 稳定性考察:在4种介质中分别加入盐酸雷诺嗪标准液,配制上述低、中、高3种浓度样品,每个浓度平行配制5份样品,按“2.3”项下方法,室温放24 h及在-20℃冷冻10 d,并且三次冷冻-解冻后考察上述样品的稳定性。结果3种浓度样品在上述条件下的4种不同介质中均稳定,相对误差RE均在 ± 10%之内,RSD < 15%,符合生物样品的分析要求。
2.5 人标准血浆和大鼠中蛋白总量的测定
2.5.1 标准曲线[4]:取”2.1”项下BSA溶液,用纯化水稀释成10、30、50、70、90 μg/ml系列浓度的溶液,采用Lowry法(中国药典2005年版),于650 nm波长处测定标准蛋白溶液的吸光度(A)。以A对血浆蛋白溶液浓度(C)作线性回归,得回归方程为:A=0.0027C-0.0011,r=0.9996(n=5)。
2.5.2 蛋白总量测定:取大鼠及人血浆,用水稀释至蛋白质浓度100 mg/L以内,取1.0 ml置10 ml试管中,按“2.5.1”项下操作,测定A。以标准曲线法计算,测得试验所用大鼠和人血浆中的蛋白总量分别为55.20 g/L和75.52 g/L。
2.6 血浆蛋白结合率的测定
2.6.1 实验方法:采用平衡透析法[5]测定。在装有磷酸盐缓冲液的试管中,分别放置装有0.5 ml各浓度含药血浆(0.25、0.5、1.0、2.5 mg/L)的透析袋,在4℃的冰箱内透析至平衡后,用三氯醋酸试剂检查袋外透析液有无蛋白漏出。按“2.3”项下方法取透析袋两侧介质进行测定,以标准曲线法计算药物浓度。
另取8份,其中4份袋内外均为磷酸盐缓冲液,袋内药物浓度为1.0 mg/L;另外4份未用半透膜,将药物直接加至磷酸盐缓冲液,观察药物和透析袋之间的结合情况。另取4份,在透析袋内外只含磷酸盐缓冲液的情况下,考察透析袋对测定的影响。结果表明,药物与透析袋之间,以及透析袋本身均不影响测定结果。
2.6.2 测定透析平衡时间:透析袋内外均加磷酸盐缓冲液,其中袋内含盐酸雷诺嗪(1 mg/L),共20份,分成5组,分别于24、48、72、96 h于袋两侧取样,照“2.3”项下方法测定。不同时间血浆蛋白结合率分别为:(36.5±4.1)%、(78.1±4.4)%、(94.6±3.3)%、(95.7±3.8)%。应用SPSS 13.0统计软件分析,根据试验数据和统计分析结果,最终确定72 h为透析达平衡时间。
2.6.3 蛋白结合率:用上述方法对盐酸雷诺嗪(4种质量浓度)样品透析平衡后,测定透析袋内外药物总浓度(Dt、Df)。根据公式:fb=(Dt-Df)/Dt×100%计算血浆蛋白结合率。结果表明,盐酸雷诺嗪与各种属血浆的蛋白结合率均大于50%,且蛋白结合率随药物浓度的增加而升高。见表2。
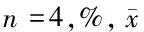
表2 不同种属血浆中的蛋白结合率 ±s
2.6.4 计算βp及Kdp[6]:根据公式:Df=βp×[P]·Df/(Df+Dt-Df·W)-Kdp计算出蛋白结合药物的表观最大能力(βp)和药物与蛋白复合物的解离常数(Kdp),其中Dt和Df需要折合成摩尔浓度进行计算,W为血浆中的含水量,[P]单位为g/L。以Df作纵坐标(Y),[P]·Df/(Df+Dt-Df·W)作横坐标(X),进行线性回归,大鼠蛋白结合药物的表观最大能力和解离常数均最大。表明盐酸雷诺嗪与各血浆蛋白结合参数之间有很大的差异,因此在临床研究中应考虑到不同种属之间的区别。见表3。

表3 盐酸雷诺嗪与各种属血浆蛋白的βp及Kdp
3 讨论
药物与血浆蛋白结合率的研究越来越引起重视,涉及到的测定方法有平衡透析法、超速离心法和白蛋白微球测定法等,因为平衡透析法操作简单,测定结果稳定,故本文采用平衡透析法。
试验中对流动相的选用[乙腈-水、甲醇-水、甲醇-水(醋酸-醋酸铵缓冲溶液,pH值4.0)、甲醇-水(醋酸-醋酸铵缓冲溶液,pH值4.5)、甲醇-水(醋酸-醋酸铵缓冲溶液,pH值5.5)]和样品处理时的萃取溶剂(石油醚、乙醚和乙酸乙酯)进行比较,结果发现,流动相中加入醋酸-醋酸铵缓冲溶液(pH值4.5),不仅可以改善峰形,而且更利于分离,故最终确定流动相为甲醇-水(醋酸-醋酸铵缓冲溶液,pH值4.5)。通过比较不同萃取溶剂时血浆中盐酸雷诺嗪的提取回收率,发现乙醚做萃取溶剂时回收率最高,且萃取后较容易挥干,故最终确定乙醚为提取溶剂。
本文通过建立盐酸雷诺嗪血浆蛋白结合率的HPLC测定方法,计算不同种属血浆蛋白的相关参数,为盐酸雷诺嗪的临床应用提供了理论和实验依据,对该药在国内的应用奠定了实验基础。
1 Stone PH.Ranolazine: new paradigm for management of myocardial ischemia,myocardial dysfunction,and arrhythmias.Cardiol Clin,2008,26:603-604.
2 张浩.新型抗心绞痛药物盐酸雷诺嗪的研究进展.中国处方药,2007,10:18-19.
3 贾晶莹,刘罡一,陈钧,等.高效液相色谱法测定犬血浆中雷诺嚓的含量及相对生物利用度.中国新药与临床杂志,2011,30: 537-540.
4 李敏,王春英,景秀娟,等.高效液相色谱法测定间尼索地平不同对映体在血浆中的蛋白结合率.中国医院药学杂志,2011,31:181-185.
5 张均田主编.现代药理实验方法.第4版.北京:北京医科大学、中国协和医科大学联合出版社,1998.1669-1672.
6 姜纪荣,束汉麟,许国英,等.我国人和动物的磺胺药血浆蛋白结合率.药学通报,1981,16:705.
10.3969/j.issn.1002-7386.2014.21.057
063000 河北省唐山市,中国人民解放军第255医院药械科(王艳梅、王俊学);河北医科大学第二医院肝胆外科(李秀轻)
R 914.1
A
1002-7386(2014)21-3339-03
2014-05-11)

