达玛烷苷元对睡眠干扰所致小鼠学习记忆障碍的改善作用
卜兰兰, 石 哲,武宏伟,卢 聪、王克柱,李莹辉,曲丽娜,刘新民
(1.湖南中医药大学 病理学教研室,湖南,长沙 410208;2.中国医学科学院 北京协和医学院 药用植物研究所,北京 100193;3.中国航天员中心航天医学基础与应用国家重点实验室,北京 100094;4.湖南省实验动物中心 湖南省药物安全评价研究中心,湖南 长沙 410331)
人参是现代药理研究最多和最充分的传统中药之一,而以改善各种学习记忆障碍的研究报导最多。现代研究证明人参皂苷为人参的主要活性成分,对神经系统有多种调节作用,如改善学习记忆障碍、抗抑郁、镇静安神、兴奋中枢等。研究表明,人参皂苷Rg1、Rb1能改善多种学习记忆障碍模型动物的学习记忆障碍[1-3],保护多种条件下的神经细胞损伤和凋亡[4-6]。本实验室前期研究也发现,人参皂苷Rg1、Rb1对睡眠干扰大鼠认知能力有改善作用,人参皂苷Rg1、Rb1、Rh1、PPT对东莨菪碱模型小鼠认知能力有改善作用[7,8]。本实验旨在通过研究人参苷元类化合物DS-1226对睡眠干扰致认知障碍小鼠学习记忆能力的影响,为改善睡眠障碍致学习记忆损害的药物研究提供参考。
1 材料
1.1 药物
DS-1226,dammarane sapogenins,成分:原人参二醇[20(S)-aglycone protopanaxadiol, aPPD],原人参三醇[20(S)-aglycone protopanaxatriol, aPPT],人参皂苷Rh2(ginsenoside Rh2),PAM120等。成分含量:aPPD >12%,aPPT >26%,Rh2 >8%。由加拿大天马药业集团惠赠。
1.2 动物
ICR小鼠,雄性,5-6周龄,体重22±2 g,130只,SPF级,购自军事医学科学院实验动物中心,许可证号[SCXK-(军)2007-004]。使用合格证号:[SYXK( 京) 2003-0009]。
1.3 仪器
小鼠自主活动实时检测分析处理系统、小鼠Morris水迷宫计算机自动控制和图像分析处理系统、小鼠避暗实验检测系统、滚筒式大小鼠睡眠干扰仪均由中国航天员科研训练中心和中国医学科学院药用植物研究所联合研发。
2 实验方法
2.1 动物分组及给药
2.1.1 分组:采用随机数字表法分为水迷宫组(环境对照组,模型组,DS-1226低、中、高剂量组)和避暗组(环境对照组,模型组,DS-1226低、中、高剂量组),共10组,每组13只。
2.1.2 给药:DS-1226低剂量18.75 mg/kg,中剂量37.5 mg/kg,高剂量75 mg/kg。分析天平称取药物,加蒸馏水配成混悬液,0.2 mL/10 g灌胃。环境对照组及模型组给等体积蒸馏水。造模开始前(8 am)开始给药,每天1次。行为学检测期间,每只动物检测前1 h给药。给药持续直至行为学检测完成。
2.2 睡眠干扰实验
每天3 h ( 8~11 am),连续3 d滚筒适应 ( 1 min/r,间隔5 min )后,将模型组及各给药组动物灌胃给药后放入滚筒(8 AM)开始干扰。滚筒以1 min/r 间隔5 min模式[9]运转并开始计时。15 d时间到(8 am)取出水迷宫/避暗测试组与其环境对照组动物进行相应行为学检测。检测结束后,将干扰组动物放回滚筒继续干扰(除行为学检测期间取出动物外,其余时间动物均在滚筒中)。如此直至相应行为学检测结束。
2.3 水迷宫实验
睡眠干扰15 d时间到(8 am)后,自主活动实验结束后进行水迷宫定位航行实验。
小鼠Morris水迷宫计算机自动控制和图像分析处理系统在本实验室原有仪器[10]基础上开发,由一个不锈钢喷塑圆柱形水池(直径100 cm,高38 cm)和图像采集分析系统组成。平台直径6 cm,高14 cm。按东西南北将水池划分为4 象限( NE,SE,SW,NW),象限池壁圆弧中点为动物入水点。向池中注水并用墨汁调黑保证目标准确识别。软件记录动物游泳轨迹,用于指标提取和分析。
2.3.1 定位航行: Day1-6: 平台固定于NE 象限中心,水面下1.5 cm。实验室物品及人员位置固定作为小鼠空间参照物。每天训练3次,每次从不同入水点( SE、SW、NW) 将动物面向池壁放入水中。检测时间90 s,在台上停留超过2 s视为寻台成功,每次测试前将动物放在台上适应10 s (前适应),测试完毕无论寻台是否成功均将其放在台上适应10 s (后适应)。将动物入水到寻台成功所需时间记作潜伏期,寻台失败潜伏期记90 s。用潜伏期评价动物空间学习能力。
2.3.2 空间探索:Day 7: 撤去平台,从实台所在象限对角象限SW入水。以90 s内穿台次数、目标象限游程比率、目标象限时间比率评价动物空间记忆能力。
2.4 避暗实验
睡眠干扰15 d时间到(8 am)后,自主活动实验结束后进行避暗训练。
小鼠避暗实验检测系统[11]由避暗测试箱和图像采集分析系统组成。避暗测试箱为封闭结构,内含两个测试箱,每个测试箱分明暗两室(20 cm × 12 cm × 60 cm),两室之间均有一个小门(5 cm × 3 cm),底部为可独立控制通断电的不锈钢栅栏,应用软件控制实验流程并自动分析动物活动信息,提取指标。
2.4.1 避暗训练:Day1: 将动物从明室放入自由活动5 min后取出。设置参数: 再现模式B(摄像头识别到动物在暗室,暗室栅栏通电,动物离开,暗室断电)、刺激电压31V、实验时间5 min。将动物放入暗室开始实验,动物遭受电击逃到明室。以5 min内错误次数(第1次被电不计入错误次数),潜伏期(第1次从暗室到明室的时间)、暗室(错误区)时间、明室(安全区)时间、暗室路程评价动物避暗学习能力。
2.4.2 避暗检测:Day 2: 避暗训练后24 h进行。参数设置同前。将动物放入明室开始实验,以5 min 内错误次数(进入暗室的次数),潜伏期(第1次从明室到暗室的时间)、暗室时间、明室时间、暗室路程评价动物避暗记忆能力。
2.5 自主活动实验
睡眠干扰15 d时间到(8 am),水迷宫定位航行Day 1/避暗训练Day 1前进行。
小鼠自主活动实时检测分析处理系统[12]由一个封闭箱体(80 cm × 80 cm × 155 cm)、4个可移动锥桶(底直径30 cm,上口直径40 cm,高60 cm) 和图像采集分析系统组成。检测时,将小鼠沿壁放入桶内,设定参数后开始实验。软件自动采集分析动物10 min内运动轨迹,通过总路程、平均速度、运动总时间、静息总时间反映动物自主活动情况。
3 统计学方法

4 实验结果
4.1 DS-1226对睡眠干扰小鼠水迷宫成绩的影响
如表1所示,与对照组比较,模型组定位航行D5、D6潜伏期增加(P<0.05);与模型组和低剂量组比较,DS-1226中剂量组D6潜伏期降低(P<0.05);与模型组比较,DS-1226高剂量组D1-D6潜伏期降低(P<0.01);与低剂量组比较,DS-1226高剂量组D2、D4潜伏期降低(P<0.05),D1、D3、D5、D6潜伏期明显降低(P<0.01);与中剂量组比较,DS-1226高剂量组D1潜伏期降低(P<0.05),D2-D5潜伏期明显降低(P<0.01)。
如表2示,与对照组比较,模型组目标象限穿台次数减少(P<0.01)、目标象限游程比率减少(P<0.05);与模型组比较,DS-1226高剂量组目标象限穿台次数增加(P<0.01)、目标象限游程比率和目标象限时间比率增加(P<0.05);与低剂量组比较,DS-1226高剂量组目标象限游程比率增加(P<0.05);与中剂量组比较,DS-1226高剂量组目标象限穿台次数增加(P<0.05)。

表1 DS-1226对睡眠干扰小鼠定位航行潜伏期的影响(n=13)

表2 DS-1226对睡眠干扰小鼠空间探索的影响(n=13)

表3 DS-1226对睡眠干扰小鼠避暗学习的影响(n=13)
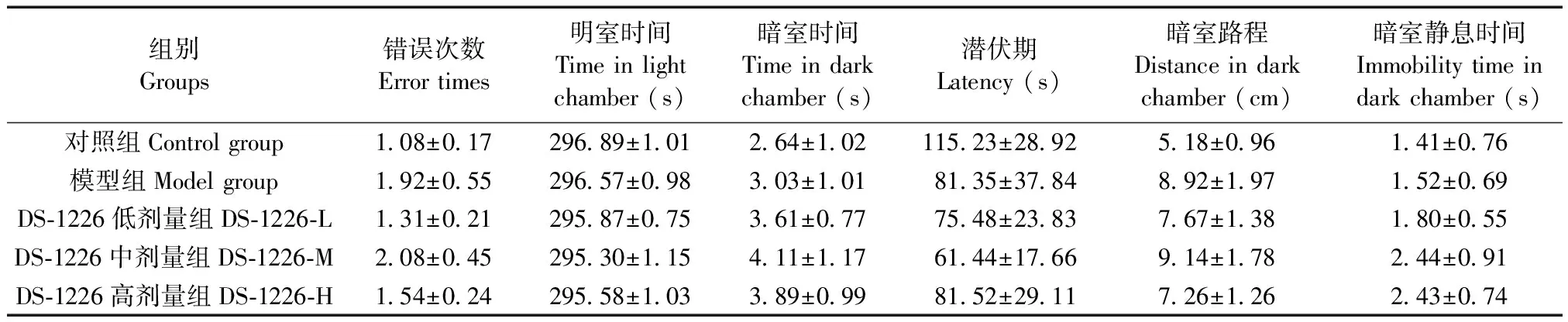
表4 DS-1226对睡眠干扰小鼠避暗巩固的影响(n=13)

表5 DS-1226对睡眠干扰小鼠自主活动的影响(n=13)
4.2 DS-1226对睡眠干扰小鼠避暗成绩的影响
如表3所示,与对照组比较,模型组错误次数、暗室路程增加(P<0.01),暗室时间、暗室静息时间增加(P<0.05);与模型组比较,DS-1226低剂量组错误次数减少(P<0.05),暗室路程减少(P<0.01),DS-1226中剂量组错误次数、暗室路程减少(P<0.01),DS-1226高剂量组错误次数、暗室路程减少(P<0.01),暗室时间、暗室静息时间减少(P<0.05),明室时间增加(P<0.05);与低剂量组比较,DS-1226高剂量组暗室时间及暗室静息时间减少,明室时间增加(P<0.01)。
如表4示,模型组与对照组以及各给药组与模型组之间,错误次数、明室时间、暗室时间、潜伏期、暗室路程、暗室静息时间均无统计学差异。
4.3 DS-1226对睡眠干扰小鼠自主活动的影响
如表5示,与对照组比较,模型组在以上各指标上无差异;与模型组比较,DS-1226低剂量组总路程、平均速度、运动总时间增加(P<0.05),DS-1226中、高剂量组总路程、平均速度、运动总时间均增加(P<0.01)。
5 讨论
人参是五加科植物人参Panax ginseng C. A. Mey. 的根。《神农本草经》上经(品)中记载,人参“主补五脏,安精神,定魂魄,止惊悸,除邪气,明目,开心益智。久服,轻身延年”。因其作用广泛神奇享有“百草之王”的美誉而备受国内外学者的重视。关于其开心益智作用的研究也成了热门。随着现代分离技术和分析技术的进步,人参的化学成分得到进一步阐明,人参皂苷被认为是人参的主要有效物质。有研究表明,口服人参皂苷对睡眠干扰大鼠学习记忆能力受损有明显的保护作用[13]。另有研究表明,口服人参皂苷Rb1、腹腔注射人参皂苷Rd对东莨菪碱和环己米特所致的小鼠获得性及巩固性记忆障碍均具有明显的改善作用[14]。在实验室前期研究的基础上,本实验选用人参皂苷碱水解后得到的人参次苷和人参苷元混合物DS-1226,探索其对滚筒法睡眠干扰致学习记忆损害的影响。
水迷宫实验结果表明,睡眠干扰一定时间(15 d)后会造成动物空间学习记忆能力下降。DS-1226高剂量(75 mg/kg)给药则可以显著改善小鼠空间学习和记忆能力,效果优于中剂量。避暗实验结果表明,模型组小鼠避暗学习能力受损,DS-1226低、中、高三个剂量给药均可改善造模动物避暗学习能力,且高剂量优于低、中剂量。研究发现人参皂苷Rg1、Rb1可以提高东莨菪碱痴呆动物的水迷宫空间定位学习和记忆能力[15],人参茎叶皂甙对睡眠干扰大鼠“Y”迷宫空间分辨学习能力有明显改善作用[16]。人参皂苷的主要促智成分Rb1和Rg1可增强胆碱能系统的功能,增加脑突触受体对3H-胆碱的摄取,增加乙酰胆碱的合成与释放[17]。睡眠干扰后大鼠脑干中缝核群5-HT明显增加且随着扰时间延长而加大,连续口服人参皂甙可使短时间干扰大鼠脑中缝核群5-HT增加,对于长时间干扰,则使5-HT累积程度减轻[18]。还有研究报道,人参皂苷对中枢5-HT的影响呈双向性,中枢5-HT能系统对学习记忆的影响是与胆碱能系统交互作用的结果,5-HT不但作为递质,而且作为调质发挥作用[19]。张均田等为评价人参Rg1的益智作用,建立了多种记忆障碍模型,包括老年鼠、应激鼠、缺血-再灌注、东莨菪碱及β淀粉样蛋白等所致的认知障碍,研究证明Rg1通过多种途径和机制增加神经可塑性,如提高突触效能和结构可塑性、中枢乙酰胆碱含量和M-胆碱受体密度增加和FOS蛋白、BDNF表达增加[20-22]。DS-1226改善睡眠干扰动物空间定位学习记忆能力及避暗学习能力可能与以上机制有关,有待进一步研究。至于避暗巩固结果显示模型组避暗记忆能力未受损害,各给药组与模型组之间避暗记忆也无差别,可能与电击这种恐怖记忆一旦获得就很难忘记有关[23]。
从自主活动结果来看,睡眠干扰15d对ICR小鼠自主活动影响较小。这也与前期研究结果一致,可能是因为动物对滚筒滚动已经产生了适应,同时也再次验证了滚筒法睡眠干扰结果的稳定性和可靠性[9]。人参对中枢神经系统的镇静和兴奋双向调节作用与用药时神经系统的功能状态、用药剂量及人参不同成分有关[24]。DS-1226给药各剂量组动物自主活动均显示总体活动增加,这可能与以上三种因素相关,还需进一步研究。
综上所述,DS-1226口服给药可以改善滚筒法睡眠干扰15 d导致的小鼠空间定位学习、记忆能力及避暗学习能力障碍,且高剂量(75 mg/kg)效果最为明显,可为益智中药的研究提供参考。
参考文献:
[1] 王晓英, 陈霁, 张均田. 人参皂苷Rg1对β-淀粉样肽(25-35)侧脑室注射所致小鼠学习记忆障碍的改善作用及其机制 [J]. 药学学报, 2001, 36(01): 1-4.
[2] Tohda C, Matsumoto N, Zou K, et al. Abeta(25-35)-induced memory impairment, axonal atrophy, and synaptic loss are ameliorated by M1, a metabolite of protopanaxadiol-type saponins [J]. Neuropsychopharmacology, 2004, 29(5): 860-868.
[3] 罗天飞, 刘姗姗, 葛鹏飞, 等. 人参皂甙Rb1对短暂脑缺血后神经元损伤的保护作用 [J]. 中国老年学杂志, 2008, 28(19): 1892-1894.
[4] 吴蕾, 陈云波, 王奇,等. 人参皂苷对Aβ_(25-35)蛋白诱导的老年性痴呆体外模型NG108-15神经元细胞凋亡的抑制作用 [J]. 广州中医药大学学报, 2007, 24(02): 126-131.
[5] Liao B, Newmark H, Zhou R. Neuroprotective effects of ginseng total saponin and ginsenosides Rb1 and Rg1 on spinal cord neurons in vitro [J]. Exp Neurol, 2002, 173(2): 224-234.
[6] 魏翠柏, 贾建平, 王芬, 等. 人参皂苷Rg1及Rb1对Aβ25-35诱导CHO细胞毒性影响 [J]. 中华中医药杂志, 2008, 23(07): 616-618.
[7] 金剑. 一种基于睡眠干扰动物模型的中药药效研究方法 [D]. 吉林长春:长春中医药大学药学院, 2013.
[8] Wang Q, Sun LH, Jia W, et al. Comparison of ginsenosides Rg1 and Rb1 for their effects on improving scopolamine induced learning and memory impairment in mice [J]. Phytother Res, 2010, 24(12):1748-1754.
[9] 卜兰兰, 石哲, 孙秀萍, 等. 一种辅助改善记忆保健食品功能评价的动物模型 [J]. 中国食品卫生杂志, 2011, 23(5):402-406.
[10] 刘新民, 陈善广, 王圣平, 等. 益智中草药研究中的一种新方法 [J]. 中草药, 1998, 29(03):174-177.
[11] 薛丹, 陈善广, 徐淑萍, 等. 构建自动、智能及敏感度高的避暗实验检测系统 [J]. 中国组织工程研究与临床康复, 2010, 14(15):2778-2782.
[12] 王琼, 买文丽, 李翊华, 等. 自主活动实时测试分析系统的建立与开心散安神镇静作用验证 [J]. 中草药, 2009, 40(11):1773-1779.
[13] 杨国愉, 皇甫恩, 张大均, 等. 人参皂甙对睡眠剥夺大鼠学习记忆和活动性的影响 [J]. 中国临床心理学杂志, 2007, 15(1):81-84.
[14] 陈声武, 王丽娟, 王岩, 等. 人参皂苷Rb1和Rd对不同类型记忆障碍模型小鼠学习记忆功能的影响 [J]. 中国药理学与毒理学杂志, 2001, 15(5):330-332.
[15] Chen SW, Wang LJ, Wang Y, et al. Effects of ginsenoside Rbl and Rd on learning and memory function of mice [J]. Chin J Pharmacol Toxicol, 2001, 15: 330-332.
[16] Wafford KA, Ebert B. Emerging anti-insomnia drugs: tackling sleeplessness and the quality of wake time [J]. Nat Rev Drug Discov, 2008, 7(6): 530-540.
[17] Salim KN, McEwen BS, Chao HM. Ginsenoside Rb1 regulates ChAT, NGF and trkA mRNA expression in the rat brain [J]. Brain Res, 1997, 47(1-2): 177-182.
[18] 杨国愉, 冯正直, 皇甫恩, 等. 人参皂甙对睡眠剥夺下大鼠脑干中缝核群5-HT的影响 [J]. 第三军医大学学报, 2002, 24(2):158-160.
[19] Thakkar M, Mallick BN. Effect of rapid eye movement sleep deprivation on rat brain monoamine oxidases[J ]. Neuroscience, 1993, 55 (3): 677-683.
[20] Wang XY, Zhang JT. Effect of ginsenoside Rg1 on synaptic plasticity of freely moving rats and its mechanism of action [J]. Acta Pharmacol Sin, 2001, 22 (7): 657-662.
[21] Zhang JT, Liu M. Modern research on the noontropic and anti-aging effects of ginseng [C]. Adv Pharmacol Clin Res, 1996:170-179.
[22] Zhang JT. New progress in the study of ginsenoside Rg1 and Rb1 [C]. The 14th Symposium on Natural Products Research, 1999:1-4.
[23] Tinsley MR, Quinn JJ, Fanselow MS. The role of muscarinic and nicotinic cholinergic neurotransmission in aversive conditioning: comparing Pavlovian fear conditioning and inhibitory avoidance [J]. Learn Mem, 2004, 11(1):35-42.
[24] 黎阳, 张铁军, 刘素香, 等. 人参化学成分和药理研究进展 [J]. 中草药, 2009, 40(1):164,附1, 附2.

