沙棘树干茎流液中总氮总磷联合消解的测定方法
王玉功, 王 华, 刘建军, 余志峰
(国土资源部兰州矿产资源监督检测中心, 甘肃 兰州 730050)
沙棘树干茎流液中总氮总磷联合消解的测定方法
王玉功, 王 华, 刘建军, 余志峰
(国土资源部兰州矿产资源监督检测中心, 甘肃 兰州 730050)


树干茎流研究是国内外森林水文学研究中的重要内容。树干茎流是指林冠截持的降雨经树叶、树枝沿树干流向地面的雨水[1]。树干茎流淋洗树冠得到的养分直接进入林木根际区, 促进森林水分和养分再循环,影响着土壤—植物—大气连续体中不同圈层间的水分和养分循环的速度与方向[2-3],对树木生长起着相当重要的作用。氮、磷是植物生长的必需养分,它们是植物活细胞的组成部分。可以合成较多的蛋白质,促进细胞的分裂和增长。近年来研究树干茎流特征及其生态水文效应的文章较为常见[1-8],因此测定树干茎流液中总氮、总磷的含量,对于研究树干茎流特征及其生态水文环境治理有着重要的意义。
目前国家标准GB11893—89[9]和HJ 636—2012[10]规定了水中总磷、总氮分别测定的标准方法。总氮用碱性过硫酸钾消解,紫外分光光度法测定;而总磷则是用中性硫酸钾消解,分光光度法测定。两种国家标准方法分别取样、消解,费时费力,分析效率低。本文综合两种国家标准方法,在参考文献[11-19]的基础上,探讨建立了在一份样品中用过硫酸钾一次消解,分光光度法联合测定树干茎流的总氮、总磷的方法,通过实验确定了消化时间、K2S2O8用量、消化温度等最佳消解条件,提高了分析效率。
1 实验部分
1.1 仪器和主要试剂
紫外可见分光光度计:UV-1950SPC(北京普析通用有限公司)。
医用压力蒸汽灭菌器。
碱性过硫酸钾溶液:称取40 g过硫酸钾(K2S2O8)溶于200 mL蒸馏水中,加入15 g的NaOH溶解后稀释至1000 mL。
钼酸铵锑储备溶液(150 g/L 钼酸铵-5 g/L酒石酸锑钾):称取15 g钼酸铵溶于100 mL蒸馏水中,缓缓加到300 mL的50%硫酸中,不断搅拌,冷却。再加100 mL的0.5%酒石酸锑钾溶液,摇匀,贮存于棕色瓶中。
钼锑抗溶液(显色剂):量取100 mL钼酸铵锑溶液(150 g/L 钼酸铵-5 g/L酒石酸锑钾),加入1.5 g抗坏血酸溶解后即得。此溶液不稳定,宜在使用前配制。
标准溶液的试剂为基准试剂,其他试剂均用分析纯。
用去离子水蒸馏除氨制得无氨蒸馏水。
1.2 树干茎流液采集
本文所用的茎流样品均由甘肃省农业科学院提供。
在选定的每株标准木上,采用剖开的胶皮管螺旋形地围绕(绕2~3圈)刮平树皮的树干上做成闭合截水环,然后用导管连通截水环,把茎流水引入地面上的集水器中。
1.3 总氮和总磷联合消解原理和方法

过硫酸钾水溶液在60℃时可分解产生:
K2S2O8+2H2O→2KHSO4+O2+2H+
由方程式可知,1 moL的K2S2O8可分解产生1 moL的O2和2 moL的H+。如果将等物质的量的K2S2O8和NaOH混合液作为茎流液消解的氧化剂,则消解反应开始时,溶液呈碱性。由于K2S2O8分解产生的O2将茎流液中不同形态的氮氧化成硝酸盐,同时K2S2O8分解产生的H+不断中和NaOH,当NaOH被H+完全中和后,溶液逐渐变成酸性。在弱酸性溶液中,K2S2O8分解产生的O2又将含磷化合物氧化成正磷酸盐。故把等物质的量的K2S2O8和NaOH混合溶液作为氧化剂加入样品溶液中,于高压锅内(125℃)加热40 min,它能依次完成总氮、总磷的全部消解过程。
1.4 总氮和总磷测定方法
吸取10 mL茎流液于25 mL比色管中,加入碱性过硫酸钾溶液5 mL,以无氨蒸馏水冲洗至刻度,加盖摇匀。将比色管装入一小布袋中并用绳扎紧。将比色管置于高压消毒器中,待压力达到0.1 MPa,相应温度为125℃时,保持40 min。开阀放气,自然冷却。取出比色管,分取10 mL消解液加入2 mL的10%盐酸,定容至25 mL,在紫外分光光度计上用1 cm石英比色皿,以新鲜无氨水作参比,分别在波长220 nm及275 nm处测量吸光度,用校正的吸光度(ΔA=A220-2A275)绘制校准曲线。再将剩下的15 mL消解液加入2 mL钼锑抗溶液(显色剂),充分混匀,放置15 min,用2 cm比色皿,以零浓度溶液为参比,于波长700 nm处测量吸光度。随同做空白试验。
1.5 分析结果计算
式中,0.2558—由硝酸根质量换算为总氮质量的系数;0.3261—由磷酸根质量换算为总磷质量的系数。
2 结果与讨论
2.1 硝酸盐和磷酸盐混合标准系列配制


图 1 联合消解工作曲线Fig.1 Working curve of with combined digestion method

图 2 联合消解工作曲线Fig.2 Working curve of with combined digestion method
2.2 碱性过硫酸钾用量的选择
消解过程中加入碱性过硫酸钾的量过多,过硫酸钾消解不完全,使得空白值偏高,也浪费试剂;若加入碱性过硫酸钾的量过少,氮、磷的转化不完全[14-17]。为了确定碱性过硫酸钾的加入量,由国家环保总局标准物质中心购得标准物质GBW(E) 081020(标准值:总氮2.56 mg/L,总磷0.417 mg/L),按实验方法加入不同量的碱性过硫酸钾溶液,每组做3个平行实验,结果见表1。由表1可以看出,当加入碱性过硫酸钾的量少于3 mL时,氮、磷的消解不完全,总氮和总磷的测定值偏低;当加入4 mL碱性过硫酸钾时,氮消解完全,总氮的测定值与标准值接近,而磷没有完全消解,总磷的测定值偏低;当加入碱性过硫酸钾的量大于5 mL时,氮、磷均能消解完全,总氮和总磷的测定结果较为准确。故本文选择碱性过硫酸钾溶液的用量为5 mL。
从文明进程看,人工智能在现阶段的意义仍在于进一步解放人力,类似工业革命时蒸汽机解放了人力,人工智能革命将人从低等脑力劳动中解放了出来,因此也必将像集装箱的发明取消了码头工人这个职业那样,取代很多脑力“码头工人”的工作。长期和整体来看,技术进步总是改善人类整体福利,并为个体更好实现自身内在价值提供外在条件。
2.3 消解时间的选择
研究表明,在波长220 nm处碱性过硫酸钾本身有强烈的吸收[20-23],125℃时如果消解时间过短,碱性过硫酸钾分解不完全,给分析结果带来正干扰,随着消解时间的延长,碱性过硫酸钾的吸光度降低至一个稳定的水平。从表2可以看出,加热时间少于30 min时,碱性过硫酸钾不能完全分解;加热时间大于30 min时,碱性过硫酸钾逐渐分解完全,吸光度降低并保持稳定的水平。考虑到茎流液氮、磷的含量比一般水质样品高,所以选择消解时间为40 min。
表 1 碱性过硫酸钾用量实验
Table 1 The experiment on dosage of alkaline potassium persulfate

碱性过硫酸钾用量(mL)总氮(mg/L)测定平均值标准值总磷(mg/L)测定平均值标准值2.02.322.560.3770.4173.02.452.560.3910.4174.02.552.560.4030.4175.02.572.560.4200.4176.02.512.560.4220.4178.02.532.560.4140.417
表 2 不同消解时间碱性过硫酸钾的吸光度
Table 2 The absorbance of alkaline potassium persulfate at different digestion time

消解时间(min)220nm处吸光度消解时间(min)220nm处吸光度0∞300.1~0.05100.8~0.7400.03~0.02200.7~0.350<0.02
2.4 消解温度的选择
为了使茎流液中氮、磷完全转化,必须确定样品的消解温度。将已知浓度的氮混合液(氯化铵、亚硝酸钠、硝酸盐)稀释至总氮的浓度约为20 mg/L,将磷混合液(叉磷酸、三元磺酸、磷酸二氢钾)稀释至总磷的浓度约为5 mg/L,再将氮、磷的混合溶液等体积混匀作为模拟树干茎流液。选择5个不同的消解温度绘制消解率曲线(图3)。由图3可以看出,当温度在120℃时氮消解完全,磷消解不完全;当温度在125℃时不影响氮消解,磷可以消解完全,故实验选择消解温度为125℃。
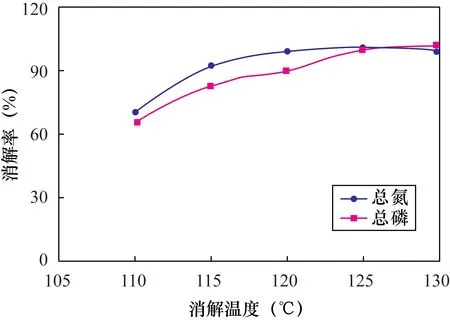
图 3 消解温度实验Fig.3 The experiment on digestion temperature
2.5 方法精密度
对实际茎流液样品,按实验方法进行精密度试验。表3结果表明,方法精密度(RSD,n=5)总氮为0.1%~1.3%,总磷为0.6%~3.3%,说明本方法能够满足茎流样中总氮、总磷的测定要求。
2.6 方法准确度
用本法对国家标准物质GBW(E) 081020进行分析,由表4结果可见,总氮和总磷的测定值与标准值基本吻合。按照本法可以准确测定树干茎流液中总氮、总磷的含量。
表 3 方法精密度试验
Table 3 Precision tests of the method

待测项目本法分次测定值(mg/L)平均值(mg/L)RSD(%)总氮23.7523.8123.8023.7423.7723.770.14.354.274.244.354.254.291.3总磷1.251.201.261.211.301.243.35.435.445.385.395.455.420.6
表 4 方法准确度试验
Table 4 Accuracy tests of the method

待测项目含量(mg/L)标准值本法分次测定值平均值相对误差(%)总氮2.562.5202.6202.5802.6002.6102.5902.4总磷0.4170.4160.4220.4250.4260.4240.4231.4
2.7 方法回收率
按实验方法,选取3个不同含量范围的茎流液做回收试验。由表5结果可见,测定总氮的回收率在98.0%~104.2%,总磷的回收率在94.0%~107.0%,结果令人满意。
表 5 总氮和总磷回收率
Table 5 Recovery tests for total nitrogen and total phosphorus of the method
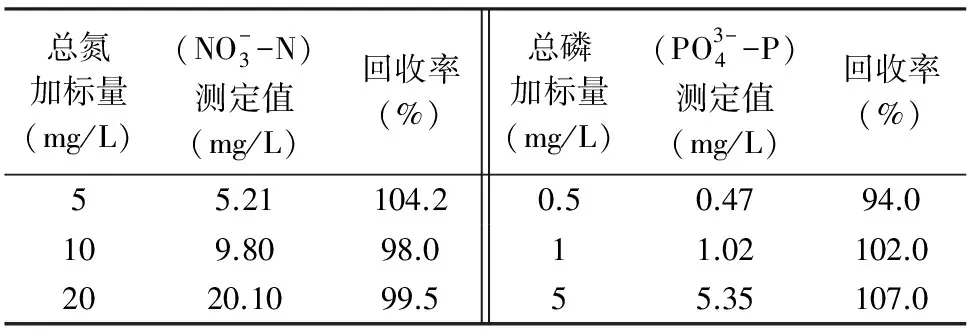
总氮加标量(mg/L)(NO-3-N)测定值(mg/L)回收率(%)总磷加标量(mg/L)(PO3-4-P)测定值(mg/L)回收率(%)55.21104.20.50.4794.0109.8098.011.02102.02020.1099.555.35107.0
2.8 方法检出限及线性范围

表 6 方法检出限及线性范围
Table 6 Detection limits and linear range of the method

测定项目检出限(mg/L)线性范围(mg/L)本法国家标准方法相关系数(R)NO-3-N0.0450~250.05~40.9998PO3-4-P0.0080~20.01~0.60.9994
4 结语
本法将国家标准法分别测定水中总氮、总磷的方法进行综合改进,即将配制两条标准系列、两次高压消解转变为配制一条标准系列、一次消解,应用于树干茎流液中总氮、总磷的测定,大大减少了工作量,提高了分析效率。同时茎流液不易采得,一次消解可以节省50%的样品使用量。本方法能为研究树干茎流特征及其生态水文环境治理提供科学依据。
方法适合于有机质含量较低的树干茎流液的分析。当有机质含量较高时,样品本身带有黄色或褐色,在本法条件下一次不易消解清亮,影响了总氮、总磷的光度法测定。
[1] 周择福,张光灿,刘霞,薄金燕,李小磊.树干茎流研究方法及其述评[J].水土保持学报,2004,18(3):137-140,145.
[2] 王震洪,段昌群,陈明,王克勤.云南中部三种典型人工林生态系统水文生态规律研究[J].水土保持学报,2003,17(1):148-151.
[3] 王正宁,王新平.荒漠灌丛树干茎流及其入渗、再分配特征[J].中国沙漠,2010,30(5):1108-1113.
[4] 欧阳惠.森林林冠截留效益计量的研究[J].科技通报,2001,17(4):25-31.
[5] 杨志鹏,李小雁,伊万娟.荒漠灌木树干茎流及其生态水文效应研究进展[J].中国沙漠,2010,30(2):303-311.
[6] 徐先英,严平,郭树江,柴成武.干旱荒漠区绿洲边缘典型固沙灌木的降水截留特征[J].中国沙漠,2013,33(1):141-145.
[7] 陈小红,段争虎,宋耀选,肖洪浪.兰州市南北两山人工灌木林地土壤水分动态[J].中国沙漠,2006,26(4):532-535.
[8] 王新平,康尔泗,张景光,李新荣.荒漠地区主要固沙灌木的降水截留特征[J].冰川冻土,2004,26(1):89-94.[9] GB 11893—89,水质分析国家标准方法汇编[M].
[10] HJ 636—2012,水质分析国家标准方法汇编[M].
[11] 张冬英.过硫酸铵消化-氯化亚锡还原光度法测定地面水中总磷[J].黑龙江环境通报,2002,26(3):72-73,106.
[12] 李自弘,张琼芬,涂学炎,舒燕,吕红梅.碱性过硫酸钾快速消解的紫外分光光度法测定水质总氮[J].云南大学学报(自然科学版),2004,26(增刊):154-156.
[13] 刘菁,蒋丹凤.烘箱法测定地表水中的总氮[J].污染防治技术,2005,18(5):50-52.
[14] 刘辉利,纪锐琳.地表水总氮总磷联合消解测定方法的研究[J].干旱环境监测,2005,19(2):65-67,79.
[15] 李飞,王丽.联合测定水中总磷和总氮[J].环境监测管理与技术,2004,16(5):31-32.
[16] 刘赛亮.同步消解的总磷、总氮测定方法探讨[J].化学工程与装备,2007(3):50-52.
[17] 俞是聃.在同一消解液中同时测定总磷和总氮[J].干旱环境监测,2002,16(3):133-134,147.
[18] Katsaounos C Z, Giokas D L, Vlessidis A G, Paleologos E K, Karayannis M I.The use of surfactant-based separation techniques for monitoring of orthophosphate in natural waters and wastewater [J].ScienceoftheTotalEnvironment,2003,305(1-3):157-167.
[19] Colombini S, Polesello S, Valsecchi S.Use of column-switching ion chromatography for the simultaneous determination of total nitrogen and phosphorus after microwave assisted persulphate digestion[J].JournalofChromatographyA,1998,822(9):162-166.
[20] 何江,张丰如.微波-H2O2消解法联合快速测定水中总氮总磷[J].广东化工,2008,35(7):141-143.
[21] 邓志华,周成,宁平.碱性过硫酸钾消解法测定总氮空白降低方法的探讨[J].现代化工,2010,30(2):346-349.
[22] 郭小颖.水中总磷测定有关问题的探讨[J].环境科技,2009,15(3):43-45.
[23] 国家环境保护总局.水和废水监测分析方法(第四版)[M].北京:中国环境科学出版社,2002.
Determination Method on Total Nitrogen and Total Phosphorus in Sea-buckthorn Stem Flow Liquid with Combined Digestion
WANGYu-gong,WANGHua,LIUJian-jun,YUZhi-feng
( Lanzhou Testing and Quality Supervision Center for Geological and Mineral Products, Ministry of Land and Resources, Lanzhou 730050, China)

stemflow solution; total nitrogen; total phosphorus; combined digestion; Spectrophotometry
2013-12-17;
2014-03-25; 接受日期: 2014-04-29
甘肃矿产资源勘查与综合利用工程技术研究项目(1306FTGA011)
王玉功,高级工程师,主要从事水质检测、岩石矿物分析研究。E-mail: wangyugong586@sohu.com。
0254-5357(2014)05-0665-05
O613.61; O613.62; O657.32
B

