培美曲塞或雷替曲塞联合顺铂一线治疗恶性胸膜间皮瘤的疗效与安全性观察
张淼慈,哈敏文
辽宁医学院附属第一医院 肿瘤科,辽宁锦州 121000
培美曲塞或雷替曲塞联合顺铂一线治疗恶性胸膜间皮瘤的疗效与安全性观察
张淼慈,哈敏文
辽宁医学院附属第一医院 肿瘤科,辽宁锦州 121000
目的 探讨雷替曲塞或培美曲塞联合顺铂一线治疗恶性胸膜间皮瘤(malignant pleural mesothelioma,MPM)的疗效和安全性。方法 2010年1月- 2013年1月辽宁医学院附属第一医院肿瘤科收治的36例失去根治性手术机会的MPM患者,随机分为两组,RP组18例接受雷替曲塞/顺铂方案,PP组18例接受培美曲塞/顺铂方案,比较两组的疗效和不良反应。结果 RP组和PP组客观有效率(22.2% vs 38.9%)、疾病控制率(72.2% vs 83.3%)、中位无疾病进展生存期(5.0个月vs 5.5个月)和中位总生存期(11.2个月vs 11.8个月)差异均无统计学意义(P>0.05)。虽然PP组血液学毒性发生率高于RP组,但两组不良反应发生率均无统计学差异(P>0.05)。结论 两方案一线治疗MPM的临床疗效相当,对于无经济条件而接受培美曲塞或希望尽可能避免血液学毒性的患者,雷替曲塞/顺铂方案可作为优选方案。
恶性胸膜间皮瘤;培美曲塞;雷替曲塞;顺铂
恶性胸膜间皮瘤(malignant pleural mesothelioma,MPM)是一种起源于胸膜间皮细胞的恶性肿瘤,暴露在空气中的石棉纤维是其发生、发展的主要危险因素[1-2]。自20世纪50年代,石棉的广泛应用导致其发病率和死亡率大幅度增加[3]。MPM侵袭性高、预后差,中位生存期<12个月[4-5]。对于多数MPM患者,全身化疗是唯一可能的治疗选择[6]。目前,培美曲塞/顺铂方案是其治疗的标准方案,但培美曲塞昂贵的价格限制了其在临床治疗中的应用。培美曲塞/顺铂治疗MPM的Ⅲ期研究(Evaluation of Mesothelioma in a PhaseⅢTrial of Pemetrexed with Cisplatin,EMPHACIS)与欧洲癌症治疗研究组织(European Organization for Research and Treatment of Cancer,EORTC)08983研究表明,培美曲塞/顺铂或雷替曲塞/顺铂分别与顺铂单药相比,均可提高近3个月的生存期,且不影响生活质量[7-8]。本研究比较雷替曲塞/顺铂或培美曲塞/顺铂治疗MPM的疗效及安全性,以期为MPM患者选择个体化的治疗方案提供参考。
资料和方法
1 一般资料 纳入标准:1)签署知情同意书;2)经病理组织学证实为MPM,不能行根治性切除的患者;3)存在单径或双径可测量病灶;4)WHO行为状态评分0 ~ 2分,年龄>18岁,预期寿命>12周;5)良好的肝肾功能和骨髓储备;6)可获得完整的随访资料。排除标准:1)既往接受过化疗、放疗或免疫治疗;2)第二原发恶性肿瘤;3)中枢神经系统转移;4)不能使用皮质类固醇激素;5)不能应用非甾体类抗炎药。按以上标准,2010年1月-2013年1月在辽宁医学院附属第一医院肿瘤科共有36例失去根治性手术机会的MPM患者纳入本研究。雷替曲塞/顺铂组(RP)18例,培美曲塞/顺铂组(PP)18例。两组患者在年龄、性别、KPS评分、病理类型、临床分期等方面分布平衡(P>0.05),具有可比性。见表1。

表1 MPM患者资料Tab. 1 Parameters of MPM patients included in this study (n)
2 治疗方法 雷替曲塞/顺铂组:雷替曲塞(南京正大天晴制药有限公司)3 mg/m2,d1,静脉注射>15 min;后给予顺铂80 mg/m2,静脉注射1 ~ 2 h,21 d为1周期。培美曲塞/顺铂组:培美曲塞(江苏豪森药业股份有限公司)500 mg/m2,d1,静脉输注>10 min;培美曲塞结束30 min后给予顺铂75 mg/m2,静脉输注>2 h,21 d为1周期。为了减轻不良反应,培美曲塞治疗过程中必须补充叶酸、维生素B12及皮质类固醇。每日口服叶酸400 μg,用药前1周开始,直至化疗结束后21 d;在用药前1周肌肉注射维生素B121 000 μg,每9周重复1次;培美曲塞治疗前1 d、当天和治疗后次日口服地塞米松4 mg,一日两次,以减少皮疹的发生。两组均给予标准的水化和止吐治疗。
3 疗效及不良反应评价标准 每2个化疗周期复查CT,评价近期疗效,由不参加本研究的两位医师依据实体瘤疗效评价标准1.0(Response Evaluation Criteria in Solid Tumors 1.0,RECIST 1.0)独立判断疗效。将近期疗效分为完全缓解(complete response,CR)、部分缓解(partial response,PR)、疾病稳定(stable disease,SD)和疾病进展(progressive disease,PD)。客观有效率(objective response rate,ORR)= (CR+PR)/总例数×100%。疾病控制率(disease control rate,DCR)=(CR+PR+SD)/总例数×100%。无疾病进展生存期(progression-free survival,PFS)定义为自患者接受化疗至疾病进展的时间。总生存期(overall survival,OS)定义为自患者接受化疗至随访截止或死亡的时间。化疗不良反应参照WHO抗肿瘤药物急性及亚急性不良反应分度评价标准进行评价。
4 统计学方法 应用SPSS17.0软件进行数据处理。两组临床病理特征、近期疗效及不良反应采用χ2检验。Kaplan-Meier法绘制OS、PFS曲线,生存差异采用Log-Rank法进行显著性检验。P<0.05为差异有统计学意义。
结 果
1 近期疗效 所有患者均接受2 ~ 8个周期的化疗。两组中均无CR。两组ORR分别为22.2%、38.9%;两组DCR分别为72.2%、83.3%。两组近期疗效差异无统计学意义(P>0.05)。见表2。

表2 近期疗效评价Tab. 2 Assessment of short-term effect (n)
2 远期疗效 末次随访时间为2014年4月2日。RP组中位无疾病进展生存期(median progressionfree survival, mPFS)为5.0个月(95% CI 3.129 ~ 6.871个月),中位总生存期(median overall survival,mOS)为11.2个月(95% CI 8.705 ~ 13.695个月)。PP组mPFS为5.5个月(95% CI 2.797 ~ 8.203个月),mOS为11.8个月(95% CI 7.226 ~16.374个月)。两组mPFS及mOS差异均无统计学意义(P>0.05)。见图1,图2。
3 不良反应 两组主要不良反应为胃肠道反应及骨髓抑制。PP组血液学不良反应发生率高于RP组,但两组差异无统计学意义(P>0.05)。两组间其余不良反应发生率差异均无统计学意义(P>0.05)。见表3。
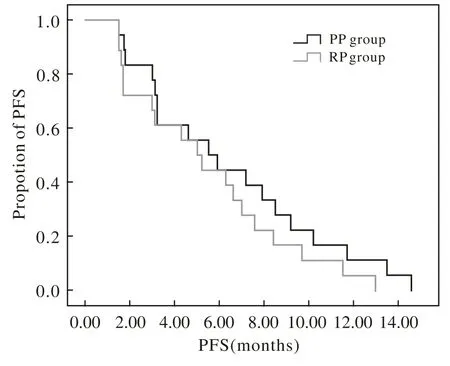
图 1 两组患者的PFS曲线Fig. 1 Progression-free survival curves of two groups
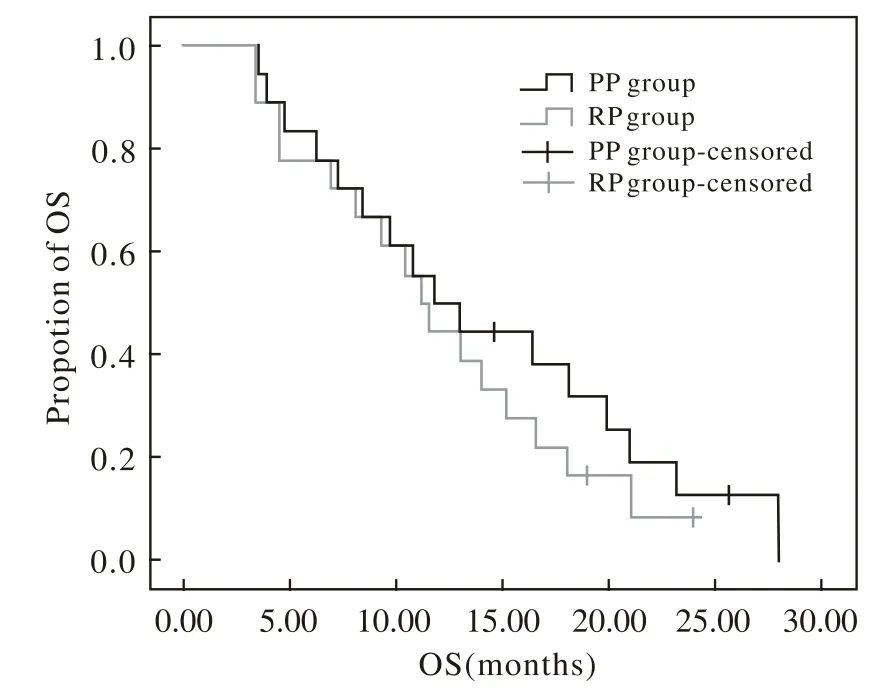
图 2 两组患者的OS曲线Fig. 2 Overall survival curves of two groups
讨 论
第三代抗叶酸新药(培美曲塞或雷替曲塞)联合顺铂是目前治疗晚期恶性胸膜间皮瘤的标准一线方案[9]。培美曲塞是一种新型多靶点叶酸拮抗剂,通过破坏细胞复制所必须的叶酸依赖性代谢过程抑制细胞复制[10]。体外研究显示,培美曲塞是通过抑制胸苷酸合成酶、二氢叶酸还原酶和甘氨酰胺核苷酸甲酰转移酶的活性发挥作用,这些酶都是胸腺嘧啶核苷酸和嘌呤核苷酸生物再合成的关键性叶酸依赖酶[11-12]。研究证实,与培美曲塞相比,雷替曲塞只特异性地抑制TS,导致脱氧尿嘧啶核苷酸生成脱氧胸腺嘧啶核苷酸减少,从而使DNA合成与修复所需的三磷酸胸苷减少[13-14]。
2003年,Vogelzang等[7]报道了多中心的培美曲塞Ⅲ期临床研究。448例不能手术的MPM患者随机分为培美曲塞联合顺铂组(n=226)和顺铂单药组(n=222)。培美曲塞联合顺铂组在117例患者入组后加用叶酸和维生素B12以减轻培美曲塞导致的血液系统和胃肠道不良反应。两组mOS(12.1个月vs 9.3个月,P=0.020)、mPFS(5.7个月vs 3.9个月,P=0.001)、ORR(41.3% vs 16.7%,P<0.001)均无统计学差异。2005年,Van Meerbeeck等[8]在JCO杂志上报道了EORTC的另一项Ⅲ期随机研究(EORTC 08983),这项研究招募了249例失去手术机会的MPM患者。患者随机分为雷替曲塞联合顺铂组(n=125)和顺铂单药组(n=124)。两组mOS为(11.4个月vs 8.8个月,P=0.048)有统计学差异,mPFS(5.3个月 vs 4.0个月,P=0.058)、ORR(23.6% vs 13.6%,P=0.056)无统计学差异。雷替曲塞联合顺铂的毒性可以耐受。本研究中,RP组与PP组的mOS(11.2个月vs 11.8个月,P>0.05)、mPFS(5.0个月vs 5.5个月,P>0.05),ORR(22.2% vs 38.9%,P>0.05)均无统计学差异。mPFS和mOS数值略低于上述Ⅲ期临床试验结果,可能与本研究样本例数相对不足有关。
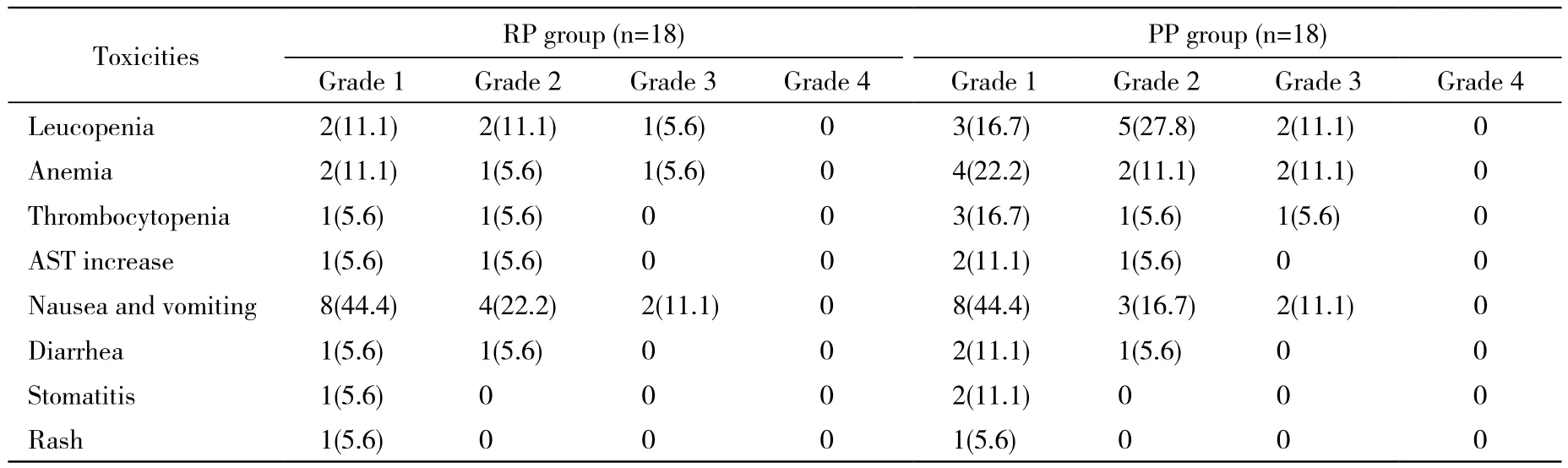
表3 两组不良反应Tab. 3 Adverse reactions of two groups (n, %)
雷替曲塞与培美曲塞均为抗叶酸制剂,且均能靶向抑制TS,都存在着剂量依赖性的血液学毒性和黏膜损伤。尽管预防性应用叶酸和维生素B12可以减少培美曲塞导致的血液学不良反应发生率,但在本研究中发现的主要血液学不良反应与预防性用药无关,提示二者的差异可能是由于与雷替曲塞相比,培美曲塞同时还作用于叶酸代谢的另外两个酶[15]。
两方案在临床疗效相当的情况下,雷替曲塞/顺铂方案存在以下3方面优势:应用该方案治疗的患者无需补充叶酸及维生素B12来降低化疗带来的骨髓抑制及胃肠道不良反应,使其在临床应用中更加方便,患者依从性更好;雷替曲塞/顺铂方案的血液学不良反应发生率相对较低,对于老年或骨髓造血功能不良的患者来说更易耐受;该方案可减轻患者的经济负担。
综上所述,雷替曲塞/顺铂方案一线治疗恶性胸膜间皮瘤的临床疗效与培美曲塞/顺铂方案相当,且安全性高、依从性好,对于无法承受培美曲塞治疗费用或希望尽可能避免血液学不良反应的患者,雷替曲塞/顺铂方案更有优势,更易被患者接受,可作为治疗MPM的优选方案。
1 Zhang J, Zhang Q, Zhao W, et al. Pleural resection and pleural infusion chemotherapy for therapy of malignant pleural mesothelioma[J]. Genet Mol Res, 2014, 13(1): 483-489.
2 Porpodis K, Zarogoulidis P, Boutsikou EA, et al. Malignant pleural mesothelioma: current and future perspectives[J]. J Thorac Dis,2013, 5(4): S397-S406.
3 Pinto C, Novello S, Torri V, et al. Second Italian consensus conference on malignant pleural mesothelioma: state of the art and recommendations[J]. Cancer Treat Rev, 2013, 39(4): 328-339.
4 张红梅,刘培.一例胸膜间皮瘤的循证治疗[J].海南医学,2012,23(9):128-131.
5 Zucali PA, De Vincenzo F, Simonelli M, et al. Future developments in the management of malignant pleural mesothelioma[J]. Expert Rev Anticancer Ther, 2009, 9(4): 453-467.
6 Ray M, Kindler HL. Malignant pleural mesothelioma: an update on biomarkers and treatment[J]. Chest, 2009, 136(3):888-896.
7 Vogelzang NJ, Rusthoven JJ, Symanowski J, et al. Phase III study of pemetrexed in combination with cisplatin versus cisplatin alone in patients with malignant pleural mesothelioma[J]. J Clin Oncol,2003, 21(14): 2636-2644.
8 Van Meerbeeck JP, Gaafar R, Manegold C, et al. Randomized phase III study of cisplatin with or without raltitrexed in patients with malignant pleural mesothelioma: an intergroup study of the European Organisation for Research and Treatment of Cancer Lung Cancer Group and the National Cancer Institute of Canada[J]. J Clin Oncol, 2005, 23(28):6881-6889.
9 Stahel RA, Weder W, Lievens Y, et al. Malignant pleural mesothelioma: ESMO Clinical Practice Guidelines for diagnosis,treatment and follow-up[J]. Ann Oncol, 2010, 21(S5):v126-v128.
10 Wu YL, Sun Y, Zhou CC, et al. Survival without common toxicity criteria grade 3/4 toxicity following second-line treatment with pemetrexed for nonsquamous non-small cell lung cancer in Chinese patients[J]. Chin Med J (Engl), 2013, 126(24): 4624-4628.
11 Schultz RM, Chen VJ, Bewley JR, et al. Biological activity of the multitargeted antifolate, MTA (LY231514), in human cell lines with different resistance mechanisms to antifolate drugs[J]. Semin Oncol, 1999, 26(2 Suppl 6): 68-73.
12 Mendelsohn LG, Shih C, Chen VJ, et al. Enzyme inhibition,polyglutamation, and the effect of LY231514 (MTA) on purine biosynthesis[J]. Semin Oncol, 1999, 26(2 Suppl 6): 42-47.
13 Baas P, Ardizzoni A, Grossi F, et al. The activity of raltitrexed(Tomudex (R)) in malignant pleural mesothelioma: an EORTC phase II study (08992)[J]. Eur J Cancer, 2003, 39(3): 353-357.
14 Lv YT, Du PJ, Wang QY, et al. A novel approach to cloning and expression of human thymidylate synthase[J]. Asian Pac J Cancer Prev, 2013, 14(12): 7523-7527.
15 Surmont VF, Van Meerbeeck JP. Raltitrexed in mesothelioma[J]. Expert Rev Anticancer Ther, 2011, 11(10): 1481-1490.
本刊对来稿中统计学符号书写要求
本刊常用统计学符号书写要求如下:
Efficacy and safety of pemetrexed or raltitrexed in combination with cisplatin as first-line chemotherapy for malignant pleural mesothelioma
ZHANG Miao-ci, HA Min-wen
Department of Oncology, The First Affiliated Hospital of Liaoning Medical University, Jinzhou 121000, Liaoning Province, China
HA Min-wen. Email: hmw2015@163.com
Objective To evaluate the efficacy and safety of pemetrexed or raltitrexed in combination with cisplatin as first-line chemotherapy for malignant pleural mesothelioma. Methods A total of 36 patients with malignant pleural mesothelioma who were not candidates for curative surgery admitted to Department of Oncology, First Affiliated Hospital of Liaoning Medical University from January 2010 to January 2013 were randomly divided into RP group (n=18) and PP group (n=18). In RP group, raltitrexed in combination with cisplatin was applied, while in PP group, pemetrexed combined with cisplatin was administered. The efficacy and adverse reactions in two groups were observed and compared. Results No statistically significant differences were found in the objective response rate, disease control rate, median progression-free survival and median overall survival between RP group and PP group (22.2% vs 38.9%, 72.2% vs 83.3%, 5.0 months vs 5.5 months, 11.2 months vs 11.8 months, P>0.05). The incidence of hematological toxicity was higher in PP group than in RP group, but no statistically differences in adverse reaction were found between the two groups (P>0.05). Conclusion The clinical efficacy of the two regimens as first-line chemotherapy for malignant pleural mesothelioma is similar, raltitrexed/cisplatin is a preferred regimen for patients who can not afford pemetrexed or try to avoid hematological toxicity as much as possible.
malignant pleural mesothelioma; pemetrexed; raltitrexed; cisplatin
R 734.3
A
2095-5227(2014)10-1004-04
10.3969/j.issn.2095-5227.2014.10.008
时间:2014-07-15 09:49
http://www.cnki.net/kcms/detail/11.3275.R.20140715.0949.003.html
2014-06-03
张淼慈,女,在读硕士。研究方向:非小细胞肺癌的治疗。Email: Cindy11@yeah.net
哈敏文,男,博士,主任医师,主任。Email: hmw2015 @163.com

