聚(L-乳酸)体内外降解相关性研究
鲍时根,张 云,朱玉俊,杨怀志,杜 军,马建华
(1.合肥工业大学控释药物研究所,安徽 合肥 230009;2.安徽中人科技有限责任公司,安徽 合肥 230088)
◇药学研究◇
聚(L-乳酸)体内外降解相关性研究
鲍时根1,2,张 云1,2,朱玉俊1,2,杨怀志2,杜 军2,马建华1,2
(1.合肥工业大学控释药物研究所,安徽 合肥 230009;2.安徽中人科技有限责任公司,安徽 合肥 230088)
目的 考察聚(L-乳酸)(PLLA)植入剂体内外降解特性黏数和失重变化的相关性。方法 以辛酸亚锡为催化剂,通过直接缩聚法制备聚(L-乳酸)(PLLA)树脂,经精制得药用辅料;将药用辅料通过特定设备压制成空白植入剂,考察其在大白兔体内的降解情况,并与其在 pH7.4的磷酸盐缓冲液的体外降解相比较。结果 聚(L-乳酸)植入剂样品降解后的特性黏数与降解时间(wk)呈指数关系,失重百分率与降解时间(wk)呈线性关系。结论 体内的特性黏数与体外的特性黏数数值相近,体外失重比体内快。
聚(L-乳酸);直接缩聚;体内外降解;特性黏数;失重
聚(L-乳酸)是一种重要的可生物降解的人工合成高分子材料,因其具有良好的生物相容性和生物可吸收性,已在骨折内固定、组织工程支架、医疗植入、外科缝合线、药物缓控释体系等方面得到了广泛应用,国内外有不少科研人员对其在体内外的降解 情况进行了大量试验研究[1-5],但对聚(L-乳酸)空白植入剂体内外降解的特性黏数和失重的变化规律研究并不多。由于药用辅料对纯度要求较高而对材料的机械强度要求不是很高,因此可以选用医药级的 L-乳酸,以辛酸亚锡为催化剂,通过直接缩聚制备聚(L-乳酸)(PLLA)树脂,经精制后可得高纯度的聚(L-乳酸)药用辅料。辅料经压制后制成空白植入剂,分别观察空白植入剂在大白鼠体内和磷酸盐缓冲液中的降解情况,测试降解前后聚(L-乳酸)的特性黏数和重量,并考察其特性黏数和失重的变化规律。
1 仪器和试剂
L-乳酸:医药级,Purac公司;辛酸亚锡 (Sn (oct)2)、三氯甲烷、甲醇、磷酸二氢钾、氢氧化钠均为分析纯,中国医药集团上海化学试剂公司;微孔滤膜 φ25 mm、孔径0.45 μm,上海半岛实业有限公司净化器材厂。
10 L玻璃反应釜:杭州亿捷科技有限公司;植入剂压药机:安徽中人科技有限责任公司;内径0.38 mm毛细管黏度计:国药集团上海玻璃仪器公司。
健康新西兰大白兔,雌雄不限,安徽中人科技有限责任公司药理中心提供。
2 方法与结果
2.1 聚(L-乳酸)的制备 按文献[6]的合成方法,将 L-乳酸与辛酸亚锡按摩尔比8 000∶1的比例加料于10 L玻璃反应釜中,于 180℃、2 kPa的压力下,直接缩聚,分别于 8、16、24 h取样(分别记为 1#、2#、3#样),放出合成的聚(L-乳酸)树脂,经粉碎后,加三氯甲烷溶解,用甲醇沉淀。真空过滤,滤饼于105℃、2 kPa的条件下,干燥 24 h,得成品聚(L-乳酸)。分别测试1#、2#、3#精制后成品辅料的特性黏数为22.58、33.18、47.21,测试条件:溶剂为三氯甲烷、温度25℃、毛细管为0.38 mm的乌式黏度计。
2.2 聚(L-乳酸)空白植入剂的制备 取聚(L-乳酸)1#,2#,3#样品适量,分别过 120目筛,将滤过的粉料于植入剂压药机中进行压制,制得直径(0.90 ±0.02)mm、长(3.0±0.2)mm的空白植入剂。
2.3 聚(L-乳酸)空白植入剂的体内植入 大白兔经 25 g·L-1巴比妥钠按 1 mg·kg-1耳缘静脉麻醉后[3],于无菌条件下将 1#、2#、3#空白植入剂植入(各24个试样),每个试样中有4粒空白植入剂,分8组随机植入 24只兔脊柱两侧皮下组织中。每只兔植入1个试样(4粒空白植入剂),脊柱每侧各 2粒。于2、4、8、16、32、64、128及144 wk按预定分组取样,样品包括试样和纤维包膜。清洗干净后放入三氯甲烷溶液中,经0.45 μm微孔滤膜过滤,加甲醇沉淀,过滤,真空干燥样品。分别于 2、4、8、16、32、64、128及 144 wk(无法测试)测试样品的特性黏数和失重百分率,具体数据分别见表1,2。
表1 聚(L-乳酸)植入后体内外特性黏数测试结果[(±s),n=5]
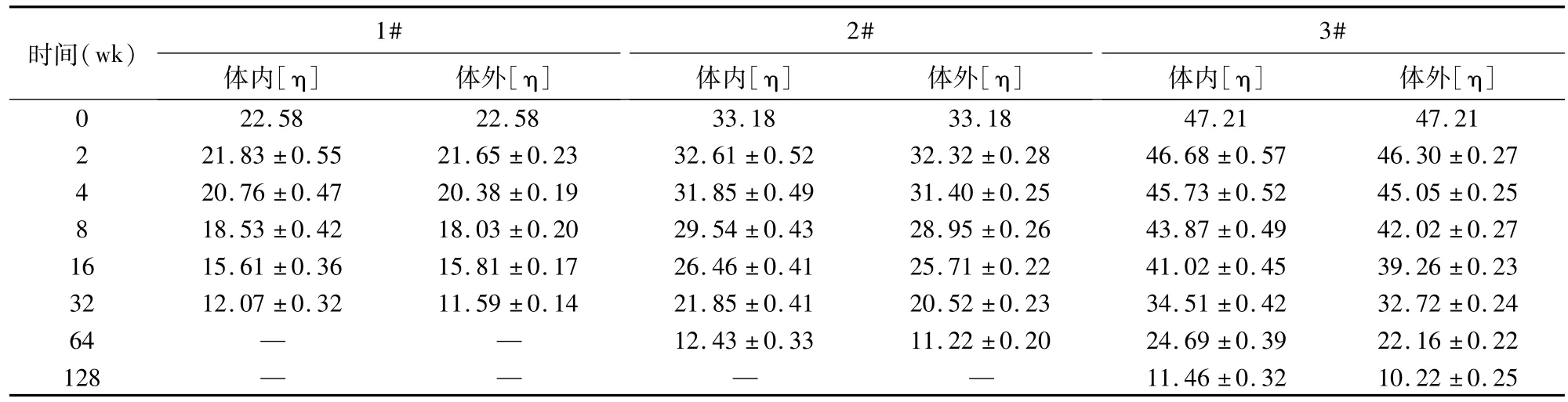
表1 聚(L-乳酸)植入后体内外特性黏数测试结果[(±s),n=5]
注:“—”表示无法测试。
时间(wk)1#体内[η] 体外[η]2#体内[η] 体外[η]3#体内[η] 体外[η]0 11.46±0.32 10.22±0.25 22.58 22.58 33.18 33.18 47.21 47.21 2 21.83±0.55 21.65±0.23 32.61±0.52 32.32±0.28 46.68±0.57 46.30±0.27 4 20.76±0.47 20.38±0.19 31.85±0.49 31.40±0.25 45.73±0.52 45.05±0.25 8 18.53±0.42 18.03±0.20 29.54±0.43 28.95±0.26 43.87±0.49 42.02±0.27 16 15.61±0.36 15.81±0.17 26.46±0.41 25.71±0.22 41.02±0.45 39.26±0.23 32 12.07±0.32 11.59±0.14 21.85±0.41 20.52±0.23 34.51±0.42 32.72±0.24 64 — — 12.43±0.33 11.22±0.20 24.69±0.39 22.16±0.22 128 — — — —
表2 聚(L-乳酸)植入后体内外失重测试结果[(±s),n=5]
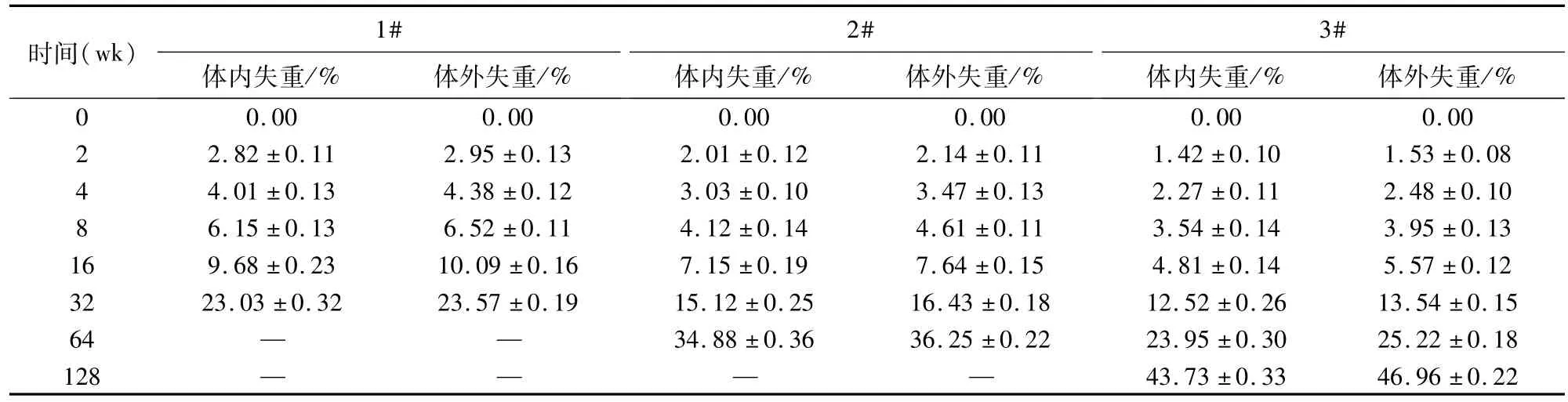
表2 聚(L-乳酸)植入后体内外失重测试结果[(±s),n=5]
注:“—”表示无法测试。
时间(wk)1#体内失重/% 体外失重/% 2#体内失重/% 体外失重/% 3#体内失重/% 体外失重/% 0 0.00 0.00 0.00 0.00 0.00 0.00 2 43.73±0.33 46.96±0.22 2.82±0.11 2.95±0.13 2.01±0.12 2.14±0.11 1.42±0.10 1.53±0.08 4 4.01±0.13 4.38±0.12 3.03±0.10 3.47±0.13 2.27±0.11 2.48±0.10 8 6.15±0.13 6.52±0.11 4.12±0.14 4.61±0.11 3.54±0.14 3.95±0.13 16 9.68±0.23 10.09±0.16 7.15±0.19 7.64±0.15 4.81±0.14 5.57±0.12 32 23.03±0.32 23.57±0.19 15.12±0.25 16.43±0.18 12.52±0.26 13.54±0.15 64 — — 34.88±0.36 36.25±0.22 23.95±0.30 25.22±0.18 128 — — — —
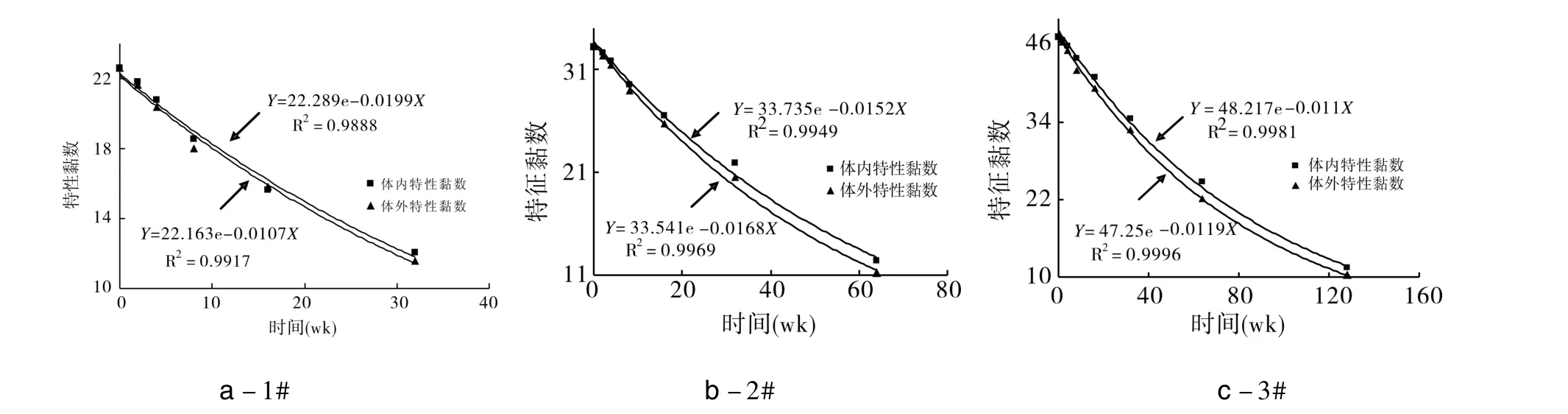
图1 a-1#,b-2#,c-3#体内、外降解时间与特性黏数关系(n=5)
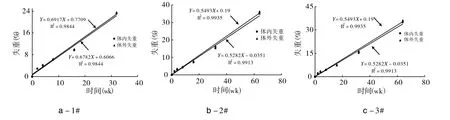
图2 a-1#,b-2#,c-3#体内、外降解时间与失重的关系(n=5)
2.4 聚(L-乳酸)空白植入剂的体外降解 将 2 g聚(L-乳酸)空白植入剂置入由磷酸二氢钾、氢氧化钠制备的 pH=7.4的缓冲液中,体积为 1 L,温度(37±1)℃,每周更换缓冲液一次,分别于2、4、8、16、32、64、128及144 wk(无法测试)取样,清洗、精制干燥。分别测试试样降解前后的特性黏数和重量,各时间的特性黏数和失重百分率具体数据分别见表1,2。分别将1#、2#、3#样体内外降解数据统计学处理,见图1,2。结果表明:无论是体内还是体外,起始特性黏数为20~50的聚(L-乳酸)空白植入剂试样降解后的特性黏数与降解时间(wk)呈指数关系,且体内的特性黏数数值与体外的特性黏数数值相近,体内的特性黏数数值约为体外的 1.2倍。同时体内和体外的失重百分率与降解时间呈线性关系,且体内失重速度比体外的失重速度要慢。另外特性黏数大的聚(L-乳酸)空白植入剂与特性黏数小的相比,无论体内还是体外特性黏数大的失重速度比特性黏数小的慢。
3 讨论
聚(L-乳酸)空白植入剂通过体内外的降解试验,可以发现降解后残留的聚(L-乳酸)试样体内的特性黏数数值大于体外的特性黏数数值,同时体外的失重百分率大于体内的失重百分率。造成这种情况的原因可能是由于聚(L-乳酸)试样被植入到体内一段时间后,被其周围新长出的包膜所包裹,难以充分吸收周围组织中的水分,致使体内的聚(L-乳酸)试样降解相对较慢。另外特性黏数大即分子量相对较大的聚(L-乳酸),与特性黏数小的聚(L-乳酸)相比较,分子链相对较长,吸水后链段中酯键断裂的速度相对较慢,这就导致特性黏数大的比特性黏数小的聚(L-乳酸)无论是体内还是体外失重速度都相对较慢。
[1] 金玉顺,商育伟,郭文莉,等.聚 DL-乳酸的合成与降解性能研究[J].化学与黏合,2008,30(5):35-37.
[2] 张 力,熊成东,吕春堂.可吸收内固定材料 L/DL-聚乳酸的体外降解特性[J].中国组织工程研究与临床康复,2011,15 (29):5347-5351.
[3] 陈宇轩,吕春堂,雷德林,等.生物可吸收材料 L/DL-聚乳酸的生物相容性及体内降解[J].第四军医大学学报,2000,21(4):417-420.
[4] 杨 帆,陈一岳,林 茵,等.聚乳酸的降解性能及其微球剂的研究[J].中国药房,2002,13(5):263-265.
[5] Pistner H,Gutwald R,Ordung R,et al.Poly(L-lactide):a longterm degradation study in vivo[J].Biomaterials,1993,14(9):671 -677.
[6] 赵耀明,张 军,麦杭珍.直接聚合法合成聚乳酸的研究[J].合成纤维,2001,30(3):3-5.
Poly(L-lactic acid)degradation correlation study in vivo and in vitro
BAO Shi-gen1,2,ZHANG Yun1,2,ZHU Yu-jun1,2,et al
(1.Sustained-Release Drug Laboratory of Hefei University of Technology,Hefei,Anhui 230009,China;2.Anhui Zhong Ren Science and Technology Co.,Ltd.,Hefei,Anhui 230088,China)
Objective To investigate the correlation of intrinsic viscosity and weightlessness in vivo and in vitro degradation of poly(L-lactic acid)(PLLA)implants.Methods Stannous octoate as a cataly,through polycondensation preparation of poly(L-lactic acid)(PLLA)resin,was refined to obtain a pharmaceutic excipient,which was pressed into the blank implants by a particular device.We studied its characteristics of degradation in rabbits in vivo,and compared with its degradation in phosphate buffer in vitro.Results Intrinsic viscosity of poly(L-lactic acid)was exponentially related to the degradation time(wk),while that weightlessness showed a linear correlation of the degradation time(wk).Conclusions The intrinsic viscosity numbers of poly(L-lactic acid)in vivo are similar to that in vitro.The weight of poly(L-lactic acid)reduces faster in vitro than that in vivo.
poly(L-lactic acid);polycondensation;in vivo and in vitro degradation;intrinsic viscosity;weightlessness
10.3969/j.issn.1009-6469.2014.05.005
2013-08-20,
2013-12-20)
国家自然科学基金(No C03031702);科技型中小企业技术创新基金(No 12C26213403306)

