自组装法制备载有阿奇霉素的聚己内酯纳米微球的研究
张幼维,赵炯心
(纤维材料改性国家重点实验室,东华大学材料科学与工程学院,上海 201620)
研究论文
自组装法制备载有阿奇霉素的聚己内酯纳米微球的研究
张幼维,赵炯心
(纤维材料改性国家重点实验室,东华大学材料科学与工程学院,上海 201620)
在没有表面活性剂存在的条件下,通过微相逆转法,阿奇霉素与聚己内酯自组装形成了载有阿奇霉素的聚己内酯纳米微球。采用动态激光光散射、扫描电镜观察、原子力显微镜观察、紫外分光光度法等手段表征了纳米微球的大小、形态以及包封率和载药量,并探讨了纳米微球的形成机理。研究结果表明,采用微相逆转法可以成功制得高包封率和高载药量的载药纳米微球,且其水分散液在低温下十分稳定。
阿奇霉素 聚己内酯 自组装
阿奇霉素是新一代大环内酯类抗生素,主要用于呼吸道、皮肤和软组织感染[1]。阿奇霉素具有对酸稳定、半衰期长、在感染部位组织及细胞内浓度高等优点,但存在体内分布广泛,对肝、肾有一定损害,不能长期使用等缺点。为降低阿奇霉素的不良反应,美国辉瑞制药公司开发的阿奇霉素缓释制剂,已于2005年6月经FDA批准上市,用于成人轻中度急性细菌性鼻炎(ABS)和社区获得性肺炎(CAP)的治疗。
通常采用乳化溶剂挥发法和乳化溶剂扩散法等,制备各种载药的缓释微球[2-4],但由此制备得到的微球,其尺寸较大,通常在微米级,因而无法通过粘膜或经体循环直接把药物输送到靶向组织;同时由于其疏水的表面,微球也极易被蛋白质吸附和被网状内皮系统的巨噬细胞识别并捕捉。为克服这种缺陷,现有文献或专利采用引入亲水性嵌段或接枝链的方法,制备两亲性嵌段或接枝共聚物,然后将其作为载体材料,通过与药物在选择性溶剂中共胶束化,制备得到核由疏水嵌段或接枝链和疏水药物组成、壳由亲水嵌段或接枝链组成的载药纳米微球[5-6]。
笔者报道了一种简便的制备载药纳米微球的方法——微相逆转法。选用具有良好人体安全性及可生物降解性的聚己内酯(PCL)作为载体材料,通过微相逆转方法制备了载有阿奇霉素的PCL纳米微球,对微球的尺寸、形态以及载料量、包封率等进行了表征。
1 实 验
1.1 原料
阿奇霉素(Azi,纯度≥95%),上海华蓝化学科技有限公司;
阿奇霉素标准品,纯度为92.8%,中国药品生物制品检定所;
聚己内酯(PCL),深圳市易生新材料有限公司(Mn=8.938×104g/mol,Mw=9.852×104g/mol,D=1.1);
N,N-二甲基甲酰胺(DMF),分析纯,国药集团化学试剂有限公司;
甲醇,分析纯,国药集团化学试剂有限公司;纤维素半透膜,截留分子质量为14 000,上海绿鸟科技有限公司。
1.2 载有阿奇霉素的聚己内酯纳米微球的制备
首先,将装有适量PCL和DMF的容量瓶放在磁力搅拌器上搅拌过夜,配制浓度为15 mg/m L的PCL/DMF溶液母液(其他浓度的PCL/DMF溶液由该母液稀释得到)。然后,用移液管移取5 mL PCL/DMF溶液,并加入适量的阿奇霉素粉末,磁力搅拌10 min使其溶解并均匀分散。接着,将上述含有阿奇霉素和PCL的DMF溶液用上海奥尔科特生物科技有限公司生产的ALC-IP型精密微量注射泵以2m L/h的速度注入50 m L处于磁力搅拌的去离子水中。注入结束后,继续搅拌30 min。然后将其转入透析袋中,对水透析3天,每天换3~4次水,以除去DMF以及未包封的阿奇霉素。将制备得到的载有阿奇霉素的聚己内酯纳米微球的水分散液置于4℃冰箱中保存。
1.3 载药量和包封率的测定
将阿奇霉素标准品溶于甲醇中,精确配制一系列已知浓度的阿奇霉素/甲醇溶液。然后采用UV-7504PC型紫外可见分光光度计测定溶液在205 nm处的紫外吸收值,绘制标准曲线。
将1.2制备的载药纳米微球的水分散液冷冻干燥,得到微球粉末。精密称取适量的载药纳米微球粉末搅拌分散于10 m L甲醇中。静置后取上清液,并用0.2μm的有机相滤器过滤后,测定其在205 nm处的紫外吸收。根据标准曲线计算微球粉末中阿奇霉素的含量,并计算载药量(LC)和包封率(EE)。

1.4 分析测试
纳米微球的流体力学直径和多分散性系数用Malvern粒径仪(DTS1060)测定,重复测定3次,取平均值。微球的形态用philips XL 30扫描电镜和Nanoscope IV(Digital Instruments)原子力显微镜(AFM)观察。将5μL的纳米微球分散液小心滴在洗净的玻璃小片上,待水基本挥干后,转入干燥器中干燥48 h,经喷金后进行扫描电镜测试。将5μL的纳米微球分散液小心滴在新辟开的云母片上,在室温下干燥12 h后转入40℃的烘箱中干燥2 h,进行AFM测试,在空气中采用Tapping mode观察。
2 结果与讨论
2.1 聚己内酯-阿奇霉素纳米微球的制备
通常高分子材料的微粒化需要大量乳化剂的辅助。笔者在研究中发现[7],在没有表面活性剂的存在下,聚己内酯(PCL)可以通过微相逆转方法生成纳米粒子。即,将PCL的有机溶剂(二甲基甲酰胺,四氢呋喃,二氧六环)的稀溶液逐滴缓慢加入大量处于搅拌的去离子水中,就会出现纳米聚集体特有的淡蓝色乳光。形成的PCL纳米粒子的尺寸随着溶剂极性的增大而减小。将PCL/有机溶剂溶液滴加入水中后,体系由原先的PCL的良溶剂转变为不良溶剂,PCL分子链会聚集坍塌,亲水性的PCL端羧基和端羟基会选择性地迁移并富集在聚集体的表面,从而使其得以稳定(图1)。
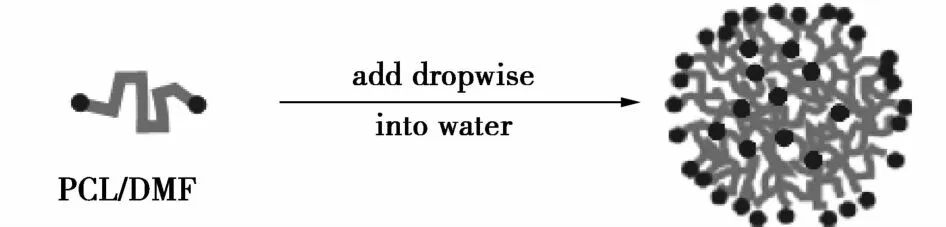
图1 无皂PCL纳米粒子的形成示意图
PCL具有优越的可生物降解性和生物相容性,并获得了美国FDA的批准,因而是一种理想的药物载体材料[8]。在本文中,笔者尝试采用这种微相逆转方法来制备载药纳米微球。将阿奇霉素和PCL共同溶解于DMF中,然后将溶液缓慢注入处于搅拌的大量去离子水中,制备得到了带有淡蓝色乳光的分散液。当保持溶液与水的体积比为1∶10时,在PCL浓度小于20 mg/m L、阿奇霉素浓度小于10 mg/m L条件下,制备得到的分散液透明,没有出现宏观沉淀物。
笔者认为,在相转变过程中,由于阿奇霉素的疏水性,阿奇霉素会和PCL一起聚集坍塌,从而形成内部为阿奇霉素和PCL、表层为PCL端基的聚己内酯-阿奇霉素纳米微球(即载药纳米微球)(图2)。
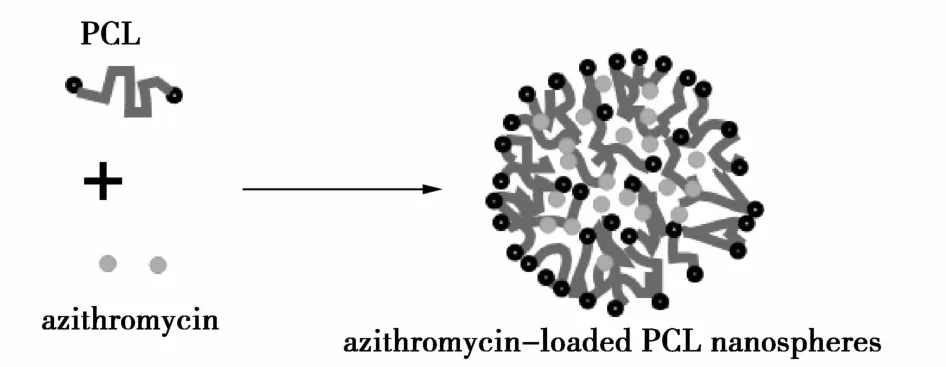
图2 载有阿奇霉素的PCL纳米微球的形成示意图
2.2 载药纳米微球的尺寸和形态
图3、图4和图5分别是PCL浓度为12.5 mg/m L、阿奇霉素浓度为5.0 mg/mL的PCL/AZ/DMF溶液制备得到的载药PCL纳米微球的流体力学直径分布图、扫描电镜照片和原子力显微镜照片。从图3中可以看到,微球尺寸分布在59~250 nm之间,尺寸较小(<Dh>=107.5 nm),分布也较窄(PDI=0.09)。由图4可以看出,载药纳米微球基本呈圆形,粒径在60~220 nm之间,与动态光散射的结果相吻合(图3)。
从图5载药PCL纳米微球的AFM照片可以看到,纳米微球具有很好的圆形轮廓,表面光滑,且直径的分布较均匀,同时坍塌十分严重(直径在120~230 nm之间,而高度<10 nm)。在AFM制样过程中,为加速微球的干燥,笔者将样品在40℃烘箱中放置了2 h。由于PCL的玻璃化转变温度很低,约为-60℃,其熔点也仅为60℃,因而,在40℃热处理条件下,PCL大分子链可能会发生明显的形变,从而导致微球在基底上严重坍塌。
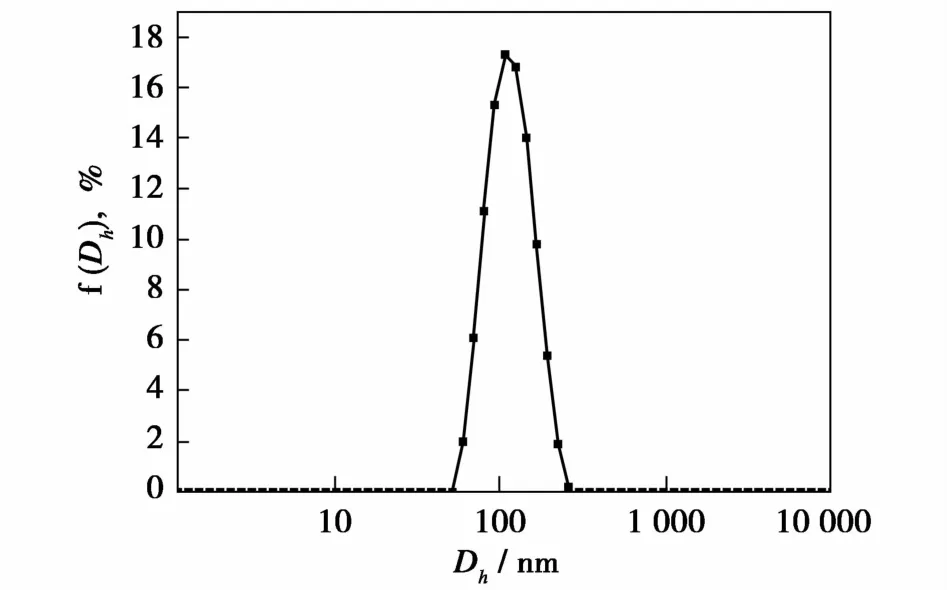
图3 载药PCL纳米微球的流体力学直径分布图

图4 载药PCL纳米微球的SEM照片
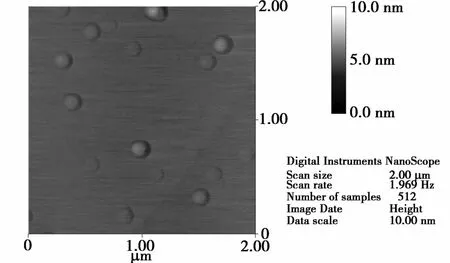
图5 载药PCL纳米微球的AFM照片
2.3 制备条件对载药微球的尺寸、载药量和包封率的影响
表1为固定初始溶液中PCL的浓度,改变阿奇霉素投料量制备得到的一系列载药微球的尺寸、多分散性系数、载药量和包封率数据。从表1中可以看出,随着初始溶液中阿奇霉素的投料浓度从0增加到4.0 mg/m L,载药PCL纳米微球的尺寸稍有变大(<Dh>从90 nm增加至104 nm),多分散系数(μ/Г2)基本保持不变。当阿奇霉素的投料浓度继续增大到5.0 mg/m L时,载药PCL纳米微球的粒径和多分散系数均明显增大(<Dh>从104 nm增至124 nm;μ/Г2由0.13增至0.27),且其流体力学直径分布曲线为双峰分布,说明体系中开始出现尺寸较大的聚集体。从表1中还可以看到,随着阿奇霉素投料浓度的增加,载药微球的载药量逐渐增加;在1.0~4.0 mg/m L的阿奇霉素浓度范围内,载药微球的包封率均很大,当阿奇霉素浓度增至5.0 mg/m L时,包封率开始有所下降,但仍较大(92.5%)。高的包封率可归因于PCL与阿奇霉素结构的相似性。PCL和阿奇霉素均为内酯类结构(图6),两者都含有大量的酯基,因此具有良好的相容性。此外,阿奇霉素还含有大量的羟基,可与PCL的酯羰基形成氢键作用,这也有助于两者的相容。
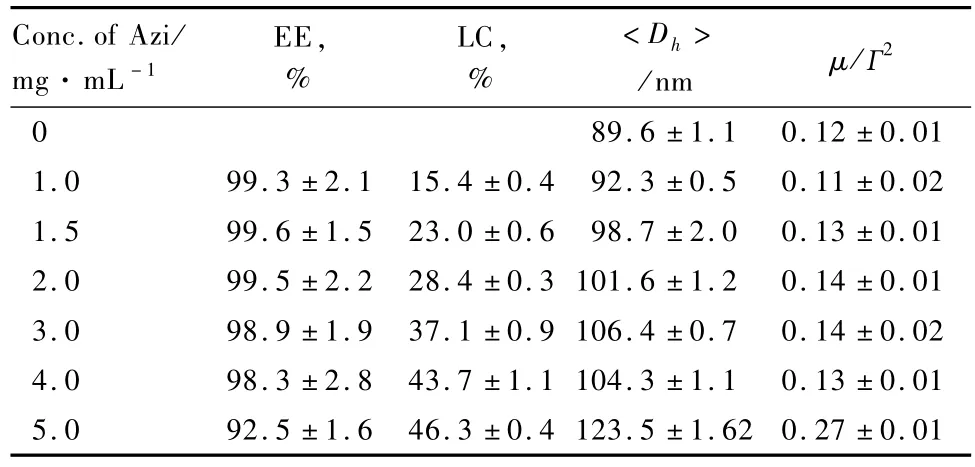
表1 阿奇霉素(Azi)的浓度对载药微球尺寸、多分散性系数(μ/Г2)、载药量(LC)和包封率(EE)的影响
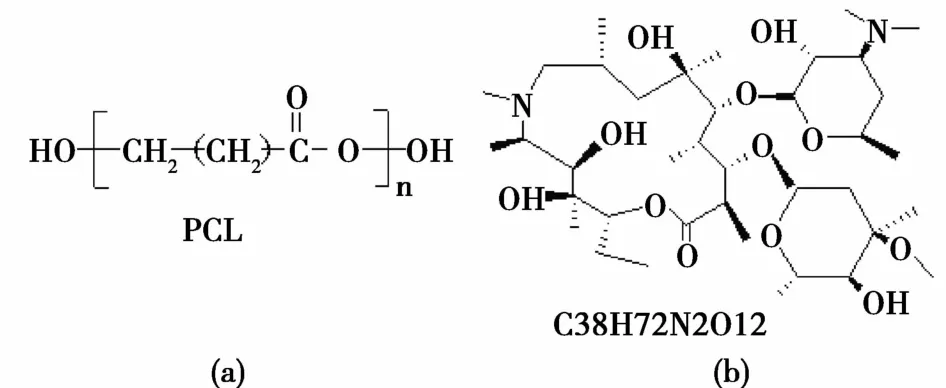
图6 PCL和阿奇霉素的化学结构式

表2 初始PCL浓度对载药微球尺寸、多分散性系数(μ/Г2)、载药量和包封率的影响
表2为固定初始溶液中阿奇霉素与PCL的投料比例,改变PCL浓度制备得到的一系列载药微球的尺寸、多分散性系数、载药量和包封率数据。从表2中可以看出,随着PCL浓度从5 mg/m L增加到15 mg/m L,载药微球的尺寸先是减少然后增加。从整体上看,载药微球的尺寸变化幅度较小(<Dh>在87~114 nm之间)。从表2中还可以看到,当维持较低的阿奇霉素投料量(投料载药量为28.6%)时,载药微球的包封率很高,在98%以上。
2.4 载药微球的稳定性
将PCL浓度为12.5 mg/m L、阿奇霉素浓度为5.0 mg/m L条件下制备得到的载药PCL纳米微球的水分散液在4℃冰箱中存放6个月后,溶液表观没有发生变化。0,1,2,4,6个月的载药量分别为27.9%,27.8%,27.4%,26.9%和27.6%;粒径分别为107.3,109.2,108.8,106.5,106.2 nm。说明在低温下,载药 PCL纳米微球的水分散液十分稳定。
3 结 论
通过微相逆转方法,阿奇霉素和聚己内酯可以在水中自组装形成稳定分散的载药PCL纳米微球。该方法简便,无需使用表面活性剂,包封率和载药量均较高。同时,载药PCL纳米微球的水分散液具有良好的稳定性。
[1] 陈亦芳,李寒,郝风兰,等.Azithromycin的体外抗菌作用[J].中国抗生素杂志,1995,20:178-185.
[2] 王哲,张秀梅,倪宏哲,等.聚乳酸载阿奇霉素微球包裹和体外释放行为[J].中国生物医学工程学报,2009,28:314-316.
[3] 钱一鑫,高坤,张伟,等.乳化溶解扩散法制备阿奇霉素缓释微球[J].中国药剂学杂志,2008,6:6-13.
[4] 王健松,朱家壁,吕瑞勤,等.肺靶向阿奇霉素脂质体的制备及其在小鼠体内的分布[J].药学学报,2005,40:274-278.
[5] 霍美蓉,张勇,周建平,等.紫杉醇壳聚糖自组装纳米胶束冻干粉针的制备及理化性质研究[J].中国药学杂志,2009,43:199-204
[6] Choucair A,Soo P L,Eisenberg A.Active loading and tunable release of doxorubicin from block copolymer vesicles[J].Langmuir,2005,21:9308-9313.
[7] Zhang YW,Jiang M,Zhao JX,et al.pH-responsive core-shell particles and hollow spheres attained by macromolecular self-assembly[J].Langmuir,2005,21:1531-1538.
[8] 艾合麦提·玉素甫,王振斌,朱良.可生物降解材料聚己内酯在医学上的应用进展[J].国际生物医学工程杂志,2005,28:19-23.
Preparation of Poly(ε-cap rolactone)-Azithrom ycin Nanospheres via Self-assem b ly
Zhang Youwei,Zhao Jiongxin
(State Key Laboratory for Modification of Chemical Fibers and Polymer Materials,College of Material Science and Engineering,Donghua University,Shanghai 201620,China)
In the absence of surfactants,azithromycin(Azi)and poly(ε-caprolactone)(PCL)self-assemble into PCL-Azinanospheres viamini-phase inversion method.Dynamic light scattering,SEM and AFM observations,as well as ultraviolet spectroscopy were used to characterize the size,morphology,encapsulation efficiency(EE)and loading capacity(LC)of PCL-Azi nanospheres.Also,the formation mechanism of the nanospheres was discussed. The results show that PCL-Azi nanospheres with high EE(>90%)and LC(>40%)can be facilely prepared via the mini-phase inversion method,and the water dispersion of the nanospheres was very stable at low temperatures.
azithromycin;poly(ε-caprolactone);m ini-phase inversion method;self-assembly
O69;TQ46
A
1006-334X(2014)04-0001-04
2014-10-25
张幼维(1974—),女,浙江奉化人,教授,研究方向为聚合物基纳米微球。

