AlCl3在海绵钛生产中的危害及其解决措施
张 静,陈德明,马艳琴,陈映志
(攀枝花钢企欣宇化工有限公司,四川 攀枝花 617064)
0 引 言
在富钛料(包括钛渣、人造金红石及天然金红石和钛精矿等)加碳氯化生产四氯化钛过程中,由于富钛料中含有1%~3%的Al2O3,氯化炉内衬耐火材料也含有30%以上的Al2O3,在氯化过程中,这些Al2O3将部分被氯化生成AlCl3进入四氯化钛中。另外,在铝粉除钒精制工艺中,低价钛制备过程中产生的AlCl3也会进入四氯化钛中。AlCl3在四氯化钛中的溶解度受温度的影响比较大,如在25 ℃常温下的溶解度仅为0.07%,而在125 ℃时溶解度上升到4.8%。因此,四氯化钛中的AlCl3在低温下很容易饱和结晶析出,沉积粘附在热交换器的管道内壁,一方面会使热交换器换热效果大大降低,另一方面有可能堵塞管道[1],严重影响生产。此外,AlCl3是一种酸性很强的路易斯酸,可对钢制设备产生强烈的腐蚀[2]。Hans H.Glaeser等人对四氯化钛中AlCl3对钢板的腐蚀速率进行了试验研究,发现含2.5% AlCl3的四氯化钛溶液对钢板(ASTM1020)的腐蚀速率可达200~250 μm/月,如果含有8%的AlCl3,对钢板的腐蚀速率可达900~1 500 μm/月[3]。因此,当四氯化钛中的AlCl3含量过高时,四氯化钛设备经常会被严重腐蚀,导致设备维修成本过高。
针对上述问题,对欣宇化工前期生产中因四氯化钛中AlCl3偏高严重影响生产的情况进行分析,查阅参考了国外四氯化钛中AlCl3含量控制及去除技术,并结合欣宇化工的设备及工艺现状,提出了控制和降低粗四氯化钛中AlCl3含量的措施。
1 AlCl3偏高对海绵钛生产的影响
欣宇化工采用沸腾氯化→铝粉除钒精制→镁法还蒸工艺生产海绵钛,因此,四氯化钛中AlCl3可能来自于以下三个方面:一是来自于高钛渣,高钛渣中含有1%~2%的Al2O3,在氯化过程中,大部分 Al2O3被氯化生成AlCl3进入粗四氯化钛中;二是来自于氯化炉内衬耐火材料,内衬耐火材料含有45%的Al2O3,在沸腾氯化过程中,Al2O3被冲刷、氯化生成AlCl3进入粗四氯化钛中;三是来自于低价钛,在低价钛制备过程中,氯气与铝粉反应产生的AlCl3催化剂与低价钛料浆溶解到四氯化钛中,TiCl4与铝粉反应产生的AlCl3以0.33AlCl3·TiCl3络合物固体颗粒进入四氯化钛。
四氯化钛中AlCl3的存在对海绵钛生产会带来危害,以下针对四氯化钛中的AlCl3对欣宇化工的氯化、精制、还蒸系统的影响情况进行分析。
1.1 三氯化铝对氯化系统的影响
1.1.1 氯化系统中AlCl3的来源分析
表1为2010—2012年欣宇化工生产的粗TiCl4中杂质成分统计结果。从表1可以看出,2010年、2011年及2012年生产的粗TiCl4中AlCl3平均含量分别为0.14%、0.22%和0.35%,呈逐年上升的趋势。

表1 2010—2012年欣宇化工生产的粗TiCl4中杂质成分(w/%)Table 1 Impurities in rude TiCl4 from 2010 to 2012
2010年,欣宇化工只有1#氯化生产线运行,且仅有极少量含AlCl3的预蒸馏釜底泥浆返回至氯化浓密机内,对全年粗TiCl4中AlCl3含量影响不大,并且氯化生产线运行比较顺行,停炉周期短,因此,生产的粗TiCl4中的AlCl3主要来源于高钛渣中Al2O3的氯化。
2011年,有2条氯化生产线运行,从6月开始,有部分AlCl3含量为5%~10%的预蒸馏釜底泥浆返回氯化浓密机,这是造成粗TiCl4中AlCl3含量升高的主要原因。
2012年,仍是有2条氯化生产线运行,预蒸馏釜底泥浆虽未返回精制系统,但2条氯化线均停炉3个月以上后重新启动生产,在停炉期间,由于氯化炉的耐火材料表面吸水,长期在酸性条件下被腐蚀粉化,重新启动后耐火材料中的Al2O3被氯化生成AlCl3,造成了粗TiCl4中AlCl3含量异常高。类似的情况在国内其他四氯化钛生产厂家均出现过,因此,在组织生产方面,要避免长期停炉造成的耐火材料腐蚀粉化现象,一般在停炉期间要将氯化炉密封起来,防止其吸水。
1.1.2 粗四氯化钛中AlCl3对氯化系统的影响
粗四氯化钛中AlCl3对氯化系统的影响主要表现在以下两个方面。
一是腐蚀设备,AlCl3是一种酸性很强的路易斯酸,对钢制设备具有很强的腐蚀性,如1#氯化生产线运行半年后,循环泵槽壁厚从最初的6 mm减薄至4.5 mm,不得不对整体进行了更换。另外,1#氯化生产线循环泵槽因泥浆沉积问题,多次停炉用水清洗,也是槽壁腐蚀变薄原因。
二是易造成套管冷凝器和循环淋洗塔(特别是1#塔)堵塞,以及降低套管冷凝器的换热效果。表2为欣宇化工生产的粗TiCl4中AlCl3含量与套管堵塞周期。从表2可以看出,套管冷凝器堵塞周期与粗TiCl4中的AlCl3含量有关,AlCl3含量越高,套管冷凝器堵塞周期越短。主要原因是AlCl3有较高的挥发性[4]和在四氯化钛中溶解度受温度的影响比较大等。
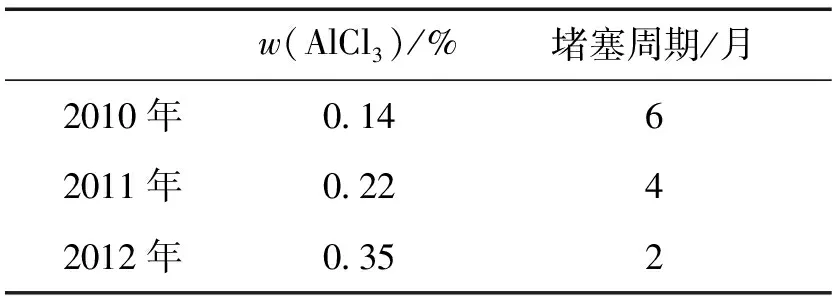
表2 粗TiCl4中AlCl3含量与套管冷凝器堵塞周期Table 2 AlCl3 content of rude TiCl4 and blocking period of pipe cooler
图1为被堵塞的套管冷凝器照片,表3为套管冷凝器内堵塞物的主要成分。可以看出,整个套管基本被完全堵死,套管冷凝器内堵塞物的主要成分为AlCl3。

图1 被堵塞的氯化系统套管Fig.1 The images of blocking in pipe cooler

表3 套管冷凝器内堵塞物的成分Table 3 The components within the blockage pipe cooler
1.2 AlCl3对精制系统的影响
精制系统中AlCl3主要来源于粗TiCl4原料和低价钛料浆。AlCl3对精制系统的影响主要表现在使蒸馏系统负荷增加以及造成设备管道的腐蚀。
由于AlCl3具有易升华性(升华温度177.8 ℃)、高挥发性以及在四氯化钛中的溶解度较高(在100 ℃以上时)的特点[5],若四氯化钛中AlCl3含量过高,采用蒸馏工艺去除比较困难。表4为2011年二级精馏系统的釜液和回流液中FeCl3和AlCl3含量。可以看出,相对于FeCl3来说,采用蒸馏工艺去除AlCl3

表4 二级馏精系统的釜液和回流液中FeCl3和AlCl3含量(w/%)Table 4 Average content of kettle liquid and reflux liquid in second rectification system
的效果比较差,在相同工艺操作参数条件下,FeCl3的平均含量可以从0.002 3%降到0.000 2%,去除率高达91%以上;而AlCl3的平均含量从0.230%降到0.132%,去除率只有42%左右。在2011年四氯化钛精制生产过程中,由于系统中的AlCl3偏高,导致预蒸馏塔TiCl4蒸气出口处的不锈钢波纹管被腐蚀穿孔,回流管被腐蚀开裂。
1.3 AlCl3对还蒸系统的影响
精TiCl4中AlCl3含量偏高时也会对还蒸系统造成影响,主要表现在对四氯化钛管道、真空系统管道以及真空泵的腐蚀与堵塞。
表5为2011年还蒸工序所使用的精TiCl4中各杂质的含量。可以看出,AlCl3的平均含量为0.10%,远远超过原乌克兰的设计指标(0.005%)。这导致还蒸高位槽到反应器的四氯化钛管道严重堵塞和腐蚀,不得不全部拆下进行清洗或更换,严重影响还蒸工序的生产。

表5 2011年还蒸工序所使用的精TiCl4中杂质含量(w/%)Table 5 Quality of TiCl4 used in reduction-distillation in 2011
在还原过程中,精TiCl4中的AlCl3会发生以下反应:
3Mg +2AlCl3=3MgCl2+ 2Al (727 ℃)
(1)
3TiCl4+Al=3TiCl3+AlCl3(136~400 ℃)
(2)
在蒸馏过程,会发生以下反应:
3TiCl4+4Al=3Ti+4AlCl3(1 000 ℃)
(3)
海绵钛质量指标没有对Al杂质提出要求,然而,由于AlCl3具有易升华(182.7 ℃)的特性,在蒸馏过程中由于发生(3)式反应,还原反应器中的AlCl3杂质被真空抽入冷凝反应器中,因冷凝反应器的温度在200~500 ℃,在这个温度范围内不能被冷凝下来,而是直接进入真空管道和真空泵,可能造成真空管道和真空泵堵塞和腐蚀。图2为被堵塞的废气真空管道。

图2 被堵塞的废气真空管道Fig.2 Blockage of vacuum waste gas pipe
2 国外AlCl3杂质去除技术
由于四氯化钛中的AlCl3对系统设备有巨大的危害性,国外对其除杂工艺进行了大量的研究。
美国及前苏联[6]曾主要通过在TiCl4中加入水,使AlCl3水解产生沉淀,从而达到去除AlCl3的目的。这种方法成本低,但由于这种方法在添加水时,加入量必须比AlCl3理论需求量高10%以上才能有效去除AlCl3,导致钛的损失。
美国还采用在液态粗四氯化钛中加入NaCl和H2O的方法去除AlCl3。该方法是通过NaCl和H2O与粗TiCl4中的AlCl3在适度搅拌并加热的条件下形成不溶性的含铝固体化合物而被沉降分离出来[3]。该方法相比加水的方法而言,具有钛损失少、HCl产生量少等优点。然而,该方法需增加设备,且很难解决根据AlCl3含量等比例加入NaCl和H2O的问题,同时,NaCl和H2O相互间的比例也是关键,如果比例不合适将会影响去除AlCl3的效果。另外,在温度较低时,AlCl3与(NaCl+H2O)化合速度比较慢,也会降低去除AlCl3的效果。此外,该方法对NaCl质量的要求较高。
美国采用的另一种去除AlCl3的方法[7-8]是在气态粗四氯化钛中加入NaCl,NaCl与AlCl3反应生成固体化合物NaAlCl4,NaAlCl4可通过冷凝方式收集下来,达到去除AlCl3的目的。该方法的优点是工艺简单,NaCl与AlCl3、FeCl3都会反应生成固体化合物被收集下来,同时,过量的石油焦粉尘也可以被分离出来。其缺点是与液态粗四氯化钛中加入NaCl和H2O的方法相比,NaCl的用量大,运行成本相对较高;此外,该方法在去除AlCl3的同时,去除了FeCl3,使后续的水解工序中净水剂较少,需添加新的净水剂;另外,NaCl与AlCl3之间的反应需要在800~1 000 ℃时才会迅速发生,达到较好的处理效果。
3 改进措施
欣宇化工原有的去除AlCl3的途径主要有:①精制工序粗TiCl4水解后,AlCl3进入泥浆,泥浆返回氯化炉或收尘器,从氯化炉或收尘器排出;②AlCl3从精制系统的矿浆蒸发炉渣出来。这两种途径均是对氯化工序中已存在的AlCl3进行去除。如果能在氯化系统的前端提前将AlCl3去除,可以降低其对氯化、精制设备及管道系统的影响,对于稳定生产具有重要意义。
欣宇化工使用的是沸腾氯化法生产粗四氯化钛,采用的设备为沸腾氯化炉。沸腾炉内,高钛渣、石油焦及氯气相互混合并充分反应,炉内反应段温度在800~1 100 ℃之间。对比以上国外的技术并结合欣宇化工实际情况,采用在氯化炉内添加NaCl固体的方法从技术的角度上是可行的,并且是最经济的。
当NaCl加入至氯化炉内时,与氯化过程产生的AlCl3及FeCl3发生如下反应:
NaCl+AlCl3=NaAlCl4
(4)
NaCl+FeCl3=NaFeCl4
(5)
NaAlCl4及NaFeCl4的熔点在188~430 ℃之间,当温度低于188 ℃时,NaFeCl4、NaAlCl4为固体状态,在冷凝收尘过程中即可去除。
根据(4)式及(5)式可知,NaCl的添加量与高钛渣中的Al、Fe元素的含量相关,且1 mol AlCl3和1 mol FeCl3分别需要1 mol NaCl进行反应。表6为欣宇化工历年使用的高钛渣的杂质含量统计数据。从表6看,Al2O3平均含量为2.54%,Fe的总量为2.25%,按NaCl加入量与高钛渣中Al和Fe的物质的量相同计算,每消耗1 t高钛渣需加入52 kg的NaCl。

表6 欣宇化工历年使用的高钛渣的杂质含量(w/%)Table 6 Average content of high titanium slag used in three years
欣宇化工的高钛渣加料速度一般为800 kg/h,因此,NaCl的加料速度应控制在41.6 kg/h左右,但由于沸腾氯化法的特点,部分NaCl在炉内气体的作用下可能未参与反应即被带出氯化炉,为保证AlCl3的去除效果,NaCl的加料速度应稍大于41.6 kg/h。
4 经济效益分析
按每吨粗TiCl4消耗0.52 t高钛渣计算,每吨TiCl4消耗NaCl的质量为27.04 kg,按目前NaCl价格820元/t,每吨TiCl4需增加成本22元。管道堵塞及设备腐蚀的情况统计较为复杂,因此,这里仅对较容易统计的避免套管冷凝器堵塞带来的效益进行分析。以2010年最好的生产状态计算,每年套管堵塞2次,每次清洗或更换套管至少需要停产2天。采用该方法则可避免套管的堵塞,按每天生产粗四氯化钛35 t计,全年可增加产量140 t,按粗四氯化钛价格5 000元/t计,可增加产值70万元。除此之外,采用该方法,在氯化工序收尘之前将AlCl3除去,可以减少氯化设备、管道的腐蚀和堵塞;甚至可以取消精制车间预水解工序,减少四氯化钛的损失、提高钛的收率,降低设备运行及维护成本和人工成本。
[1] 邓国珠,王武育.钛冶金 [M]. 北京:冶金工业出版社,2010.
[2] Lee D W,Lee H M,Wang J P.Chemical synthesis of aluminum chloride (AlCl3) by cost-effective reduction process[J].Rev Adv Mater Sci,2011(28):40-43.
[3] Hans Glaeser.Removal of AlCl3from crude TiCl4by addition of H2O and NaCl: United States,US4125586A[P].1978-01-20.
[4] Achim Hartmann,Hans Thumm.Process for the production of nearly aluminium chloride-free titanium tetrachloride:United States,US4521384[P].1985-06-04.
[5] 杜清枝,杨继舜. 物理化学第二版[M]. 重庆:重庆大学出版社,2005.
[6] Edward Rick Christian,Lewis Kay William.Purification of titanium tetrachloride: United States,US2600881A[P].1952-06-17.
[7] Horning Robert M,Kaznoff Alexis I.Purification of metal chlorides:United States,US3066010A[P].1962-11-27.
[8] James Cronin,Thomas Elkins,Hans Glaeser,et al. Process for controlling the passivation of aluminum chloride formed in the chlorination:United States Patent,US2001016182A1[P]. 2001-08-23.

