黑色页岩水岩化学作用实验研究
巫锡勇, 廖 昕, 赵思远, 凌斯祥, 朱宝龙
1)西南交通大学地质工程系, 四川成都 611756; 2)西南交通大学高速铁路线路工程教育部重点实验室, 四川成都 610031; 3)西南科技大学土木工程与建筑学院, 四川绵阳 621010
黑色页岩水岩化学作用实验研究
巫锡勇1, 2), 廖 昕1)*, 赵思远1), 凌斯祥1), 朱宝龙3)
1)西南交通大学地质工程系, 四川成都 611756; 2)西南交通大学高速铁路线路工程教育部重点实验室, 四川成都 610031; 3)西南科技大学土木工程与建筑学院, 四川绵阳 621010
水岩作用是黑色页岩化学风化的重要途径, 并与岩体矿物组分、工程性质及地质环境有着密切的联系。利用自制的流通实验装置对取自三江县团结电站附近的寒武系清溪组黑色页岩与富含溶解氧去离子水的化学反应进行试验模拟研究, 并利用离子分析仪、电感耦合等离子体质谱仪对反应后溶液离子浓度进行分析, 使用扫描电子显微镜观察反应前后岩样微观特征, 结合岩样渗透系数的变化监测, 对岩样中黄铁矿氧化动力学速率以及受黄铁矿氧化影响形成的酸性环境下硅元素释放速率进行计算分析。结果表明, 黄铁矿氧化行为使得岩体渗透率降低约 70%, 在黑色页岩自身矿物化学组分和岩石物理性质的共同影响下,所含黄铁矿氧化速率与纯黄铁矿颗粒的氧化速率非常接近, 同时黄铁矿氧化形成的酸性溶液可溶蚀岩体中石英和伊利石, 由于两者含量未能精确测定, 因此所测得硅元素释放速率仅表示两者溶解的总反应速率。
黑色页岩: 黄铁矿氧化; 水岩化学作用; 流通实验; 动力学速率
水岩作用作为岩石化学风化的重要形式, 是地表岩层形态和工程性质发生变化的主要因素之一,其本质是各种水介质与岩体中各组成矿物发生物理化学反应的过程。前人对于水岩化学作用的研究已积累了丰富的研究成果(Lasaga, 1984; 李德文等, 2002), 其中大部分集中在不同水介质与纯矿物之间的反应, 如溶解、吸附、运移等(Cripps et al., 1981; Brantley et al., 2008; Rimstidt et al., 1980; 岳梅等, 2005)。由于岩体内所含矿物种类繁多且化学反应途径非常复杂, 所以对于水介质与多种矿物集合体形成的岩体进行化学反应的动力学速率研究一直处于探索之中。
黑色页岩因富含有机物和分散状黄铁矿等硫化矿物, 在地表或近地表富氧环境下, 与水作用可形成侵蚀性酸性水和一系列影响岩体工程性质的风化产物(巫锡勇等, 2001, 2008; 彭渤等, 2005; Liao et al., 2012)。其化学风化过程主要体现在以黄铁矿为代表的硫化矿物氧化作用上。前人对于纯黄铁矿氧化机理及反应速率已积累大量的成果(Moses et al., 1991; Nordstrom, 2011; Williamson et al., 1994;岳梅等, 2005), 但是对于岩体中黄铁矿氧化动力学行为目前研究较少。此外, 在黑色页岩化学风化过程中, 随着矿物成分不断转变, 岩体物理化学性质将随之发生变化, 同时可对黄铁矿氧化的影响因素产生促进或抑制效果。因此, 黑色页岩的矿物化学成分与岩石物理性质, 可从内在因素上反映岩体内黄铁矿化学氧化动力学行为与其他岩体风化行为的差异性。
本文以广西三江地区强化学风化沉积环境下寒武系黑色页岩作为研究对象(王自强等, 2009), 在试验获得岩石样本的矿物化学成分和岩石物理参数后, 通过设计流通实验来模拟水岩作用过程, 对富氧入渗水与岩石样本反应前后的岩体表面微观结构特征、实验过程岩体渗透性能变化以及反应后溶液离子浓度进行分析, 并对黑色页岩在含氧水作用下所含黄铁矿氧化动力学行为特征进行探讨。
1 样品采集与分析
1.1 样本采集
实验样本取自三江地区寒武系清溪组黑色页岩, 研究区取样点如图1所示。研究区黑色页岩为深黑色, 所含杂质较少, 易污手, 质地坚硬, 小刀很难沿层理面将其分裂, 肉眼可见细微石英晶体颗粒和不同形态非均质黄铁矿浸染分布, 沉积构造为平行层理, 呈层纹状构造, 页理厚度小于 0.6 cm,层理面细微颗粒表面凹凸不平, 手感较粗糙, 肉眼可见微孔隙密集分布, 局部有折线状石膏脉体穿插于岩体内部, 推测为黄铁矿氧化形成的硫酸根离子与钙离子的反应产物, 体积膨胀时, 可导致岩石结构和力学性质变化。通过 pH试纸测得研究区内采集的黑色页岩边坡裂隙水pH值约2.7。

图1 广西寒武系清溪组地层分布及采样点Fig. 1 Distribution of Cambrian Qingxi Formation and the sampling location in Guangxi
1.2 样本物理化学性质
1.2.1 矿物成分
在所取岩样中挑选出四件清溪组黑色页岩样本研磨至200目以下, 进行X衍射矿物分析。测试条件设定为20 kV、50 mA, 衍射角度3°~40°, 扫描速度2°/min。分析结果如图2所示。由图可看出, 该样本中矿物以石英和伊利石为主, 其他矿物峰值不明显, 不能明显看出黄铁矿的衍射峰, 推测是由于岩样中以浸染颗粒形式存在的黄铁矿含量相对石英和伊利石很低, 因此未能从图形上看出其峰值。
1.2.2 化学成分
将黑色页岩样本研磨后采用粉末压片法, 进行X射线荧光光谱法分析其化学成分, 所测主要元素的质量分数如表1所示。该黑色页岩样本中化学成分主要为 SiO2(58.42%), 其次为 CO2(17.50%)和Al2O3(16.00%), 然后是 K2O(3.89%)、MgO(1.52%)和SO3(1.35%), 其中硫元素含量在非金属元素中仅低于碳、氧元素含量, 其他元素质量分数均在1%以下。对岩样中有机碳和无机碳的含量进行测试分析,其中TOC含量为3.13%, TIC含量为1.73%, 说明岩样中含碳有机物含量较高。

图2 黑色页岩样本XRD矿物分析Fig. 2 XRD patterns of black shale samples

表1 黑色页岩样本化学成分表/%Table 1 Chemical compositions/% of black shale sample
1.2.3 岩石物理性质
采用水银压入法对两件黑色页岩样本的孔隙结构及其分布特征进行测定。通过混流泵渗透试验对样品渗透系数进行测量, 以及常规土工试验对岩样密度和含水量进行测定, 试验结果如表 2所示。所测黑色页岩样本的干密度和天然密度分别约为2.55 g/cm3和2.25 g/cm3, 孔隙度约为12.0%, 平均孔隙直径、中位数直径和模数直径均较小, 接近于0.01 μm, 比表面积为 11.92~16.05 m2/g; 含水量为6.49%, 渗透系数约为0.75×10-9~0.80×10-9cm/s, 表明该样本渗透性较低。
2 实验方法与设备
图3所示为本实验装置示意图。实验前将黑色页岩制成直径50 mm、厚度5 mm的圆饼状岩样, 放置于60oC烘箱中24 h, 避免微生物对实验反应速率产生影响。然后将岩样表面残留细颗粒清洁干净,放入抽真空机内, 排出岩样内部气体。实验中控制进水压力保持(0.300±0.005) MPa, 室内温度(25.0±1.0)℃。该实验分为两个阶段, 第一个阶段使用饱和氮气去离子水, 通过氮气瓶的压力作用将岩样中初始孔隙水排出, 避免初始孔隙水成分对下阶段检测结果产生影响; 第二阶段, 通过将饱和溶解氧去离子水压入岩体孔隙, 使黑色页岩与溶解氧饱和孔隙水发生反应。反应后渗出溶液依次流经电导率计(EC计)、pH计的测定容器, 最后流入放置于电子天平上由塑料膜覆盖的容器内。以0.5天或1天的间隔, 用注射器取样1~2 mL进行离子浓度分析。原实验设计中, 在电导率测定容器前设置了溶解氧测定仪及盛水容器, 由于渗透液流速过低, 溶解氧测定仪不能准确地测得该值, 故在实验第二阶段将其移除。
实验阶段对渗出溶液的电导率和 pH值进行实时监测, 使用仪器为佐藤商事 YK-22CT电导率计和 pH计。离子浓度分析通过电感耦合等离子体发射光谱仪(岛津 ICPS-8000)和离子色谱仪(DKK-TOA IA-100)对水样中 8种主要离子成分进行浓度测定。测定前均通过0.45 μm的过滤筛进行过滤。此外, 采用扫描电子显微镜(基恩士VE-8800)对实验前后的岩样表面进行微观形态观察。
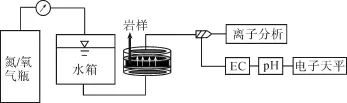
图3 实验装置示意图Fig. 3 Schematic illustration of the experimental system
3 实验结果
3.1 pH、EC变化
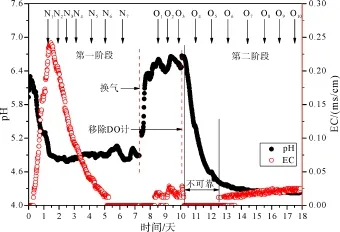
图4 实验过程pH、EC值随时间改变曲线(Ni, Oj(i=1~7, j=1~10))箭头代表渗出水样取样编号及对应时间)Fig. 4 Changes in pH and EC with time(arrows and Ni, Oj(i=1~7, j=1~10) indicate timing of solution sampling)
图4所示为整个实验阶段渗出溶液pH、EC值监测结果。第一阶段, EC曲线呈反转“V”字形态,在第 2天时达到峰值 0.24 ms/cm, 然后快速下降,在5.2天后降为0 ms/cm, 表明初始溶液中大部分离子已被排出, 所测溶液主要为含溶解氧的去离子水。pH值则是在前2天内从6.2降到4.9, 然后一直保持在该值附近。初始pH值6.2基本上与常压下溶解二氧化碳的水溶液pH值相一致。2天后pH值稳定在 4.9左右, 表明第一阶段后期的渗出溶液中仅残留少量氢离子。因此在实验第7天时换成氧气瓶开始第二阶段实验。
第二阶段开始前, 对所有监测计进行重新标定,导致在该阶段初期pH值迅速上升到6.6, 与第一阶段初始测定值相近; EC值继续保持为0 ms/cm。在8.3—10.3天期间EC值升高且变化趋势与pH值变化相似, 由于EC值和pH值监测值之间存在时间滞后, 根据渗出溶液流速与容器静容积计算, 可看出EC和pH值呈相反的变化规律。当pH下降时, EC表现出上升的趋势, 反之亦然。在10.3天时, 由于溶解氧测定计的移除使得实验监测系统受到影响,造成移除后两天渗出溶液的EC、pH值数据不能真实反映渗透溶液情况。因此在 10.3—12.5天期间, EC值始终保持为0 ms/cm, pH值上升至6.6后快速降低到 4.4左右, 虽然该段时间内监测数据不可靠,但仍能反映渗出溶液性质变化趋势。在12.5天之后, EC和 pH值变化缓慢, 直到最终达到稳定状态: pH=4.22, EC=0.022 ms/cm。
3.2 溶液渗出速率变化
由于实验中渗出溶液的密度和粘度变化可忽略不计, 因此根据其渗出速度以及测试样本的孔隙率, 可计算得到水岩作用过程中岩样渗透系数变化曲线(图5)。由图5可看出, 在两个阶段后期渗透系数均达到较稳定状态, 但两者变化规律有明显差异。第一阶段表现为线性下降, 降低缓慢, 降幅约12.5%; 第二阶段呈指数形式下降, 降低迅速, 下降幅度约69%, 最后稳定在1.0×10-9cm/s左右。
3.3 初始孔隙水离子成分
第一阶段在饱和氮气水排挤下, 初始孔隙水主要表现为稀释和排出, 其离子浓度分析结果如图6a所示。其中硫酸根离子和含铁离子相比其他离子物种浓度较高, 分别为100.28mmol/L和10-0.02mmol/L;含硅离子浓度从初始 10-0.90mmol/L持续降低至10-1.12mmol/L, 含铁、铝、钠、镁离子均逐渐降低至0 mmol/L; 含镁离子浓度始终为0 mmol/L。由于在阴离子检测结果中, 虽然氯离子可检测到, 但由于实测值均小于1 mg/L, 低于离子分析仪的最低检测限, 故该阶段未对其进行分析。
3.4 含氧水作用下渗流水化学组分
图 6b为第二阶段饱和溶解氧孔隙水与岩样作用后渗出溶液主要离子浓度分析结果。由图可看出含硅、铁离子与硫酸根离子浓度变化呈相同变化规律, 在 8—9天有轻微的下降, 随后保持上升趋势;含钙、镁离子在 8—13天内浓度保持在相对较高水平(Ca: 7.13×10-2~8.46×10-2mmol/L, Mg: 1.56×10-2~1.86×10-2mmol/L), 14—17天两者显著降低, 钙离子直接降至 0 mol/L, 镁离子则降低了约3/4 (4.0×10-3~5.7×10-3mmol/L); 含铝、钠离子物种,总体变化范围微小, 含钠离子浓度在第9天后降为0 mmol/L。从浓度上看, 该阶段含硅离子浓度最高, 为1.24×10-1~2.55×10-1mmol/L, 其次为硫酸根离子浓度为 7.66×10-2~13.49×10-2mmol/L, 由于氯离子浓度低于1 mg/L, 所以第二阶段氯离子作用仍未予以考虑。

图5 渗透系数随时间变化趋势Fig. 5 Changes in hydraulic conductivity with elapsed time
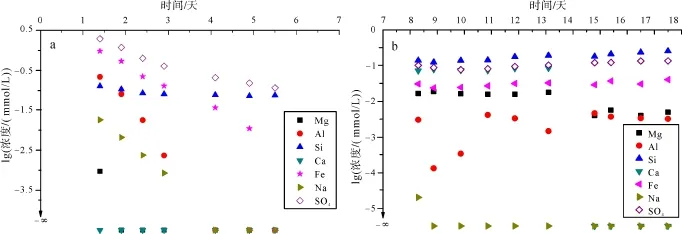
图6 第一阶段(a)、第二阶段(b)渗出溶液化学成分分析结果(-∞代表浓度0 mmol/L)Fig. 6 Results of monitoring and analyses of seepage water at the first stage(a) and the second stage(b) (-∞ represents the content of 0 mmol/L)
3.5 岩体表面微观特征
使用扫描电镜对黑色页岩实验岩样在3种不同状态下的微观形态特征进行观察分析。图7a为实验前用超声波清洗仪对岩体表面清洁后的表面特征,表面总体较为平滑, 孔隙孔径较小且孔隙壁周围较光滑。图7b为实验后的页岩表面微观形态特征, 可见岩体表面孔隙数量显著增加, 表面孔径也随之增大数倍, 孔隙壁表面被侵蚀呈参差不齐的阶梯状。图7c为实验后实验样本纵剖面的形态特征, 岩样外层与内部结构相比具有显著区别, 外层具有含较多微孔隙薄片状构造, 内部岩样相对较为完整、致密。通过观察发现该岩样多处表面微观形态均具有上述特征, 因此可推断水岩化学作用可显著改变岩样的微观形态学特征, 其影响程度由外至内逐渐减弱。

图7 实验前后岩样的SEM图像Fig. 7 SEM photographs of rock samples

图8 第一阶段初始孔隙水硫酸根离子与铁离子浓度比(a)与第二阶段渗出溶液硫酸根离子与铁离子浓度比(b)Fig. 8 Ratio of sulfate to iron ions in original pore water at the first stage(a) and ratio of sulfate to iron ions in seepage water at the second stage(b)
4 分析与讨论
4.1 初始孔隙水特征
第一阶段在氮气饱和去离子水的物理排挤作用下, 岩体内初始孔隙水通过稀释和扩散作用排出,主要离子浓度呈指数形式下降。从EC、pH值的监测结果可看出, 尽管第一阶段末期 EC值保持在0 ms/cm, 但是pH值却稳定在4.9左右, 表明此时孔隙水中仍有少量氢离子存在。由于测试浓度均是溶液稀释后测量结果, 所以各项离子浓度真实值应高于测量值, 实际pH值则低于4.9, 说明该岩样在实验前受化学风化作用, 其中部分硫化矿物已被氧化,并使得孔隙水溶液呈酸性。图8a为初始孔隙水中所测铁离子与硫酸根离子浓度关系, 两者摩尔比例1.89, 非常接近黄铁矿(FeS2)的硫铁元素计量系数比, 因此可推测岩样中氧化分解的硫化矿物主要为黄铁矿, 其氧化产物中除铁离子和硫酸根离子外,还有大量氢离子生成。除硫酸根离子和总铁离子外,含硅和铝的离子浓度相对最高, 主要与岩样中石英和伊利石(化学成分以SiO2和Al2O3为主)含量最高有关。
4.2 水岩化学作用后渗出溶液特征
由上述分析知清溪组黑色页岩中硫化矿物主要为黄铁矿, 在第二阶段溶解氧饱和溶液与岩体中黄铁矿发生反应后, 反应产物硫酸根离子和总铁离子浓度随实验时间不断增加, 其中值得注意的是在第8—9天期间, 两者浓度均比第10天高(图6b), 推测是由于在第一阶段物理淋滤冲刷作用下, 一些细小颗粒物质(如粘土矿物)被溶解、带走, 使得分布在孔隙表面的黄铁矿有效反应面积增大, 即水岩化学作用的有效反应物浓度增大, 因此生成的产物浓度也较高。当这些暴露在孔隙表面的过剩黄铁矿逐渐被消耗后, 其有效反应表面积减少至正常水平, 故两者离子浓度在第8—10天呈下降趋势。
对第二阶段硫酸根离子和总铁离子摩尔浓度比值进行线性回归分析, 其摩尔浓度比为 3.09, 高于第一阶段浓度比(图8b)。在中性条件下黄铁矿氧化生成的 Fe2+易吸附在反应矿物表面(Moses et al., 1991), 而黄铁矿与溶解氧短期反应内(1—4天)不会生成Fe3+(McKibben et al., 1986), Kamei等(2000)则通过实验发现黄铁矿在溶解氧作用下, 约 12天后在矿物表面出现疑似三价铁氢氧化物的蚀变层。在本实验中流动性溶液在岩体孔隙内滞留时间要短于Fe3+或 Fe(OH)3的形成时间(见 4.3.1节), 且实验结束后在岩样和玻璃质过滤膜表面未观察到三价铁的析出物, 因此推断本实验中检测到的含铁离子仅为Fe2+。
其他离子成分主要表现为酸性环境下的溶解行为, 含硅、铝元素的石英、伊利石等矿物与氢离子反应后, 含硅离子表现为缓慢上升, 与硫酸根离子变化趋势相似, 含铝离子则表现为在低浓度小范围内波动,由岩样化学成分分析知SiO2和Al2O3含量最高, 因此在酸性溶解作用下, 测得含硅离子浓度最高; 含钠、钙、镁离子表现为初期有一定浓度, 六天后含镁离子浓度降低了约3/4, 含钠、钙离子急剧下降为0 mmol/L,说明分布在孔隙壁上含有这些元素的矿物在酸性水溶蚀作用下逐渐被分解带走。
4.3 黑色页岩水岩化学作用动力学速率
4.3.1 黄铁矿氧化速率
过去对黄铁矿氧化速率研究主要是针对纯黄铁矿, 并没有涉及黄铁矿在岩样中的氧化动力学速率。根据前人对黄铁矿氧化过程的研究, 主要可概括为以下几个总反应方程式:


在对矿物反应速率进行测定时, 通常需选取一个基本反应进程变量。在本文中, 由于岩样中反应后黄铁矿含量不能精确测定, 溶液中溶解氧可被黑色页岩中有机物等物质消耗(Manaka, 2003), H+易与岩样中其他矿物发生反应, 生成的 Fe2+又可吸附在岩体表面影响分析结果(Moses et al., 1991), 因此最终选定 SO42-作为反应进程变量, 黄铁矿氧化反应速率表达式根据式(1)中计量系数关系可得:

式中 Rvol为体积反应速率(mol/L/s)。由于在第二阶段初始两天(第 8~9天)SO42-浓度较高, 表现异常。因此为了获得准确的反应速率值, 未考虑初始两天离子浓度。由于水岩作用化学反应前后孔隙率变化不大(Scholz et al., 1995; Tenthorey et al., 1998; Aharonov et al., 1998), 所以反应溶液在岩体内滞留反应时间可通过下式求得:

式中Vt为总孔隙水体积(cm3), φ为孔隙率, Vr为岩样总体积(cm3), u为传递速度(cm3/h), 即实验所测得渗出溶液流速, t为溶液在岩石中滞留时间,将式(5)代入(6)可得:

取岩样N1岩石物理参数测试结果代入计算: 初始孔隙率11.8%, 圆饼状岩样尺寸为直径50 mm、厚度5 mm。渗出溶液的流速则通过电子天平监测流量数据求得, 相关计算参数及数据如表 3所示。绘出SO42-浓度随时间变化关系图(如图9所示), 通过线性回归分析得到黑色页岩中黄铁矿的氧化速率为(6.50±0.32)×10-9mol/(L·s)。
Mckibben等(1986)提出矿物化学反应速率公式:

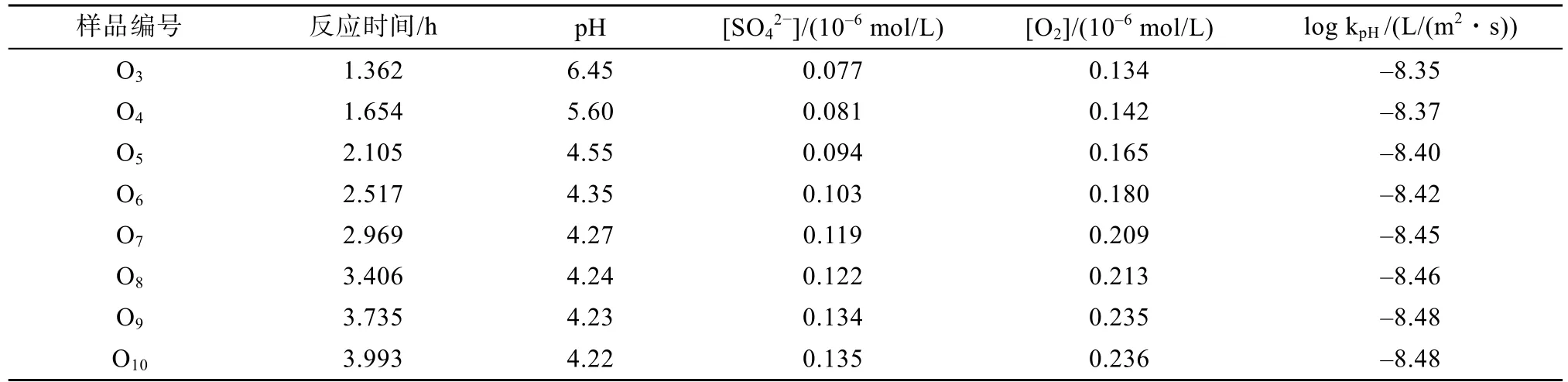
表3 25℃下黑色页岩中黄铁矿氧化速率计算参数Table 3 Calculated parameters for pyrite oxidation contained in black shale at 25℃
式中Rsp为特定速率(mol/(m2· s)), k为速率常数(L/(m2· s)), A为黄铁矿表面积(m2), V为溶液可进入的张开裂隙体积(L), Mi为影响反应速率的物质摩尔浓度(mol/L), ni为反应速率对影响物质依存级数, ∏为连乘符号。
基于过去对开放式氧气系统下黄铁矿被溶解氧氧化速率的研究, 本文中黄铁矿氧化速率对溶解氧的依存级数取值为 0.5。而对氢离子的依存级数在不同 pH环境条件下有较小差异, 不能简单估算得到(McKibben et al., 1986; Holmes et al., 2000; Williamson et al., 1994)。因此笔者选择了在指定pH值时的速率常数 kpH代替 k, 然后将 kpH和[O2]0.5代入式(8)和(9)得到:

式中A/V的值参考Chigira等(1994)的研究成果,可表示为:

式中 Asp为比表面积(m2/g), ρbulk为岩样的体积密度(g/cm3), P%为岩样的黄铁矿含量百分比, φ为岩样孔隙率。由于岩石中进行反应的比表面积很难测得, 通过与Nakata先生讨论, 建议反应的比表面积值采用水银压入法测得值的三倍大小(Nakata et al., 1999)。将式(12)代入(10)可得:

式(13)中反应消耗的溶解氧含量可通过反应式(1)中生成硫酸根离子的化学计量系数比计算获得,计算参数和结果列于表3。由表3可看出, 在25℃、pH=4.2~6.5条件下log kpH为(-8.42±0.06) (L/(m2· s)),因此黑色页岩样品中黄铁矿在溶解氧作用下氧化速率公式为:

对比前人对黄铁矿在溶解氧作用下氧化动力学速率研究成果, 本文所得到的氧化速率常数与McKibben等(1986)和Williamson等(1994)的研究结果相近。推测是由于岩石中其他矿物对于黄铁矿氧化反应影响较小, 主要矿物石英和伊利石与氢离子反应速率缓慢, 实验期间内对孔隙水 pH值影响基本可忽略不计。实验所得到的黄铁矿氧化速率与纯黄铁矿颗粒在溶解氧作用下反应速率基本一致, 说明该反应速率主要是指镶嵌于岩体孔隙中的黄铁矿所暴露在岩体表面部分的氧化速率。

图9 硫酸根离子浓度与孔隙水溶液在岩体内反应时间关系Fig. 9 Relationship of residence time of flowing solutions to sulfate concentrations
4.3.2 硅元素释放速率
由 XRD矿物分析可知, 清溪组黑色页岩含有硅元素的矿物主要为石英和伊利石。在页岩内黄铁矿氧化形成的酸性溶液环境下, 可引起石英和伊利石与氢离子反应发生溶解。由于无法准确获得两种矿物的含量, 且不能确定含硅离子在渗透溶液中的存在形式, 因此本实验中仅能获得硅元素的释放速率, 不能得到两种矿物分别在酸性环境下的溶解速率与机制。采用与硫酸根离子数据相同处理方法,在去除第二阶段初始两天含硅离子浓度较高的数据后, 对其离子浓度和反应时间做线性拟合分析(如图10), 由图10知含硅离子浓度与反应时间呈线性相关, 换算时间单位后得到含硅离子释放速率为(1.14±0.14)×10-5mol/L/s。此外, 由图6b可知, 在第二阶段后期除铁元素外, 其他金属离子浓度总和比硅元素浓度低近一个数量级, 排除含铝元素伊利石少量溶解作用的影响, 可推测此时硅元素主要由石英溶解释放, 但两者在岩石中具体的溶蚀过程和机理还有待进一步研究。
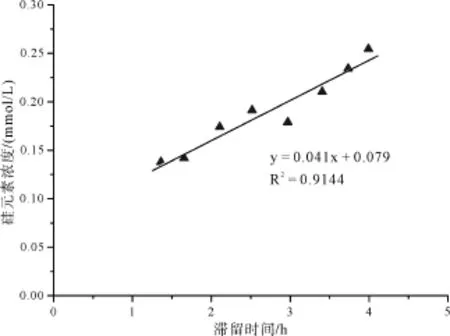
图10 含硅离子浓度与孔隙水溶液在岩体内反应时间关系Fig. 10 Relationship of residence time of flowing solutions to silicon concentrations
4.4 黄铁矿氧化行为对渗透率的影响作用
通过以上实验结果和分析可知, 实验中两个阶段的水岩反应很显然是由不同的作用机理控制。在第一阶段由于使用的是纯氮气饱和溶液, 不与黑色页岩中矿物发生化学反应, 在岩体内部主要表现为物理力学淋滤过程。第二阶段使用纯氧气饱和溶液,与岩体内所含黄铁矿发生氧化反应可产生酸性水,因此该阶段主要为化学氧化和溶解过程, 该阶段渗透系数的急剧降低说明黄铁矿的氧化对实验中岩样的渗透性有相当重要的影响。结合 SEM扫描电镜微观形态观察, 实验前后岩样孔隙周围的微观形态特征发生了显著变化, 由初始的平整状变成参差不齐的阶梯状(图 7), 与前人对含黄铁矿和有机物的黑色页岩风化的微观观察结果相一致(McKibben et al., 1986; Fischer et al., 2005)。由岩样的孔隙尺寸参数可知(表 2), 孔隙平均直径范围为 0.01~0.02 μm,远低于黑色页岩岩样中矿物和有机物的直径。由此可推断在酸性和氧化性溶液共同作用下, 岩样表面的黄铁矿、有机物和粘土矿物等容易被(氧化)溶解成为细小颗粒, 随孔隙水流动迁移。当这些分散的微小颗粒运移进入孔隙喉颈时, 容易造成孔隙连通性的阻塞(Bernabé et al., 2003)。
4.5 岩性特征对黄铁矿氧化速率的影响
从上述实验结果可知: 在25℃, pH=4.2~5.6的饱和溶解氧溶液作用下, 黑色页岩所含黄铁矿氧化速率与黄铁矿颗粒的氧化速率非常接近。一方面,是由于清溪组黑色页岩中主要矿物成分为石英和伊利石(图 2), 两者基本不与黄铁矿氧化后形成的硫酸根离子和亚铁离子发生反应, 仅消耗少量氢离子,且与氢离子反应速率缓慢, 从而可维持反应溶液呈酸性; 另一方面, 在岩样渗透系数影响下, 氧化性溶液在岩体孔隙内滞留时间不足以使生成的Fe2+氧化为 Fe3+, 从而影响黄铁矿氧化速率。因此, 本实验所得到的黄铁矿氧化速率基本没有受到其他矿物化学组分和岩石物理参数的影响。
对于同样含有黄铁矿的其他黑色岩石来说, 如黑色泥岩中含量较高的粘土矿物(如蒙脱石、高岭石等), 通过离子交换作用可引起铁离子的迁移和氧化态的改变(王随继等, 1998), 而泥岩组分颗粒大小及分布特征对岩石的孔隙率和渗透率均有较大影响(Dewhurst et al., 1998)。渗透率、孔隙率大的岩体,溶液在孔隙内流动速率较快, 可能与孔隙表面出露黄铁矿反应时间较短, 反之, 在流速慢的孔隙溶液中, 黄铁矿氧化产物可与溶解氧或其他矿物继续发生化学反应, 影响黄铁矿氧化速率。如黑色灰岩中含有较多碳酸盐矿物(如方解石、白云石), 可立即与黄铁矿氧化生成的氢离子发生反应, 很难在岩体内形成酸性环境, 同时由于灰岩渗透率相对较高(余钟波等, 2008), 碳酸盐矿物的迅速溶解可造成岩体内部孔隙增大, 一方面导致岩体渗透性进一步增强,另一方面可能增加黄铁矿有效反应面积, 从而在反应溶液性质和反应环境上影响黄铁矿氧化速率。由此可见, 岩性特征对岩体内赋存的黄铁矿氧化速率有着很大的影响, 同时黄铁矿在岩体内部的氧化行为对岩体物理性质参数也将产生反馈作用。
5 结论
通过对广西三江地区清溪组含黄铁矿黑色页岩的水岩作用流通实验研究, 主要得到以下结论:
1)初始孔隙水为酸性水, 其水质成分富含氢离子、(亚)铁离子和硫酸根离子, 说明该岩样已经历化学风化作用, 所含黄铁矿已发生部分氧化。
2)含溶解氧去离子水溶液沿岩体内部孔隙通过黑色页岩后, 岩样渗透率降低约 70%, 该结果主要是由于岩体所含黄铁矿与溶解氧发生化学反应后产生酸性溶液, 在酸性溶蚀过程中形成的细微颗粒(如黄铁矿、有机物和粘土矿物等), 随着孔隙水迁移堵塞了孔隙喉颈所致。
3)黑色页岩内部所含黄铁矿被富含溶解氧孔隙水氧化后生成了亚铁离子和硫酸根离子, 通过浓度变化分析计算, 得到该反应氧化动力学速率为Rsp=10-8.42±0.06[O2]0.5(mol/(m2·s)) (pH=4.2~5.6, 25℃),该速率主要反映为嵌入在岩体内部孔隙表面处黄铁矿与溶解氧反应的速率, 因此该结果与前人对纯黄铁矿颗粒氧化的速率相一致。
致谢: 诚挚感谢京都大学防灾研究所千木良雅弘教授和松四雄骑副教授对实验操作的帮助和指导。
李德文, 崔之久, 刘耕年. 2002. 风化壳研究的现状与展望[J].地球学报, 23(3): 283-288.
彭渤, 吴甫成, 肖美莲, 谢淑容, 吕焕哲, 戴亚南. 2005. 黑色页岩的资源功能和环境效应[J]. 矿物岩石地球化学通报, 24(2): 153-158.
王随继, 曾凡刚, 黄杏珍, 牛木林, 孟庆华. 1998. 含油气盆地中粘土矿物的穆斯堡尔效应及应用——以柴达木盆地第三系为例[J]. 沉积学报, 16(2): 109-112.
王自强, 尹崇玉, 高林志, 唐烽. 2009. 黔南—桂北地区南华系化学地层特征[J]. 地球学报, 30(4): 465-474.
巫锡勇, 朱宝龙, 罗健. 2008. 黑色岩层的风化过程及其热力学分析[M]. 北京: 科学出版社.
巫锡勇, 贺玉龙, 魏有仪, 喻洪平. 2001. 黑色岩层的风化特征研究[J]. 地质地球化学, 29(2): 17-23.
余钟波, 黄勇. 2008. 地下水水文学原理[M]. 北京: 科学出版社.
岳梅, 赵峰华, 孙红福. 2005. 煤系黄铁矿氧化溶解地球化学动力学研究[J]. 煤炭学报, 30(1): 75-79.
References:
AHARONOV E, TENTHOREY E, SCHOLZ C H. 1998. Precipitation sealing and diagenesis: 2. Theoretical analysis[J]. Journalof Geophysical Research, 103: 23969-23981.
BERNABÉ Y, MOK U, EVANS B. 2003. Permeability-porosity relationships in rocks subjected to various evolution processes[J]. Pure and Applied Geophysics, 160: 937-960.
BRANTLEY S L, CONRAD C F. 2008. Kinetics of water-rock interaction-Chapter 1: Analysis of rates of geochemical reactions[M]. Springer: 1-37.
CHIGIRA M, WATANABE M. 1994. Silica precipitation behavior in a flow field with negative temperature gradients[J]. Journal of Geophysical Research, 99: 15539-15548.
CRIPPS J C, TAYLOR R K. 1981. The engineering properties of mudrocks[J]. Engineering Geology and Hydrogeology, 14: 325-346.
DEWHURST D B, APLIN A C, SARDA J P, YANG Y L. 1998. Compaction-driven evolution of porosity and permeability in natural mudstones: An experimental study[J]. Journal of Geophysical Research, 103: 651-661.
FISCHER C, GAUPP R. 2005. Change of black shale organic material surface area during oxidative weathering: Implications for rock-water surface evolution[J]. Geochimica et Cosmochimica Acta, 69: 1213-1224.
HOLMES P R, CRUNDWELL F K. 2000. The kinetics of the oxidation of pyrite by ferric ions and dissolved oxygen: an electrochemical study[J]. Geochimica et Cosmochimica Acta, 64: 263-2740.
KAMEI G, OHMOTO H. 2000. The kinetics of reactions between pyrite and O2-bearing water revealed from in situ monitoring of DO, Eh and pH in a closed system[J]. Geochimica et Cosmochimica Acta, 64: 2585-2601.
LASAGA A C. 1984. Chemical kinetics of water-rock interactions[J]. Journal of Geophysical Research, 89: 4009-4025.
LI De-wen, CUI Zhi-jiu, LIU Gen-nian. 2002. Present situation and prospects of researches on weathering Crust[J]. Acta Geoscientia Sinica, 23(3): 283-288(in Chinese with English abstract)
LIAO Xin, WU Xi-yong, ZHU Bao-long, FENG Jun. 2012. Study on the characteristics of black strata geochemical weathering and its disaster-causing mechanism[J]. Disaster Advances, 5(4): 1461-1466.
MANAKA M. 2003. The effective diffusion coefficient of dissolved oxygen and oxidation rate of pyrite by dissolved oxygen in compacted purified and crude sodium bentonites in carbonate buffered solution[J]. Nuclear Technology, 143: 335-346.
MCKIBBEN M A, BARNES H L. 1986. Oxidation of pyrite in low temperature acidic solutions: Rate laws and surface textures[J]. Geochimica et Cosmochimica Acta, 50: 1509-1520.
MOSES C O, HERMAN J S. 1991. Pyrite oxidation at circircum-neutral pH[J]. Geochimica et Cosmochimica Acta, 55: 471-482.
NAKATA E, WATANABE M. 1999. Dissolution and precipitation between pH 3.8-CO2dissolved-solution and anorthite rich tuffaceous sandstone by using high temperature flow-through reactor[J]. Japanese Magazine of Mineralogical, 38: 162-175(in Japanese with English abstract)
NORDSTROM D K. 2011. Mine waters: Acidic to circumneutral[J]. Elements, 7: 393-398.
PENG Bo, WU Fu-cheng, XIAO Mei-lian, XIE Shu-rong, LÜ Huan-zhe, DAI Ya-nan. 2005. The resource functions and environment effects of black shales[J]. Bulletin of Mineralogy, Petrology and Geochemistry, 24(2): 153-158(in Chinese with English abstract)
RIMSTIDT J D, BARNES H L. 1980. The kinetics of silica-water reactions[J]. Geochim. Cosmochim. Acta, 44: 1683-1699.
SCHOLZ C H, LÉGER A, KARNER S L. 1995. Experimental diagenesis: Exploratory results[J]. Geophysical Research Letters, 22: 719-722.
TENTHOREY E, SCHOLZ C H, AHARONOV E. 1998. Precipitation sealing and diagenesis: 1. Experimental results[J]. Journal of Geophysical Research, 103: 23951-23967.
WANG Sui-ji, ZENG Fan-gang, HUANG Xin-zhen, NIU Mu-lin, MENG Qing-hua. 1998. The mössbauer effect of clay minerals in oil basin and its application: Taking tertiary system of qaidam basin as an example[J]. Acta Sediment Ologica Sinica, 16(2): 109-112(in Chinese with English abstract).
WANG Zi-qiang, YI Chong-yu, GAO Lin-zhi, TANG Feng. 2009. Chemostratigraphic characteristics of the Nanhua system in southern Guizhou-northern guangxi area[J]. Acta Geoscientia Sinica, 30(4): 465-474(in Chinese with English abstract)
WILLIAMSON M A, RIMSTIDT J D. 1994. The kinetics and electrochemical rate-determining step of aqueous pyrite oxidation[J]. Geochimica et Cosmochimica Acta, 58: 5443-5454. WU Xi-yong, ZHU Bao-long, LUO Jian. 2008. Analysis on the process and thermodynamics of the black rock weathering[M]. Beijing: Science Press(in Chinese).
WU Xi-yong, HE Yu-long, WEI You-yi, YU Hong-ping. 2001. Study on weathering characteristics of black strata[J]. Geology Geochemistry, 29(2): 17-23(in Chinese with English abstract).
YU Zhong-bo, HUANG Yong. 2008. The theory of groundwater hydrology[M]. Beijing: Science Press(in Chinese).
YUE Mei, ZHAO Feng-hua, SUN Hong-fu. 2005. The kinetics of oxidation reaction of pyrites from coal-bearing measure[J]. Journal of China Coal Society, 30(1): 75-79(in Chinese with English abstract).
Experimental Study of the Water-rock Chemical Reaction in Black Shale
WU Xi-yong1, 2), LIAO Xin1)*, ZHAO Si-yuan1), LING Si-xiang1), ZHU Bao-long3)
1) Department of Geological Engineering, Southwest Jiaotong University, Chengdu, Sichuan 611756; 2) MOE Key Laboratory of High-speed Railway Engineering, Southwest Jiaotong University, Chengdu, Sichuan 610031; 3) School of Civil Engineering and Architecture, Southwest University of Science and Technology, Mianyang, Sichuan 621010
Being an important form of chemical weathering of black shales, the water-rock interaction is closely related to the mineral compositions, engineering properties and geological environments. A China-designed flow-through experiment was used to study the oxidation kinetic behavior of pyrite contained in black shale during the water-rock interaction. The ion concentrations of outflow solutions were measured by the ion analyzer and inductively coupled plasma mass spectrometry. The micro-features of the rock sample before and after the experiment were observed with a scanning electron microscope. Combined with the changes of rock permeability, the kinetic rate of pyrite oxidation and Si release in acid water were examined. The results obtained by the authors indicated that the behavior of pyrite oxidation caused the decrease of the rock permeability by 70%, and the oxidizing reaction coefficient of pyrite embedded in rocks under the effects of mineralogical and chemical compositions and petrophysical properties of the black shale was consistent with that of free pyrite grains reported by previous researchers. Besides, the quartz and illite were dissolved in the acidic solution produced by pyrite oxidation. Due to their uncertain content, the release rate of Si only represented their total dissolution rate.
black shale; pyrite oxidation; water-rock chemical interaction; flow-through experiment; kinetic rate
P588.22; P592
A
10.3975/cagsb.2014.05.07
本文由国家自然科学基金项目“黑色岩层黏土化过程的硫化矿物氧化动力学机理研究”(编号: 41172261)、四川省科技支撑计划项目“黑色岩层酸性弱化与边坡修复技术研究”(编号: 2012SZ0051)和中央高校基本科研业务费专项资金资助项目(编号: 2682014BR013)联合资助。
2013-10-11; 改回日期: 2014-05-28。责任编辑: 张改侠。
巫锡勇, 男, 1963年生。教授, 博士生导师。主要从事岩石风化及其工程特性评价、岩土体稳定性研究。通讯地址: 611756,四川省成都市高新区西部园区西南交通大学地质工程系。E-mail: wuxiyong@126.com。
*通讯作者: 廖昕, 男, 1986年生。博士, 讲师。主要从事岩石风化及其工程特性评价、地质灾害研究。E-mail: xinliao@swjtu.edu.cn。

