4,9-脱水河豚毒素国家标准样品的研制*
陈伟珠,谢全灵,张怡评,洪专,方华,洪碧红,易瑞灶
(1.国家海洋局第三海洋研究所,福建厦门 361005; 2.厦门大学化学化工学院化学系,化学生物学福建省重点实验室,福建厦门 361005)
4,9-脱水河豚毒素国家标准样品的研制*
陈伟珠1,2,谢全灵1,张怡评1,洪专1,方华1,洪碧红1,易瑞灶1
(1.国家海洋局第三海洋研究所,福建厦门 361005; 2.厦门大学化学化工学院化学系,化学生物学福建省重点实验室,福建厦门 361005)
研制4,9-脱水河豚毒素国家标准样品。以河豚鱼卵巢为原料,提取制备4,9-脱水河豚毒素,采用红外光谱(IR)、高分辨质谱和核磁共振谱(NMR)进行结构确证。样品分装成140瓶后,采用柱后衍生-高效液相荧光法进行均匀性、稳定性检验和定值分析。从样品中随机抽取15瓶进行均匀性检验,经F检验表明在95%的置信区间范围内样品均匀性良好;稳定性考察按照40℃加速试验稳定性(6个月)进行,结果表明在考察期间内样品稳定性良好;标准样品经国内8家具有分析资质的实验室进行协同定值,并评定了定值结果的不确定度,4,9-脱水河豚毒素标准样品定值结果为97.77%,相对扩展不确定度为0.4% (k=1.96)。该标准样品达到国家标准样品的技术要求,可用于有关脱水河豚毒素的方法校正和质量控制。
4,9-脱水河豚毒素;标准样品;柱后衍生-高效液相荧光色谱法;定值;不确定度
4,9-脱水河豚毒素(4,9-anhydrotetrodotoxin)是一种氨基全氢喹唑啉型化合物,与河豚毒素结构极其相似,是河豚毒素的一种重要衍生物[1],在自然界中与河豚毒素共存,主要存在于河豚鱼的卵巢、肝脏、皮肤和肠胃中。4,9-脱水河豚毒素跟河豚毒素一样,也是神经细胞膜Na+通道的阻断剂,其生理作用是可快速阻断Na+通道,可广泛应用于神经生物学、生理学及其它科学研究。4,9-脱水河豚毒素的生物毒性比河豚毒素更弱,表现出更大的生物安全性,是一种具有广阔药用前景的化合物[2]。目前,国内外未见4,9-脱水河豚毒素标准样品研制的报道,也无4,9-脱水河豚毒素纯品可以购买,限制了对4,9-脱水河豚毒素的深入研究。4,9-脱水河豚毒素国家标准样品的研制,能解决海洋天然活性物质结构近似的河豚毒素衍生物化合物难以分离的共性技术问题,提供4,9-脱水河豚毒素纯品实物样品,为进一步的生物活性研究提供物质基础,加速4,9-脱水河豚毒素的理论研究与应用基础研究进程,为海洋生物毒素药源开发与药用研究提供物质基础和重要依据。为此笔者研制了4,9-脱水河豚毒素标准样品。
1 实验部分
1.1 主要仪器与试剂
高效液相色谱仪:Waters Alliances 系列,(Waters 2695 separations Module,Waters 2475 Multi λFluorescence Detector,Waters Reagent Manager,Waters Temperation Control Module II,Waters Post Column Reaction Module),美国Waters 公司;
紫外可见分光光度计:HP-8452 型,美国惠普公司;
红外光谱仪:Nicolet Ftir-670 型,美国Thermo Scientific 公司;
高分辨质谱仪:Lct Premier TM XE 型,美国Waters公司;
天平:AL/104型,瑞士梅特勒-托利多集团;
纯水机:Milli-Q型,美国Millipore公司;
磷酸氢二钠、磷酸二氢钠、氢氧化钠:分析纯,国药集团化学试剂有限公司;
庚烷磺酸钠:分析纯,美国Regis Technologies公司;
实验用水均来自Milli -Q 纯水系统。
1.2 脱水河豚毒素样品的制备
以河豚鱼卵巢为原料,首先经浸提、预过滤、膜分离、浓缩等步骤后获得毒素粗品,然后再采用制备色谱分离、浓缩、结晶、干燥等精制方法获得纯度不小于97%的4,9-脱水河豚毒素。
1.3 定性分析
采用红外吸收光谱、高分辨质谱及核磁共振谱等对脱水河豚毒素标准样品进行定性分析。
1.4 定值分析
标准样品定值一般情况下采用技术有效、严谨认可的方法来完成。4,9-脱水河豚毒素的特定检测方法未见相关报道。由于4,9-脱水河豚毒素与河豚毒素有类似的结构,在NaOH溶液中加热同样能产生带有荧光的物质,可以利用荧光检测器测定4,9-脱水河豚毒素的含量,因此选择柱后衍生高效液相色谱-荧光法[3]进行测定。
1.4.1 色谱条件
色谱柱:ZORBAX C8(250 mm×4.6 mm,5 μm);流动相:庚烷磺酸钠的磷酸盐缓冲液(庚烷磺酸钠浓度为2.5 mmol/L,磷酸氢二钠、磷酸二氢钠浓度为0.03 mol/L),流量为0.3 mL/min;荧光检测波长:激发波长为365 nm,发射波长为510 nm;进样体积:10 μL;衍生试剂:4 mol/L氢氧化钠;柱温:28℃;检测器:Waters 2475型荧光检测器。
1.4.2 样品溶液配制
打开盖子后,往西林瓶里加适量的0.03% HAc溶液溶解,然后转移到100 mL的容量瓶,再洗西林瓶5次,并将洗液转移到量瓶中,稀释至标线。然后按照上述的色谱条件进行纯度检测,每个样品重复进样3次。
1.5 均匀性检验
标准样品均匀性是指特性量值在空间分布的均匀程度,它是对标准样品总体空间分布的评价,是标准样品的重要质量指标之一。对同一批制备的脱水河豚毒素样品进行分装,每瓶标准样品净重为1.000 mg,共140瓶。按照GB/T 15000.3-2008[4]规定,本项目确定抽样数目为15个,采用单因素多水平试验方差分析法对4,9-脱水河豚毒素标准样品进行纯度均匀性检验,测定方法采用柱后衍生高效液相色谱-荧光法,每个样品重复测定3次。检测数据用方差分析法进行分析以判断标准样品的均匀性是否合格。
1.6 稳定性检验
为了考察样品的稳定性,确定其有效期,取本标准样品模拟上市包装,在温度为(40±2)℃、相对湿度为75%±5%的条件下进行加速试验6个月。分别于1、2、3、6个月取样,在1.4.1色谱条件下进行检测,考察其样品纯度的变化。
2 结果与讨论
2.1 脱水河豚毒素的定性分析
脱水河豚毒素通过红外吸收光谱、高分辨质谱及核磁共振谱进行定性分析。
4,9-脱水河豚毒素的结构式见图1。对该样品进行核磁共振测试,核磁数据见表1。从表1可知,该化合物的各质子、各碳的化学位移与文献[5]数据基本一致,且质子个数、碳原子个数与脱水河豚毒素的分子式一致。
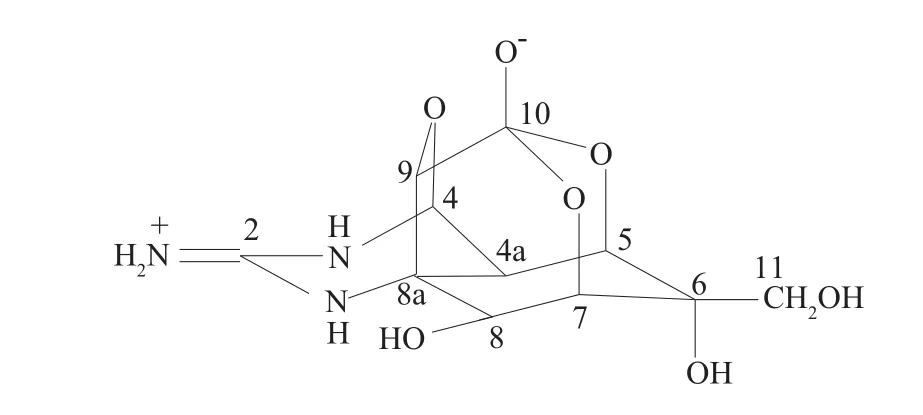
图1 脱水河豚毒素的结构式
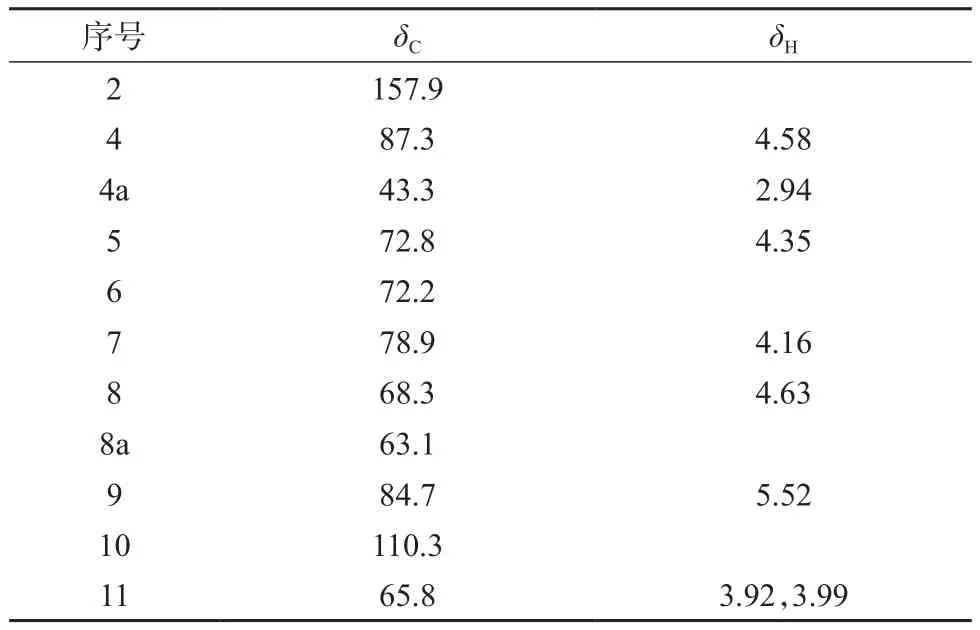
表1 脱水河豚毒素的核磁共振数据
样品的红外光谱说明结构中存在羟基、胺基、胍和亚甲基等,与脱水河豚毒素的官能团一致。高分辨质谱测得该样品的精确质量数为302.097 1,与脱水河豚毒素的质子加合峰一致(理论值C11H16N3O7[M+H]+302.098 8)。综上所述,可以确证该样品是脱水河豚毒素。
2.2 均匀性试验
标准样品的均匀性检验是标准样品研制过程中不可缺少的程序。因此在对样品进行分装后,对4,9-脱水河豚毒素标准样品进行纯度均匀性检验,均匀性检验结果见表2与表3。
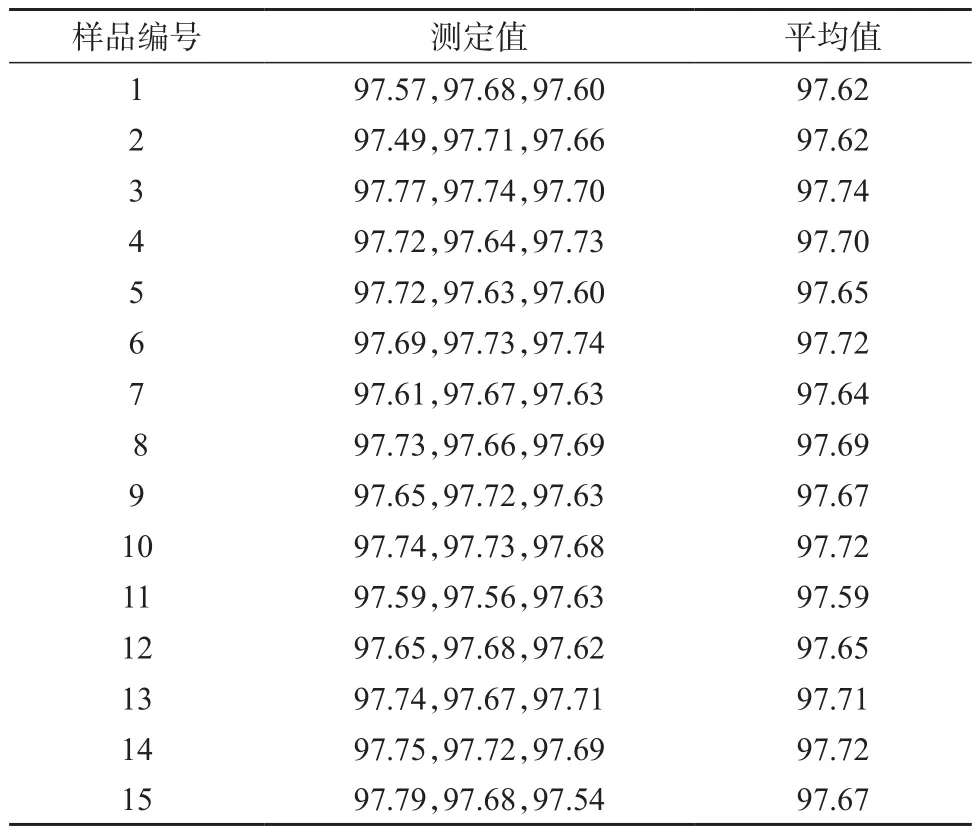
表2 脱水河豚毒素标准品纯度均匀性检验结果 %
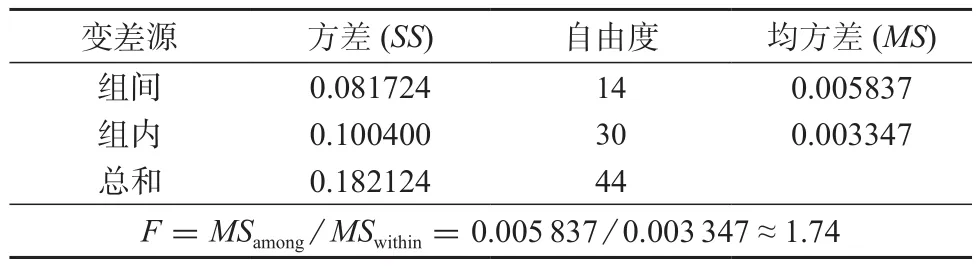
表3 方差分析结果
F(0.05,14,30)=2.04,由表3可知,F<F(0.05,14,30),说明在95%的置信区间4,9-脱水河豚毒素样品均匀性良好。
2.3 稳定性试验
按1.6进行稳定性重点考察项目检测试验,结果见表4。

表4 加速试验结果
采用直线模型作为经验模型,对4,9-脱水河豚毒素长期稳定性获得的数据进行分析。
直线的斜率:
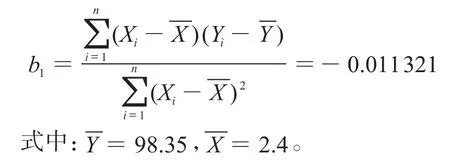
直线的截距:
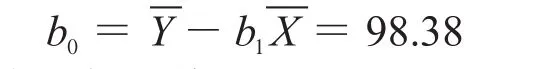
直线上点的标准偏差:
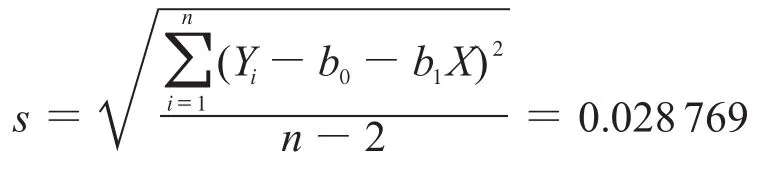
与斜率相关的不确定度:
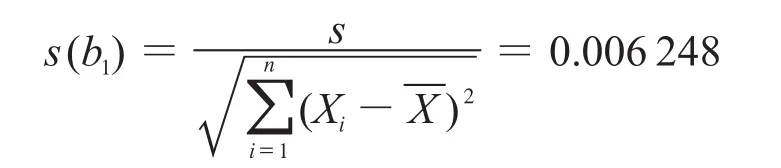
自由度为n-2和P=0.95(95%置信水平)的t因子t0.95,n-2=3.18。
t0.95,n-2·s(b1)= 3.18×0.006 248= 0.019 619,由于|b1|<t0.95,n-2·s(b1),故斜率不显著,因而未观测到不稳定性,说明经(40±2)℃、相对湿度(75±5)%加速试验样品稳定性良好。
参照药典的说明,如果样品在加速试验条件下(30~40℃,RH=75%,3个月),各项质量仍然良好,可初步确定其稳定性为2年。因此将4,9-脱水河豚毒素国家标准样品的最终有效期暂定为2年。
2.4 定值结果及其不确定度评定
2.4.1 定值结果
4,9-脱水河豚毒素标准样品按照GB/T15000.3-2008[4]标准要求,采用多个实验室协作定值,选择获得国家或部门认可的具备资质的8家实验室进行样品定值。随机抽取8瓶样品,每个定值实验室送1瓶,采用柱后衍生高效液相色谱荧光法进行测定,应用面积归一法进行定量,定值结果见表5。
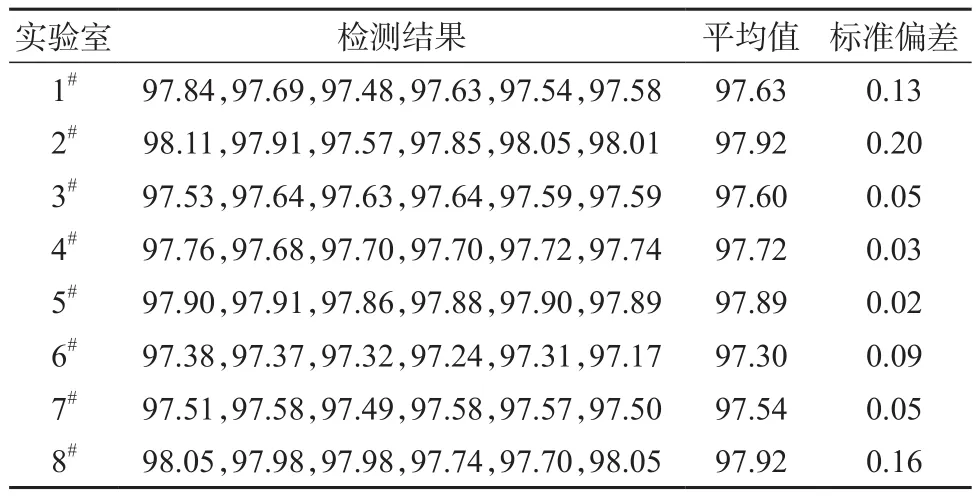
表5 8家实验室定值结果 %
汇集各家实验室的检测数据后,对每家实验室的数据按大小顺序排列,用Grubb’s法和峰度法正态性检验组内数据的异常值,结果没有异常值。所有数据进行下一步统计,用Grubb’s法对每家实验室的平均值进行检验,将其看成一组测定值进行异常值检验,经检验无异常值。因此将各家实验室测得的数据作为无偏估计值,计算8家测定结果的平均值及标准偏差。然后对各实验室测定结果的标准偏差S进行Cochran检验,计算统计量:
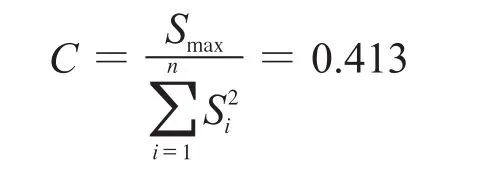
式中:Si——各实验室测定结果的标准偏差;
Smax——Si中的最大值。
C8,6(0.05)=0.360,C>C8,3(0.05),表明各实验室间的测量不属于等精度测量,因此计算加权平均值作为最佳值得到脱水河豚毒素标准样品的定值结果。总平均值X=97.77%。
2.4.2 定值结果的不确定度评定
根据GB/T 15000.3-2008标准规定,定值结果由标准值和不确定度组成。标准样品特性标准值的测量不确定度u由标准值定值实验引入的不确定度u(X)、均匀性检验引入的不确定度ubb和稳定性检验引入的不确定度ults组成。依据全部测定结果,计算4,9-脱水河豚毒素标准样品的特性标准值和不确定度。
(1)标准值定值试验引入的不确定度u(X)。按照加权法计算得到标准样品定值的不确定度u(X)=0.19%。
(2)均匀性检验引入的不确定度ubb。瓶间方差:

式中:MSamong——组间均方差,来自表3;
MSwithin——组内均方差,来自表3。
则均匀性检验引入的不确定度:
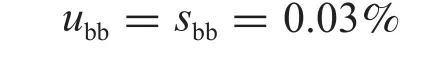
(3)稳定性检验引入的不确定度ults。由2.3稳定性检验试验可知,稳定性检验引入的不确定度:

标准样品定值结果的不确定度:
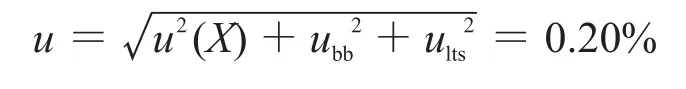
扩展不确定度:
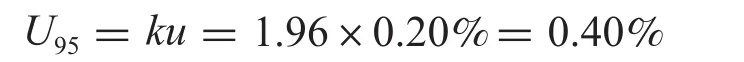
4,9-脱水河豚毒素标准样品的定值结果:97.77%±0.40%(k=1.96)。
3 结语
研制了4,9-脱水河豚毒素标准样品脱水河豚毒素标准样品,对其进行了均匀性检验、稳定性考察,结果表明该标准样品符合标准样品均匀性与稳定性的要求。研制的4,9-脱水河豚毒素标准样品对食品安全、环境监测、卫生检验检疫等方面的测量和科学研究提供了技术支撑和量值溯源保证,具有重要意义。
[1]Toshio Nakagawa,Junho Jang,Mari Yotsu-Yamashita. Hydrophilic interaction liquid chromatography-electrospray ionization mass spectrometry of tetrodotoxin and its analogs [J]. Analytical Biochemistry,2006,352: 142-144.
[2]谢全灵,易瑞灶,许晨,等.高纯脱水河豚毒素的结构表征与毒力测定研究[J].中国海洋药物,2009,28(5): 21-24.
[3]陈伟珠,洪专,张怡评,等.河豚毒素的高效液相/荧光精确定量技术研究[J].中国卫生检验,2009,19(2): 261-262.
[4]GB/T 15000.3-2008 标准样品工作导则(3) 标准样品定值的一般原则和统计方法[S].
[5]Takeshi Y,Mari Y,Michio M. New tetrodotoxin analogues from the newt cynopsensicauda[J]. J Am Chem Soc,1988,110: 2 344-2 345.
Development of Anhydrotetrodotoxin Certified Reference Material
Chen Weizhu1,2, Xie Quanling1, Zhang Yiping1, Hong Zhuan1, Fang Hua1,Hong Bihong1, Yi Ruizao1
(1. The Third Institute of Oceanography of the State Oceanic Administration, Xiamen 361005, China; 2. Department of Chemistry and Key Laboratory Chemical Biology of Fujian Province, Xiamen University, Xiamen 361005, China)
4,9-anhydrotetrodotoxin certified reference material was developed. 4,9-anhydrotetrodotoxin was made from the ovarium of pufferfish. The structure of anhydrotetrodotoxin certified reference material was comfirmed by mass spectrometry and NRM,infrared spectroscopy (IR). 4,9-anhydrotetrodotoxin was divided into 140 bottles. The homogeneity and stability testing and quantitative analysis were evaluated by post column derivation high performance liquid chromatography-fluorescent detection (HPLC-FLD) method. According to analysis procedure of homogeneity,15 bottles of sample were randomly taken from 140 bottles,and the results were validated by F-test statistical method. The stability inspection was carried on the short-term(6 months),and the results indicated that the period for anhydrotetrodotoxin of storage was 6 months at 40℃. A cooperative certification was conducted with 8 qualified laboratories. The certified purity value of the reference material of 4,9-anhydrotetrodotoxin was 97.77% with relative expaned uncertainty of 0.40%(k=1.96). The reference material can conform to the technical requirement of the certified reference material. The material was intended for use in the method validation and quality control regarding anhydrontetrodotoxin.
4,9-anhydrotetrodotoxin; certified reference material; post column derivation-HPLC-FLD; certification; uncertainty
O652.3
A
1008-6145(2014)03-0001-04
10.3969/j.issn.1008-6145.2014.03.001
*广东海洋经济发展区域示范项目(GD2012-D01-001);海洋生物产业化中试技术研发公共服务平台(12PZP001SF10);厦门市重大科技创新平台项目(3502Z20111001);国家科技支撑计划(NO.2011BAK04B09)
联系人:洪专;E-mail: hzh@tio.org.cn
2014-02-12

