原发性肝癌质子射束与三维适形放疗计划的比较
陈 庆 宋婷婷 李家敏 毕 斌 魏清龙 刘素文
(山东淄博万杰肿瘤医院质子治疗中心,山东 淄博 255213)
原发性肝癌质子射束与三维适形放疗计划的比较
陈 庆 宋婷婷 李家敏 毕 斌 魏清龙 刘素文
(山东淄博万杰肿瘤医院质子治疗中心,山东 淄博 255213)
目的对原发性肝癌(PLC)患者质子射束治疗(PBT)计划与X线三维适形放射治疗(3D-CRT)计划进行比较,寻求降低原发性肝癌放射治疗引起放射性肝病(RILD)发生率更有效的放射治疗方式,分析质子射束治疗原发性肝癌的物理优势和设野数对剂量分布的影响。方法选取临床治疗的12例肿瘤直径<5 cm的原发性肝癌患者,采用等中心归一方法,中心剂量为66 Gy,质子治疗分别选用单野、两野和三野进行治疗计划的计算,三维适形放射治疗选用3~6野进行治疗计划的计算,通过剂量体积直方图(DVH)分析比较其剂量分布的差异。结果肿瘤直径<5 cm的原发性肝癌患者3D-CRT等中心剂量为66 Gy时正常肝脏组织的平均剂量为18.78 Gy,其V5、V10、V20和V30分别为70.01%、53.71%、36.58%和22.95%。相同等中心剂量下,单个质子射束治疗计划正常肝脏组织的平均剂量为7.21 Gy,其V5、V10、V20和V30分别为17.30%、15.60%、13.32%和11.52%,两个质子射束治疗计划正常肝脏组织的平均剂量为8.23 Gy,其V5、V10、V20和V30分别为23.95%、21.40%、17.59%和11.16%,三个质子射束治疗计划正常肝脏组织的平均剂量为9.83 Gy,其V5、V10、V20和V30分别为35.03%、30.99%、16.31%和11.46%。12例患者无论是采用质子射束单野照射、两野照射还是三野照射,脊髓、右侧肾脏、胃和胰腺的受照剂量均明显低于3D-CRT(P<0.002)。结论无论采用质子射束单野照射、两野照射还是三野照射,均较3D-CRT明显降低了正常肝脏、脊髓、右侧肾脏和胃以及胰腺的照射剂量。随着质子射束数量的增加,正常肝脏、脊髓、右侧肾脏和胃及胰腺的照射剂量呈逐渐递增的趋势,但递增速度缓慢。质子治疗肿瘤直径<5 cm的原发性肝癌,两个射束足以满足治疗肿瘤和保护正常肝脏组织的需要,继续增加设野数,无明显优势。
原发性肝癌;放射性肝病;质子束治疗;三维适形放射治疗;治疗计划
原发性肝癌是我国常见的高发恶性肿瘤之一,患者大多有慢性肝炎及肝硬化病史。肝硬化的严重程度是影响原发性肝癌患者治疗及预后的重要因素。原发性肝癌的放射治疗由于受到肝脏放射耐受量差的限制,全肝放射治疗的疗效不理想,很少应用。随着近年来三维适形放射治疗(three dementional conformal radiation therapy,3D-CRT)的开展,降低了肝脏照射剂量,提高了肿瘤局部的照射剂量和疗效[1]。但仍然因为光子射线的穿射效应,剂量分布的指数衰减规律,不能最大限度的保护正常肝脏,并可能导致放射诱发的肝病(radiation induced liver disease,RILD)。质子束具有Bragg峰的物理学特性优势,末端剂量快速跌落,其能量传递是以量子的形式释放,可有效的降低正常肝脏组织及其周围器官的有效照射体积和剂量,提高肿瘤治疗剂量和疗效,最大限度的降低放射诱发RILD的概率。
1 材料与方法
1.1 病例选择:2005年4月至2009年7月间在淄博万杰质子治疗中心进行治疗肿瘤直径≤5 cm的ⅠA 期原发性肝癌12例,男10例,女2例,平均年龄51岁。诊断依据临床表现、实验室和影像学检查,全部患者均符合2001年9月在广州召开的第八届全国肝癌学术会议上由中国抗癌协会肝癌专业委员会制定的“原发性肝癌的临床诊断与分期标准”[2],其中7例经病理证实。
1.2 治疗计划系统:分别采用Varian公司的Eclipse Proton质子计划系统(版本号:7.2.3)和Eclipse Photon三维治疗计划系统。所有治疗计划均在同一评估模式下进行比对。每周应用美国CIRS公司Model 62 CT密度体模对不同组织CT值对应电子密度值及不同组织CT值对应组织本领比(Stopping Power)进行校准、比对。
1.2.1 体位固定及靶区勾画:12例患者均仰卧位,真空负压垫固定体位,训练患者平静均匀呼吸,GE公司Ge LightSpeed 8排CT扫描,平扫后同床位病灶区域强化扫描,层厚5 mm,可重建2.5 mm层厚。由高年资影像科医师与肿瘤科医师及医学放射物理师共同勾画靶区GTV及危及器官(OAR)。PTV根据患者的膈肌呼吸动度在GTV基础上头脚方向外扩1.5~2.5 cm,左右方向外扩1.0~1.5 cm。
1.2.2 治疗计划设计:质子束流由等时回旋加速器产生,该加速器可产生固定能量为230 Mev的质子束,通过降能器得到能量范围为70~230 MeV的质子束流。由射程调制器获得所需的展宽的Bragg峰以使得照射在三维方向上与靶区适形。治疗采用双散射模式。质子治疗分别采用单野、两野、三野进行剂量分布的计算,组织射程补偿器模糊计算(Smearing)矩阵采用5 mm,尽量避开危及器官,等中心归一方式95%剂量线包绕PTV。3D-CRT采用3~6个射野进行治疗计划剂量计算,射野应用楔形板,相同归一方式95%剂量线包绕PTV,减少入射束经过危及器官。
1.2.3 治疗计划的评价:采用剂量体积直方图分别对质子一野、质子两野、质子三野及X线三维适形放疗计划进行评价。评价指标:①肝脏平均剂量、V5、V10、V20、V30;②脊髓最大点剂量、右肾、胃和胰腺的平均受照剂量。
1.3 统计学方法:采用配对资料t检验比较计划剂量的差异。
2 结 果
从图1和图2可以看出质子束单野、两野、三野95%剂量线均可很好的包绕GTV和PTV,质子束单野因方向容易选择,可很好的避开肾脏、胃及胰腺,使其平均剂量几近为零,肿瘤前方正常组织较两野及三野略高。质子束两野、三野计划因平均了单野前方在肝脏上的剂量,正常肝脏高剂量区域体积减少,低剂量区域V5、V10随着设野数目的增加明显增加,V20、V30无明显增加趋势。因此,在充分考虑治疗过程中肝脏因呼吸动度对剂量分布造成的影响的前提下,应用两野可满足肿瘤照射剂量和尽可能保护正常肝组织的要求,增加设野数目对于提高靶区包绕和减少正常肝脏组织平均受量并无明显优势。
由图2和图3可以看到质子束单野、两野及三野剂量分布与3D-CRT比较,均明显降低了正常肝脏、脊髓、右侧肾脏和胃以及胰腺的照射剂量(表1、2)。
肿瘤直径<5 cm的原发性肝癌患者3D-CRT等中心剂量为66 Gy时正常肝脏组织的平均剂量为18.78 Gy,其V5、V10、V20和V30分别为70.01%、53.71%、36.58%和22.95%。相同等中心剂量下,单个质子射束治疗计划正常肝脏组织的平均剂量为7.21 Gy,其V5、V10、V20和V30分别为17.30%、15.60%、13.32%和11.52%,两个质子射束治疗计划正常肝脏组织的平均剂量为8.23 Gy,其V5、V10、V20和V30分别为23.95%、21.40%、17.59%和11.16%,三个质子射束治疗计划正常肝脏组织的平均剂量为9.83 Gy,其V5、V10、V20和V30分别为35.03%、30.99%、16.31%和11.46%。
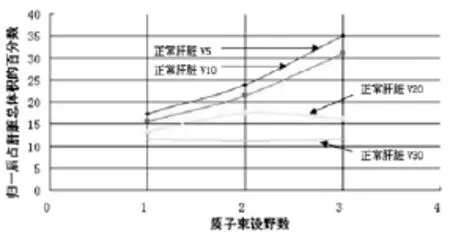
图1 正常肝脏V5、V10、V20、V30随设野数变化照射剂量的变化(V5、V10、V20、V30分别为受到5 Gy、10 Gy、20 Gy、30 Gy照射剂量的正常肝脏组织的百分比)
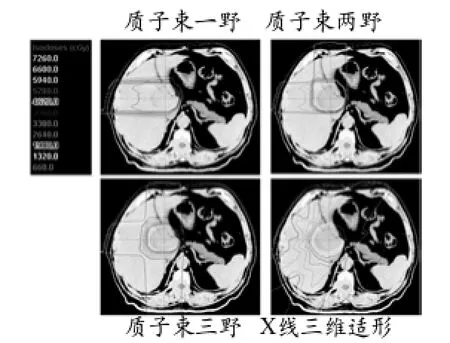
图2 质子束一野、两野、三野剂量分布与X线三维适形放疗计划剂量比较(图中浅绿色涂抹为GTV,浅褐色涂抹为PTV)

图3 质子束两野与3D-CRT GTV、PTV、肝脏、胃、脊髓、胰腺受量DVH比较(质子束治疗用实线表示,X线三维适形治疗用虚线表示,同一器官颜色相同。右肾、脊髓、胃及胰腺的质子治疗剂量接近为0)
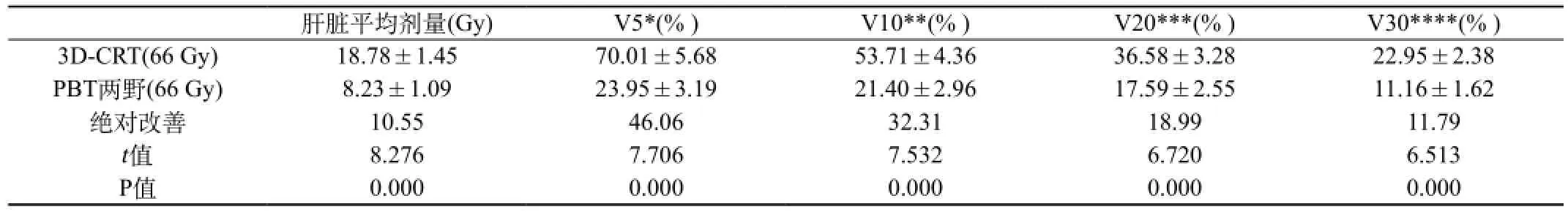
表1 原发性肝癌(直径≤5 cm)患者PBT两野与3D-CRT治疗计划正常肝脏组织剂量比较

表2 原发性肝癌(直径≤5 cm)患者脊髓最大剂量、右肾、胃和及胰腺平均剂量的比较
3 讨 论
放射性肝病(radiation-induced liver disease,RILD)是PLC进行3DCRT最主要的并发症之一,也是影响PLC 3DCRT放射耐受量的最主要因素[3]。肝脏在解剖上由无数肝小叶组成,肝小叶为肝脏的功能亚单位,其组合方式为并连型。因此,肝脏放射损伤的严重程度与它受照射的体积密切相关[1]。梁世雄,蒋国梁等报告,全肝平均剂量与RILD的发生有关(P=0.027)。当V5、V10和V20≤81%、69%和42%且全肝平均剂量≤28 Gy时RILD的发生概率<5%(P=0.029、0.044、0.029和0.043)[4]。曾昭冲对肝癌施以低分割三维适形放疗持有异议,因为其放射性肝炎发生率高达32%,由此导致的病死率相当高。肝细胞癌的α/β值>11 Gy[5],而正常肝细胞的α/β值为1~2 Gy[6]。如果用LQ模式{BED=nd[1+d/(α/β)}将6 Gy/次×9次的低分割转化为常规分割剂量,即可计算出,当α/β值介于1~2 Gy时,正常肝组织受量相当于常规分割剂量的108~126 Gy;而α/β值介于12~16 Gy(相当于肝细胞癌时),肿瘤组织受量仅66.0~69.4 Gy。也就是低分割放疗对正常肝组织的损伤重于对肿瘤的杀伤。适形放疗采取多野以求靶区剂量均匀,结果正常肝组织普遍受到剂量不等的放射,肝细胞再增生能力受影响,而普通放疗的设野简单,留有正常肝组织在放射野外,得以代偿性增生。放射野设计必须考虑留有正常肝组织不受到照射[7]。质子治疗计划设两野即可满足靶区的剂量均匀,又可保留正常肝组织不受到照射。这是因为质子束的能量巨大,在达到靶区的途中与组织形成的散射线远小于电子线,在照射区域周围半影非常小。而且,质子束峰锐减(尾),所以肿瘤后面与侧面的正常组织可以得到保护,而肿瘤区域以前的受量也只有X线、电子线的一半,其正常组织损伤也是非常少的[8]。Herman S早在2001年就预见,因为质子束在剂量分布上的优势,质子将在未来的20~30年内替代光子射线(γ射线、X射线等)治疗成为常规的治疗手段[9]。质子束治疗效果好,可能由于质子束LET比γ线要高,质子束照射后所产生的潜在性致死损伤修复小于γ线,质子束的这一优点有可能成为解释质子治疗肿瘤疗效好的新理论基础[8]。
[1] 殷蔚伯,余子豪.肿瘤放射治疗学[M].4版.北京:中国协和大学出版社,2008:829-836.
[2] 杨秉辉,夏景林.原发性肝癌的临床诊断与分期标准[J].中华肝脏病杂志,2001,9(6):324.
[3] Lawrence TS,Ten-Haken RK,Kessler ML,et al.The use of 3-D dose wolume analysis to predict radiation hepatitis[J].Int J Radiat Oncol Biol Phys,1992,23(4):781-788.
[4] 梁世雄,蒋国梁.原发性肝癌三维适形放疗后放射性肝病的影响因素[J].中华放射肿瘤学杂志,2005,14(4):284-288.
[5] Zeng ZC,Jiang GL.DNA-PKcs subunits in radiosensitization by hyperthermia on hepatocellular carcinoma Hep G2 cell line[J].World J Gastroenterol,2002,8(5):797-803.
[6] Fisher DR,Hendry JH.Dose fractionation and hepatocyte clonogens: α/β≈1~2Gy,and β decreases with increasing delay before assay[J]. Radial Res,1988,113(1):51-57.
[7] 曾昭冲.肝癌放疗应采用何种分割剂量[J].中华放射肿瘤学杂志,2006,15(4):347.
[8] 唐劲天,左焕琮.质子治疗肿瘤的现状与发展趋势[J].中华肿瘤杂志,2001,23(1):7-10.
[9] Herman S.The gray lecture 2001: comning technical advances in radiation oncology[J].Int J Radiation Oncology Biol Phys,2002, 53(4):798-809.
R735.7
B
1671-8194(2014)29-0115-02

