电化学氢化物发生技术在原子光谱分析领域的应用进展
祖文川,汪 雨,武彦文,陈舜琮
(北京市理化分析测试中心,北京市食品安全分析测试工程技术研究中心,北京100089)
电化学氢化物发生技术在原子光谱分析领域的应用进展
祖文川,汪 雨,武彦文,陈舜琮
(北京市理化分析测试中心,北京市食品安全分析测试工程技术研究中心,北京100089)
电化学氢化物发生法(EcHG)是原子光谱仪发展的一种实用气态进样技术。该技术通过采用电化学发生池内的电极反应代替传统化学还原的方法来生成氢化物和汞蒸气。与传统的化学法硼氢化钾(钠)-酸氢化物发生体系相比,EcHG技术仅需要支持电解质,氢化物(汞蒸气)在阴极室内发生后直接导入原子光谱仪的原子化器,在降低分析成本和溶液配制时间的同时,分析过程引入的空白值也大大降低,更加绿色环保。近年来,EcHG原子光谱分析已经从单一的元素总量测定发展到元素形态分析,从微量元素分析发展到痕量超痕量元素分析,发生元素涵盖了砷、硒、铅、镉、锡、锑、锗和汞,应用范围涉及食品、环境、烟草、饲料等实际样品。EcHG技术应用于原子荧光光谱分析,特征元素检出限能够达到0.1 μg/L级(汞为ng/L级);应用于原子吸收光谱与等离子体发射光谱分析,适用元素检出限能够达到μg/L级,相对标准偏差均小于10%,回收率在90%~110%之间。EcHG技术相关的机理研究也已经起步,这为该技术在原子光谱分析领域的应用提供了理论基础。但是,EcHG技术的分析范围目前仅限于部分元素的无机态,对元素的有机形态分析是本领域发展的难点之一。本文提出,关于电化学氢化物发生的机理研究、电化学流通池结构的优化、形态分析范围的拓展等将成为该技术的重要发展方向。
电化学氢化物发生;原子荧光光谱;原子吸收光谱;等离子体发射光谱;研究进展
电化学氢化物发生法(EcHG)是原子光谱仪发展的一种实用的气态进样技术。该技术针对易于发生氢化物(单质蒸气)的特征元素,通过采用电化学发生池内的电极反应代替传统化学还原的方法来生成氢化物和汞蒸气。与传统的化学法硼氢化钾(钠)-酸氢化物发生体系相比,EcHG技术仅需要采用支持电解质溶液,无需其他化学试剂,在降低了分析成本和溶液配制时间的同时,分析过程引入的空白值也大大降低,更加绿色、环保。近年来EcHG技术已经从单一的总量测定发展到元素的形态分析,从适用微量分析发展到满足痕量乃至超痕量分析的要求;其相关的机理研究也已经起步,这为该技术在原子光谱分析领域的应用提供了理论基础。就分析性能而言,EcHG技术的分析范围涵盖了砷、硒、铅、镉、锡、锑、锗和汞等大部分常规化学法氢化物发生的元素,已经应用于食品、环境、烟草、饲料等诸多实际样品的测定。EcHG技术在原子光谱分析领域有了较大的发展,应用于原子荧光光谱分析,特征元素检出限能够达到0.1 μg/L级(汞为ng/L级);应用于原子吸收光谱与等离子体发射光谱分析,适用元素检出限能够达到μg/L级;相对标准偏差均小于10%,回收率在90%~110%之间。但是,目前EcHG技术的分析范围仅限于部分元素的无机态,对元素的有机形态分析尚未涉及,成为本领域发展的热点及难点之一。关于电化学氢化物发生的机理研究、电化学流通池结构的进一步优化、形态分析范围的拓展等是该技术的重要发展方向。
氢化物发生法(HG)是应用于原子荧光光谱仪、原子吸收光谱仪以及等离子体发射光谱仪等各种原子光谱仪器的气态进样技术[1-3]。氢化物发生技术实现了分析元素与基体的分离,具有干扰少、进样效率高等优点,成功应用于砷、硒、铅等易于形成氢化物的元素和汞的定量分析。该技术最早由Holak[4]提出,并较迅速地在原子吸收光谱(AAS)分析中得到运用。就氢化物发生方法而言,主要包括金属-酸还原体系(Marsh反应)、硼氢化钠(钾)-酸体系、碱性模式还原以及电解还原法四种[5]。其中,硼氢化钠(钾)-酸体系是目前在商品化原子光谱分析中应用最为广泛的氢化物发生方法,但存在着发生效率受元素价态影响显著、对采用试剂的纯度要求严格、干扰显著以及方法空白偏高等缺点。
EcHG是一种实用的氢化物发生技术,通过采用电解还原的方法获取氢化物和汞蒸气。由于采用了电极还原的方式,除支持电解质外,无需采用其他化学试剂,在降低分析成本的同时也大大避免了传统化学氢化物发生法对高纯度化学试剂的依赖,显著降低了方法空白。并且EcHG具有选择性好、易于实现价态分析等诸多优点。李淑萍等[6]在2001年对EcHG早期研究的电解池结构、电极材料选择以及干扰情况等诸多方面进行了详细的综述。近年来,EcHG在原子吸收光谱(AAS)、原子荧光光谱(AFS)以及电感耦合(微波诱导)等离子体发射光谱(ICP-AES/MIP-AES)等原子光谱分析领域有了较大的发展,已经成为原子光谱进样技术的重要研究领域之一。
1 EcHG氢化物发生机理及结构
1.1 EcHG氢化物发生机理
电化学氢化物发生是在电化学流通池的阴极室中完成的。通过电化学还原的方式,特征元素可以由离子态转化为氢化物(单质蒸气)。该进样技术相关机理研究能够为其在原子光谱分析的应用提供理论基础。目前,相关研究已有涉及。Francisco等[7]认为电化学氢化物发生分四步进行(如图1所示):①氢化物发生元素离子扩散到阴极表面;②氢化物发生元素离子电化学还原成自由原子并沉积在阴极表面;③自由原子在阴极表面形成氢化物;④氢化物扩散离开阴极表面。而步骤③以三价氢化物形成过程为例,自由原子形成氢化物的过程分为两种形式:(a)水分子还原成氢原子,进而化学吸附自由原子形成单氢共价氢化物,每个单氢共价氢化物分子经历两个歧化反应形成最终三价氢化物;(b)自由原子与两分子水作用形成二氢共价氢化物,而后经历一个歧化反应形成三价氢化物。
1.2 电化学流通池结构设计
EcHG氢化物发生的核心装置为电化学流通池。通常采用的电化学流通池结构如图2所示,流通池分为阴极室、阳极室两部分,由离子交换膜隔开。电化学流通池的电极材料、形状、表面积大小以及支持电解质及浓度等各异,直接影响氢化物的发生效率,是在电化学流通池结构设计过程中需要重点考虑和优化的因素。

图1 EcHG氢化物发生机理示意图(黑条代表阴极)[7]Fig.1 Mechanism of electrochemical hydride generation (Modified from Reference[7])

图2 EcHG电化学流通池结构示意图[7]Fig.2 Configuration of electrolytic flow cell for EcHG (Modified from Reference[7])
2 EcHG在原子荧光光谱分析中的应用
2.1 EcHG-AFS应用于元素定量分析
氢化物发生-原子荧光光谱技术(EcHGAFS)是具有完全中国自主知识产权的分析技术,该技术已经很好地应用于As、Se等元素的定量测定。EcHG技术取代氢化物发生法,是拓展氢化物发生体系与方法的重要尝试,并展现了良好的分析性能。该技术分析的元素涵盖As、Sb、Hg、Ge、Sn等,其相关应用列于表1。就分析性能而言,在优化的EcHG电化学流通池工作条件下,检出限达到0.1 μg/L级(Hg为ng/L级);相对标准偏差均小于5%,线性范围达到3个数量级,回收率在90%~110%之间。应用范围涉及土壤、沉积物、河水等环境样品以及食品、饲料、烟草等其他领域样品。
总体上,EcHG-AFS虽然尚未实现商品化,但与传统商品化HG-AFS技术相比优势显著,具有很大的发展潜力,EcHG-AFS可以实现与之相当的检出限和稳定性。EcHG-AFS的商品化需要有坚实的理论基础作为支撑,因此,针对机理的研究有助于分析工作者进一步从本质上了解该技术,进而完善和发展该技术,EcHG的理论研究将成为EcHGAFS的重要发展方向之一。

表1 EcHG-AFS技术的应用研究Table 1 Application study of EcHG-AFS technology
2.2 EcHG-AFS应用于元素形态分析
EcHG-AFS技术在特征元素总量测定的基础上,也经拓展到元素形态分析领域,并且已有较大进展。EcHG-AFS技术应用于元素形态分析无需借助色谱分离,因此很大程度上降低了形态分析的仪器成本,引起了广大分析工作者的广泛关注。
张王兵[16]将EcHG-AFS技术应用于环境样品中四价硒Se(Ⅳ)和六价硒Se(Ⅵ)的价态分析,该法采用热水浴在线还原技术,将Se(Ⅵ)在高浓度盐酸介质中120 s内还原成Se(Ⅳ),通过电化学氢化物发生技术生成氢化物,成功地进行硒的在线价态分析;Se(Ⅳ)和Se(Ⅵ)的相对标准偏差分别为2.6%和3.1%;Se(Ⅳ)和总硒的检出限分别为0.32 μg/L和0.27 μg/L。申屠超课题组[17-19]将EcHG -AFS技术与离子色谱法联用,实现了As和Sb的形态分析。通过该联用技术,在5 min内实现了五价锑Sb(Ⅴ)和三价锑Sb(Ⅲ)的价态分析,相对标准偏差均小于5%,Sb(Ⅴ)和Sb(Ⅲ)的检出限分别为5.39和5.42 μg/L,并且较好地应用于中药当归中Sb的价态分析。该课题组还将EcHG-AFS技术应用于牙髓失活材料中As的形态分析,As(Ⅲ)、二甲基砷酸(DMA)、一甲基砷酸(MMA)的线性范围为5~200 μg/L,As(Ⅴ)的线性范围为10~200 μg/L;As(Ⅲ)、DMA、MMA和As(Ⅴ)检出限分别为3.04、4.27、3.97和9.30 μg/L。作者课题组[20]对EcHG-AFS技术应用于无机汞、甲基汞、乙基汞及苯基汞等不同形态汞分析的性能进行了考察,并成功分析了海产品中甲基汞的含量,甲基汞检出限达到1.88 ng/L,相对标准偏差2.0%,平均回收率94.4%。
总体而言,EcHG-AFS技术在元素形态分析领域有了显著发展,有利于扩展我国自主知识产权原子荧光光谱仪的分析范围。目前,EcHG-AFS形态分析的元素范围已经涵盖As、Se、Sb及Hg元素,且针对这些元素的不同形态具有检出限低、线性范围宽等优点。由于该技术无需借助色谱分离而实现元素形态分析,分析仪器更趋简单化,分析成本更加低廉化。但EcHG-AFS分析元素形态范围目前仅限于部分元素的无机态,对元素的有机形态分析成为本领域发展的难点之一。作者课题组[20]对有机汞分析研究表明该技术具有应用于元素有机形态分析的可能。
3 EcHG在原子吸收光谱分析中的应用
3.1 EcHG-AAS应用于元素定量分析
化学氢化物发生法是目前AAS法测定As、Se等易于形成氢化物元素常采用的进样方式,HGAAS作为一种成熟的分析技术已经广泛应用于实际样品分析[21-25]。近年来,EcHG取代传统的氢化物发生技术,应用于AAS分析的进样系统有了一定发展,这主要体现在电化学流通池阴极材料的改善以及由此带来的氢化物发生效率的提升等方面。EcHG-AAS技术的相关研究及应用列于表2,应用领域包括食品、环境及生物样品等,分析元素涵盖Pb、Cd、Se、Sb;就分析性能而言,在优化条件下,检出限达到μg/L级,相对标准偏差均小于10%,方法准确度满足实际分析的要求。
相较HG-AAS技术,EcHG-AAS展现了分析空白值低、试剂消耗少、干扰少等优点。但是,EcHG -AAS的分析灵敏度还有待进一步改善,且与EcHG-AFS技术类似,EcHG-AAS的商品化同样需要理论基础的进一步完善。

表2 EcHG-AAS的应用研究Table 2 Application study of EcHG-AAS
为了实现更好的灵敏度,电化学氢化物发生法应用于石墨炉原子吸收光谱仪,构成的电化学氢化物发生-石墨炉原子吸收光谱法(EcHG-GFAAS)已经有相关尝试和报道[34-36]。基于石墨炉原子化器采用石墨管进样并加热的特点,EcHG-GFAAS需要对氢化物蒸气进行原位捕集。Mahboubeh等[34]采用锡铅合金作为电解池的阴极材料,发生镉的氢化物,采用铱涂层石墨管原位捕集后GFAAS法测定。优化条件下,该法在0.5~5 ng/L镉浓度范围内线性良好,检出限为0.05 ng/L,相对标准偏差为5.5%,回收率在91%~101%之间,较好地应用于河水和自来水等实际样品的分析。该研究组还将该法应用于锡元素的测定[35],优化条件下,在1~200 μg/L锡浓度范围内线性良好,检出限为0.8 μg/L,相对标准偏差为6.2%,回收率在93.1% ~115%之间。Šíma等[36]将EcHG-GFAAS法应用于硒元素分析,分别采用铅丝和铅粒作为两种薄层电解池的阴极材料,1 mol/L盐酸作为阴极电解质,2 mol/L硫酸作为阳极电解质,电解电流分别为1.2 A和0.8 A,载气流量分别为40和70 mL/min。采用钯涂层石墨管原位捕集后,GFAAS测定的结果表明:铅粒电极H2Se发生、传输和捕集效率为80%± 5%,高于铅丝电极的效率(71%±7%)。该法绝对检出限为50 pg,相对标准偏差2.4%,可以获得与HG-GFAAS法相当的分析性能。
EcHG-GFAAS较之EcHG-AAS在检出限、灵敏度等性能上有了较大的改善,但受到石墨管进样模式制约,需要对氢化物进行原位捕集,这必然带来分析对象的损失。因此,EcHG-GFAAS技术的发展需要捕集效率更高的涂层石墨管。
3.2 EcHG-AAS应用于元素形态分析
在总量分析以外,EcHG-AAS技术也已经向元素的形态分析方面发展。李勋等[37]通过控制不同的电流条件,采用EcHG-AAS有效地实现了无机砷形态分析。在电流强度0.6 A和1.0 A条件下,As(Ⅲ)和As(Ⅴ)在0~40 μg/L浓度范围内呈良好的线性关系,As(Ⅲ)和As(Ⅴ)检出限分别为0.3 μg/L和0.6 μg/L,加标回收率为96% ~104%,该法已经成功应用于食用鲜牛奶的无机砷形态分析。
研究组还将EcHG-AAS技术应用于人发标准物质中无机砷形态分析,测定值与证书标准值相符,并成功应用于中药中无机砷形态分析[38-39]。Pyell等[40]在自制的两种不同结构的电化学发生池中分别选择性发生As(Ⅲ)和Se(Ⅳ),采用L-半胱氨酸在线还原As(Ⅴ),氢溴酸离线还原Se(Ⅵ),实现了As(Ⅴ)和Se(Ⅵ)的分析,As(Ⅲ)和As(Ⅴ)的检出限分别为0.4 μg/L和0.6 μg/L,相对标准偏差分别为1.9%和2.2%;Se(Ⅳ)和Se(Ⅵ)的检出限分别为0.2 μg/L和0.9 μg/L,相对标准偏差分别为2.2%和2.4%。Denkhaus等[41]考察了不同电极材料应用于EcHG-AAS对不同价态无机砷、硒、锑、锡分析的影响,结果表明Hg-Ag电极适合于无机砷和锑的形态分析;玻碳为 Sn(Ⅳ)、Se(Ⅳ)、As(Ⅲ)和Sb(Ⅲ)氢化物发生的最佳电极材料。
EcHG-AAS应用于元素形态分析的范围有待进一步拓展,这需要对不同元素、不同形态的元素氢化还原特性及条件进行更加深入、细微的剖析。
4 EcHG在等离子体发射光谱分析中的应用
等离子体发射光谱作为原子光谱的重要分支,在元素测定领域发挥着重要作用。根据产生等离子体方式的不同,等离子体发射光谱目前有电感耦合等离子体发射光谱(ICP-AES)和微波诱导等离子体发射光谱(MIP-AES),而后发展形成微波等离子体炬原子发射光谱(MPT-AES)等类型[42-43]。为了获得较好的分析灵敏度,对于As、Se等易于形成氢化物元素的定量分析,等离子体发射光谱仪经常采用氢化物发生的进样方式[44-49]。EcHG凭借其较之氢化物发生的特有优势,也开始应用于等离子体发射光谱分析,形成了 EcHG-ICP-AES (EcHG-MIP/MPT-AES)分析方法,其相关研究及应用列于表3,应用领域包括环境及工业污染等,分析元素涵盖As、Se、Sb、Hg等。就分析性能而言,在优化条件下,该技术检出限达到μg/L级,相对标准偏差均小于10%。
由于不需要使用支持电解质以外的其他化学试剂,并且较好地实现了基体的分离,该技术可以有效地克服常规原子发射光谱谱线间的严重干扰问题;此外,线性范围宽是其显著优势,因此应用于高浓度样品检测可以避免稀释操作对分析准确度的影响。由于原子发射光谱仪更能满足多元素的同时测定,针对多元素氢化物同时电化学发生的研究对该技术的进一步发展具有现实意义。
5 结语
近年来,电化学氢化物发生技术(EcHG)在原子光谱领域的应用有了较为迅速的发展。①电化学发生池的设计上,为获得更好的氢化物发生效率,具有较高超电位的材料已经应用于电极研究,在铅、碳等传统电极外,电化学修饰电极作为电化学流通池电极材料的研究已经起步,并展现了一定活力。②在分析范围和性能上,EcHG技术应用于原子光谱分析涵盖了砷、硒、铅、镉、锡、锑、锗和汞(电化学冷蒸气发生)等大部分常规化学法氢化物发生的元素;除了测定单纯的元素总量外,已经应用于元素形态分析。EcHG原子光谱分析的检出限、准确度和稳定性有了很大的提升,能够满足实际样品微量、痕量乃至超痕量分析的检测需要。③就实际样品分析而言,EcHG技术的分析范围日趋广阔,已涵盖食品、环境、烟草、饲料等诸多领域。此外,应用于有关元素产生氢化物的机理以及干扰研究也已经有所涉及[7,55-56]。目前商品化原子光谱仪器测定砷、硒等元素采用的常规氢化物发生法存在化学试剂依赖性强、还原剂不稳定需现用现配、试剂消耗量大容易造成环境污染等缺点,EcHG技术应用于原子光谱仪器具有较高的商业应用和环境价值,具有较大的发展潜力。
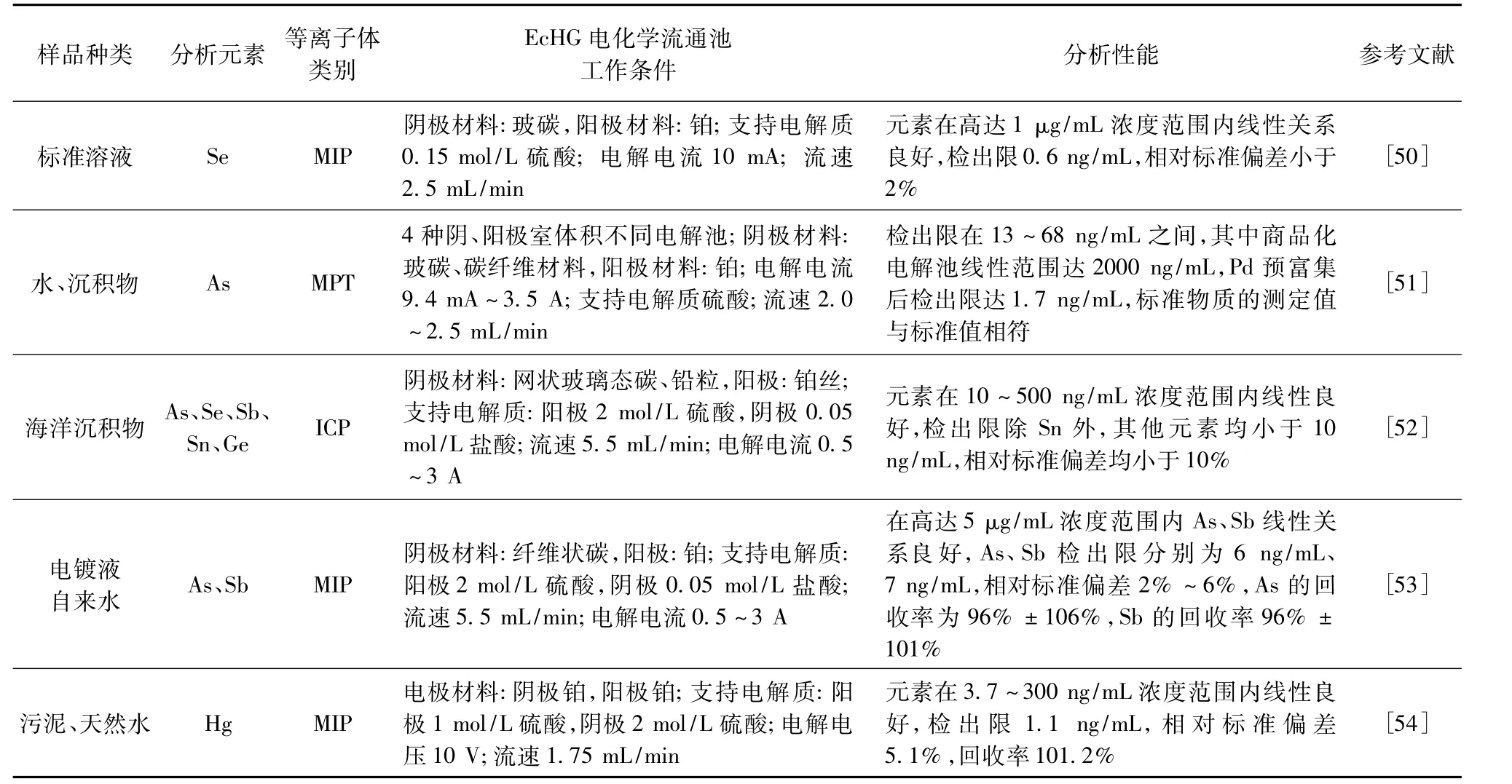
表3 EcHG-ICP(MIP/MPT)-AES的应用研究Table 3 Application study of EcHG-ICP(MIP/MPT)-AES
但EcHG技术应用于原子光谱分析仍然存在一些问题,有待进一步解决。①就电化学发生池而言,还需要对电化学流通池进行拆装,对电极进行抛光、清洁处理以消除记忆效应的影响。寻求更合理、便捷、适宜电化学流通池拆装的结构及低电极污染的电解质、电极材料、进样手段等有助于解决该问题。②EcHG对元素含量测定的检测性能有待进一步提升,这取决于更好地优化电化学发生池的结构、寻求更适合的电极材料以提升氢化物的发生效率和发生稳定性等。③EcHG应用于无机质谱进行元素分析将是其应用于原子光谱分析的有力补充[57-58],可实现检测灵敏度的进一步提升。此外,电化学氢化物发生池有待与原子光谱仪一体化,进而实现电化学氢化物发生原子光谱分析仪器的商品化。
[1] Rie R R,Rikke V H,Erik H L,Jens J S.Development and validation ofan SPE HG-AAS method for determination of inorganic arsenic in samples of marine origin[J].Analytical and Bioanalytical Chemistry,2012,403(10):2825-2834.
[2] Rauret G,Rubio R,Padró A.Arsenic speciation using HPLC-HG-ICP-AES withgas-liquidseparator[J].Fresenius'JournalofAnalyticalChemistry,1991,340(3):157-160.
[3] Sayago A,Beltránand R,Josú L,Ariza G.Hydride generation atomic fluorescence spectrometry(HG-AFS) as a sensitive detector for Sb(Ⅲ) and Sb(Ⅴ) speciation in water[J].Journal of Analytical Atomic Spectrometry,2000,15(4):423-428.
[4] Holak W.Gas-sampling technique for arsenic determination by atomic absorption spectrophotometry[J].Analytical Chemistry,1969,41:1712.
[5] 邓勃,迟锡增,刘明钟,李玉珍.应用原子吸收与原子荧光光谱分析[M].北京:化学工业出版社,2003: 38-41.
[6] 李淑萍,郭旭明,黄本立,胡荣宗,王秋泉,李彬.电化学氢化物发生法的进展及其在原子光谱分析中的应用[J].分析化学,2001,29(8):967-970.
[7] Francisco L,Eduardo B,Juan R C.Electrochemical hydride generation as a sample-introduction technique in atomic spectrometry:Fundamentals,interferences,and applications[J].Analytical and Bioanalytical Chemistry,2007,388:743-751.
[8] 侯逸众,申屠超,范云场,朱岩,陈梅兰.土壤中锑的双阳极电化学氢化物发生-原子荧光光谱法测定[J].分析测试学报,2009,28(1):109-111.
[9] 张王兵,淦五二,苏庆德,林祥钦.石墨管阴极电化学氢化物发生原子荧光法测定锗[J].分析化学,2005,33(10):1449-1451.
[10] 张王兵.电化学氢化物发生原子荧光法测定环境样品中的锑[J].应用化学,2009,26(6):738-741.
[11] 姜宪娟,淦五二.聚苯胺修饰电极-电化学氢化物发生原子荧光光谱法测定食品中锡含量[J].分析试验室,2012,31(3):101-104.
[12] 申屠超,侯逸众,范云场,朱岩.双阳极电化学氢化物发生原子荧光光谱法测定砷[J].分析化学,2008,36 (11):1592-1596.
[13] Li X,Wang Z H.Determination of mercury by intermittent flow electrochemical cold vapor generation coupled to atomic fluorescencespectrometry[J].Analytica Chimica Acta,2007,588(2):179-183.
[14] 淦五二,张王兵,苏庆德.电化学氢化物发生原子荧光法同时测定砷和锑[J].分析化学,2005,33(5): 687-689.
[15] Zhang W B,Yang X A,Dong Y P,Chu X F.Application of alkaline mode electrochemical hydride generation for the detection of As and Sb using atomic fluorescence spectrometry[J].Spectrochimica Acta Part B:Atomic Spectroscopy,2010,65(7):571-578.
[16] 张王兵.电化学氢化物发生.原子荧光法测定环境样品中的Se(Ⅳ)和Se(Ⅵ)[J].分析试验室,2009,28 (5):83-85.
[17] 侯逸众,范云场,朱岩,陈梅兰,申屠超.离子色谱-双阳极电化学氢化物发生-原子荧光光谱法测定当归中Sb(Ⅲ)和Sb(Ⅴ)[J].分析试验室,2009,28 (10):38-40.
[18] 申屠超,侯逸众,范云场,朱岩.离子色谱-双阳极电化学氢化物发生-原子荧光光谱法测定Ⅰ型牙髓失活材料中的砷形态[J].分析化学,2009,37(2):263 -266.
[19] Shen T C,Fan Y C,Hou Y Z,Wang K X,Zhu Y.Arsenic species analysis by ion chromatography-bianode electrochemical hydride generator-atomic fluorescence spectrometry[J].Journal of Chromatography A,2008,1213(1):56-61.
[20] 祖文川.电化学冷蒸气发生-原子荧光光谱联用对有机汞的检测研究[D].北京:北京师范大学,2009.
[21] Kozak L,Rudnicka M,Niedzielski P.Determination of inorganic selenium species in dietary supplements by hyphenated analytical system HPLC-HG-AAS[J].Food Analytical Methods,2012,5(6):1237-1243.
[22] Macedo S M,de Jesus R M,Garcia K S,Hatje V,de QueirozA F S,Antonio F,Ferreira S L C.Determination of total arsenic and arsenic(Ⅲ) in phosphate fertilizers and phosphate rocks by HG-AAS after multivariate optimization based on Box-Behnken design[J].Talanta,2009,80(2):974-979.
[23] Óscar M N,Raquel D G,Adela B B,José A C,José M F,Pilar B B.Determination of total selenium and selenium distribution in the milk phases in commercial cow's milk by HG-AAS [J].Analytical and Bioanalytical Chemistry,2005,381(6):1145-1151.
[24] Jutta F,Michael K,William S.Direct determination of arsenic in acid digests of plant and peat samples using HG-AAS and ICP-SF-MS[J].Analytica Chimica Acta,2005,530(2):307-316.
[25] Schloske L,Waldner H,Marx F.Optimisation of sample pre-treatment in the HG-AAS selenium analysis[J].Analytical and Bioanalytical Chemistry,2002,372(5-6): 700-704.
[26] 刘文涵,单胜艳,张丹,韩雯雯.流通式电化学氢化物发生法原子吸收测定硒的研究[J].分析测试学报,2005,24(5):69-71.
[27] Arbab-Zavara M H,Chamsaza M,Youssefib A,Aliakbari M.Electrochemical hydride generation atomic absorption spectrometry fordetermination ofcadmium [J].Analytica Chimica Acta,2005,546(1):126-132.
[28] Sáenz M,Fernández L,Domínguez J,Alvarado J.Electrochemical generation of volatile lead species using a cadmium cathode:Comparison with graphite,glassy carbon and platinum cathodes[J].Spectrochimica Acta Part B:Atomic Spectroscopy,2012,71-72:107-111.
[29] Arbab-Zavara M H,Chamsaza M,Youssefib A,Aliakbari M.Flow injection electrochemical hydride generation atomic absorption spectrometry for the determination of cadmium in water samples[J].Microchemical Journal,2013,108:188-192.
[30] Arbab-Zavara M H,Chamsaza M,Youssefib A,Aliakbari M.Multivariate optimization on flow-injection electrochemical hydride generation atomic absorption spectrometry of cadmium[J].Talanta,2012,97(15):229-234.
[31] Bolea E,Arroyo D,Laborda F,Castillo J R.Determination of antimony by electrochemical hydride generation atomic absorption spectrometry in samples with high iron content using chelating resins as on-line removal system[J].Analytica Chimica Acta,2006,569(1-2): 227-233.
[32] Arbab-Zavar M H,Chamsaza M,Yousefib A,Ashraf N.Electrochemical hydride generation of thallium[J].Talanta,2009,79:302-307.
[33] Arbab-Zavar M H,Chamsaza M,Yousefib A,Aliakbari M.Evaluation of electrochemical generation of volatile zinc hydride by heated quartz tube atomizer atomic absorption spectrometry[J].AnalyticalSciences,2012,28: 717-722.
[34] Mahboubeh M.Determination of cadmium in environmental sample by electrochemical hydride generation electrothermal atomic absorption with in situ trapping in graphite tube atomizer[J].Research Journal of Pharmaceutical,Biological and Chemical Sciences,2011,2(2):910-919.
[35] Mahboubeh M,Raham S.Electrochemical hydride generation oftin (Ⅱ) and itsdetermination by electrothermal atomic absorption spectrometry with in situ trapping in the graphite tube atomizer[J].Toxicological&Environmental Chemistry,2011,93(7): 1332-1340.
[36] Šíma J,Rychlovsky P.Electrochemical selenium hydride generation with in situ trapping in graphite tube atomizers[J].Spectrochimica Acta Part B:Atomic Spectroscopy,2003,58(5):919-930.
[37] 李勋,戚绮,薛珺,朱亚晋.电化学氢化物发生与原子吸收光谱联用对鲜牛奶中无机砷的形态分析[J].食品研究与开发,2007,28(11):121-123.
[38] 李勋,戚绮,薛珺,张晏杰.电化学氢化物发生-原子吸收光谱法测定不同价态的无机砷[J].理化检验(化学分册),2007,43(12):1027-1029.
[39] Li X,Jia J,Wang Z H.Speciation of inorganic arsenic by electrochemical hydride generation atomic absorption spectrometry[J].Analytica Chimica Acta,2006,560 (1-2):153-158.
[40] Pyell U,Dworschak A,Nitschke F,Neidhart B.Flow injection electrochemicalhydride generation atomic absorption spectrometry(FI-EHG-AAS)as a simple device for the speciation of inorganic arsenic and selenium [J].Fresenius' Journal of Analytical Chemistry,1999,363:495-498.
[41] Denkhaus E,Beck F,Bueschle P,Gerhard R,Golloch A.Electrolytic hydride generation atomic absorption spectrometry for the determination of antimony,arsenic,selenium,and tin-mechanistic aspects and figures of merit[J].Fresenius'Journal of Analytical Chemistry,2001,370:735-743.
[42] 张丽娟,赵丽巍,刘勤华,李敏晶,陈焕文,张寒琦,金钦汉,赵陆陆.在线分离富集微波等离子体发射光谱法测定Cd,Cu,Zn[J].吉林大学自然科学学报,2000(2):101-103.
[43] 李永生,赵博,孙旭辉.流动注射等离子体炬原子发射光谱峰宽定量法[J].光谱学与光谱分析,2009,29(9):2560-2564.
[44] Savio M,Pacheco P H,Martinez L D,Smichowski P,Gil R A.Optimization of methods to assess levels of As,Bi,Sb and Se in airborne particulate matter by FI-HGICP-OES [J]. Journal of Analytical Atomic Spectrometry,2010,25(8):1343-1347.
[45] Tyburska A,Jankowski K,Ramsza A,Reszke E,Strzele M,Andrzejczuk A.Feasibility study of the determination of selenium,antimony and arsenic in drinking and mineral water by ICP-OES using a dualflow ultrasonic nebulizer and direct hydride generation[J].Journal of Analytical Atomic Spectrometry,2010,25 (2):210-214.
[46] Elena P V,Adela B B,Pilar B B.Use of lanthanum hydroxide as a trapping agent to determine of hydrides by HG-ICP-OES[J].JournalofAnalyticalAtomic Spectrometry,2005,20(12):1344-1349.
[47] Suárez C A,Giné M F.A reactor/phase separatorcoupling capillary electrophoresis to hydride generation and inductively coupled plasma optical emission spectrometry (CE-HG-ICP-OES)for arsenic speciation[J].Journal of Analytical Atomic Spectrometry,2005,20(12):1395 -1397.
[48] Pohl P,Lesniewicz A,Zyrnicki W.Determination of As,Bi,Sb and Sn in conifer needles from various locations in Poland and Norway by hydride generation inductively coupled plasma atomic emission spectrometry[J].International Journal of Environmental Analytical Chemistry,2003,83(11):963-970.
[49] Moyano S,Wuilloud R G,Olsina R A,Gásquez J A,Martinez L D.On-linepreconcentration system for bismuth determination in urine by flow injection hydride generation inductively coupled plasma atomic emission spectrometry[J].Talanta,2001,54(2):211-219.
[50] Schermer S,Jurica L,Paumard J,Beinrohr E,Matysik F M,Broekaert J A C.Optimization of electrochemical hydride generation in a miniaturized electrolytic flow cell coupled to microwave-induced plasma atomic emissionspectrometry for the determination of selenium[J].Fresenius'Journal of Analytical Chemistry,2001,371: 740-745.
[51] Özmen B,Matysik F M,Bings N H,Broekaert J A C.Optimization and evaluation of different chemical and electrochemicalhydride generation systems forthe determination of arsenic by microwave plasma torch optical emission spectrometry[J].Spectrochimica Acta Part B:Atomic Spectroscopy,2004,59:941-950.
[52] Boleaa E,Labordaa F,Castilloa J R,Sturgeon R E.Electrochemical hydride generation for the simultaneous determination of hydride forming elements by inductively coupled plasma-atomic emission spectrometry[J].Spectrochimica Acta Part B:Atomic Spectroscopy,2004,59(4):505-513.
[53] Pohla P,Zapata I J,Bings N H.Optimization and comparison of chemical and electrochemical hydride generation for optical emission spectrometric determination of arsenic and antimony using a novel miniaturized microwave induced argon plasma exiting the microstrip wafer[J].Analytica Chimica Acta,2008,606(1,7):9-18.
[54] ˇCerveny V,Horváth M,Broekaert J A C.Determination of mercury in water samples by electrochemical cold vapor generation coupled to microstrip microwave induced helium plasma optical emission spectrometry[J].Microchemical Journal,2013,107:10-16.
[55] Arbab-Zavara M H,Chamsaza M,Youssefib A,Aliakbari M.Mechanistic aspects of electrochemical hydride generation for cadmium[J].Analytica Chimica Acta,2006,576(2):215-220.
[56] Martin A A,Nicolas H B,Pawel P,Jos A C B.Investigation of electrochemical hydride generation coupled to microwave plasma torch optical emission spectrometry for the determination of arsenic:Analytical figures of merit,interference studies and applications to environmentally relevant samples[J].International Journal of Environmental Analytical Chemistry,2008,88(9):625-636.
[57] Machado L F R,Jacintho A O,Menegario A A,Zagatto E A G,Gine M F.Electrochemical and chemical processes for hydride generation in flow injection ICPMS:Determination of arsenic in natural waters[J].JournalofAnalyticalAtomic Spectrometry,1998,13(12):1343-1346.
[58] Bings N H,Stefánka Z,Mallada S R.Flow injection electrochemical hydride generation inductively coupled plasma time-of-flight mass spectrometry for the simultaneous determination of hydride forming elements and its application to the analysis of fresh water samples[J].Analytica Chimica Acta,2003,479(2): 203-214.
The Application and Development of Electrochemical Hydride Generation in Atomic Spectrometry Analysis
ZU Wen-chuan,WANG Yu,WU Yan-wen,CHEN Shun-cong
(Beijing Center for Physical&Chemical Analysis,Beijing Engineering Research Center of Food Safety Analysis,Beijing 100089,China)
Electrochemical hydride generation(EcHG)is an effective gas sampling method developed for atomic spectrometers.Electrode reactions are adopted in an electrochemical cell to generate hydride and mercury vapor in the cathode chamber for EcHG instead of traditional chemical reducing method.Compared with the traditional KBH4(NaBH4)-acid chemical system,no other chemical reagents but the supporting electrolyte is needed for EcHG as electron transfer plays the reducing role instead of the reducing reagents.For EcHG,hydride and mercury vapor are directly led to the atomizer from the cathode chamber for determination.The analysis price and time for making up solutions are decreased in large degree meanwhile the blank value introduced from the analytic process is reduced remarkably for EcHG.Moreover,EcHG is lower pollution and more environmental friendly due to none chemical reagent used.Recently,rapid development has been made for atomic spectrometry analysis including Atomic FluorescenceSpectrometry(AFS),AtomicAbsorptionSpectrometry(AAS),AtomicEmission Spectrometry(AES)coupled with electrochemical hydride generation.The analytical range for this technology has been extended to speciation analysis from only total amount of element analysis.The requirement for trace or even ultra trace detection has gradually been satisfied instead of merely micro-analysis.As for the analytical performance,most of the regular chemical hydride generated elements are covered,including As,Se,Pb,Cd,Sn,Sb,Ge and Hg.Generally,μg/L level can be achieved for the detection limits of characteristic elements by EcHG coupled with AAS and Inductively Coupled Plasma-Atomic Emission Spectrometry(ICP-AES).While for EcHG-AFS,it can be reduced to 0.1 μg/L(ng/L level for mercury).The relative standard deviations are lower than 10%.The spiked recoveries are 90%-110%and determination results for standard matters are favorable.A series of real samples(foods,tobacco,fodder,etc)were successfully analyzed by this technique.The related study on mechanism has already started,by which theoretical support for this technique is supplied and it can also be found naturally.Nevertheless,the analytical range for this technique has been only focused on inorganic species of certain elements,and the organic species are still expected to be analyzed,which forms a hot and difficult spot in this area.Based on the previous studies,the mechanism for EcHG,the further configuration optimization of the electrolytic flow cell,and the extension of elemental speciation range will become the potential developing trends for this technique.
electrochemicalhydride generation;Atomic Fluorescence Spectrometry; Atomic Absorption Spectrometry;Inductively Coupled Plasma-Atomic Emission Spectrometry;research progress
O657.63
A
0254-5357(2014)02-0168-10
2013-07-05;接受日期:2013-09-04
国家重大科学仪器设备开发专项(2011YQ15004011,2011YQ140147);北京市财政资金支持项目(PXM2013_ 178305_000005);北京市科学技术研究院改革与发展专项(2013)
祖文川,硕士,工程师,从事仪器分析工作。E-mail:zuhongshuai@126.com。

