HPLC-PDA法测定兽药中非法添加四种解热镇痛抗炎类药物
李慧素,杜红鸽,吴宁鹏,臧和英,付盼盼
(1.河南省兽药监察所,郑州450008;2.河南出入境检验检疫局,郑州450003)
解热镇痛抗炎类药物包括非甾体类抗炎药(如对乙酰氨基酚、安乃近等)和甾体类糖皮质激素类抗炎药(如地塞米松、地塞米松磷酸钠等),具有良好的退热、镇痛、抗炎、抗风湿等作用。目前,一些不法企业受经济利益的驱使,通过非法添加解热镇痛抗炎类药物使其兽药具有了速效、高效、特效的优点,从而取得高额利润。由于非法添加行为是隐形的,增强药效的同时带来了药量叠加的中毒风险和药物残留隐患,通过食物链传递,给人体健康造成严重危害[1-3]。为了打击非法添加的违规行为,迫切需要建立兽药制剂中非法添加解热镇痛抗炎类药物的检测方法。
目前,对非法添加的对乙酰氨基酚、安乃近、氨基比林、安替比林和地塞米松磷酸钠进行了一种或几种药物的测定[4~6],但还未对板蓝根注射液、穿心莲注射液及氟苯尼考粉、替米考星预混剂等制剂进行监测。本文利用二极管阵列检测器,建立了高效液相色谱检查方法,可以有效监测非处方成分的干扰,提高了对非法添加药物的定性和定量测定[7]。
1 材 料
1.1 仪器与试剂 Waters HPLC高效液相色谱系统,包括二极管阵列检测器、Empower2色谱工作站;MILIPORE超纯水器;METTLER XP205电子天平。甲醇为色谱纯,其他均为分析纯,水符合实验室一级水要求。
1.2 药品 安乃近对照品(批号为H0291105,含量为100.0%)和地塞米松磷酸钠对照品(批号为H0240805,含量为94.7%),均来自中国兽医药品监察所;对乙酰氨基酚对照品(批号为100018-200408,含量为100.0%)和地塞米松对照品(批号为100129-200303,含量为100.0%),均来自中国药品生物制品检定所。安乃近、对乙酰氨基酚原料药均来自河南某兽药生产企业。
氟苯尼考粉,氟苯尼考预混剂,替米考星预混剂,磷酸泰乐菌素预混剂,穿心莲注射液,板蓝根注射液,替米考星注射液均来自市售样品,经检测均不含对乙酰氨基酚、安乃近、地塞米松和地塞米松磷酸钠。
2 方法与结果
2.1 色谱条件 色谱柱:Waters X-Bridge C18(150×4.6 mm,5 μm);柱温 30 ℃;进样量 10 μL。 流速0.8 mL/min;二极管阵列检测器,采集波长为 200~400 nm光谱图和240 nm波长处的色谱图。流动相A:磷酸二氢钠 3.0 g加水至 1000 mL,加三乙胺1 mL,用氢氧化钠调 pH 值至 7.0±0.2。 流动相 B:甲醇。按表1进行梯度洗脱。该色谱条件下,四种对照品出峰时间顺序依次是对乙酰氨基酚、安乃近、地塞米松磷酸钠和地塞米松,相邻色谱峰之间的分离度均符合要求,且色谱峰尖锐对称。结果见图1。

表1 梯度淋洗表

图1 4种解热镇痛药物的色谱图及光谱图
2.2 溶液配制
2.2.1 对照品溶液 (临用前配制)精密称取对乙酰氨基酚、安乃近,地塞米松和地塞米松磷酸钠对照品各50 mg,置50 mL量瓶中,加甲醇适量溶解并稀释至刻度,摇匀作为对照品贮备液;再分别精密量取2.0 mL于50 mL量瓶中,加甲醇稀释至刻度,摇匀,作为混合对照品溶液。
2.2.2 阴性空白溶液 取无非法添加的各制剂1.0 g或1.0 mL,置50 mL量瓶中,加甲醇适量溶解(粉散剂需要超声10 min,并放冷至室温)。用甲醇稀释至刻度,摇匀。精密量取2.0 mL,置50 mL量瓶中,用80%甲醇溶液稀释至刻度,摇匀,作为阴性空白溶液。
2.2.3 空白添加溶液 取无非法添加的各制剂,乙酰氨基酚和安乃近分别按1%、2%、5%添加,地塞米松和地塞米松磷酸钠按 0.15%、0.2%、0.5%添加,照2.2.2项下操作制备成各制剂的阴性对照溶液。
2.2.4 建立光谱数据库的溶液 以乙酰氨基酚、安乃近、地塞米松和地塞米松磷酸钠对照品溶液(40 μg/mL)作为建立光谱数据库的溶液。
2.3 峰纯度检查 对供试品溶液色谱图中四种解热镇痛类药物色谱峰进行峰纯度检查,结果见图2和表2。结果显示,各阴性空白在240 nm处均无紫外吸收,对目标分析物无干扰,四种解热镇痛类药物能达到很好的分离,且各色谱峰的纯度角度均小于纯度阈值,表明此色谱条件下,四种解热镇痛药物的出峰位置无其他干扰峰,为单一物质峰,方法可行。

图2 供试品(酒石酸泰乐菌素预混剂)添加解热镇痛类药物纯度图

表2 峰纯度检查结果表
2.4 光谱相似度检查 对供试品溶液中对乙酰氨基酚、安乃近、地塞米松和地塞米松磷酸钠的光谱图与光谱库进行匹配,匹配角度均小于匹配阈值(表2)。结果表明,供试品溶液中相应色谱峰的光谱与对乙酰氨基酚、安乃近、地塞米松和地塞米松磷酸钠光谱库的光谱非常相似,可认为是同一物质。
2.5 方法学考察
2.5.1 溶液稳定性 取混合对照品溶液(50 μg/mL),室温放置于 0、3、6、9、12、14 h 分别进样测定,四种解热镇痛药物色谱峰面积RSD均小于0.7%,表明该溶液在14 h内稳定。
2.5.2 线性关系 精密量取4种解热镇痛类药物的对照溶液适量,用80%甲醇稀释成5、10、20、50、100 μg/mL的系列混合标准溶液,从低浓度到高浓度依次注入高效液相色谱测定。以标准溶液浓度为横坐标、峰面积为纵坐标绘制标准曲线,求得线性回归方程及相关系数(表3和图3)。结果表明,4种解热镇痛类药物的浓度在5~100 μg/mL范围内呈良好的线性关系。

表3 4种解热镇痛类药物的线性方程和相关系数

图3 4种解热镇痛类药物标准曲线图
2.5.3 回收率试验 由于添加回收试验4种解热镇痛类药物使用量较大,考虑用纯度符合要求的兽药原料药代替对照品进行添加回收试验,即在空白试样中分别添加对乙酰氨基酚和安乃近原料药,而地塞米松磷酸钠和地塞米松由于原料价格昂贵,没有搜集到原料,因此用对照品溶液进行添加回收试验。
精密称取对乙酰氨基酚和安乃近原料各10、20、50 mg,各置 50 mL量瓶中,加阴性空白 1.0 g或1.0 mL,加甲醇适量,超声 10 min,放冷,甲醇稀释至刻度,摇匀。精密量取2 mL置50 mL量瓶中,加地塞米松和地塞米松磷酸钠对照品贮备液各0.6、0.8、1.0 mL,混匀,加80%甲醇溶液稀释至刻度,摇匀,每个浓度制备三份平行样品。计算回收率及批内变异系数。结果显示,对乙酰氨基酚平均回收率为84.2%~119.2%,安乃近平均回收率为 73.5% ~118.6%,地塞米松磷酸钠平均回收率为82.5%~115.1%,地塞米松平均回收率为87.9%~115.7%,批内变异系数为0.1%~5.8%,结果见表4~表10 所示。

表4 穿心莲注射液中添加4种解热镇痛类药物回收率试验结果

表5 板蓝根注射液中添加4种解热镇痛类药物回收率试验结果

表6 氟苯尼考预混剂中添加4种解热镇痛类药物回收率试验结果
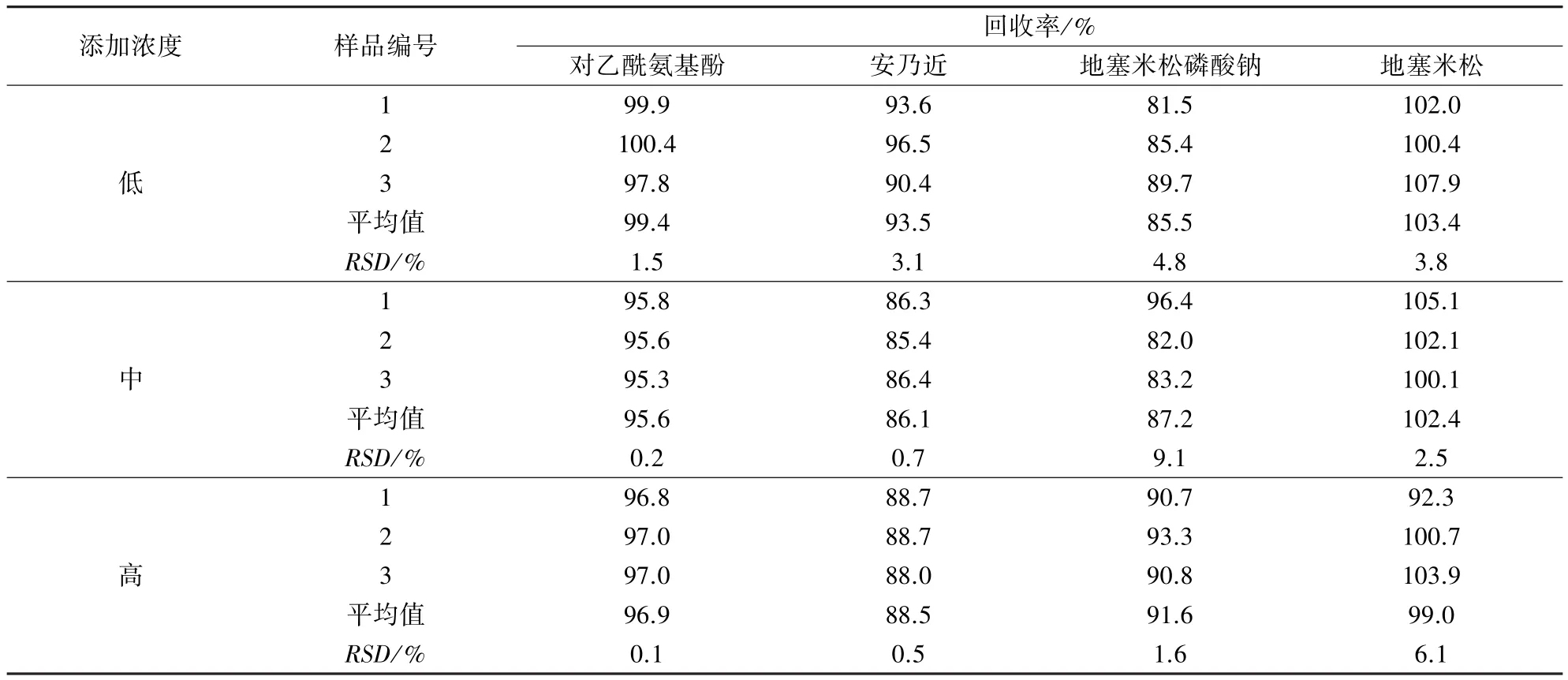
表7 氟苯尼考粉中添加4种解热镇痛类药物回收率试验结果

表8 替米考星预混剂中添加4种解热镇痛类药物回收率试验结果

表9 磷酸泰乐菌素预混剂中添加4种解热镇痛类药物回收率试验结果

表10 替米考星注射液中添加4种解热镇痛类药物回收率试验结果
2.5.4 检测限 取混合对照品溶液适量(建议取1 mL或2 mL)置50 mL量瓶中,用甲醇稀释至刻度,摇匀,梯度稀释后添加到阴性对照溶液中,进行检测,以光谱图(图4~图7)失真的最大浓度作为方法的检测限,安乃近和地塞米松磷酸钠最低检出浓度 均 为 2 μg/mL, 在 各 制 剂 中 的 检 测 限 为3.0 mg/mL(mg/g),对乙酰氨基酚和地塞米松最低检出浓度均为1 μg/mL,在各制剂中的检测限为1.5 mg/mL(mg/g)。
2.5.5 精密度 取混合对照品溶液(50 μg/mL),重复进样6次,测定峰面积。结果表明:四种成分的保留时间 RSD小于 0.1%,峰面积 RSD小于1.0%,结果符合精密度的要求。
2.5.6 耐用性 从柱温、流动相pH值、色谱柱三个方面考察方法的耐用性。分别改变柱温为25、30、35 ℃,流动相 A 的 pH 值 6.8、7.0、7.2,色谱峰出峰顺序无变化,保留时间稍有变化;使用不同品牌、不同型号的色谱柱,如 Thermo Hypersil Gold(4.6×250 mm,5 μm);Waters XBridge C18(4.6×150 mm,5 μm);Waters XBridge C18(3.5×150 mm,5 μm)等,结果四种成分仍能很好地分离且保留时间合理。在最佳实验条件的选择中流速的变化对四种成分的影响也不大,本方法的耐用性较好。
2.5.7 专属性 在满足系统适用性的条件下,4种解热镇痛类药物能够很好地分离,板蓝根和穿心莲注射液无紫外吸收,氟苯尼考、泰乐菌素和替米考星制剂中主成分和杂质均不干扰解热镇痛类药物的检测(图8~图14)。

图4 安乃近和地塞米松磷酸钠的检测限光谱图(3 mg/mL)

图5 安乃近和地塞米松磷酸钠的检测限色谱图(3 mg/mL)

图6 对乙酰氨基酚和地塞米松的检测限光谱图(1.5 mg/mL)

图7 对乙酰氨基酚和地塞米松的检测限色谱图(1.5 mg/mL)

图8 板蓝根注射液空白及空白添加色谱图
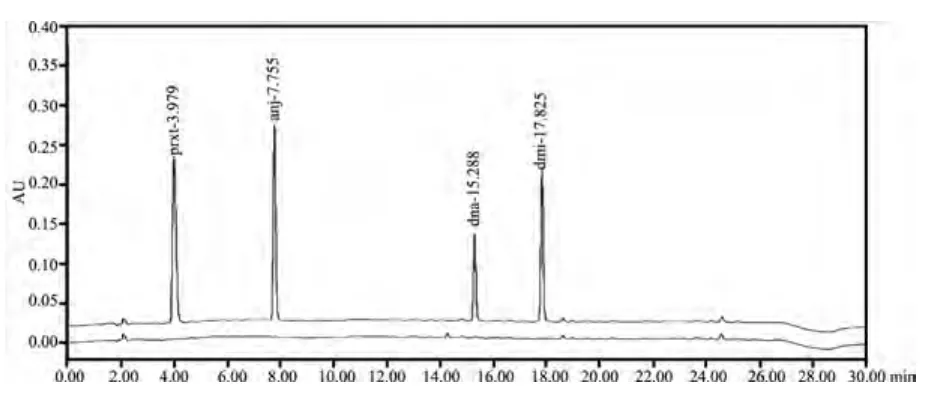
图9 穿心莲注射液空白及空白添加色谱图

图10 氟苯尼考预混剂空白及空白添加色谱图
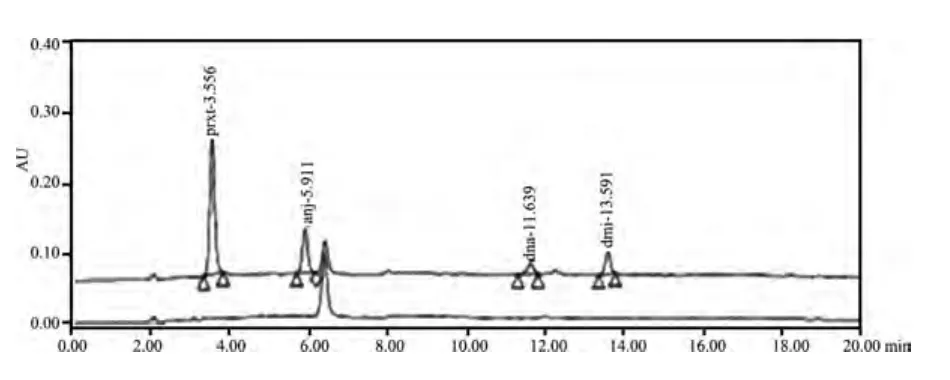
图11 氟苯尼考粉空白及空白添加色谱图
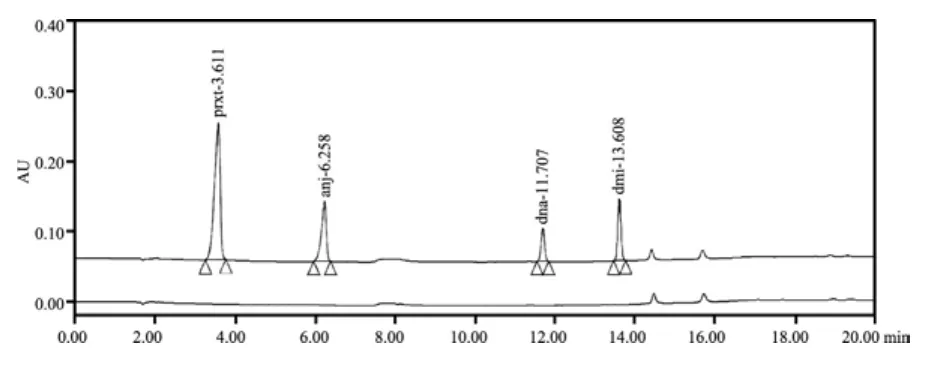
图12 酒石酸泰乐菌素预混剂空白及空白添加色谱图

图13 替米考星注射液空白及空白添加色谱图
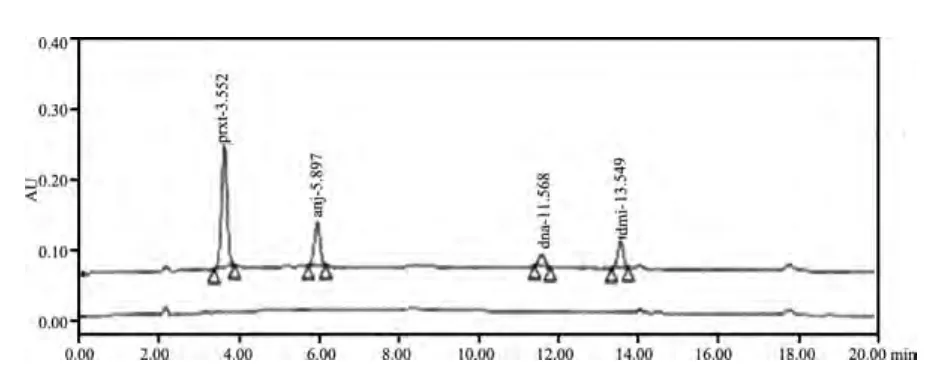
图14 替米考星预混剂空白及空白添加色谱图
3 讨论与小结
3.1 稀释溶剂的选择 本方法先后选择了甲醇[8]、80%甲醇、50%甲醇对标准贮备液进行稀释,经测定发现,50%的甲醇为溶剂时,安乃近降解比较快,产生另外一种物质;甲醇和80%甲醇溶液为溶剂时,安乃近基本未发生降解。同时文献[9]也证实,安乃近在水溶液、体内及加热的条件下极不稳定,主要产生MAA(4-甲氨基安替比林)的降解产物。而甲醇为溶剂时,个别色谱柱会出现峰型不对称的现象。因此,试验选择了80%的甲醇作为稀释溶剂,并建议样品溶液在14 h内完成测定。
3.2 流动相洗脱方式的选择 由于地塞米松和对乙酰氨基酚、安乃近极性差别较大,采用等度洗脱时,对乙酰氨基酚很快出峰,地塞米松很晚出峰甚至无法洗脱出来,当采用梯度洗脱[5]时,可以使4种解热镇痛类药物很好的分离,分离度均大于3.0,峰型对称。因此,选择梯度洗脱的方式进行测定,并且该梯度条件亦可适用于超高效液相色谱测定。
3.3 添加回收浓度选择与结果分析 由于四种药物药效浓度不同,在兽药制剂中的添加量也不同。由于掺假过程复杂,实际添加比例是未知的,为模拟兽药制剂的非法添加情况,本研究在做添加回收试验时,以各药物在制剂规格的1%、2%、5%作为三个添加浓度。
试验过程中,由于安乃近容易降解产生MAA,随着样品溶液放置时间的延长,容易造成安乃近的回收率偏低;而地塞米松和地塞米松磷酸钠采用标准溶液添加,定量添加的标准溶液体积是造成低浓度添加回收结果偏低的主要原因。
本方法采用二极管阵列检测器进行测定,实现可以检测6种制剂的主成分是否干扰对乙酰氨基酚、安乃近、地塞米松和地塞米松磷酸钠,同时可以通过峰纯度检查确保添加药物出峰处无干扰,再经光谱相似度检查锁定非法添加药物,同时通过保留时间与对照品进行比对相佐证,实现兽药中非法添加物的高效、快速、准确识别。通过方法学考察,本方法可以用于兽药中对乙酰氨基酚、安乃近、地塞米松和地塞米松磷酸钠的检测。
[1]杨秀玉,万仁玲,马玉叶,等.高效液相色谱法定性检测5种中兽药散剂中违规添加的氯霉素[J].中国兽药杂志,2006,40(12): 11-14.
[2]李 锐.中成药、保健食品中非法添加化学成分的检测[J].中国药业,2007, 16(18):10-11.
[3]周 媛,贡玉清,邵德佳.有关中兽药中非法添加化学药物的探讨[J].中兽医医药杂志, 2010, 29(4): 28-31.
[4]农业部1848号公告-黄芪多糖注射液中非法添加解热镇痛类、抗病毒类、抗生素类、氟喹诺酮类等11种化学药物(物质)检查方法[S].
[5]农业部2508号公告-1-注射用青霉素钾(钠)中非法添加解热镇痛药物检查方法[S].
[6]农业部1956公告.乳酸环丙沙星注射液中非法添加对乙酰氨基酚检查方法[S].
[7]刘 宝,周莉莉,王 骏,等.基于二极管阵列检测器的色谱峰纯度的快速直观鉴定[J].光谱实验室, 2011, 28(4): 1684-1689.
[8]中国兽药典委员会.中华人民共和国兽药典(2010年版)一部[S].
[9]郝利华,于晓辉,董玲玲,等.HPLC-PDA法同时测定黄芪多糖注射液中非法添加的四种解热镇痛类药物[J].中国兽药杂志,2014, 46(8): 28-31.

