安替可胶囊联合同步放化疗治疗不可切除胃癌30例*
张路,袁响林,彭平,刘细友,付强,肖志平
(华中科技大学同济医学院附属同济医院肿瘤中心,武汉 430030)
·药物与临床·
安替可胶囊联合同步放化疗治疗不可切除胃癌30例*
张路,袁响林,彭平,刘细友,付强,肖志平
(华中科技大学同济医学院附属同济医院肿瘤中心,武汉 430030)
目的 观察安替可胶囊联合放疗及卡培他滨同步化疗治疗不可切除局部晚期胃癌的疗效。方法将55例不可切除局部晚期胃腺癌患者随机分为两组,治疗组30例,接受局部放射治疗(放疗)+卡培他滨+安替可胶囊治疗;对照组25例,接受局部放疗+卡培他滨同步化学治疗(化疗),观察两组不良反应及有效率。结果治疗组的客观有效率及疾病控制率分别为86.7%及100.0%,均高于对照组(分别为68.0%和88.0%),但差异无统计学意义。结论在放疗+卡培他滨同步化疗标准方案的基础上加用安替可胶囊治疗不可手术局部晚期胃癌患者有望提高客观有效率及疾病控制率。
安替可胶囊;癌,胃;同步放化疗
胃癌是我国第三大常见肿瘤及农村地区最常见肿瘤,每年新发胃癌患者达40万例,死亡人数达30万例[1]。早期胃癌患者接受手术治疗后预后良好,但胃癌症状缺乏特异性,我国许多患者确诊时已是局部晚期[2],无法手术切除。紫杉类或氟尿嘧啶类药物联合放射治疗(放疗)可显著延长不可切除胃癌患者生存时间[3-4],是目前美国国立综合癌症网络(national comprehensive cancer network,NCCN)指南推荐的标准治疗方案。但报道数据均表明,不可切除胃癌患者即使接受标准放疗及两药同步化学治疗(化疗),仅10%患者能达到病理完全缓解[5],临床完全缓解率仅35%[6],中位生存期则仅为25.0和14.5个月[5-6],同步放化疗的疗效尚需进一步提高。受制于胃本身及周围正常对照组织的耐受量,胃癌放疗的处方剂量一般为45~50 Gy,难以进一步提高。探索更好的同步治疗方案有助于提高疗效,增加局部控制率,改善预后。安替可胶囊是根据传统中医理论,利用现代制药手段研发的纯中药抗癌制剂,主要成分为蟾皮、当归等,具有清热解毒、利水消肿、散结止痛作用,并在食管癌及鼻咽癌患者中表现出放射增敏作用。2011年10月至2013年4月,笔者采用放疗联合卡培他滨及安替可胶囊治疗不可切除的局部晚期胃癌患者,并与接受标准放疗+卡培他滨同步化疗的患者对比,发现加用安替可胶囊患者,其放疗+卡培他滨同步化疗的疗效有改善趋势。报道如下。
1 资料与方法
1.1 临床资料 我科收治初治的局部晚期胃癌患者55例,均经胃镜及病理组织学证实为胃腺癌,由CT、PET/CT、腹腔镜检查或剖腹探查后认为不可切除且排除远处转移,体能状况卡氏评分(KPS)>70分,无重要器官功能严重损害,血常规和肝、肾功能正常,预期生存时间>6个月。已行2周期紫杉醇类+铂类方案化疗,病灶缩小或维持稳定,采用随机数字表法随机分为治疗组和对照组。治疗组30例,男20例,女10例,年龄22~61岁,平均41.0岁。对照组25例,男18例,女7例,年龄28~63岁,平均39.3岁。两组患者临床资料基本均衡,见表1。
1.2 治疗方法 ①放疗:真空袋固定摆位,CT模拟定位后制定调强放疗计划,6 MV照射,照射靶区包括胃、瘤床及区域淋巴结(见已发表文献[7])。处方剂量4 500 cGy/25次,分次量180 cGy,5周完成,脊髓、肝、肾等重要器官照射剂量均控制在耐受剂量以内。②同步药物治疗:治疗组放疗期间口服卡培他滨及安替可胶囊(长春远大国奥药业有限公司,批准文号:国药准字Z10960071,规格:每粒0.22 g):卡培他滨825 mg·(m2)-1,po,bid,每周5 d,安替可胶囊每日3次,每次2粒,至放疗结束;对照组仅口服卡培他滨,剂量同治疗组。
1.3 疗效判定标准 所有患者治疗前均进行腹部增强CT扫描及胃镜检查作为基线期资料,治疗结束后复查腹部增强CT及胃镜了解肿瘤退缩情况,按照WHO标准评定疗效,完全缓解(complete response, CR):所有可见病变完全消失并至少维持4周以上;部分缓解(partial response,PR):肿瘤病灶的最大径及其最大垂直径的乘积减少50%,无新病灶出现并维持4周以上;病情稳定(stable disease,SD):肿瘤病灶两径乘积缩小≤25%,或增大≤25%,无新病灶出现;病变进展(progressive disease,PD):肿瘤病灶两径乘积增大>25%,或出现新病灶。客观有效率(%)=(CR+PR)/总例数×100%,疾病控制率(%)=(CR+PR+SD)/总例数×100%。

表1 两组患者临床资料比较 例
1.4 不良反应 治疗中观察记录各种不良反应,每周监测血常规及肝肾功能变化,不良反应根据WHO规定标准分为0~Ⅳ级。
1.5 统计学方法 采用SPSS19.0版统计软件进行分析,率的比较采用卡方检验。P<0.05为差异有统计学意义。
2 结果
2.1 临床疗效 55例患者均顺利完成治疗,治疗组CR 8例,PR 18例,SD 4例,PD 0例;对照组CR 7例, PR 10例,SD 5例,PD 3例,PD3例患者均因治疗后复查时在放疗野外发现新发病灶而评价为进展。治疗组客观有效率为86.7%、疾病控制率为100.0%,对照组分别为68.0%和88.0%。
2.2 不良反应 两组治疗期间发生的主要不良反应为恶心、呕吐、乏力、腹泻及贫血等,均为Ⅰ~Ⅱ度,经对症处理后缓解,无患者因此中断治疗。两组间比较差异无统计学意义(P>0.05)。见表2。腹泻对照组
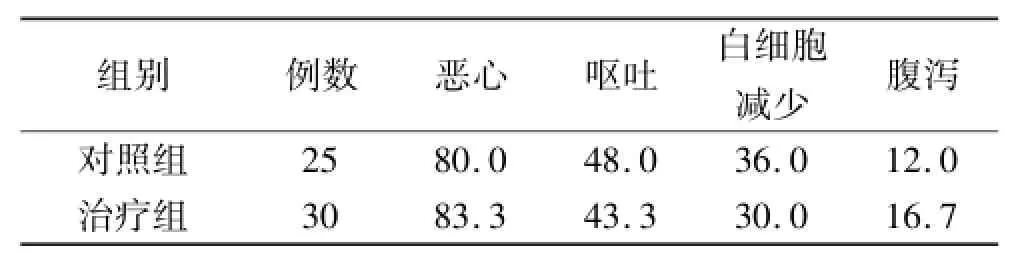
表2 两组患者主要不良反应发生率 %
3 讨论
手术是胃癌唯一的根治手段,但许多患者确诊时已失去手术机会。不可切除的局部晚期胃癌患者的标准治疗方案是同步放化疗。文献报道晚期胃癌患者经放疗联合铂类、氟尿嘧啶类或紫杉醇类药物同步化疗后中位生存期仅为14.5~25个月[5-6]。笔者采用放疗联合卡培他滨及安替可胶囊同步治疗不可手术的局部晚期胃癌患者,能够很好耐受,不增加不良反应发生率,且客观有效率及疾病控制率均高于放疗+卡培他滨组患者,显示出一定的放疗增敏作用,其差异虽未达到统计学标准,可能因样本量较小所致,值得进一步探讨。
安替可胶囊是根据传统中医理论,利用现代制药手段开发的纯中药抗癌制剂,经体内外动物实验证实对多种肿瘤细胞具有明显抑制作用,并能促进非特异性体液和细胞免疫功能[8]。安替可胶囊与放疗联合可促进鼻咽癌患者颈部转移灶消退并改善患者免疫功能[9],王四旺等[10]使用安替可胶囊联合放射治疗晚期食管癌100例,总缓解率为72.0%,比单纯放疗组(34.4%)明显提高,新近报道的一组病例也证实安替可胶囊用于食管癌具有放疗增敏作用,可明显提高放疗的有效率[11],这些报道均表明安替可胶囊具有放疗增敏作用,但在食管癌及鼻咽癌以外的肿瘤尚未见报道。笔者观察的一组病例试用放疗联合卡培他滨及安替可胶囊治疗不可手术的局部晚期胃癌患者,完全缓解率与对照组相近,但部分缓解率、客观有效率和局部控制率均高于对照组,提示安替可胶囊对胃癌也具有放疗增敏作用。其放疗增敏机制目前尚未见研究,笔者推测可能与其直接抗肿瘤作用有关,此外其主要成分当归具有促进造血和抗贫血以及改善组织缺血的作用,有可能通过增加肿瘤组织供氧、减少乏氧组织来提高放疗敏感性,但这些假设均需严格的基础研究进一步论证。
同步放化疗时化疗药物多采用耐受性良好的小剂量给药方案,目的在于保证放疗顺利进行的前提下增加放疗敏感性,提高局部控制率,而对远处微小转移灶无明显作用,因此远处转移常常成为同步放化疗失败的原因。本组病例对照组中即有3例患者治疗后出现放射野外新发病灶而疾病进展,然而治疗组在放疗期间使用卡培他滨和安替可胶囊同步治疗,所有患者均未出现放射野外新发病灶,提示放疗期间加用安替可胶囊不仅可作为放疗增敏,也具有全身治疗作用,可以减少远处转移,可能与安替可胶囊的直接抗癌作用有关[8]。
综上所述,在放疗+卡培他滨同步化疗标准方案的基础上加用安替可胶囊治疗不可手术局部晚期胃癌患者可以提高客观有效率及疾病控制率,提示安替可胶囊用于胃癌具有放疗增敏作用,值得注意的是,加用安替可胶囊后远处转移也出现减少趋势,在提高局部控制的同时可以兼顾全身治疗。不过,本观察还存在一些不足之处:样本量较小;放疗效应有一定滞后性,放疗结束后肿瘤还会进一步缩小,延长随访期可能观察到更高的有效率;未随访到患者生存数据。因此,安替可胶囊在胃癌放疗中显示出良好的增敏前景,值得进一步设计前瞻性研究证实。
[1] YANG L.Incidence and mortality of gastric cancer in China [J].World J Gastroenterol,2006,12(1):17-20.
[2] 庄庆昕,徐建明,林莉,等.636例胃癌患者临床治疗现状分析[J].中华肿瘤杂志,2012,34(4):316-320.
[3] MOERTEL C G,CHILDS D S Jr,REITEMEIER R J,et al. Combined 5-fluorouracil and supervoltage radiation therapy of locally unresectable gastrointestinal cancer[J].Lancet, 1969,2(7626):865-867.
[4] Anon.The concept of locally advanced gastric cancer.effect of treatment on outcome.The Gastrointestinal Tumor Study Group[J].Cancer,1990,66(11):2324-2330.
[5] SAIKAWA Y,KUBOTA T,KUMAGAI K,et al.PhaseⅡstudy of chemoradiotherapy with S-1 and low-dose cisplatin for inoperable advanced gastric cancer[J].Int J Radiat Oncol Biol Phys,2008,71(1):173-179.
[6] SUZUKI A,XIAO L,TAKETA T,et al.Localized gastric cancer treated with chemoradation without surgery:UTMD Anderson Cancer Center experience[J].Oncology,2012,82 (6):347-351.
[7] 袁响林,付强,胡国清,等.中晚期胃癌术后序贯放化疗36例[J].世界华人消化杂志,2007,15(36):3856-3859.
[8] 王四旺,谢艳华,李予蓉,等.安替可胶囊肮肿瘤作用及对晚期消化道肿瘤的近期疗效[J].世界华人消化杂志, 1999,7(3):236-239.
[9] 胡国清,袁响林,胡长耀.安替可配合放射治疗鼻咽癌的临床观察[J].中国肿瘤临床,2002,29(6):440-441.
[10] 王四旺,朱玲珍,林洪生,等.复方蟾皮胶囊对晚期消化道肿瘤近期疗效的观察[J].第四军医大学学报,1996,17 (2):97-100.
[11] 江晓燕,管志峰.安替可胶囊合并放射治疗食管癌近期疗效分析[J].齐齐哈尔医学院学报,2012,33(17): 2337-2338.
DOI 10.3870/yydb.2014.10.023
R286;R735.2
B
1004-0781(2014)10-1339-03
2013-09-06
2013-11-17
*国家自然科学基金资助项目(81001067)
张路(1981-),男,湖北荆州人,主治医师,博士,主要研究方向:恶性肿瘤的综合治疗及免疫治疗。电话: 027-83663406,E-mail:zhanglutjh@hotmail.com。
肖志平(1979-),男,湖南涟源人,主管技师,学士,主要研究方向:肿瘤放射治疗。电话:027-83663360,E-mail:xzp147@126.com。

